一种检测畜禽体内环丙沙星残留的方法与流程
本发明涉及兽残检测技术领域,具体涉及一种检测畜禽体内环丙沙星残留的方法。
背景技术:
喹诺酮类药物(quinolone)是一类较新的广谱抗菌药,由于其抗菌力强、口服吸收好,与其他抗菌药物无交叉耐药性,已经成为治疗细菌感染性疾病的主要药物。喹诺酮类药物按其发明先后和抗菌性能的不同,分为一、二、三、四代,环丙沙星为第三代喹诺酮类药物,具有抗菌范围广、抗菌活性大、组织穿透力强等特点,在畜禽产品生产中被广泛应用。但是该类药物存在严重持久性的不良反应,包括肌腱损伤、中枢神经系统紊乱等,也可致癌、致突变、产生过敏反应,长期食用环丙沙星残留的畜禽产品必定会给人体健康造成严重伤害。因此,实现畜禽产品中环丙沙星的快速灵敏检测在保证食品安全方面具有积极意义。
目前,兽药残留的检测通常是以宰杀后动物的组织如肌肉、肝脏等或动物的粪便为样本,但肌肉或肝脏中蛋白质及脂肪的含量较高,粪便中含有大量的金属离子及其它杂质,影响目标物的提取,进而会导致检测结果的可靠性和稳定性较低,另外,为减少基质效应对色谱分析造成干扰,一般需对提取物进行提纯处理,操作比较复杂,增加了前处理的工作量。
技术实现要素:
因此,本发明旨在提供一种可活体取样的畜禽体内环丙沙星残留的检测方法,该方法操作简单、快速灵敏且检测结果的可靠性和稳定性高。
为此,本发明提供了一种检测畜禽体内环丙沙星残留的方法,包括样品的预处理和hplc分析,所述样品的预处理包括如下步骤:
取洁净干燥的畜禽毛发,加入提取液,于不低于65℃下至少提取24h,取上清液,去除上清液中有机物,得待测样品;
所述提取液为三氟乙酸酸化甲醇,所述三氟乙酸在甲醇中浓度为0.2mol/l。
进一步地,所述待测样品的制备是在绝氧或限氧环境下进行。
更进一步地,所述去除上清液中有机物是在35~45℃下进行吹氮处理。
进一步地,向所述畜禽毛发中加入提取液前还包括如下步骤:
取畜禽脖颈区域的毛发,用纯水洗涤至少3次,剪成4~6mm小段,于40~60℃下烘干,密封待用。
进一步地,所述hplc分析的色谱条件为:
色谱柱:c18250mm×4.6nm,填充剂为十八烷基硅烷键合硅胶,粒径为5μm;
流动相:乙腈-0.05mol/l磷酸溶液(v:v=15:85);
流速:0.8ml/min;
进样量:10μl;
柱温:30℃;
检测器:荧光检测器,激发波长为280nm,发射波长为450nm。
进一步地,进行所述hplc分析前还包括环丙沙星标准溶液及待测样品溶液的配制,具体包括如下步骤:
取环丙沙星标准品,加入所述流动相稀释成至少3种不同浓度的环丙沙星标准溶液;
取所述待测样品,加入所述流动相,充分溶解所述待测样品,即得所述待测样品溶液。
进一步地,所述hplc分析包括如下步骤:
吸取不同浓度的所述环丙沙星标准溶液10μl注入hplc分析仪,根据测定结果绘制环丙沙星峰面积-溶液浓度的标准曲线图;
吸取所述待测样品溶液10μl注入hplc分析仪,根据峰面积及所述标准曲线图,计算得到所述待测样品溶液中环丙沙星的含量。
本发明的技术方案,具有如下优点:
1.本发明提供的检测畜禽体内环丙沙星残留的方法,以畜禽毛发为样品,取样方便,无任何破坏性,不会引起动物的任何伤害和疼痛,易于贮存,与以宰杀后动物的组织或动物的粪便为样本相比,本发明以畜禽毛发为样品的基质干扰影响小,并无需进一步提纯,操作简单,缩短了检测周期,降低了前期处理的工作量和投入成本;选用酸化甲醇作为提取液,一方面提高了提取效率,另一方面,还可以沉淀畜禽毛发中的钙质,降低基质干扰,有效提高检测结果的准确性。
2.本发明提供的检测畜禽体内环丙沙星残留的方法,在绝氧或限氧环境下制备所述待测样品,提高了样品的稳定性,有效避免样品变质或被污染的可能性。
3.本发明提供的检测畜禽体内环丙沙星残留的方法,选用畜禽脖颈区域的毛发为取样对象,环丙沙星的累积量较高,并且高度稳定,具有更长的检测时间窗口,提高了检测结果的可靠性和稳定性。对畜禽毛发进行清洗,有效去除脂质和其它外源性干扰,进一步提高了检测结果的准确性。
4.本发明提供的检测畜禽体内环丙沙星残留的方法,通过对流动相及各组分配比、流速、温度等条件进行优化组合,可准确检测畜禽毛发中环丙沙星的残余量,该方法具有操作简单及准确性高等特点,适用于畜禽体内环丙沙星残留的定量分析。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
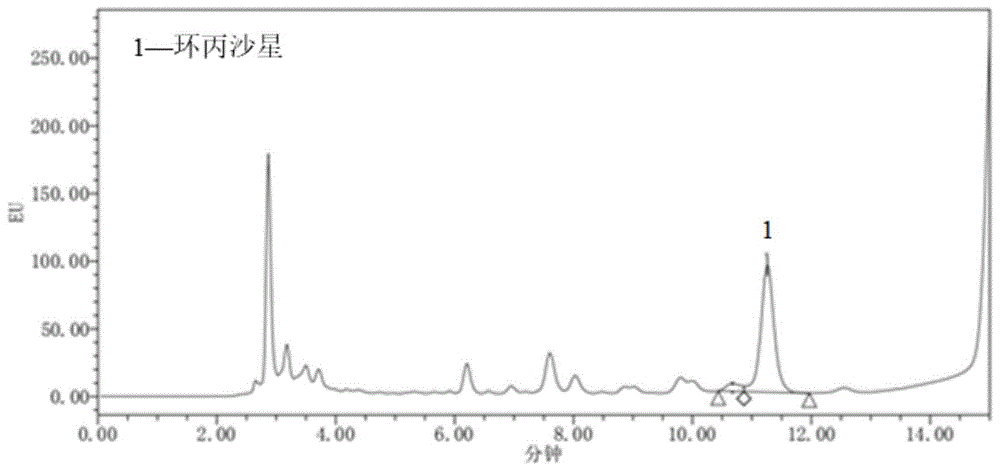
图1是本发明实施例1中待测样品溶液的hplc色谱图;
图2是本发明实施例1中加标样品溶液(加标浓度为5μg/ml)的hplc色谱图。
具体实施方式
提供下述实施例是为了更好地进一步理解本发明,并不局限于所述最佳实施方式,不对本发明的内容和保护范围构成限制,任何人在本发明的启示下或是将本发明与其他现有技术的特征进行组合而得出的任何与本发明相同或相近似的产品,均落在本发明的保护范围之内。
实施例中未注明具体实验步骤或条件者,按照本领域内的文献所描述的常规实验步骤的操作或条件即可进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规试剂产品。
实施例1
本实施例提供了一种检测畜禽体内环丙沙星残留的方法,包括如下步骤:
(1)取鸡脖颈区域的毛发,用纯水洗涤3次,剪成4~6mm的小段,在50℃下烘干,装入自封袋中并置于干燥皿中待用。
(2)称取0.15g上述处理过的鸡毛,置于螺旋玻璃厌氧管中,加入10ml三氟乙酸酸化甲醇(三氟乙酸的浓度为0.2mol/l),加热至70℃提取24h,取上清液5ml,40℃氮气条件下吹干,得待测样品。
(3)配制环丙沙星标准溶液、待测样品溶液及加标样品溶液
称取环丙沙星标准品5.0mg,置于5ml容量瓶内,用流动相(乙腈-0.05mol/l磷酸,v:v=15:85)溶解并定容至刻度线,摇匀得1mg/ml环比沙星储备液。准确吸取上述环丙沙星储备液1ml于10ml容量瓶中,用流动相(乙腈-0.05mol/l磷酸,v:v=15:85)溶解并稀释至刻度线,稀释成浓度为100μg/ml的工作液,再按照上述方法进行稀释,得到浓度为0.05μg/ml、0.1μg/ml、0.5μg/ml、1.0μg/ml、5.0μg/l、10μg/ml及50μg/ml的标准溶液,0℃下避光保存备用;
向上述待测样品中加入1ml流动相(乙腈-0.05mol/l磷酸,v:v=15:85),充分溶解,即得所述待测样品溶液;
称取0.15g步骤(1)中处理过的鸡毛,加入0.1ml5μg/ml标准溶液,静置2h,加入10ml三氟乙酸酸化甲醇(三氟乙酸的浓度为0.2mol/l),加热至65℃提取24h,取上清液5ml,40℃氮气条件下吹干,得加标待测样品,加入1ml流动相(乙腈-0.05mol/l磷酸,v:v=15:85),即得所述加标样品溶液。
(4)hplc分析
色谱分析条件:色谱柱:c18250mm×4.6nm,填充剂为十八烷基硅烷键合硅胶为,粒径为5μm;流动相:乙腈-0.05mol/l磷酸溶液(v:v=15:85);流速:0.8ml/min;进样量:10μl;柱温:30℃;检测器:荧光检测器,激发波长为280nm,发射波长为450nm。
分别吸取0.05μg/ml、0.1μg/ml、0.5μg/ml、1.0μg/ml、5.0μg/l、10μg/ml、50μg/ml及100μg/ml的环丙沙星标准溶液10μl,注入hplc分析仪,根据测定结果绘制环丙沙星峰面积-溶液浓度的标准曲线图,拟合,求回归方程和相关系数。结果表明,在0.05~100μg/ml浓度范围内,线性关系良好,相关系数均在0.999以上。
吸取待测样品溶液10μl,注入hplc分析仪,分析图谱见图1,根据环丙沙星峰面积和上述标准曲线图,得到待测样品溶液中环丙沙星的浓度,计算得到鸡毛中环丙沙星的残余量,见下表1。
吸取加标样品溶液10μl,注入hplc分析仪,分析图谱见图2,根据环丙沙星峰面积和上述标准曲线图,得到加标样品溶液中环丙沙星的浓度,计算得到加标回收率,见下表1。
表1环丙沙星残余量及加标回收率
(备注:1为待测样品溶液;2为加标样品溶液)。
由上表中的数据可知,本发明的检测方法具有良好的准确性。
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
- 还没有人留言评论。精彩留言会获得点赞!