一种基于液质联用定量多种肠道菌群有机酸的方法与流程
本申请涉及分析化学领域,尤其但不限于涉及一种基于效液相色谱/三重四级杆质谱定量肠道菌群有机酸的方法。
背景技术:
有机酸是指一些具有酸性的有机化合物。最常见的有机酸是羧酸,它是一类参与生物体生命活动的重要物质,如参与三羧酸循环,维持机体供能等;许多疾病的发生发展都与有机酸代谢失调有关,如心血管疾病、阿尔茨海默病、糖尿病等;而短链脂肪酸是肠道菌群发酵多糖产生的主要产物,具有调节菌群平衡,以及抗肿瘤、抗炎和调控基因表达等作用;中链、长链脂肪酸除了作为膜脂外,还能调节能量代谢。近年来,肠道菌群与宿主相互作用是生命学科新的研究热点,肠道菌群对宿主的直接或间接生理影响尚不清楚。因此,为了更好地研究肠道微生物与宿主之间的相互作用,建立一种能同时检测多种有机酸的高灵敏度的分析方法是迫在眉睫的。此外,一些有机酸如乙酸、棕榈酸等通常会出现强烈的背景干扰,导致定量结果的不准确。评价这些背景污染,实现准确定量的工作必不可少。
目前已有许多方法用于测定有机酸的含量,包括气相色谱、毛细管电泳、高效液相色谱等,对于非挥发性有机酸和中长链脂肪酸,气相色谱-质谱(gaschromatography-massspectrometry,gc-ms)分析通常需要甲酯化等衍生化来增加其挥发性而被检测,但gc-ms的重现性和复杂基质解析能力使得该技术受到了一定的限制。随着分析技术的快速发展,液质联用技术因其选择性强、灵敏度高、样品前处理简单等优势,成为主流技术。
技术实现要素:
以下是对本文详细描述的主题的概述。本概述并非是为了限制权利要求的保护范围。
本申请基于高灵敏度的三重四级杆质谱仪的选择反应监测(selectedreactionmonitoring,srm)模式进行数据检测,除常见高丰度有机酸外,可以涵盖更多低含量且重要的有机酸。但脂肪酸类代谢物因缺乏特征碎片离子使此方法受限。为解决脂肪酸类代谢物缺乏特征碎片离子的问题,未衍生化的样品中挥发的有机酸在液质联用上检测不到,脂肪酸类的有机酸没有特征碎片,也难于被检测。
基于以上问题,本申请引入3-硝基苯基肼(3-nitrophenylhydrazine,3-nph)或2-硝基苯肼的衍生化反应,对羧基进行衍生化,来改善其二级质谱行为并提高仪器检测的灵敏度。本申请提供了一种基于3-nph或2-nph的衍生化反应,涵盖多达42种挥发性或非挥发性的有机酸的定量;本申请的定量方法是基于高灵敏度的三重四级杆质谱仪;无放射性的6个碳13稳定同位素标记13c6-3nph衍生化试剂的引入,使每个标准品都有相应的内标,这样即保证了定量的准确性,又节省了实验成本;加入空白反应,扣除背景干扰,使得数据的可靠性得以保证。
具体地,本申请提供了一种基于液质联用对多种肠道菌群有机酸进行定量的方法,所述方法包括:
样品的制备,将所述样品进行预处理,然后用衍生化试剂进行衍生化;
空白样品的制备;
液质联用检测所述样品和所述空白样品;
样品的定量分析。
在本申请中,所述样品可以为新鲜肠道内容物、粪便、组织或血液。
在本申请中,样品的提取可以包括:用乙腈提取样品。
在本申请中,所述衍生化可以包括:
将所述样品和乙腈的混合物离心,取上清液加入3-硝基苯肼、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc·hcl)和吡啶溶液,在25℃-60℃下反应15min-30min,氮气保护下吹干备用。
在本申请中,当所述样品为新鲜肠道内容物、粪便或组织时,取10mg-100mg,或当所述样品为血液时,取10μl-100μl,加入0.1-1ml50%-70%乙腈(acn)水溶液进行匀质稀释,涡旋混匀1min-3min。将混合物于3000rpm-12000rpm室温10min-20min,取40μl-100μl上清,加入10μl-50μl200mm的3-nph的50%-70%乙腈水溶液,25μl120mm1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)溶液,其中溶剂为包含6%吡啶的50%-70%乙腈水溶液。在25℃-60℃下,反应15min-30min,在氮气保护下吹干备用。
在本申请中,所述空白样品的制备可以包括:
将乙腈、3-硝基苯肼、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐和吡啶溶液,在25℃-60℃下反应15min-30min,氮气保护下吹干备用。
在本申请中,所述空白样品的制备可以包括:取40μl-100μl50%-70%acn,加入10μl-50μl200mm的3-nph的50%-70%acn溶液,25μl120mm混有6%吡啶的1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)50%-70%乙腈水溶液。在25℃-60℃下,反应15min-30min,在氮气保护下吹干备用。
在本申请中,在所述液质联用检测中,液相色谱条件:色谱柱:acquityuplcbehc18;色谱柱温:35℃-55℃;进样量1μl-10μl;流速:0.2ml/min-0.3ml/min;流动相组成:a相为水,b相为乙腈;洗脱梯度:0-1min,2%b,1-34min,2-98%b,34-40min,98%b,40-45min,2%b,所述百分比为体积百分比。
质谱条件:利用三重四级杆质谱仪的选择反应监测模式进行检测,电喷雾电离,负离子模式扫描,喷雾电压:3000v;离子传输管温度:320℃;辅助气温度:300℃;鞘气流速:35arb;辅助气体流速:10arb;质量分析器q1和q2的分辨率:0.7fwhm;碰撞气体压力为1.5mtorr。
在本申请中,所述方法可以同时定量20-60种肠道菌群有机酸。
在本申请中,所述方法可以同时定量42种肠道菌群有机酸,所述有机酸包括以下中的任一种活更多种:甲酸、乙酸、丙酸、丁酸、异丁酸、戊酸、异戊酸、己酸、庚酸、壬酸、癸酸、十一烷酸、十二烷酸、十三烷酸、十四烷酸、十五烷酸、十六烷酸、十六碳一烯酸、十七烷酸、十八烷酸、十八碳一烯酸、十八碳二烯酸、十八碳三烯酸、十九烷酸、二十碳四烯酸、二十碳五烯酸、二十二碳六烯酸、二十四烷酸、二十四碳一烯酸、乙酰乙酸、β-羟丁酸、柠檬酸、乌头酸、异柠檬酸、α-酮戊二酸、延胡索酸、琥珀酸、苹果酸、草酰乙酸、丙酮酸、乳酸。
在本申请中,样品的定量计算包括:
以所述衍生化后的标准品的特征离子峰的峰面积与相对应的内标峰面积的比值为纵坐标,浓度为横坐标,绘制内标法的标准曲线,
将所述样品中的各个化合物的峰面积比值先扣除空白反应,再带入所述标准曲线,得到所述样品中有机酸的含量。
在本申请的某些实施方案中,可以首先进行定性分析:通过tracefinder软件提取样品的色谱峰和保留时间,与衍生化后的标准品出峰时间对比进行定性分析,并对所检测的化合物进行色谱峰的积分。然后,再进行定量分析:以衍生化后的标准品的特征离子峰的峰面积与相对应的内标峰面积的比值为纵坐标,浓度为横坐标,绘制内标法的标准曲线。将样品中的各个化合物的峰面积比值先扣除空白反应,再带入标准曲线,得到被测样本中有机酸的绝对含量。
在本申请中,所述定量分析还包括标准品母液配制:分别取上述有机酸的标准品,初始浓度为50mm,来配制有机酸的混合标准溶液,混合母液终浓度分别为200μm,用50%-70%acn依次稀释如下浓度点:100μm、50μm、25μm、10μm、5μm、2.5μm、1μm、500nm、250nm、100nm、50nm、25nm、10nm、5nm、2.5nm、1nm、0.5nm、0.25nm、0.1nm,取40μl-100μl标准液备用。
在本申请的某些实施方案中,对样品和标准品进行衍生化反应:取样品的乙腈溶液和标准品的乙腈溶液,分别加入10μl-50μl200mm的3-nph的50%-70%acn溶液,25μl120mm1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)溶液,其中溶剂为包含6%吡啶的50%-70%乙腈水溶液。在25℃-60℃下,反应15min-30min,在氮气保护下吹干备用。
在本申请中,内标衍生化反应:取有机酸混合好的标准溶液,加入10μl-50μl200mm的13c6-3nph的50%-70%acn溶液,再加入25μl120mm混有6%吡啶的1-(3-二甲氨基丙基)-3-乙基碳二亚胺溶液(edc)。在25℃-60℃下,反应15min-30min,用70%acn稀释10倍备用。
液相色谱分离:利用超高效液相色谱(ultrahighperformanceliquidchromatography,uplc)系统和反向色谱分析柱进行色谱分离,液相色谱条件包括:色谱柱:acquityuplcbehc18,色谱柱温:35℃-55℃;进样量1μl-10μl;流速:0.2ml/min-0.3ml/min;流动相组成:a相为水,b相为乙腈,质谱检测:利用高灵敏度的三重四级杆质谱仪中选择反应监测模式进行检测,电喷雾电离,负离子模式扫描,喷雾电压:3000v;离子传输管温度:320℃;辅助气温度:300℃;鞘气流速:35arb;辅助气体流速:10arb;质量分析器q1和q2的分辨率:0.7fwhm;碰撞气体压力为1.5mtorr。
数据分析:利用tracefinder定性定量分析软件提取标品、内标、空白反应和样品中所采集到的有机酸的色谱保留时间、母离子及其特征子离子信息,并对得到的色谱峰面积进行积分。通过标准品的保留时间对代谢物进行定性,代入标准曲线对代谢物进行定量分析。
由于上述技术方案的采用,与现有技术相比,本发明具有以下优势:
1.本申请的定量方法涵盖了更多的肠道菌群相关的有机酸,可以进一步研究肠道微生物与宿主之间的相互作用。
2.本申请的定量方法基于高灵敏度的三重四级杆质谱仪,可以最大程度的满足复杂样本中有机酸的检测。
3.碳13稳定同位素标记的13c6-3nph衍生化试剂的引入,可以使每个标准品都有相应的内标,保证定量的准确性,节省了实验成本。
4.加入空白反应,来扣除背景中有机酸的干扰,使得数据的可靠性得以保证。
本申请的其它特征和优点将在随后的说明书中阐述,并且,部分地从说明书中变得显而易见,或者通过实施本申请而了解。本申请的目的和其他优点可通过在说明书、权利要求书以及附图中所特别指出的结构来实现和获得。
附图说明
附图用来提供对本申请技术方案的进一步理解,并且构成说明书的一部分,与本申请的实施例一起用于解释本申请的技术方案,并不构成对本申请技术方案的限制。
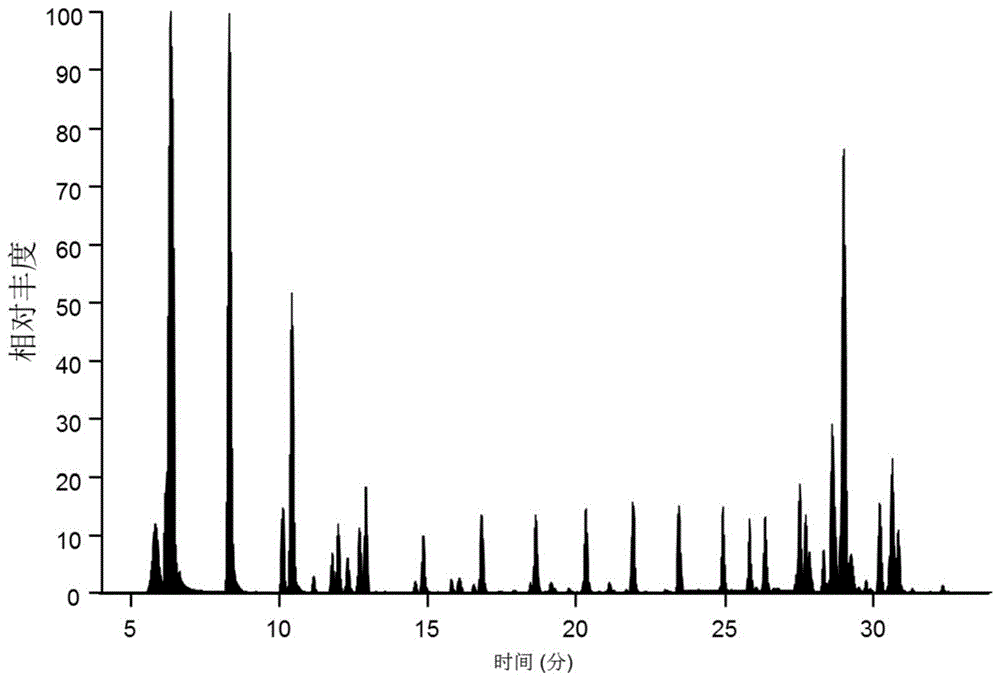
图1为小鼠粪便样本中42种有机酸和内标的总离子流色谱图。
图2为小鼠粪便样本中检测到的有机酸含量。
图3图为小鼠肝脏样本中检测到的有机酸含量。
具体实施方式
为使本申请的目的、技术方案和优点更加清楚明白,下文中将结合附图对本申请的实施例进行详细说明。需要说明的是,在不冲突的情况下,本申请中的实施例及实施例中的特征可以相互任意组合。
实施例1:测定小鼠粪便样本中有机酸的含量
1)样本前处理:收集小鼠新鲜粪便样品,称取86mg粪便,加入860μl50%acn,将样本匀浆后,经12000rpm离心15min后取30μl上清液,加入25ul200mm的3-nph,25μl120mmedc(含6%吡啶)乙腈水溶液,在40℃下,反应30min,加入等体积的内标,在氮气保护下吹干,待分析;液质联用分析:
2)液相条件:acquityuplcbehc18色谱柱(2.1*100mm,1.7μm);柱温:40℃;流速:0.25ml/min;流动相:a为100%水,b为100%乙腈。洗脱梯度:0-1min,2%b,1-34min,2-98%b,34-40min,98%b,40-45min,2%b。进样量1μl。
质谱条件:加热电喷雾离子源(heatingelectrosprayionsource,hesi),离子传输管温度320℃;辅助气温度300℃;鞘气:35arb;辅助气:10arb;负离子检测模式喷雾电压:3.5kv;扫描模式:选择反应监测模式;质量分析器q1和q2的分辨率为0.7fwhm;碰撞气为氩气,碰撞气压力为1.5mtorr。质谱测定母离子、子离子和碰撞能量的信息见表1。
表1监测的离子对信息
3)方法的准确度和精密度:同步骤1)和2)的衍生化反应和上机检测,制备三个高中低浓度的42个标准品的混合液作为质控样本(n=3),比较方法的准确度和精密度,具体结果见表2。
表2本申请的方法的准确度和精密度
4)定性和定量分析:首先,通过tracefinder软件提取样品中的色谱峰和保留时间,与42种衍生化后的标准品出峰时间对比来进行定性分析,并对所检测的化合物进行色谱峰的积分。其次,以衍生化后的标准品的特征离子峰的峰面积与相应的内标的峰面积的比值为纵坐标,浓度为横坐标,绘制标准曲线。最后,将样品中的各个化合物的峰面积比值扣除空白反应,带入标准曲线,得到小鼠粪便样本中有机酸的绝对含量。图1为定量小鼠粪便样本中有机酸的总离子流图。图2为小鼠粪便样本中检测到的有机酸含量。
实施例2:测定小鼠肝脏样本中有机酸的含量
称取小鼠新鲜肝脏样本50mg,加入500μl70%acn,将样本匀浆后,经12000rpm离心15min后取30μl上清液,加入25μl200mm的3-nph,25μl120mmedc(含6%吡啶)溶液,在40℃下,反应30min,加入等体积的内标,在氮气保护下吹干,待分析;上机检测条件同实例1中的2),进样体积为5μl。数据分析过程同实例1中的4)。图3为小鼠肝脏样本中检测到的有机酸含量。
虽然本申请所揭露的实施方式如上,但所述的内容仅为便于理解本申请而采用的实施方式,并非用以限定本申请。任何本申请所属领域内的技术人员,在不脱离本申请所揭露的精神和范围的前提下,可以在实施的形式及细节上进行任何的修改与变化,但本申请的专利保护范围,仍须以所附的权利要求书所界定的范围为准。
- 还没有人留言评论。精彩留言会获得点赞!