一种荧光检测装置及荧光检测方法与流程
本发明属于生物电子技术领域,尤其涉及一种荧光检测装置及荧光检测方法。
背景技术:
生物实验中,荧光信号是非常重要的结果指示工具。从一端利用某波长的光激发液滴中的荧光分子,在另一端用接收器获得特定波长的荧光信号,借此判断实验结果是否符合预期。在传统的数字微流控平台上,一般是通过手动控制的方式在储液槽预加4-5次反应的反应液,实验中从储液槽用电极拽出单次的液体,然后采用光学信号检测系统对反应后的液体进行检测。
然而,传统的数字微流控平台通常采用不透光的金属电极驱动液滴,无法同时在垂直方向上对电极上的液滴中的荧光分子进行激发和采集荧光信号,极大的降低了荧光检测的效率。
技术实现要素:
本发明的目的在于提供一种荧光检测装置及荧光检测方法,旨在解决传统的数字微流控平台通常采用不透光的金属电极驱动液滴,无法同时在垂直方向上对电极上的液滴中的荧光分子进行激发和采集荧光信号,极大的降低了荧光检测的效率的问题。
本申请实施例提供了一种荧光检测装置,所述荧光检测装置包括:
激发光光源;
透明微流控芯片,用于将注入的多个样本液滴进行融合,得到对应的融合液滴,并将所述融合液滴驱动至光学信号检测区,其中,所述光学信号检测区设于激发光光源输出的激发光的光路上,所述融合液滴在所述激发光的作用下生成对应的荧光信号;
荧光接收器,用于接收所述荧光信号,并将所述荧光信号转换为对应的数据信号;以及
数据处理模块,与所述荧光接收器连接,所述数据处理模块用于基于所述数据信号以及预设处理条件输出对应的检测结果。
可选的,所述透明微流控芯片包括层叠设置的透明下极板和透明上极板,其中,所述透明下极板表面形成有电极层,所述透明上极板表面形成有储液槽,所述储液槽设于所述透明下极板和所述透明上极板之间;
所述电极层用于根据接收的驱动信号对所述储液槽中的样本液滴进行驱动。
可选的,所述荧光检测装置还包括:
蠕动泵系统,用于根据用户输入的指令对所述储液槽中的样本液滴的体积进行调节。
可选的,所述蠕动泵系统包括依序连接的蠕动泵、泵管以及抽吸针;
所述泵管用于存储预设体积的样本液滴;
所述蠕动泵根据用户输入的指令产生对应的气压,以通过所述抽吸针对所述储液槽中的样本液滴的体积进行调节。
可选的,所述荧光检测装置还包括:上位机、微控制器、继电器模块以及电源驱动模块;
所述上位机用于基于用户操作编辑加电顺序得到所述透明微流控芯片的控制参数;
所述微控制器用于将所述控制参数转换为对应的电平信号;
所述继电器模块用于当所述电平信号作用到控制端时被控端闭合,使得电源驱动模块、所述继电器模块的被控端、所述透明微流控芯片形成电回路;
所述电源驱动模块用于当所述继电器模块的被控端闭合时为所述透明微流控芯片提供驱动信号,以驱动所述透明微流控芯片上的液滴移动。
可选的,所述上位机还用于控制所述蠕动泵系统的工作电压以及电源开关状态。
本申请实施例还提供了一种荧光检测方法,所述荧光检测方法包括:
采用透明微流控芯片将注入的多个样本液滴进行融合,得到对应的融合液滴,并将所述融合液滴驱动至光学信号检测区;其中,所述光学信号检测区设于所述激发光光源输出的激发光的光路上,所述融合液滴在所述激发光的作用下生成对应的荧光信号;
通过荧光接收器接收所述荧光信号,并将所述荧光信号转换为对应的数据信号;
通过数据处理模块基于所述数据信号以及预设处理条件输出对应的检测结果。
可选的,所述荧光检测方法还包括:
通过蠕动泵系统根据用户输入的指令对透明微流控芯片上的储液槽内的样本液滴的体积进行调节。
可选的,所述荧光检测方法还包括:
通过上位机基于用户操作编辑加电顺序得到所述透明微流控芯片的控制参数;
通过微控制器将所述控制参数转换为对应的电平信号;
通过继电器模块在所述电平信号作用到控制端时被控端闭合,使得所述电源驱动模块、继电器模块的被控端、透明微流控芯片形成电回路;
通过电源驱动模块在所述继电器模块的被控端闭合时为所述透明微流控芯片提供驱动信号,以驱动所述透明微流控芯片上的液滴移动。
可选的,所述荧光检测方法还包括:
通过上位机对所述蠕动泵系统的工作电压以及电源开关状态进行调节。
本申请实施例提供了一种荧光检测装置及荧光检测方法,通过透明微流控芯片根据输入的驱动信号将注入的多个样本液滴进行融合,得到对应的融合液滴,并将所述融合液滴驱动至光学信号检测区,然后通过所述激发光光源向所述融合液滴输出激发光,得到对应的荧光信号,通过光电转换系统将荧光接收器接收的荧光信号转换为对应的数据信号,通过数据处理系统基于所述数据信号以及预设处理条件输出对应的检测结果,解决了传统的数字微流控平台无法同时在垂直方向上对电极上的液滴中的荧光分子进行激发和采集荧光信号的问题。
附图说明
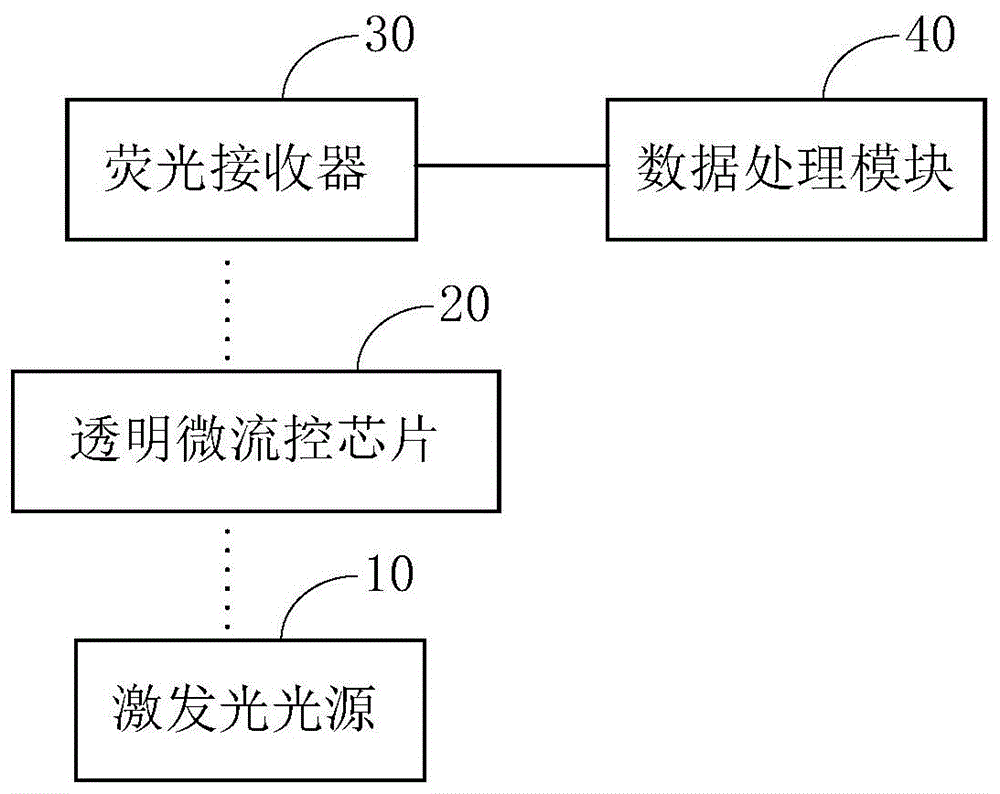
图1为本申请的一个实施例提供的荧光检测装置的结构示意图。
图2为本申请的一个实施例提供的荧光检测方法的流程示意图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
图1为本申请的一个实施例提供的荧光检测装置的结构示意图,参见图1所示,本申请实施例提供了一种荧光检测装置,所述荧光检测装置包括:
激发光光源10;
透明微流控芯片20,用于将注入的多个样本液滴进行融合,得到对应的融合液滴,并将所述融合液滴驱动至光学信号检测区,其中,所述光学信号检测区设于所述激发光光源10输出的激发光的光路上,所述融合液滴在所述激发光的作用下生成对应的荧光信号;
荧光接收器30,用于接收所述荧光信号,并将所述荧光信号转换为对应的数据信号;以及
数据处理模块40,与所述荧光接收器30连接,所述数据处理模块40用于基于所述数据信号以及预设处理条件输出对应的检测结果。
在本实施例中,通过将透明微流控芯片20设置于激发光光源10与荧光接收器30之间,并使得透明微流控芯片20上设置的光学信号检测区位于激发光光源10发射的激发光的光路上,从而使得透明微流控芯片20将融合液滴驱动至光学信号检测区后可以直接开启激发光光源10对融合液滴进行照射,并通过荧光接收器30接收融合液滴在激发光照射下受激发产生的荧光信号,并将该荧光信号转换为对应的数据信号,最后通过数据处理模块40基于所述数据信号以及预设处理条件输出对应的检测结果,该预设处理条件可以根据用户的检测需要设置,例如,在利用脂质体将有绿色荧光蛋白序列的质粒转入细胞的应用试验中,多个样本液滴包括包含细胞的液滴、包含含有质粒的脂质体的液滴和细胞培养基的液滴,将上述三种样本液滴分别通过透明微流控芯片20上设置的不同的进样孔注入,透明微流控芯片20根据接收的驱动信号将包含细胞的液滴、包含含有质粒的脂质体的液滴进行融合,得到对应的融合液滴,并将融合液滴移动到光学信号检测区,然后开启激发光光源10照射蓝紫色激发光,然后通过荧光接收器30接收融合液滴受激发生成的荧光信号,该预设处理条件为将该荧光信号转换得到的数据信号与绿色荧光信号进行比对,以判断绿色荧光蛋白是否在细胞中表达,从而进一步确定质粒是否成功转染到细胞中,即该预设处理条件可以为用户预先设置的对比荧光信号,从而将荧光接收器接收的荧光信号转换为对应的数据信号以与预设的对比荧光信号进行比对,以判断实验是否成功。
在一个实施例中,透明微流控芯片20还可以根据用户输入的驱动信号对融合液滴进行分离处理,从而从融合液滴中分离出预设的样本液滴,例如,透明微流控芯片20根据接收的驱动信号将包含细胞的液滴、包含含有质粒的脂质体的液滴进行融合,得到对应的第一融合液滴,待细胞贴壁后,可以不断将新鲜细胞培养基的液滴与第一融合液滴进行融合得到第二融合液滴,并同时从第二融合液滴中分离出一个体积相同的培养基液滴,从而保证细胞拥有新鲜的培养基,达成连续性培养的目的。
在一个实施例中,本实施例中的荧光检测装置还可以包括温控系统,该温控系统用于对透明微流控芯片20的环境温度进行调节,从而使得透明微流控芯片20可以同时完成细菌的连续培养过程以及检测过程,通过设置数据处理模块40中的预设处理条件可以完成对细菌液滴的多样性检测,例如,通过将细菌液滴驱动至光学信号检测区可以直接对培养细菌的液滴进行吸光度检测,以判断细菌生成的密度,通过荧光简介判断细菌的生长情况或者基因表达水平,还可以通过细菌的吸光度检测待测细菌的耐药性,具体的,将含待测细菌的液滴和含不同药物的液滴从多个进样点注入,通过向透明微流控芯片20提供对应的驱动信号,以将每一个含药物的液滴都和一个含待测细菌的液滴充分混合后,将这些液滴移植不同的光学信号检测区,通过从一端的激发光光源10间隔性发射紫外光,另一端的荧光接收器30进行紫外光的接收,从而通过数据处理模块40计算待测细菌液滴的吸光度,从而推导出液滴中细菌的密度,进一步判断细菌对某种药物是否有抗性。相对于现有的人工实验相比,利用本实施例中的荧光检测装置可以将重复性强且大量的工作进行自动化控制,极大地解放实验人员的劳动力,也可以比人工更快地完成耐药性检测试验。此外,和市场上现存的可以自动化进行耐药性检测的仪器相比,本本实施例中的荧光检测装置的单次实验试剂使用量很低,并可以通过增加进样点来增加可同时检测的药物。
在一个实施例中,所述透明微流控芯片20包括层叠设置的透明下极板和透明上极板,其中,所述透明下极板表面形成有电极层,所述透明上极板表面形成有储液槽,所述储液槽设于所述透明下极板和所述透明上极板之间;
所述电极层用于根据接收的驱动信号对所述储液槽中的样本液滴进行驱动。
在本实施例中,透明微流控芯片20包括层叠设置的透明下极板和透明上极板,其中,电极层形成于下极板的上表面,电极层包括多个电极,用于接收驱动信号,每个电极均被介电材料和疏水材料覆盖,介电材料起到电气绝缘作用,并在电极通电时提供电润湿力和介电泳力驱动液滴移动。上极板由透明导电材料(例如,氧化铟锡玻璃或者fto玻璃)构成,上极板和下极板的表面均涂覆有超疏水材料,例如,特氟龙等。在不通电的情况下,电极表面无法润湿,通过给电极施加驱动电压,被通电的电极表面会发生电润湿,液滴在电极电润湿的作用下移动。
在本实施例中,透明微流控芯片20上的液滴大小可以通过设置电极个数进行调整,也就是说,可以为多个相邻的电极同时施加驱动电压,使得它们驱动一个大液滴移动,也可以为单个电极施加驱动电压使其驱动一个小液滴移动。大液滴和小液滴的大小可控,大液滴可分离为小液滴,小液滴可混合成大液滴。
在一个实施例中,下极板的上表面的电极层可以通过湿法刻蚀的方式得到,首先在ito玻璃的ito镀层上用匀胶机匀一层正性光刻胶,对该正性光刻胶进行热固定,然后利用紫外曝光得到预设的电极图形,用显影液洗去多余光刻胶后,将ito玻璃至于蚀刻液中2-5分钟进行蚀刻。蚀刻结束后,采用去离子水将ito玻璃清洗干净,洗去残余的正胶,从而在下极板表面形成有预设电极图案的电极层。
在一个实施例中,上述实施例中ito玻璃可以替换为fto玻璃,ito镀层替换为fto玻璃表面的氟掺杂氧化锡镀层。
在一个实施例中,上机板上设置有多个储液槽,多个储液槽对应多个进样孔,用户可以根据需要通过进样孔对对应的储液槽中的液滴体积进行调节。
在一个实施例中,所述荧光检测装置还包括:
蠕动泵系统,用于根据用户输入的指令对所述储液槽中的样本液滴的体积进行调节。
在本实施例中,用户可以通过蠕动泵系统对透明微流控芯片20上设置的储液槽中的样本液滴的体积进行调节,例如,根据用户输入的指令控制蠕动泵系统的压力差,从而对样本液滴的体积进行精确控制,进一步的,还可以根据用户输入的指令对蠕动泵系统中的正负极进行设置从而调节蠕动泵的旋转方向,达到将储液槽中的多余的样本液滴抽回试剂管的目的,不仅节省了试剂成本,而且还避免了传统的气泵所需要的减压增压气体泵和阀,节省了液氮瓶的占用空间。
在一个实施例中,用户输入的指令还可以包括泵管切换指令,通过对蠕动泵系统中的不同内径的泵管进行切换,达到对泵管输出的样本液滴的流量进行调节的目的,在本实施例中,该泵管可以为硅胶管,通过利用硅胶管的耐高温、耐低温、耐油性以及良好的生理稳定性,可以避免蠕动泵系统在工作过程中由于泵管变形导致的误差。在一个实施例中,所述蠕动泵系统包括依序连接的蠕动泵、泵管以及抽吸针;
所述泵管用于存储预设体积的样本液滴;
所述蠕动泵根据用户输入的指令产生对应的气压,以通过所述抽吸针对所述储液槽中的样本液滴的体积进行调节。
在本实施例中,通过泵管进行样本液滴的储存,蠕动泵根据用户输入的指令进行旋转,从而产生对应的气压,以驱动抽吸针对储液槽中的样本液滴的体积进行调节,具体的,蠕动泵产生对应的气压对泵管中的空气柱进行抽吸,从而对泵管中的样本液滴的运动方向进行控制。
在一个实施例中,本实施例中的抽吸针与储液槽密封连接,可以避免荧光检测装置由于抖动产生的进样误差。
在一个实施例中,一个蠕动泵可以同时接入多根泵管,多根泵管分别与多个抽吸针一一对应,多个泵管中可以存储不同种类的样本液滴,用户可以根据需要将存储有所需样本液滴的泵管同时接入蠕动泵,通过开启蠕动泵可以实现多个样本液滴同时输入的效果,不仅节省了蠕动泵的个数,还可以同时注入多种所需的样本液滴,实现对样本液滴注入的精准控制,通过降低不同样本液滴注入的时差消除实验误差。
在一个实施例中,本实施例中的泵管可以包括多个内径不同的硅胶管,从而通过切换硅胶管实现对样本液滴的种类以及样本液滴的输出流量进行控制,达到对加样过程进行精准控制的目的,进一步的,硅胶管的尾部可以设置为半圆锥,有利于硅胶管与抽吸针之间的连接。在一个实施例中,所述蠕动泵系统还包括液滴存储器,蠕动泵的的一端从液滴存储器中吸入样本液滴,并将该样本液滴从另一端输出至泵管中,从而可以通过对液滴存储器进行加样,达到源源不断的为泵管提供样本液滴的目的,实现连续进行样本培养以及荧光检测的效果。
在本实施例中,蠕动泵的另一端采用泵管和抽吸针的结构,抽吸针可以垂直伸到芯片表面附近,通过蠕动泵加压让样本液滴打出,样本液滴打出后粘在液滴反应区的电极之外的储液槽,该储液槽可以为预设的储液槽电极,使得微升级别量级的液滴能够响应透明微流控芯片20产生的介电泳效应,具体的,由于透明微流控芯片20采用了超疏水结构,无法用类似枪头的方式加在芯片表面。通过开启储液槽电极会让储液槽表面变为亲水面,这样便可以成功的将抽吸针打出的微量样本液滴注入到透明微流控芯片20中。
在一个实施例中,本实施例中的抽吸针可以采用注射针头,该注射针头上具有半球结构的直径差,进一步的,本实施例中的蠕动泵系统还可以包括用于固定抽吸针的夹具结构,该夹具结构可以同时对多个抽吸针进行固定,从而避免抽吸针在注入样本液滴的过程中发生抖动而产生误差。
进一步的,本实施例中的夹具结构还可以用于多个固定泵管,避免泵管在蠕动泵工作时产生晃动导致样本液滴的注入产生误差。
在本实施例中,样本液滴由硅胶管流至注射针头,通过注射针头尖部的斜锥体使得样本液滴逐渐变大,然后涂在于注射针头接触的透明上极板上的储液槽,再通过透明微流控芯片驱动样本液滴进入透明微流控芯片的反应区,从而完成进样,进一步的,当用户需要抽出样本液滴时,透明微流控芯片驱动样本液滴进入储液槽,然后通过调节蠕动泵产生负压,从而将样本液滴输出至泵管中。
在一个实施例中,所述荧光检测装置还包括:上位机、微控制器、继电器模块以及电源驱动模块;
所述上位机用于基于用户操作编辑加电顺序得到所述透明微流控芯片20的控制参数;
所述微控制器用于将所述控制参数转换为对应的电平信号;
所述继电器模块用于当所述电平信号作用到控制端时被控端闭合,使得所述电源驱动模块、所述继电器模块的被控端、所述透明微流控芯片20形成电回路;
所述电源驱动模块用于当所述继电器模块的被控端闭合时为所述透明微流控芯片20提供驱动信号,以驱动所述透明微流控芯片20上的液滴移动。
在本实施例中,上位机、微控制器、继电器模块、电源驱动模块以及透明微流控芯片20形成数字微流控系统,具体的,继电器模块的被控端通过弹簧针与透明微流控芯片20上的多个电极均电连接,每个电极均包括电极序号,例如,透明微流控芯片20上电极的数目可以是92个、94个或96个。继电器模块包括多个继电器开关,每个继电器开关的控制端均与微控制器电连接,每个继电器开关的被控端均与电源驱动模块电连接且通过弹簧针与透明微流控芯片20上的一个电极电连接。上位机用于基于用户操作编辑加电顺序得到透明微流控芯片20的控制参数,并将控制参数发送至微控制器,其中,该控制参数可以包括目标电极序号、单步加电时间和单步间隔时间。因此,上位机还用于接基于用户操作编辑加电顺序得到目标电极序号、以及目标电极的单步加电时间和单步间隔时间,并发送至微控制器。
在本实施例中,上位机运行有用于液滴驱动的代码编译软件,该代码编译软件可以将基于用户操作编辑加电顺序得到的目标电极序号、单步加电时间和单步间隔时间进行编译,得到包含加电顺序、目标电极序号、单步加电时间和单步间隔时间的代码并以txt文件形式存储。在上位机运行时,上位机调用该存储有代码的txt文件,按照代码中的加电顺序、目标电极序号、单步加电时间和单步间隔时间,实现继电器模块中继电器开关的关闭顺序及间隔,从而向透明微流控芯片20发送对应的驱动信号。
在一个实施例中,上位机还用于对激发光光源10、荧光接收器30以及数据处理模块40组成的光学检测系统进行控制,从而实现光学检测系统与透明微流控芯片20同时上电,并在透明微流控芯片20驱动融合液滴至光学信号检测区时同时开启激发光光源10,避免因为检测延时产生的误差。
在一个实施例中,所述上位机还用于控制所述蠕动泵系统的工作电压以及电源开关状态。
在本实施例中,上位机还用于对蠕动泵系统进行控制,具体的,上位机可以通过对蠕动泵系统的工作电压以及电源开关状态进行调节,从而对蠕动泵系统的工作状态进行调节,例如,通过控制蠕动泵系统的电源开关状态控制蠕动泵系统是否启动,通过控制蠕动泵系统的工作电压以控制蠕动泵的转动速度,从而完成对样本液滴的流速进行控制,达到对储液槽中的样本液滴的体积进行调节的目的。
在一个实施例中,上位机可以是个人计算机,例如台式机或者笔记本电脑,同时,上位机上搭载有labview软件或者设置于fpga芯片中的exe程序文件。
在一个实施例中,上位机还可以部署有人机交互界面,人机交互界面提供了对透明微流控芯片20的自动化操作和状态监视功能,用户可以通过该人机交互界面选择目标电极,还可以通过该人机交互界面调用存储有代码的txt文件,将txt文件中的代码发送至微控制器,使得透明微流控芯片20按照代码中规定的加电顺序、目标电极序号、单步加电时间和单步间隔时间实现继电器模块中继电器开关的关闭顺序及间隔。另外,在透明微流控芯片20运行时,用户还可以通过人机交互界面实时监视各个电极的通断状态、通电时间和各个步骤的执行情况。
在一个实施例中,数字微流控系统还包括磁力模块,磁力模块与arduino通信连接,透明微流控芯片20设置于磁力模块的磁力位置处,磁力模块用于在arduino的无线遥控下将透明微流控芯片20上的磁珠与样本液滴进行分离和混合。磁珠由于其具有表面积大、化学性能稳定、表面已于修饰其他分子、易于在外加磁场中操控等优点,在生化分析(如免疫反应、核酸检测、蛋白富集)细胞分离等应用中有巨大的应用价值,在数字微流控系统中将液滴与磁珠进行结合,可以进一步提高反应的通量和缩短反应时间。例如通过化学修饰将抗体或者dna链接到磁珠上,目标分子或细胞就会与磁珠之间形成特定的相互作用。而在外加磁场也就是磁力模块的作用下,捕获的目标分子或细胞很容易被洗脱,之后用于下一步的反应或者分析。即通过磁力模块吸附磁珠并利用驱动电压驱动液滴,就能实现液滴与磁珠的分离,而在磁力模块不参与的情况下,仅利用驱动电压驱动液滴,就能实现液滴与磁珠的混合。
图2为本申请的一个实施例提供的荧光检测方法的流程示意图,参见图2所示,本实施例中的荧光检测方法包括:
步骤s10:采用透明微流控芯片20将注入的多个样本液滴进行融合,得到对应的融合液滴,并将所述融合液滴驱动至光学信号检测区;其中,所述光学信号检测区设于所述激发光光源10输出的激发光的光路上,所述融合液滴在所述激发光的作用下生成对应的荧光信号;
步骤s20:通过荧光接收器30接收所述荧光信号,并将所述荧光信号转换为对应的数据信号;
步骤s30:通过数据处理模块40基于所述数据信号以及预设处理条件输出对应的检测结果。
在本实施例中,通过将透明微流控芯片20设置于激发光光源10与荧光接收器30之间,并使得透明微流控芯片20上设置的光学信号检测区位于激发光光源10发射的激发光的光路上,从而使得透明微流控芯片20将融合液滴驱动至光学信号检测区后可以直接开启激发光光源10对融合液滴进行照射,并通过荧光接收器30接收融合液滴在激发光照射下受激发产生的荧光信号,并将该荧光信号转换为对应的数据信号,最后通过数据处理模块40基于所述数据信号以及预设处理条件输出对应的检测结果,该预设处理条件可以根据用户需要设置,例如,在利用脂质体将有绿色荧光蛋白序列的质粒转入细胞的应用试验中,多个样本液滴包括包含细胞的液滴、包含含有质粒的脂质体的液滴和细胞培养基的液滴,将上述三种样本液滴分别通过透明微流控芯片20上设置的不同的进样孔注入,透明微流控芯片20根据接收的驱动信号将包含细胞的液滴、包含含有质粒的脂质体的液滴进行融合,得到对应的融合液滴,并将融合液滴移动到光学信号检测区,然后开启激发光光源10照射蓝紫色激发光,然后通过荧光接收器30接收融合液滴受激发生成的荧光信号,该预设处理条件为将该荧光信号转换得到的数据信号与绿色荧光信号进行比对,以判断绿色荧光蛋白是否在细胞中表达,从而进一步确定质粒是否成功转染到细胞中。
在一个实施例中,透明微流控芯片20还可以根据用户输入的驱动信号对融合液滴进行分离处理,从而从融合液滴中分离出预设的样本液滴,例如,透明微流控芯片20根据接收的驱动信号将包含细胞的液滴、包含含有质粒的脂质体的液滴进行融合,得到对应的第一融合液滴,待细胞贴壁后,可以不断将新鲜细胞培养基的液滴与第一融合液滴进行融合得到第二融合液滴,并同时从第二融合液滴中分离出一个体积相同的培养基液滴,从而保证细胞拥有新鲜的培养基,达成连续性培养的目的。
在一个实施例中,所述荧光检测方法还包括:
步骤s11:通过蠕动泵系统储根据用户输入的指令对透明微流控芯片20上的储液槽内的样本液滴的体积进行调节。
在一个实施例中,所述荧光检测方法还包括:
步骤s12:通过上位机基于用户操作编辑加电顺序得到所述透明微流控芯片的控制参数;
步骤s13:通过微控制器将所述控制参数转换为对应的电平信号;
步骤s14:通过继电器模块在所述电平信号作用到控制端时被控端闭合,使得所述电源驱动模块、继电器模块的被控端、透明微流控芯片20形成电回路;
步骤s15:通过电源驱动模块在所述继电器模块的被控端闭合时为所述透明微流控芯片20提供驱动信号,以驱动所述透明微流控芯片20上的液滴移动。
在本实施例中,上位机、微控制器、继电器模块、电源驱动模块以及透明微流控芯片20形成数字微流控系统,具体的,继电器模块的被控端通过弹簧针与透明微流控芯片20上的多个电极均电连接,每个电极均包括电极序号,例如,透明微流控芯片20上电极的数目可以是92个、94个或96个。继电器模块包括多个继电器开关,每个继电器开关的控制端均与微控制器电连接,每个继电器开关的被控端均与电源驱动模块电连接且通过弹簧针与透明微流控芯片20上的一个电极电连接。上位机用于基于用户操作编辑加电顺序得到透明微流控芯片20的控制参数,并将控制参数发送至微控制器,其中,该控制参数可以包括目标电极序号、单步加电时间和单步间隔时间。因此,上位机还用于接基于用户操作编辑加电顺序得到目标电极序号、以及目标电极的单步加电时间和单步间隔时间,并发送至微控制器。
在一个实施例中,所述荧光检测方法还包括:
步骤s111:通过上位机对所述蠕动泵系统的工作电压以及电源开关状态进行调节。
在本实施例中,上位机可以通过对蠕动泵系统的工作电压以及电源开关状态进行调节,从而对蠕动泵系统的工作状态进行调节,例如,通过控制蠕动泵系统的电源开关状态控制蠕动泵系统是否启动,通过控制蠕动泵系统的工作电压以控制蠕动泵的转动速度,从而完成对样本液滴的流速进行控制,达到对储液槽中的样本液滴的体积进行调节的目的。
本申请实施例提供了一种荧光检测装置及荧光检测方法,通过透明微流控芯片20将注入的多个样本液滴进行融合,得到对应的融合液滴,并将所述融合液滴驱动至光学信号检测区,然后通过所述激发光光源10向所述融合液滴输出激发光,使得所述融合液滴在所述激发光的作用下生成对应的荧光信号,通过荧光接收器30接收所述荧光信号,并将所述荧光信号转换为对应的数据信号,通过数据处理系统基于所述数据信号以及预设处理条件输出对应的检测结果,解决了传统的数字微流控平台无法同时在垂直方向上对电极上的液滴中的荧光分子进行激发和采集荧光信号的问题。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!