三种血清蛋白联合用于强直性脊柱炎诊断的用途的制作方法
本发明属于疾病检测诊断领域,涉及生物标志物在疾病诊断方面的应用,具体涉及三种血清蛋白联合用于强直性脊柱炎诊断的用途。
背景技术:
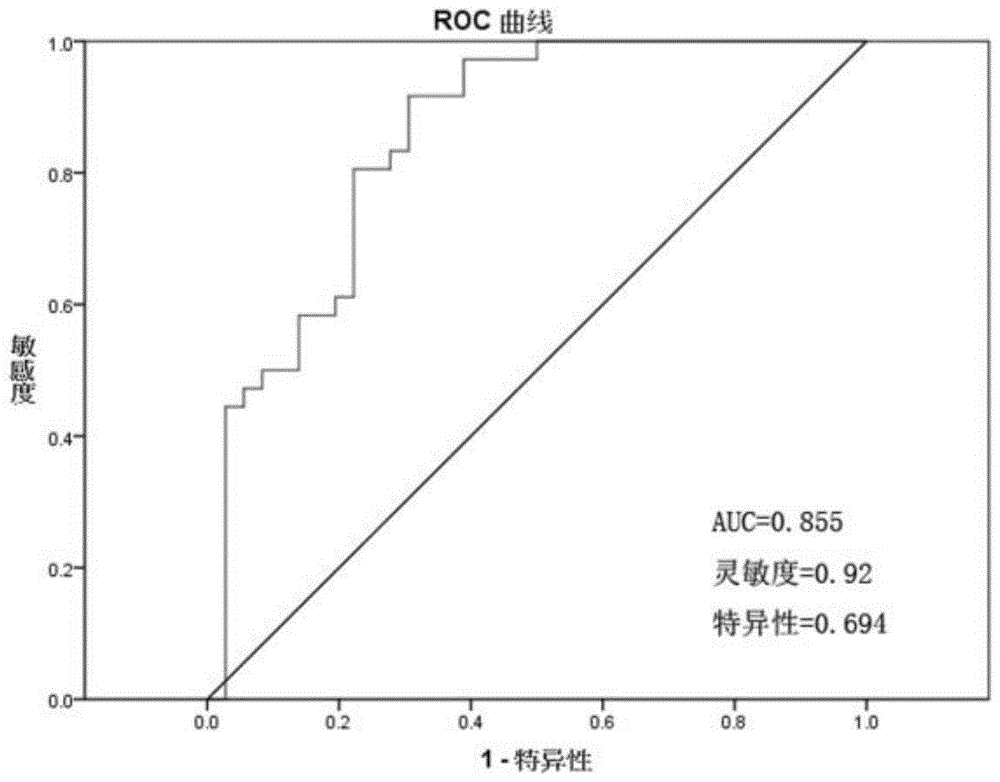
:强直性脊柱炎以骶髂关节和脊柱炎症为特征的一种全身性、慢性、炎性风湿性疾病,非常影响患者的身体功能和生活质量。据报道,中国汉族人群的患病率为0.2-0.45%,美国为0.2-0.5%。强直性脊柱炎的病因尚不清楚,但目前认为与免疫介导有关。它与人类白细胞抗原(hla)-b27、内肽酶-内质网氨基肽酶(erap1)、白细胞介素-23受体等有关。目前最有效的治疗药物为肿瘤坏死因子抑制剂。然而,病人确诊为强直性脊柱炎需要漫长的时间(平均时间为14年)。这种诊断的延误严重影响了病人的治疗与生活质量。因此,寻找到可诊断强直性脊柱炎的生物标志物非常有意义。c反应蛋白(crp)是属于戊聚糖家族的一种多肽分子,主要由肝脏通过激活转录因子stat3、c/ebp家族成员和nf-κb对某些促炎细胞因子(il-1β和il-6)反应而合成。它在先天性免疫中起着重要作用,因此被认为是各种疾病的一种众所周知的标志物,如炎性风湿病、感染、组织损伤和肿瘤。据报道,crp对强直性脊柱炎具有一定的诊断价值。血清淀粉样蛋白a1(saa1)是急性期蛋白之一,主要在肝脏中合成,以响应促炎刺激,主要由il-1和il-6型细胞因子的刺激。人类粘蛋白2(orm2)是由两个α-1-酸糖蛋白(agp)基因之一编码的急性期蛋白之一,主要通过糖皮质激素和细胞因子(il-1β、tnf-α和il-6)的活化在肝脏合成。目前尚未见saa1、orm2对强直性脊柱炎具有诊断价值的报道。虽然crp对强直性脊柱炎具有一定的诊断价值,但诊断准确度只能达到中等,有待提高。目前也不知道哪些标志物与crp联用可以提高其诊断强直性脊柱炎的准确度。技术实现要素:本发明的目的在于克服现有技术的不足,提供三种血清蛋白crp、saa1和orm2联合用于强直性脊柱炎诊断的用途。本发明上述目的通过如下技术方案实现:c反应蛋白、血清淀粉样蛋白a1和人类粘蛋白2联合用于制备诊断强直性脊柱炎的诊断试剂盒的用途。进一步地,所述诊断试剂盒中含有分别用于测定c反应蛋白、血清淀粉样蛋白a1和人类粘蛋白2含量的elisa试剂。有益效果:虽然crp对强直性脊柱炎具有一定的诊断价值,但诊断准确度只能达到中等,还有待提高。本发明发现,saa1和orm2与crp联合用于诊断强直性脊柱炎时,准确度比crp独立诊断强直性脊柱炎的准确度显著提高,高达96.3%,取得了出人意料的效果。因此,可以将crp、saa1和orm2联合用于制成诊断强直性脊柱炎的试剂盒,该试剂盒中包括用于测定crp、saa1和orm2含量的elisa试剂。附图说明图1为测试集中crp单独诊断强直性脊柱炎患者的roc曲线;图2为测试集中saa1单独诊断强直性脊柱炎患者的roc曲线;图3为测试集中orm2单独诊断强直性脊柱炎患者的roc曲线;图4为测试集中crp、saa1与orm2联合诊断强直性脊柱炎患者的roc曲线;图5为验证集中crp、saa1、orm2单独诊断强直性脊柱炎患者的样本分布图,其中a为crp单独诊断结果,b为saa1单独诊断结果,c为orm2单独诊断结果;图6为验证集中crp.、saa1与orm2联合诊断强直性脊柱炎患者的样本分布图。具体实施方式下面结合附图和实施例具体介绍本发明实质性内容,但并不以此限定本发明的保护范围。一、实验样本和试剂测试集样本:收集江苏省中医院,按照严格的筛选和排除标准经过年龄、性别和体重指数(bmi)匹配的36例健康受试者和36例强直性脊柱炎患者;验证集样本:收集南京鼓楼医院,按照严格的筛选和排除标准经过年龄、性别和体重指数(bmi)匹配的40例健康受试者和40例强直性脊柱炎患者。强直性脊柱炎患者与健康受试者的入组标准如下:强直性脊柱炎患者:根据1984年美国纽约修订标准符合放射学标准和l项以上临床标准,可诊断为强直性脊柱炎:1、临床标准:①腰痛、僵3个月以上,活动改善,休息无改善;②腰椎额状面和矢状面活动受限;③胸廓活动度低于相应年龄、性别的正常人;2、放射学标准(1966年as纽约标准):①0级:正常;②ⅰ级:可疑变化;③ⅱ级:轻度异常,可见局限性侵蚀、硬化,但无关节间隙的改变;④ⅲ级:明显异常,为中度或进展性骶髂关节炎,伴有以下1项或1项以上改变(侵蚀、硬化、关节间隙增宽或狭窄,或部分强直);⑤ⅳ级:严重异常,完全性关节强直;放射学标准为双侧骶髂关节炎≥2级或单侧骶髂关节炎3~4级。每名患者至少患有6个月强直性脊柱炎,未接受过任何形式的物理或医学治疗,无其他疾病。健康人受试者:无心血管、呼吸、肝脏、肾脏、胃肠道、内分泌、血液、精神、或神经系统疾病以及上述疾病病史,无急性或者慢性疾病。无药物过敏史,筛选时临床实验室检查结果在正常的参考范围内。主要实验试剂:saa1elisa试剂盒购买于杭州联科生物技术股份有限公司;crpelisa试剂盒购买于贝克曼库尔特公司;orm2elisa试剂盒购买于elabsciencebiotechnologyinc。二、实验方法1、血清样本的采集及储存采集患者清晨空腹外周血并将其置于不含抗凝剂的试管内,在室温下自然凝集30-60min,待血液凝固,以2000rpm速度离心10min,小心吸取上层清亮血清液体于无菌冻干管中,标记后放入-80℃冰箱储存备用。2、elisa测定血清中目标蛋白的含量严格按照elisa试剂盒流程操作测定血清中crp、saa1和orm2的含量。3、数据处理方法建立测试集中单个目标蛋白的roc曲线,计算曲线下面积(auc)及95%可信区间;对于多个目标蛋白,运用logistic回归建立回归方程,产生一组新变量logit[p],对该新变量进行roc曲线分析。验证集中,以roc曲线得到的最佳cut-off值为阈值计算单个目标蛋白或其联合对于强直性脊柱炎的诊断准确度。三、实验结果1、目标蛋白在强直性脊柱炎患者与健康受试者血清中的丰度差异在训练集中,与健康受试者比,强直性脊柱炎患者血清crp、saa1与orm2的绝对含量上调,测定结果如下表所示。组别crp含量(μg/ml)saa1含量(μg/ml)orm2含量(μg/ml)强直性脊柱炎患者19.28±37.382.42±1.830.016±0.003健康受试者2.71±1.500.66±0.420.014±0.0022、目标蛋白单独诊断区分强直性脊柱炎患者与健康受试者的roc曲线roc曲线评价法的原理:诊断试验的基本评价指标有敏感度、特异性等,综合评价指标有youden指数、roc、auc等。对于诊断试验的评价,首先需要通过金标准知道待测样本的真实组别。对于按金标准确定的疾病组(相当于本发明中的强直性脊柱炎组)和健康组,采用诊断试验检测的结果可以分为如下情况:阳性(truepositive,tp);诊断试验检测为阳性(与金标准结果一致);阴性(truenegative,tn);诊断试验检测为阴性(与金标准结果一致);假阳性(falsepositive,fp):诊断试验检测为阳性(与金标准结果不一致);假阴性(falsenegative,fn):诊断试验检测为阴性(与金标准结果不一致)。可以用下表表示:诊断试验的敏感度=a/(a+c);诊断试验的特异性=d/(b+d)。通过敏感度和特异性可以得出诊断试验相对于金标准的诊断灵敏程度和特异程度。敏感度高代表将疾病例诊断为阴性的个数少,漏诊率低;特异性高代表将健康例诊断为阳性的个数少,误诊率低。roc曲线正是基于上述敏感度和特异性绘制出的曲线。以诊断试验中可能的诊断界值作为诊断点,根据上述表格计算出相应的敏感度和特异性。然后,以敏感度为纵坐标,1-特异性为横坐标,将各诊断点时各点的敏感度和特异性点在坐标图中标出,连接坐标点得到平滑曲线,该曲线即为roc曲线。诊断点设置的越多越密,得到的roc曲线就越平滑。roc曲线是以每一个检测结果作为可能的诊断界值,其曲线下面积auc的大小表明了诊断试验准确度的大小。roc曲线下面积auc作为诊断试验真实性评价的固有准确度指标已被普遍认可,auc为0.5时,即无诊断意义;auc在0.5~0.7时,表示诊断准确率较低;auc在0.7~0.9时,表示诊断准确性中等;auc>0.9时,表示诊断有较高的准确性。crp、saa1、orm2单独诊断区分健康受试者和强直性脊柱炎患者的roc曲线结果如表1和图1-3所示。表1目标蛋白单独诊断区分健康受试者和强直性脊柱炎患者的roc曲线从roc曲线结果可以看出,crp、saa1与orm2单独对强直性脊柱炎患者和健康受试者仅具有中等的诊断区分能力,特异性都较低,进一步根据roc曲线的坐标计算维登指数=特异性+灵敏度-1,维登指数最大值时对应的蛋白含量为能进行诊断区分强直性脊柱炎患者vs健康受试者的最佳cut-off值,如表2所示。表2目标蛋白单独诊断区分健康受试者和强直性脊柱炎患者的最佳cut-off值目标蛋白强直性脊柱炎患者vs健康受试者crp0.443saa10.390orm20.3873、crp、saa1和orm2联合诊断区分强直性脊柱炎患者人与健康受试者的roc曲线以训练集样本中三个目标蛋白的含量作为自变量(设x1=crp绝对含量,x2=saa1绝对含量,x3=orm2绝对含量),以组别(即健康受试者和强直性脊柱炎患者)作为应变量,对三个目标蛋白在健康受试者和强直性脊柱炎患者血清样本中的含量进行二元逻辑回归,得到二元逻辑回归方程:logit[p]=10.502-0.665x1-1.092x2-451.569x3;再将各血清样本中三个目标蛋白的绝对含量代入该二元逻辑回归方程,即可得到各个血清样本的回归值logit[p],以可能的回归值logit[p]作为诊断点,计算灵敏度和特异性,据此绘制roc曲线(如图4所示),auc为0.922,具有较高的准确性。根据roc曲线的坐标计算维登指数=特异性+灵敏度-1,维登指数最大值时对应的logit[p]值为能进行诊断区分健康受试者vs强直性脊柱炎患者的最佳cut-off值0.395。4、验证目标蛋白单独诊断区分强直性脊柱炎患者与健康受试者的准确度在验证集中,以crp、saa1、orm2单独区分健康受试者与强直性脊柱炎患者的最佳cut-off值为诊断阈值对健康受试者和强直性脊柱炎患者的血清样本进行预测,以预测正确的样本数除以总样本数(40+40=80)即为该目标蛋白区分健康受试者vs强直性脊柱炎患者的准确度。crp诊断区分强直性脊柱炎患者与健康受试者的准确度为87.5%;saa1诊断区分强直性脊柱炎患者与健康受试者的准确度为78.8%;orm2诊断区分强直性脊柱炎患者与健康受试者的准确度为51.25%,样本分布图如图5所示。5、验证crp、saa1和orm2联合诊断区分强直性脊柱炎患者与健康受试者的准确度在验证集中,将健康受试者和强直性脊柱炎患者血清样本中crp、saa1、orm2绝对含量代入crp、saa1和orm2联合区分健康受试者vs强直性脊柱炎患者的二元逻辑回归方程,计算得到每个样本的回归值logit[p],以上述crp、saa1和orm2联合区分健康受试者vs强直性脊柱炎患者的最佳cut-off值为诊断阈值进行预测,以预测正确的样本数除以总样本数(40+40=80)即为crp、saa1和orm2联合区分健康受试者vs强直性脊柱炎患者的准确度,准确度为96.3%,样本分布图如图6所示。上述实验结果表明,saa1和orm2与crp联合用于诊断强直性脊柱炎时,准确度比crp独立诊断强直性脊柱炎的准确度显著提高,高达96.3%,取得了出人意料的效果。因此,可以将crp、saa1和orm2联合用于制成诊断强直性脊柱炎的试剂盒,该试剂盒中包括用于测定crp、saa1和orm2含量的elisa试剂。因此,可以将crp、saa1和orm2联合用于制成诊断强直性脊柱炎的试剂盒,该试剂盒中包括分别用于测定血清中crp、saa1和orm2含量的elisa试剂。上述实施例的作用在于具体介绍本发明的实质性内容,但本领域技术人员应当知道,不应将本发明的保护范围局限于该具体实施例。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1