巯基改性硅胶、制备方法和应用,以及检测水中烷基汞的方法与流程
本发明涉及有机金属污染领域,特别是涉及一种巯基改性硅胶、制备方法和应用,以及检测水中烷基汞的方法。
背景技术:
烷基汞,包括甲基汞、乙基汞,是一类剧毒并且有强致癌作用的有机金属化合物,此类化合物脂溶性强,易残留在自然水体中的生物体脂肪组织中,并在水体食物链中富集,进而对人类及生活在水生生态系统和湿地生态系统中的动物产生严重危害,是具有严重生物毒性的环境污染物。
烷基汞中甲基汞毒性最强,环境中任何形式的汞(金属汞、无机二价汞和烷基汞等)均可在一定条件下转化为有剧烈毒性的甲基汞,即汞的甲基化。汞的甲基化反应主要发生在水体中,并在食物链中富集,浓度逐渐增大。当人们饮用被汞污染的水和食用受汞污染的食物时,就会发生汞中毒事件。水体汞污染来源多为汞的开采冶炼、氯碱、化工、仪表、颜料等工业企业排出的废水及含汞农药的使用。水中胶体颗粒、悬浮物、泥土颗粒、浮游生物等能吸附汞,而后通过重力作用沉降进入底泥,底泥中的汞在微生物的作用下可转变为甲基汞或二甲基汞,甲基汞能溶于水,又可从底泥返回水中。因此,无论汞或甲基汞污染的水体均可造成危害。其中最为典型的例子就是日本熊本县水俣湾地区的居民因长期食用受甲基汞污染的鱼贝类而引起的慢性甲基汞中毒,即水俣病。日本所发生的水俣病,是一种中毒性神经疾病,是工业污染引起的有机汞中毒事件。
自20世纪70年代以来,由烷基汞引起的中毒事件频繁发生,烷基汞污染物引起了人们的高度重视,各国政府在制定本国的环境法律、法规和标准时,都将烷基汞类化合物放在首要地位加以考虑。我国国家环境保护总局发布的各类环保标准中也包括该类化合物,并将其作为目前环境监测的一项重要指标。测定和研究烷基汞的手段,对于减轻污染、保护生态环境有重要应用价值。
目前对于水中烷基汞的检测手段,主要是基于固相萃取-气相色谱法,常用的固相萃取吸附材料主要有活性炭、吸附树脂、改性硅胶等。
实际应用中,既可利用有机试剂改性活性炭,然后再吸附金属离子;也可将试液中的痕量待测金属离子转化为可被吸附的有机化合物,再用活性炭吸附,目前,有机试剂改性活性炭的应用比较多。虽然活性炭的比表面积大,吸附能力强,但是很难将目标物从吸附剂上完全洗脱下来,使得回收率有所降低。
吸附树脂,按其化学结构可以分为非极性、中极性和极性吸附树脂。非极性吸附树脂中电荷分布均匀不带任何功能基,主要是由苯乙烯和二乙烯苯聚合而成。中极性吸附树脂的分子结构中存在酯基等中等极性基团。极性吸附树脂也叫螯合树脂,其分子结构中含有酰胺基、亚砜基、腈基等极性较强的基团,极性基团含n、o、s等原子,能与目标金属离子进行选择性螯合作用。
改性硅胶,也称有机硅胶,含有si-c键、且至少有一个有机基团直接与硅原子相连。其中以硅氧键(-si-o-si-)为骨架的聚硅烷是应用最广的一类。与其它材料相比,有机硅胶具有耐高低温、耐氧化稳定性、耐候性、耐腐蚀、无毒无味等特点,应用广泛。巯基对铅、镉、铜、汞等金属元素都具有良好的螯合吸附作用,以巯基作为螯合基团的改性硅胶作为固相吸附材料用于烷基汞的吸附研究较为广泛。但是对于微含量的水体中的烷基汞,现有的巯基改性硅胶的吸附效果并不理想,吸附效率不高。
技术实现要素:
基于此,有必要提供一种巯基改性硅胶、制备方法和应用,以及检测水中烷基汞的方法。
本发明提供一种巯基改性硅胶,包括硅胶基体和形成在所述硅胶基体表面的树枝状修饰基团,所述修饰基团包括通式(ⅰ)所示的结构单元:
其中,m选自0-3的整数,n1、n2各自独立的选自2~3的整数,r1、r2各自独立的选自氢原子或碳原子数为1~2的烷基或取代烷基。
在其中一个实施例中,r1、r2均为氢原子。
在其中一个实施例中,n1、n2选自相同的整数。
在其中一个实施例中,所述硅胶基体为粒径在30目至100目的颗粒。
本发明还提供一种所述的巯基改性硅胶的制备方法,包括以下步骤:
将含有羟基的活化硅胶与化学通式为nh2(ch2)msix3的硅烷偶联剂发生键合反应,x为可水解的基团,得到包含第一修饰基团的第一改性硅胶,所述第一修饰基团的结构单元如通式(ⅱ)所示;
使所述第一改性硅胶中的所述第一修饰基团结构单元的氨基中的两个氢均与丙烯酸酯类化合物发生1,2-加成反应,得到包含第二修饰基团的第二改性硅胶,所述第二修饰基团的结构单元如通式(ⅲ)所示,其中r3、r4独立的选自碳原子数为1至3的烷基或取代烷基;
将所述第二改性硅胶与碳原子数为2~3的二胺类化合物发生酯的氨解反应,得到包含第三修饰基团的第三改性硅胶,所述二胺类化合物为包含两个伯胺的直链烷烃,所述第三修饰基团结构单元如通式(ⅳ)所示:
将所述第三改性硅胶与硫代苹果酸发生酰胺反应,得到所述的巯基改性硅胶。
在其中一个实施例中,所述活化硅胶和所述硅烷偶联剂的质量比为2:1至3:1;所述第一改性硅胶和所述丙烯酸酯类化合物的质量比为7:5至7:1;所述第二改性硅胶和所述二胺类化合物的质量比为1:1至3:1;所述第三改性硅胶和所述硫代苹果酸的质量比为3:1至5:1。
在其中一个实施例中,所述活化硅胶的制备方法为通过盐酸活化硅胶,所述盐酸的浓度为3mol/l至12mol/l,所述盐酸与所述硅胶的质量比为1:1至4:1。
本发明还提供一种所述的巯基改性硅胶在吸附烷基汞中的应用。
本发明进一步提高一种检测水中烷基汞的方法,包括以下步骤:
提供所述的巯基改性硅胶并将所述巯基改性硅胶填充于固相萃取小柱;
将待测水样通过所述固相萃取小柱进行过柱操作,使所述待测水样中的烷基汞吸附在所述固相萃取小柱上;
用洗脱液对所述吸附烷基汞的固相萃取小柱进行洗脱;
所述洗脱后的洗脱液用有机溶剂进行萃取;以及
所述萃取后的溶液通过气相色谱检测烷基汞浓度。
在其中一个实施例中,所述过柱操作中,所述待测水样的过柱流速为8ml/min~12ml/min。
在其中一个实施例中,所述洗脱液为相同体积的nacl和hcl的混合溶液,所述混合溶液中nacl浓度为2mol/l,hcl浓度为2mol/l。
在其中一个实施例中,所述洗脱液用量大于等于3ml。
本发明实施例提供的巯基改性硅胶,包括硅胶基体和形成在所述硅胶基体表面的树枝状修饰基团,修饰基团为具有分支的长分子链和巯基的结构单元,多个结构单元分布在硅胶表面形成树枝状分子结构,这种树枝状分子结构具有多个分支,且综合了基团的空间位阻效应和化学键合的影响设计而成,在待测水体中可起到类似于绒毛的效果,大大增加了所述巯基改性硅胶与待测水体的接触面积,提高了烷基汞的捕捉机率,有效提升了对待测水体中微量烷基汞的吸附率。该修饰基团中还含有大量的羰基、羧基、氨基,对烷基汞也有吸附作用,可更进一步增强对烷基汞的吸附。
附图说明
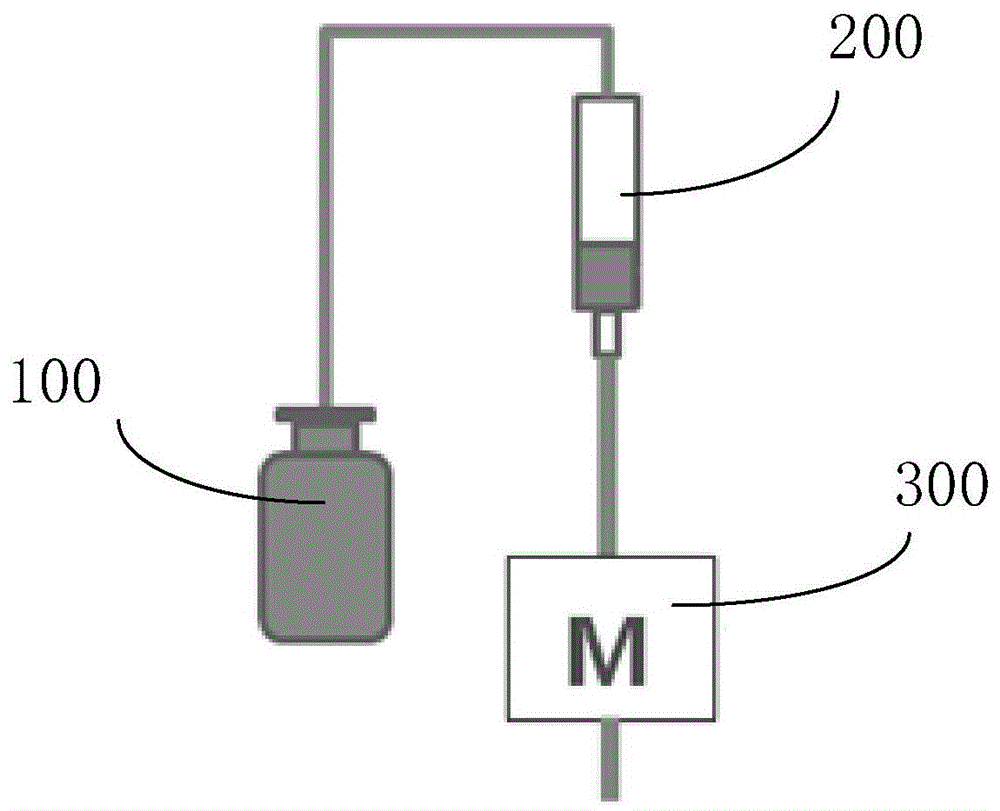
图1为本发明实施例的分离富集装置的结构示意图;
图2为本发明实施例又一分离富集装置的结构示意图;
图3为本发明实施例第一改性硅胶、巯基改性硅胶以及吸附烷基汞后的巯基改性硅胶的红外光谱图;
图4为本发明实施例不同过柱流速对烷基汞回收率的影响曲线图;
图5为本发明实施例不同洗脱液用量对烷基汞回收率的影响曲线图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下通过实施例,并结合附图,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。
本发明实施例提供一种巯基改性硅胶,包括硅胶基体和形成在所述硅胶基体表面的树枝状修饰基团,所述修饰基团包括通式(ⅰ)所示的结构单元:
其中,m选自0-3的整数,n1、n2各自独立的选自2~3的整数,r1、r2各自独立的选自氢原子或碳原子数为1~2的烷基或取代烷基。
本发明实施例提供的巯基改性硅胶,包括硅胶基体和形成在所述硅胶基体表面的树枝状修饰基团,修饰基团为具有分支的长分子链和巯基的结构单元,多个结构单元分布在硅胶表面形成树枝状分子结构,这种树枝状分子结构具有多个分支,且综合了基团的空间位阻效应和化学键合的影响设计而成,在待测水体中可起到类似于绒毛的效果,大大增加了所述巯基改性硅胶与待测水体的接触面积,提高了烷基汞的捕捉机率,有效提升了对待测水体中微量烷基汞的吸附率。该修饰基团中还含有大量的羰基、羧基、氨基,对烷基汞也有吸附作用,可更进一步增强对烷基汞的吸附。
由于空间位阻的影响,所述结构单元中长分子链上具有的支链越少越好,在一优选实施例中,r1、r2均为氢原子。
在一实施例中,n1、n2选自相同的整数,所述的巯基改性硅胶对待测水体中的烷基汞具有更好的吸附捕获能力。
所述硅胶基体为硅胶颗粒,在一实施例中,所述硅胶基体的粒径大小为30目至100目。
本发明实施例还提供一种所述的巯基改性硅胶的制备方法,包括以下步骤:
s10,将含有羟基的活化硅胶与化学通式为nh2(ch2)msix3的硅烷偶联剂发生键合反应,x为可水解的基团,得到包含第一修饰基团的第一改性硅胶,所述第一修饰基团的结构单元如通式(ⅱ)所示;
s20,使所述第一改性硅胶中的所述第一修饰基团结构单元的氨基中的两个氢与所述丙烯酸酯类化合物发生1,2-加成反应,得到包含第二修饰基团的第二改性硅胶,所述第二修饰基团的结构单元如通式(ⅲ)所示,其中r1、r2独立的选自碳原子数为1~2的烷基或取代烷基;
s30,将所述第二改性硅胶与碳原子数为2~3的二胺类化合物发生酯的氨解反应,得到包含第三修饰基团的第三改性硅胶,所述二胺类化合物为包含两个伯胺的直链烷烃,所述第三修饰基团结构单元如通式(ⅳ)所示:
s40,将所述第三改性硅胶与硫代苹果酸发生酰胺反应,得到所述的巯基改性硅胶。
在步骤s10中,所述含有羟基的活化硅胶可通过盐酸活化硅胶得到,所述盐酸的浓度为3mol/l至12mol/l,所述盐酸与所述硅胶的质量比为1:1至4:1。
所述化学通式为nh2(ch2)msix3的硅烷偶联剂中x可以为氯基、甲氧基、乙氧基、甲氧基乙氧基、乙酰氧基等,优选的,所述硅烷偶联剂为γ-氨丙基三乙氧基硅烷、γ-氨丙基三甲氧基硅烷、乙烯基三乙氧基硅烷、乙烯基三甲氧基硅烷、乙烯基三(β-甲氧乙氧基)硅烷中的一种或多种;活化硅胶和所述硅烷偶联剂的质量比为1:1至5:1,优选为2:1至3:1。通过所述硅烷偶联剂,在硅胶上接枝了端基为氨基的分子链。
所述活性硅胶和所述硅烷偶联剂反应的溶剂不限,优选为甲苯,反应温度为60℃至80℃,反应时间为6小时至12小时,所述活性硅胶和所述硅烷偶联剂反应后的产物为第一产物,可选用甲苯和乙醇依次对所述第一产物进行洗涤,洗涤后的所述第一产物优选在40℃至60℃真空干燥,干燥时间可以为4小时至8小时,干燥后即可得到所述第一改性硅胶。
步骤s20中,所述丙烯酸酯类化合物为烯基和酯基相连接的化合物,优选的,所述酯基碳原子数为1~3。所述丙烯酸酯类化合物可以为丙烯酸甲酯、丙烯酸乙酯、甲基丙烯酸甲酯、甲基丙烯酸乙酯。在一实施例中,所述丙烯酸酯类化合物优选为丙烯酸甲酯。所述第一改性硅胶包含的第一修饰基团结构单元(如通式(ⅱ)所示)中氨基可与所述丙烯酸酯类化合物发生1,2-加成反应,并且所述氨基中的两个氢均与所述丙烯酸酯类化合物发生1,2-加成反应,其分子链在原有的主链上分支出两条分子链,且分子链的端基为酯基。所述第一改性硅胶与所述丙烯酸酯类化合物的质量比为7:5至7:1。
所述第一改性硅胶和所述丙烯酸酯类化合物反应的溶剂不限,优选为甲醇,反应温度为40℃至60℃,反应时间为24小时至48小时,所述第一改性硅胶和所述丙烯酸酯类化合物反应后的产物为第二产物,可选用甲醇对所述第二产物进行洗涤以除去过量的所述丙烯酸酯类化合物,洗涤后的所述第二反应产物优选在40℃至60℃真空干燥,干燥时间可以为4小时至8小时,干燥后即可得到所述第二改性硅胶。
步骤s30中,所述二胺类化合物为含有两个伯胺的直链烷烃,例如乙二胺、丙二胺中的一种或多种。优选为,乙二胺。所述第二改性硅胶包含的第一修饰基团结构单元(如通式(ⅲ)所示)分子链中端基为酯基,所述酯基可与所述二胺类化合物发生酯的氨解反应,且得到的分子链端基为氨基。所述第二改性硅胶和所述二胺类化合物的质量比为1:13至:1。
所述第二改性硅胶和所述二胺类化合物反应的溶剂不限,优选为甲醇,反应温度为40℃至60℃,反应时间为24小时至48小时,所述第二改性硅胶和所述二胺类化合物反应后的产物为第三产物,可选用甲醇对所述第三产物进行洗涤以除去过量的所述二胺类化合物,洗涤后的所述第三反应产物优选在40℃至60℃真空干燥,干燥时间可以为4小时至8小时,干燥后即可得到所述第三改性硅胶。
步骤s40中,所述硫代苹果酸中含有巯基,可作为吸附烷基汞的功能基团。所述第三改性硅胶表面的所述第三修饰基团结构单元(如通式(ⅳ)所示)中氨基可与所述硫代苹果酸中的羧基发生酰胺反应,从而将巯基功能基团接枝到硅胶上,得到所述巯基改性硅胶。所述硫代苹果酸还含有羧酸基团等含氧官能团,可进一步提高烷基汞的吸附。所述第三改性硅胶和所述硫代苹果酸的质量比为3:1至5:1。
优选的,通过羧基活化剂活化所述硫代苹果酸,促进其与所述第三改性硅胶的酰胺反应。在一实施例中,所述羧基活化剂为1-乙基-(3-二甲氨基丙基)碳二亚胺盐酸盐(edc·hcl)和n-羟基琥珀酰亚胺(nhs)。所述1-乙基-(3-二甲氨基丙基)碳二亚胺盐酸盐(edc·hcl)和所述硫代苹果酸的摩尔质量比为1:1至3:1,所述1-乙基-(3-二甲氨基丙基)碳二亚胺盐酸盐(edc·hcl)与n-羟基琥珀酰亚胺摩尔质量比为2:1至8:1。
所述第三改性硅胶与硫代苹果酸反应的溶剂优选为n,n-二甲基甲酰胺dmf,反应温度可室温,反应时间为24小时至48小时。
本发明实施例还提供一种所述的巯基改性硅胶在吸附烷基汞中的应用。
本发明实施例进一步提供一种检测水中烷基汞的方法,包括以下步骤:
s100,提供所述的巯基改性硅胶并将所述巯基改性硅胶填充于固相萃取小柱;
s200,将待测水样通过所述固相萃取小柱进行过柱操作,使所述待测水样中的烷基汞吸附在所述固相萃取小柱上;
s300,用洗脱液对所述吸附烷基汞的固相萃取小柱进行洗脱;
s400,所述洗脱后的洗脱液用有机溶剂进行萃取;以及
s500,所述萃取后的溶液通过气相色谱检测烷基汞浓度。
本发明实施例提供的检测水中烷基汞的方法,利用所述巯基改性硅胶作为固相吸附材料填充固相萃取小柱,通过过柱使待测水样中烷基汞富集,再进行洗脱、萃取,最后用气相色谱进行检测,优化了样品处理程序,操作简便,回收率高,且检测效率大大提高。
步骤s100中,所述巯基改性硅胶即为步骤s40制备得到的所述巯基改性硅胶,将所述巯基改性硅胶填充于固相萃取小柱中,所述巯基改性硅胶可填充至所述固相萃取小柱体积的1/3至2/3。
步骤s200中,所述将待测水样通过所述固相萃取小柱进行过柱操作时,为了方便操作,可将所述待测水样盛装入容器100中,通过导管将容器100与固相萃取小柱200一端连接,再将所述固相萃取小柱200另一端连接蠕动泵300,组成分离富集装置,请参阅图1。通过调节所述蠕动泵300使所述待测水样以恒定的流速通过所述固相萃取小柱200。在一实施例中,蠕动泵300可连接多个固相萃取小柱200,实现多个样品的同时处理,如图2所示。在一实施例中,所述待测水样的过柱流速为8ml/min~12ml/min。
步骤s300中,所述洗脱液可以为相同体积的hno3-hcl混合溶液、hcl-nacl混合溶液和硫脲-nacl混合溶液,优选的,所述洗脱液为相同体积的nacl和hcl的混合溶液,所述混合溶液中nacl浓度为2mol/l,hcl浓度为2mol/l。在一实施例中,所述洗脱液用量大于等于3ml。
步骤s400中,萃取用的所述有机溶液优选为甲苯。
步骤s500中,气相色谱条件优选为:
色谱柱温度:160℃保持10min,进样口温度230℃;进样量1μl;进样方式为分流进样,分流比5:1;载气为氮气;恒流模式,流量5.0ml/min;ecd检测器温度为230℃。
实施例1
(1)将粒径为100目的硅胶置于250ml三口瓶中,加入150ml的6.0mol/l的盐酸,120℃加热回流5小时,冷却后过滤,用蒸馏水将硅胶洗涤至中性,真空干燥得到活化硅胶。
(2)称取30.0g活化硅胶置于250ml三口瓶中,分别加入100ml甲苯(甲苯以浸没硅胶表面5~6cm为更优)、15.0mlγ-氨丙基三乙氧基硅烷,70℃搅拌回流6小时,冷却后过滤得到固体,固体用甲苯、乙醇依次洗涤2~3次,50℃真空干燥6小时,得到第一改性硅胶。
(3)称取30.0g第一改性硅胶、8ml丙烯酸甲酯、100ml甲醇于250ml三口瓶中,50℃加热搅拌24小时,停止反应,反应液静置,反应产物用甲醇洗涤反应液除去过量的丙烯酸甲酯,抽滤去除甲醇,再置于干燥箱中50℃条件下干燥6小时,得到第二改性硅胶。
(4)称取25g第二改性硅胶,加入到100ml甲醇中,加入12ml乙二胺,50℃下搅拌24小时,停止反应,反应液静置,反应产物用甲醇洗涤去除过量乙二胺,抽滤去除甲醇,再置于干燥箱中50℃条件下干燥6小时,得到第三改性硅胶。
(4)称取4.505g硫代苹果酸,8.626g1-乙基-(3-二甲氨基丙基)碳二亚胺盐酸盐(edc·hcl),1.036g(0.009mol)n-羟基琥珀酰亚胺(nhs),先将硫代苹果酸溶于n,n-二甲基甲酰胺(dmf)中,然后依次加入nhs、edc·hcl充分溶解,最后加入第三改性硅胶,常温(25℃)搅拌24小时,停止反应,反应产物用dmf、乙醇洗涤,抽滤,置于干燥箱中50℃条件下干燥6小时,得到巯基改性硅胶。
第一改性硅胶、巯基改性硅胶以及吸附烷基汞后的巯基改性硅胶进行红外光谱测试,如图3所示。图3中a曲线表示第一改性硅胶的红外谱图,1070cm-1处的强吸收峰为si-o-si的反对称伸缩振动吸收峰,在796cm-1出现si-o-si的对称伸缩振动吸附峰,这是硅胶骨架的典型特征峰,在3390cm-1处的吸收峰为硅胶表面-oh的伸缩振动和n-h振动的重叠峰;在1570cm-1~1650cm-1处出现n-h特征吸收峰,表明在硅胶表面已经成功引入了氨基基团;图3中b曲线表示巯基改性硅胶的红外谱图,1560cm-1~1660cm-1处出现n-h的伸缩振动吸收峰,1740cm-1出现羧酸与酰胺基团中c=o的特征吸收峰,2570cm-1处出现s-h伸缩振动引起的强度相对较弱特征吸收峰,说明硫代苹果酸通过酰胺反应成功键合到硅胶上;图3中c曲线表示吸附烷基汞后的巯基改性硅胶的红外谱图,图中并没有出现新的特征吸收峰,但是位于2570cm-1处的s-h的伸缩振动吸收峰消失了;且吸附了烷基汞以后,c=o的吸收峰蓝移至1730cm-1,n-h的吸收峰蓝移至1550cm-1~1670cm-1,说明hg与-sh、c=o、n-h发生配位键合作用。
应用例1
将实施例1制备得到的3g巯基改性硅胶填充于固相萃取小柱,并组成如图1所示的分离富集装置。取500ml含有100ng(加标量)甲基汞或含有100ng乙基汞(加标量)的水样,调节蠕动泵使水样以不同的流速过柱,过柱后用3ml的nacl和hcl混合溶液对固相萃取柱进行洗脱,混合溶液中nacl浓度为2mol/l,hcl浓度为2mol/l,洗脱液再用1ml甲苯进行萃取,用气相色谱检测萃取液中甲基汞和乙基汞的浓度即待测水样测定值,根据测定结果计算回收率,回收率=(待测水样测定值-加标量)/加标量×100%。
测试仪器为:shinwaulbonhr-thermon-hg烷基汞专用色谱柱;柱长为15m,直径为530μm;
测试条件为:
色谱柱温度:160℃保持10min,进样口温度230℃;进样量1μl;进样方式为分流进样,分流比5:1;载气为氮气;恒流模式,流量5.0ml/min;ecd检测器温度为230℃。
即将检测出的甲基汞和乙基汞的浓度与待测水样中不同过柱流速对烷基汞回收率的影响如图4所示,从图4中可以看出,过柱流速对烷基汞的吸附有明显影响,且甲基汞和乙基汞呈现一致的变化规律。水样流速在1.0~9.0ml/min之间时回收效率随流速增加而增加,从74%增加至85%,但当流速升高至9ml/min后,回收率则呈现随流速增加而降低的趋势,在15ml/min时回收率降低到80%左右,由此可见,最佳过柱流速为9ml/min。
应用例2
采用应用例1的操作步骤对洗脱过程中洗脱液的类型进行优化。提供不同的洗脱液,包括相同体积的hno3-hcl混合溶液、hcl-nacl混合溶液和硫脲-nacl混合溶液,并采用不同弄得的洗脱液进行洗脱,结果如表1所示。从表1可以看出,采用2mol/lnacl-2mol/lhcl作为洗脱液,回收率最高,在此洗脱液洗脱条件下,甲基汞和乙基汞的回收率分别为84.7%和84.0%。
表1不同洗脱液对甲基汞和乙基汞的洗脱效率影响
应用例3
根据应用例1的操作步骤对洗脱过程中洗脱液的用量进行优化。
将含100ng的烷基汞标准溶液均匀的注入填充2gtmsg的烷基汞小柱中,用氮气将溶剂吹干,再分别用1、2、3、5、7、10ml的洗脱液进行洗脱。收集的洗脱液定容至10ml,用甲苯对洗脱液进行萃取,萃取液浓缩至1ml后进行同应用例1的气相色谱测定,计算回收率。
不同洗脱液用量对回收率的影响如图5所示,从图5中可以看到,当洗脱液小于3ml时,烷基汞的烷基汞的回收率较低,洗脱不完全;当洗脱液大于等于3ml时,回收率达到84%并趋于平稳。
烷基汞氯化效果验证
分别将含100ng的烷基汞和100ng氯化烷基汞的标准溶液加入到3ml2mol/lnacl+1mol/lhcl的洗脱液中,旋涡振荡器充分振荡2min;然后以甲苯溶液进行液液萃取,浓缩定容至1ml,气相色谱进行分析。
结果表明:直接将烷基汞加入洗脱液进行萃取的回收率在87.1%~91.3%;将氯化烷基汞直接加入洗脱液进行萃取的回收率为86.6%~90.9%;烷基汞及氯化烷基汞在2mol/lnacl+1mol/lhcl的洗脱液体系中回收率基本一致,烷基汞在此洗脱液中能够全部氯化。此外,相较于固相萃取小柱的洗脱-萃取过程,直接萃取的回收率提高了大约7%,说明在固相萃取小柱的洗脱-萃取过程的回收率在93%左右。
此外,烷基汞的加标量为50ng-100ng的水样按照应用例1进行重复多次回收,加标回收率在75%-85%之间。
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!