一种快速检测孕妇可溶性血管内皮生长因子受体-1的免疫层析检测卡及其制备方法与流程
本发明属于体外诊断领域,涉及一种快速检测孕妇可溶性血管内皮生长因子受体-1的免疫层析检测卡及其制备方法。
背景技术:
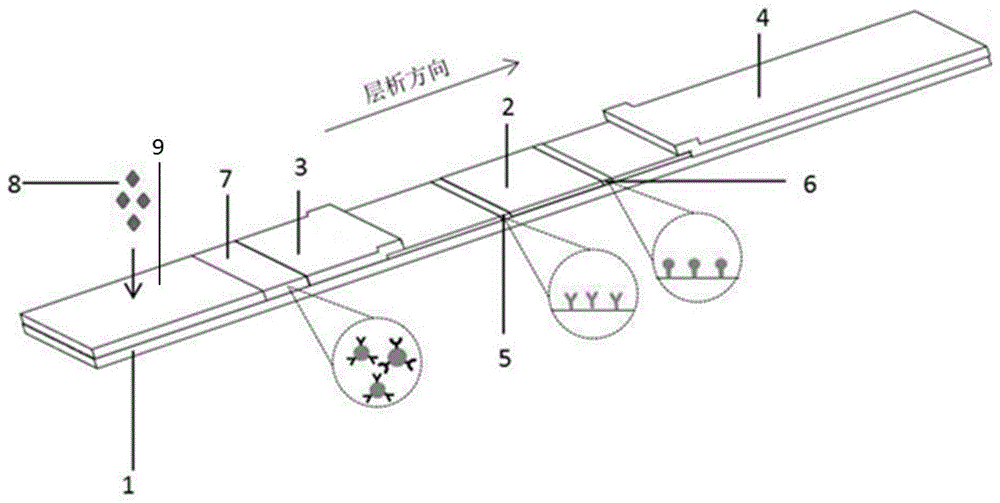
:vegfr是受体酪氨酸激酶(rtk)家族成员,含有细胞外配体结合区,具有七个免疫球蛋白(ig)样结构域,跨膜区段和细胞质结构域内的酪氨酸激酶(tk)结构域。该受体与vegfr-a,vegfr-b和plgf结合,在血管生成和血管发生中起重要作用。在血管内皮细胞,胎盘滋养层细胞和外周血单核细胞中发现该受体的表达。内皮细胞表达三种不同的血管内皮生长因子(vegf)受体,它们被命名为vegfr-1(flt-1),vegfr-2(kdr/flk-1),vegfr-3(flt-4)。已经发现了编码该基因的不同同种型的多种转录物变体。包括全长跨膜受体同种型和缩短的可溶性同种型。flt-1胞外域剪接后形成可溶性血管内皮生长因子受体-1(sflt-1),sflt-1保留了与plgf、vegf结合的高亲和力特性,能使plgf、vegf的酪氨酸激酶活性丧失,因此认为,sflt-1是plgf、vegf的拮抗剂。sflt-1与先兆子痫的发作有关。sflt-1在子痫前期的发病过程中其重要作用,其高表达可降低plgf、vegf的表达水平,导致血管生成障碍、内皮细胞损伤,进而影响血管壁的完整性和通透性,出现蛋白尿、水肿和血液浓缩等。体内和体外实验均证实,胎盘组织缺氧后sflt-1表达水平上升。技术实现要素:有鉴于此,本发明的主要目的在于提供一种快速检测孕妇可溶性血管内皮生长因子受体-1的免疫层析检测卡及其制备方法。为了实现上述目的,本发明提供了如下技术方案:一种快速检测孕妇可溶性血管内皮生长因子受体-1的免疫层析检测卡,包括试纸条,所述试纸条包括检测线及质控线,所述检测线上包被有一株鼠抗人sflt-1单克隆抗体,所述质控线上包被有羊抗兔多克隆抗体。在本发明的一个具体方案中,其中所述试纸条还包括pvc板,所述pvc板上固定有依次连接的样品垫、标记物垫、包被垫及吸水垫,所述包被垫上依次设有检测线及质控线,所述样品垫和标记物垫连接为一体。在本发明的一个具体方案中,其中所述包被垫靠近检测线的一端连接有标记物垫,靠近质控线的一端连接有吸水垫。在本发明的一个具体方案中,其中所述标记物垫上包被有另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球和兔igg标记的表面活化的荧光乳胶微球,所述另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球和兔igg标记的表面活化的荧光乳胶微球的摩尔比为1:(0.2~4)。在本发明的一个具体方案中,其中所述快速检测孕妇可溶性血管内皮生长因子受体-1的免疫层析检测卡还包括用于卡设试纸条的卡壳。在本发明的一个具体方案中,其中所述卡壳包括:底槽,其连接于所述pvc板;上盖,其连接于所述底槽,所述上盖上设置有用于向所述样品垫上加样的加样孔;观察窗,其设置于上盖上并用于检测线和质控线的数据采集。一种快速检测孕妇可溶性血管内皮生长因子受体-1的免疫层析检测卡的制备方法,包括以下步骤:1)包被垫的制备:将一株鼠抗人sflt-1单克隆抗体和羊抗兔多克隆抗体分别包被到硝酸纤维素膜上,干燥备用;2)标记物垫的制备:将另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球和兔igg标记的表面活化的荧光乳胶微球混合后,喷涂在玻璃纤维素膜上,干燥备用;3)组装试纸条:在pvc板上粘接包被垫,并在靠近该包被垫上的质控线的一端搭接吸水垫,在靠近该包被垫上的检测线的一端搭接标记物垫及其连接的样品垫;然后将其切成所需宽度的试纸条,之后将该试剂条放入卡壳。在本发明的一个具体方案中,其中所述表面活化的荧光乳胶微球通过以下步骤制得:1)取表面活性剂加入0.1~0.5mol/l,ph值为8~10的硼酸-硼砂缓冲溶液(包含0.5wt%~3wt%的peg2000)中,再加入二甲基甲酰胺、n,n’-二环己基碳二亚胺和n-羟基琥珀酰亚胺,搅拌反应;2)取表面带有羧基的荧光乳胶微球的分散液,以硼酸-硼砂缓冲溶液(包含0.5wt%~3wt%的peg2000)调ph至8~10后,加入到步骤1)所得的产物中,在25℃下搅拌反应1~5h,反应完毕后,离心去除上清液,得到表面活化的荧光乳胶微球,用硼酸-硼砂缓冲溶液复溶备用。在本发明的一个具体方案中,其中所述表面活性剂包含有n,n'-双月桂酰基乙二胺二丙烯酸钠、聚乙二醇单月硅酸酯、十二烷基苯磺酸盐和月桂酰谷氨酸盐,四者的重量比为(0.5~6):(4~9):(0.8~3):(5~14);所述表面活性剂与所述氨基表面的荧光乳胶微球的重量比为(0.5~120):1。在本发明的一个具体方案中,其中所述另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球通过以下步骤制得:取表面活化的荧光乳胶微球加入碳化二亚胺(edc)和n-羟基琥珀酰亚胺(nhs)中室温搅拌2~6h,然后加入另一株鼠抗人sflt-1单克隆抗体,室温下搅拌1~4h,再加入10~50mgbsa封闭液,继续搅拌1~4h;在2~8℃下,按照11000r/min的转速离心30min,除去上清液;最后,用0.01m~0.5m的磷酸盐缓冲溶液(ph=7.4)将固体沉淀物复溶,再加入proclin300在4℃下保存待用。在本发明的一个具体方案中,其中所述表面活化的荧光乳胶微球与另一株鼠抗人sflt-1单克隆抗体的质量比例为1:(0.01~4)。本发明的有益效果:1、本发明所提供的快速检测孕妇可溶性血管内皮生长因子受体-1的免疫层析检测卡,其可用于血清、血浆和全血的检测,以用于预测子痫前期相关疾病的诊断;2、本发明所提供的快速检测孕妇可溶性血管内皮生长因子受体-1的免疫层析检测卡,其样本用量小,检测在5~20min之内即可完成,线性检测范围为10pg/ml~10000pg/ml,极大地提高了检测效率;3、本发明所提供的快速检测孕妇可溶性血管内皮生长因子受体-1的免疫层析检测卡,其灵敏度高、稳定性强、线性范围宽,具有优异的准确性和精密度;4、本发明所提供的快速检测孕妇可溶性血管内皮生长因子受体-1的免疫层析检测卡,在样本采集后,无需长时间等待,即可进行样本检测,操作简单,样本处理时间短,降低了时间成本,适用于临床快速诊断检测;5、本发明所提供的快速检测孕妇可溶性血管内皮生长因子受体-1的免疫层析检测卡,其通过采用表面活化的荧光乳胶微球,克服了市面上荧光染料灵敏度差和湿式荧光微球稳定性差的缺陷,能够保证颗粒间的相对距离不易团聚,无需缓冲液,加入待测样本后能即刻复溶并顺利层析。附图说明图1为本发明所提供的快速检测孕妇sflt-1的免疫层析试纸条示意图;图2a为本发明所提供的快速检测孕妇sflt-1的免疫层析检测卡中一种上盖的内部结构示意图;图2b为本发明所提供的快速检测孕妇sflt-1的免疫层析检测卡中一种底槽的内部结构示意图;图3为本发明实施例1中孕妇sflt-1的校准曲线;图4为本发明实施例2中孕妇sflt-1的校准曲线;图5为本发明实施例3中孕妇sflt-1的校准曲线;图6为本发明实施例4中孕妇sflt-1的校准曲线;其中,1-pvc板,2-包被垫,3-标记物垫,4-吸水垫,5-检测线,6-质控线,7-标记物结合处,8-样本,9-样品垫,11-上盖,12-底槽,13-加样孔,14-观察窗,15-试纸条放置区域,16-定位柱,17-定位孔,18-第一限定部,19-第二限定部,20-第三限定部。具体实施方式为了进一步理解本发明,下面结合实施例对本发明优选实施方案进行描述,但是应当理解,这些描述只是为进一步说明本发明的特征和优点,而不是对本发明权利要求的限制。以下材料或试剂,除非特别说明,均为市售。实施例1:1.孕妇sflt-1的免疫层析检测卡的制备1)表面活化荧光乳胶微球的制备:n,n'-双月桂酰基乙二胺二丙烯酸钠、聚乙二醇单月硅酸酯、十二烷基苯磺酸盐和月桂酰谷氨酸盐,四者的重量比为1:4:1:5。取表面活性剂(包含1mg的n,n'-双月桂酰基乙二胺二丙烯酸钠、4mg的聚乙二醇单月硅酸酯、1mg的十二烷基苯磺酸盐和5mg的月桂酰谷氨酸盐)加入0.2mol/l,ph=8.4的硼酸-硼砂缓冲溶液(包含0.5wt%~3wt%的peg2000)中,再加入1ml二甲基甲酰胺、1mg的n,n’-二环己基碳二亚胺和0.5mgn-羟基琥珀酰亚胺,在120r/min的搅拌速度下进行反应;②取1ml,含1wt%表面带有羧基的荧光乳胶微球分散液(购自上海甄准生物技术有限公司),用10ml,0.2mol/l,ph=8.4的硼酸-硼砂缓冲溶液(包含0.5wt%~3wt%的peg2000)稀释分散均匀后,加入到步骤①所得的产物中,在25℃,120r/min的搅拌速度下反应2h,反应完毕后,120r/min的搅拌速度下离心30min去除上清液,得到表面活化的荧光乳胶微球,用0.2mol/l,ph=8.4的硼酸-硼砂缓冲溶液复溶至1ml备用。2)另一株鼠抗人sflt-1单克隆抗体标记表面活化的荧光乳胶微球取0.5ml步骤1)中制备的表面活化的荧光乳胶微球加入1mg碳化二亚胺(edc),1mgn-羟基琥珀酰亚胺(nhs),于室温,120r/min的转速下搅拌2h,然后加入50μl另一株鼠抗人sflt-1单克隆抗体,室于室温,120r/min的转速下搅拌2h,再加入20mgbsa封闭液,继续搅拌2h。在2~8℃下,按照11000r/min的转速离心30min,除去上清液。最后,用0.2m的磷酸盐缓冲液(ph=7.4)将固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。3)兔igg多克隆抗体标记表面活化的荧光乳胶微球取0.5ml步骤1)中制备的表面活化的荧光乳胶微球加入1mg碳化二亚胺(edc),1mgn-羟基琥珀酰亚胺(nhs),于室温,120r/min的转速下搅拌2h,然后加入50μlmg羊兔igg多克隆抗体,于室温,120r/min的转速下搅拌2h,再加入20mgbsa封闭液,继续搅拌2h。在2~8℃下,按照11000r/min的转速离心30min,除去上清液。最后,用0.2m的磷酸盐缓冲液(ph=7.4)将固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。4)包被垫的制备将一株鼠抗人sflt-1单克隆抗体和羊抗兔多克隆抗体分别用0.2m的磷酸盐缓冲液(ph=7.4)稀释成1mg/ml,用划膜喷金仪在硝酸纤维素膜(nc膜)上进行划膜。含有一株鼠抗人sflt-1单克隆抗体的作为检测线(t线)5,含有羊抗兔多克隆抗体的作为质控线(c线)6,然后在37℃,湿度<30%的环境下干燥4h制成包被垫。5)标记物垫的制备①将玻璃纤维素膜在0.2m的磷酸盐缓冲液(ph=7.4)中浸泡5h,然后在35℃下干燥6h,备用。②将摩尔比为1:1的另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球和兔igg标记的表面活化的荧光乳胶微球混合均匀后,按照10μl/cm的速度喷涂在玻璃纤维素膜上,然后放置在37℃下干燥1h制成标记物垫3。标记物垫上包被有另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球和兔igg标记的表面活化的荧光乳胶微球的地方叫做标记物结合处7。设置标记物结合处7的目的在于:将待测血液样本8滴加到样品垫9上,在吸水垫4的作用下,血液样本向前层析,在标记物结合处7的血液样本中的sflt-1与标记物结合处包被的另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球反应,反应后的物质、未参加反应的另一株鼠抗人sflt-1单克隆抗体标记的荧光乳胶微球、兔igg标记的荧光乳胶微球随着尿液样本继续层析,在检测线处参加反应的另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球与检测线包被的一株鼠抗人sflt-1单克隆抗体反应而停留在检测线,在质控线处兔igg标记的荧光乳胶微球与质控线包被的羊抗兔多克隆抗体反应而停留在质控线,其他物质继续层析,最后通过荧光免疫层析仪分别采集检测线的荧光微球的信号(记作t)和质控线的荧光微球的信号(记作c),计算t/c值,从sflt-1的标准曲线中读取血液样本中sflt-1的浓度。(6)免疫层析检测卡的组装首先在pvc板1上粘接包被垫2,然后在靠近包被垫2上的质控线6的一端搭接吸水垫,在靠近包被垫2的检测线5的一端搭接标记物垫3及其连接的样品垫9,用切条机切成4mm±0.1mm的试纸条(见图1),将试纸条放入卡壳中制备成孕妇sflt-1免疫层析检测卡。所述卡壳选自现有技术,例如,所述卡壳(如图2a、图2b所示)可以包括:底槽12,其连接于所述pvc板1;上盖11,其连接于所述底槽12,所述上盖11上设置有用于向所述样品垫9上加样的加样孔13;观察窗14,其设置于上盖11上,用于检测线5和质控线6的数据采集。如图2b所示,所述底槽12包括:位于其内表面的对称分布的多个定位孔17,多个所述定位孔17之间设有多个用于限定试纸条横向移动的第一限定部18以及用于限定试纸条纵向移动的第二限定部19;对称设置的所述第一限定部18与所述第二限定部19围设成纸条放置区域15(虚线区域),用于放置试纸条;如图2a所示,所述上盖11包括:与多个所述定位孔17相配合的多个定位柱16,这样配合使用以将上盖11和底槽12固定在一起;所述上盖11还包括用于限定试纸条的上下移动的第三限定部20。所述包被垫2的上方设有用于数据采集的观察窗14,以露出全部所述检测线5和质控线6,用于收集其检测结果;且所述观察窗14开设于所述上盖11上与试纸条放置区域15的中部相对应的位置。所述上盖11在与所述样品垫9相对应的位置处开设有加样孔,以用于样品垫9上滴加样本8。所述检测线距离加样孔15-25mm。2.检测取60μl的待测样本滴加到步骤1制备的sflt-1免疫层析检测卡的加样孔13(对应试纸条的样品垫9)中待测样本,室温静置15min,然后将sflt-1免疫层析检测卡插入到荧光免疫分析仪进行检测,即时可获得检测结果。3.试纸条的评价1)配置不同浓度的sflt-1校准品(0、10、50、400、2000、10000pg/ml),用本实施例1步骤1制备的sflt-1免疫层析检测卡按照步骤2的检测过程依次进行测定,空白检测线不高于10pg/ml,检测范围为10~10000pg/ml。检测结果如表1所示,以样本浓度为横坐标,检测线与质控线的比值(t/c)为纵坐标,用logistic(四参数)进行曲线拟合,拟合度r2分别为0.9996,n=6,制备的sflt-1校准曲线如图3所示,t/c值与校准品在浓度为10-10000pg/ml的范围内具有良好的相关性。表1检测数据标准浓度pg/ml01050400200010000t/c值0.21540.73221.04161.70772.15982.51902)定量限定量限(limitofquantitation,loq),参照clsi发布的ep17-a2文件。依据临床要求和室间质量评价的允许误差,设定本试剂sflt-1的总误差目标为30%。在不考虑分析偏差的情况下,允许总误差(tea)=2cv,即cv=1/2tea。sflt-1浓度在10.00pg/ml时检测的cv为12.88%,小于15%,符合质量目标要求,因此loq=10.00pg/ml,表明sflt-1荧光微球免疫层析检测卡的具有较高的灵敏度。3)精密度抽取三个批次的sflt-1免疫层析检测卡,分别检测浓度为50、400、2000pg/ml的样本进行检测,每个浓度点平行测定10次,计算三个批号检测试纸条的批内变异系数和批间变异系数,从表2中可以看出批间和批内变异系数均小于13.03%,说明sflt-1荧光免疫层析检测卡的精密度较高。表2检测数据4)回收率取三批次浓度为10000pg/ml的sflt-1校准品,分别加入到浓度接近于0的阴性样本中,其中所加入的sflt-1校准品与阴性样本的体积比为1:9,重复测定3次,计算回收率。三批样本校准品回收率的结果分别为99.02%、106.87%、93.65%,回收率均在90%-110%之间,说明测定结果符合标准。5)比对实验收集20位临床样本,采用本实施例制备的sflt-1免疫层析检测卡与罗氏的sflt-1检测试剂盒(电化学发光法)进行比对实验。表3检测数据从表3的检测结果中可以看出,本发明实施例1制备的sflt-1免疫层析检测卡复检测三次,检测1分别与检测2、检测3的结果进行相关性分析,回归方程分别为:y=1.0257x-5.3198,r2=0.9992;y=0.9894x+5.5201,r2=0.9976;表明实施例1制备的tau蛋白免疫层析检测卡的稳定性良好。将实施例1制备的sflt-1免疫层析检测卡与罗氏sflt-1蛋白检测试剂盒(电化学发光法)的结果进行相关性分析,回归方程为:y=1.0177x-7.5540,r2=0.9985,n=20,表明本发明实施例1制备的sflt-1免疫层析检测卡与罗氏sflt-1检测试剂盒(电化学发光法)的检测结果显著相关。因此本发明的sflt-1免疫层析检测卡可以满足辅助临床诊断的需求。实施例21.孕妇sflt-1的免疫层析检测卡的制备1)表面活化荧光乳胶微球的制备:n,n'-双月桂酰基乙二胺二丙烯酸钠、聚乙二醇单月硅酸酯、十二烷基苯磺酸盐和月桂酰谷氨酸盐,四者的重量比为2:5:2:8。①取表面活性剂(包含2mg的n,n'-双月桂酰基乙二胺二丙烯酸钠、5mg的聚乙二醇单月硅酸酯、2mg的十二烷基苯磺酸盐和8mg的月桂酰谷氨酸盐)加入0.2mol/l,ph=8.4的硼酸-硼砂缓冲溶液(包含0.5wt%~3wt%的peg2000)中,再加入1ml二甲基甲酰胺、1mg的n,n’-二环己基碳二亚胺和0.5mgn-羟基琥珀酰亚胺,在120r/min的搅拌速度下进行反应;②取1ml含1wt%,表面带有羧基的荧光乳胶微球分散液(购自上海甄准生物技术有限公司),用10ml,0.2mol/l,ph=8.4的硼酸-硼砂缓冲溶液(包含0.5wt%~3wt%的peg2000)稀释分散均匀后,加入到步骤①所得的产物中,在25℃,120r/min的搅拌速度下反应3h,反应完毕后,按照12000r/min的转速离心30min去除上清液,得到表面活化的荧光乳胶微球,用0.2mol/l,ph=8.4的硼酸-硼砂缓冲溶液复溶至1ml备用。2)另一株鼠抗人sflt-1单克隆抗体标记表面活化的荧光乳胶微球取0.5ml步骤1)中制备的表面活化的荧光乳胶微球加入1mg碳化二亚胺(edc),1mgn-羟基琥珀酰亚胺(nhs),于室温,120r/min的转速下搅拌3h,然后加入100μl另一株鼠抗人sflt-1单克隆抗体,于室温,120r/min的转速下搅拌1h,再加入10mgbsa封闭液,继续搅拌1h。在2~8℃下,按照11000r/min的转速离心30min,除去上清液。最后,用0.2m的磷酸盐缓冲液(ph=7.4)将固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。3)兔igg多克隆抗体标记表面活化的荧光乳胶微球取0.5ml步骤1)中制备的表面活化的荧光乳胶微球加入1mg碳化二亚胺(edc),1mgn-羟基琥珀酰亚胺(nhs),于室温,120r/min的转速下搅拌3h,然后加入100μlmg羊兔igg多克隆抗体,于室温,120r/min的转速下搅拌1h,再加入10mgbsa封闭液,继续搅拌1h。在2~8℃下,按照11000r/min的转速离心30min,除去上清液。最后,用0.2m的磷酸盐缓冲液(ph=7.4)将固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。4)包被垫的制备将一株鼠抗人sflt-1单克隆抗体和羊抗兔多克隆抗体分别用0.2m的磷酸盐缓冲液(ph=7.4)稀释成1mg/ml,用划膜喷金仪在硝酸纤维素膜(nc膜)上进行划膜。含有一株鼠抗人sflt-1单克隆抗体的作为检测线(t线)5,含有羊抗兔多克隆抗体的作为质控线(c线)6,然后在37℃,湿度<30%的环境下干燥4h制成包被垫。5)标记物垫的制备①将玻璃纤维素膜在0.2m的磷酸盐缓冲液(ph=7.4)中浸泡6h,然后在35℃下干燥8h,备用。②将摩尔比为1:1的另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球和兔igg标记的表面活化的荧光乳胶微球混合均匀后,按照10μl/cm的速度喷涂在玻璃纤维素膜上,然后放置在45℃下干燥2h制成标记物垫。标记物垫上包被有另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球和兔igg标记的表面活化的荧光乳胶微球的地方叫做标记物结合处7。设置标记物结合处7的目的同实施例1。6)免疫层析检测卡的组装首先在pvc板1上粘接包被垫2,然后在靠近包被垫2上的质控线6的一端搭接吸水垫,在靠近包被垫2的检测线5的一端搭接标记物垫3及其连接的样品垫9,用切条机切成4mm±0.1mm的试纸条(见图1),将试纸条放入卡壳中制备成孕妇sflt-1免疫层析检测卡。所述卡壳的结构同实施例1。2.检测取60μl的待测样本滴加到步骤1制备的sflt-1免疫层析检测卡的加样孔(对应试纸条的样品垫9)中待测样本,室温静置15min,然后将sflt-1免疫层析检测卡插入到荧光免疫分析仪进行检测,即时可获得检测结果。3.试纸条的评价1)配置不同浓度的sflt-1校准品(0、10、50、400、2000、10000pg/ml),用本实施例2步骤1制备的sflt-1免疫层析检测卡按照步骤2的检测过程依次进行测定,空白检测线不高于10pg/ml,检测范围为10~10000pg/ml。检测结果如表4所示,以样本浓度为横坐标,检测线与质控线的比值(t/c)为纵坐标,用logistic(四参数)进行曲线拟合,拟合度r2分别为0.9957,n=6,制备的sflt-1校准曲线如图4所示,t/c值与校准品在浓度为10-10000pg/ml的范围内具有良好的相关性。表4检测数据标准浓度pg/ml01050400200010000t/c值0.11560.68751.11581.50982.11452.46442)定量限定量限(limitofquantitation,loq),参照clsi发布的ep17-a2文件。依据临床要求和室间质量评价的允许误差,设定本试剂sflt-1的总误差目标为30%。在不考虑分析偏差的情况下,允许总误差(tea)=2cv,即cv=1/2tea。sflt-1浓度在10.00pg/ml时检测的cv为14.26%,小于15%,符合质量目标要求,因此loq=10.00pg/ml,表明sflt-1荧光微球免疫层析检测卡的具有较高的灵敏度。3)精密度抽取三个批次的sflt-1免疫层析检测卡,分别检测浓度为50、400、2000pg/ml的样本进行检测,每个浓度点平行测定10次,计算三个批号检测试纸条的批内变异系数和批间变异系数,从表5中可以看出批间和批内变异系数均小于12.68%,说明sflt-1荧光免疫层析检测卡的精密度较高。表5检测数据4)回收率取三批次浓度为10000pg/ml的sflt-1校准品,分别加入到浓度接近于0的阴性样本中,其中所加入的sflt-1校准品与阴性样本的体积比为1:9,重复测定3次,计算回收率。三批样本校准品回收率的结果分别为96.25%、102.11%、96.88%,回收率均在90%-110%之间,说明测定结果符合标准。实施例31.孕妇sflt-1的免疫层析检测卡的制备1)表面活化荧光乳胶微球的制备:n,n'-双月桂酰基乙二胺二丙烯酸钠、聚乙二醇单月硅酸酯、十二烷基苯磺酸盐和月桂酰谷氨酸盐,四者的重量比为4:5.5:2:12。①取表面活性剂(包含4mg的n,n'-双月桂酰基乙二胺二丙烯酸钠、5.5mg的聚乙二醇单月硅酸酯、2mg的十二烷基苯磺酸盐和12mg的月桂酰谷氨酸盐)加入0.2mol/l,ph=8.4的硼酸-硼砂缓冲溶液(包含0.5wt%~3wt%的peg2000)中,再加入1ml二甲基甲酰胺、1mg的n,n’-二环己基碳二亚胺和0.5mgn-羟基琥珀酰亚胺,在120r/min的搅拌速度下进行反应;②取1ml,含1wt%表面带有羧基的荧光乳胶微球分散液(购自上海甄准生物技术有限公司),用10ml,0.2mol/l,ph=8.4的硼酸-硼砂缓冲溶液(包含0.5wt%~3wt%的peg2000)稀释分散均匀后,加入到步骤①所得的产物中,在25℃,120r/min的搅拌速度下反应5h,反应完毕后,按照12000r/min的转速离心30min去除上清液,得到表面活化的荧光乳胶微球,用0.2mol/l,ph=8.4的硼酸-硼砂缓冲溶液复溶至1ml备用。2)另一株鼠抗人sflt-1单克隆抗体标记表面活化的荧光乳胶微球取0.5ml步骤1)制备的表面活化的荧光乳胶微球加入1mg碳化二亚胺(edc),1mgn-羟基琥珀酰亚胺(nhs),于室温,120r/min的转速下搅拌3h,然后加入200μl另一株鼠抗人sflt-1单克隆抗体,于室温,120r/min的转速下搅拌4h,再加入30mgbsa封闭液,继续搅拌3h。在2~8℃下,按照11000r/min的转速离心30min,除去上清液。最后,用0.2m的磷酸盐缓冲液(ph=7.4)将固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。3)兔igg多克隆抗体标记表面活化的荧光乳胶微球取0.5ml步骤1)中制备的表面活化的荧光乳胶微球加入1mg碳化二亚胺(edc),1mgn-羟基琥珀酰亚胺(nhs),于室温,120r/min的转速下搅拌6h,然后加入200μlmg羊兔igg多克隆抗体,于室温,120r/min的转速下搅拌4h,再加入30mgbsa封闭液,继续搅拌3h。在2~8℃下,按照11000r/min的转速离心30min,除去上清液。最后,用0.2m的磷酸盐缓冲液(ph=7.4)将固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。4)包被垫的制备将一株鼠抗人sflt-1单克隆抗体和羊抗兔多克隆抗体分别用0.2m的磷酸盐缓冲液(ph=7.4)稀释成1mg/ml,用划膜喷金仪在硝酸纤维素膜(nc膜)上进行划膜。含有一株鼠抗人sflt-1单克隆抗体的作为检测线(t线)5,含有羊抗兔多克隆抗体的作为质控线(c线)6,然后在37℃,湿度<30%的环境下干燥4h制成包被垫。5)标记物垫的制备①将玻璃纤维素膜在0.2m的磷酸盐缓冲液(ph=7.4)中浸泡2h,然后在35℃下干燥6h,备用。②将摩尔比为1:0.5的另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球和兔igg标记的表面活化的荧光乳胶微球混合均匀后,按照5μl/cm的速度喷涂在玻璃纤维素膜上,然后放置在37℃下干燥3h制成标记物垫。标记物垫上包被有另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球和兔igg标记的表面活化的荧光乳胶微球的地方叫做叫做标记物结合处7。设置标记物结合处7的目的同实施例1。6)免疫层析检测卡的组装首先在pvc板1上粘接包被垫2,然后在靠近包被垫2上的质控线6的一端搭接吸水垫,在靠近包被垫2的检测线5的一端搭接标记物垫3及其连接的样品垫9,用切条机切成4mm±0.1mm的试纸条(见图1),将试纸条放入卡壳中制备成孕妇sflt-1免疫层析检测卡。所述卡壳的结构同实施例1。2.检测取60μl的待测样本滴加到步骤1制备的sflt-1免疫层析检测卡的加样孔(对应试纸条的样品垫9)中待测样本,室温静置15min,然后将sflt-1免疫层析检测卡插入到荧光免疫分析仪进行检测,即时可获得检测结果。3.试纸条的评价1)配置不同浓度的sflt-1校准品(0、10、50、400、2000、10000pg/ml),用本实施例3步骤1制备的sflt-1免疫层析检测卡按照步骤2的检测过程依次进行测定,空白检测线不高于10pg/ml,检测范围为10~10000pg/ml。检测结果如表6所示,以样本浓度为横坐标,检测线与质控线的比值(t/c)为纵坐标,用logistic(四参数)进行曲线拟合,拟合度r2分别为0.9986,n=6,制备的sflt-1校准曲线如图5所示,t/c值与校准品在浓度为10-10000pg/ml的范围内具有良好的相关性。表6检测数据标准浓度pg/ml01050400200010000t/c值0.18650.76871.07541.49782.10132.64242)定量限定量限(limitofquantitation,loq),参照clsi发布的ep17-a2文件。依据临床要求和室间质量评价的允许误差,设定本试剂sflt-1的总误差目标为30%。在不考虑分析偏差的情况下,允许总误差(tea)=2cv,即cv=1/2tea。sflt-1浓度在10.00pg/ml时检测的cv为12.45%,小于15%,符合质量目标要求,因此loq=10.00pg/ml,表明sflt-1荧光微球免疫层析检测卡的具有较高的灵敏度。3)精密度抽取三个批次的sflt-1免疫层析检测卡,分别检测浓度为50、400、2000pg/ml的样本进行检测,每个浓度点平行测定10次,计算三个批号检测试纸条的批内变异系数和批间变异系数,从表7中可以看出批间和批内变异系数均小于14.43%,说明sflt-1荧光免疫层析检测卡的精密度较高。表7检测数据4)回收率取三批次浓度为10000pg/ml的sflt-1校准品,分别加入到浓度接近于0的阴性样本中,其中所加入的sflt-1校准品与阴性样本的体积比为1:9,重复测定3次,计算回收率。三批样本校准品回收率的结果分别为96.34%、105.34%、94.64%,回收率均在90%-110%之间,说明测定结果符合标准。实施例41.孕妇可溶性血管内皮生长因子受体sflt-1免疫层析检测卡的制备1)表面活化的荧光乳胶微球的制备:n,n'-双月桂酰基乙二胺二丙烯酸钠、聚乙二醇单月硅酸酯、十二烷基苯磺酸盐和月桂酰谷氨酸盐,四者的重量比为5.5:8:2:14。①取表面活性剂(包含5.5mg的n,n'-双月桂酰基乙二胺二丙烯酸钠、8mg的聚乙二醇单月硅酸酯、2mg的十二烷基苯磺酸盐和14mg的月桂酰谷氨酸盐)加入0.2mol/l,ph=8.4的硼酸-硼砂缓冲溶液(包含0.5wt%~3wt%的peg2000)中,再加入1ml二甲基甲酰胺、1mg的n,n’-二环己基碳二亚胺和0.5mgn-羟基琥珀酰亚胺,在120r/min的搅拌速度下进行反应;②取1ml,含1wt%表面带有羧基的荧光乳胶微球分散液(购自上海甄准生物技术有限公司),用10ml,0.2mol/l,ph=8.4的硼酸-硼砂缓冲溶液(包含0.5wt%~3wt%的peg2000)稀释分散均匀后,加入到步骤①所得的产物中,在25℃下搅拌反应2.5h,反应完毕后,按照12000r/min的转速离心30min去除上清液,得到表面活化的荧光乳胶微球,用0.2mol/l,ph=8.4的硼酸-硼砂缓冲溶液复溶至1ml备用。2)另一株鼠抗人sflt-1单克隆抗体标记表面活化荧光乳胶微球取0.5ml步骤1)中制备的表面活化的荧光乳胶微球加入1mg碳化二亚胺(edc),1mgn-羟基琥珀酰亚胺(nhs),于室温,120r/min的转速下搅拌3h,然后加入500μl另一株鼠抗人sflt-1单克隆抗体,于室温,120r/min的转速下搅拌6h,再加入50mgbsa封闭液,继续搅拌4h。在2~8℃下,按照11000r/min的转速离心30min,除去上清液。最后,用0.2m的磷酸盐缓冲液(ph=7.4)将固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。3)兔igg多克隆抗体标记表面活化的荧光乳胶微球取0.5ml步骤1)中制备的表面活化的荧光乳胶微球加入1mg碳化二亚胺(edc),1mgn-羟基琥珀酰亚胺(nhs),于室温,120r/min的转速下搅拌3h,然后加入500μlmg羊兔igg多克隆抗体,于室温,120r/min的转速下搅拌6h,再加入50mgbsa封闭液,继续搅拌4h。在2~8℃下,按照11000r/min的转速离心30min,除去上清液。最后,用0.2m的磷酸盐缓冲液(ph=7.4)将固体沉淀物复溶至1ml,再加入1μl的proclin300在4℃下保存待用。4)包被垫的制备将一株鼠抗人sflt-1单克隆抗体和羊抗兔多克隆抗体分别用0.2m的磷酸盐缓冲液(ph=7.4)稀释成1mg/ml,用划膜喷金仪在硝酸纤维素膜(nc膜)上进行划膜。含有一株鼠抗人sflt-1单克隆抗体的作为检测线(t线)5,含有羊抗兔多克隆抗体的作为质控线(c线)6,然后在37℃,湿度<30%的环境下干燥4h制成包被垫。5)标记物垫的制备①将玻璃纤维素膜在0.2m的磷酸盐缓冲液(ph=7.4)中浸泡4h,然后在35℃下干燥6h,备用。②将摩尔比为1:2的另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球和兔igg标记的表面活化的荧光乳胶微球混合均匀后,按照20μl/cm的速度喷涂在玻璃纤维素膜上,然后放置在37℃下干燥4h制成标记物垫。标记物垫上包被有另一株鼠抗人sflt-1单克隆抗体标记的表面活化的荧光乳胶微球和兔igg标记的表面活化的荧光乳胶微球的地方叫做标记物结合处7。设置标记物结合处7的目的同实施例1。6)免疫层析检测卡的组装首先在pvc板1上粘接包被垫2,然后在靠近包被垫2上的质控线6的一端搭接吸水垫,在靠近包被垫2的检测线5的一端搭接标记物垫3及其连接的样品垫9,用切条机切成4mm±0.1mm的试纸条(见图1),将试纸条放入卡壳中制备成孕妇sflt-1免疫层析检测卡。所述卡壳的结构同实施例1。2.检测取60μl的待测样本滴加到步骤1制备的sflt-1免疫层析检测卡的加样孔(对应试纸条的样品垫9)中待测样本,室温静置15min,然后将sflt-1免疫层析检测卡插入到荧光免疫分析仪进行检测,即时可获得检测结果。3.试纸条的评价1)配置不同浓度的sflt-1校准品(0、10、50、400、2000、10000pg/ml),用本实施例4步骤1制备的sflt-1免疫层析检测卡按照步骤2的检测过程依次进行测定,空白检测线不高于10pg/ml,检测范围为10~10000pg/ml。检测结果如表8所示,以样本浓度为横坐标,检测线与质控线的比值(t/c)为纵坐标,用logistic(四参数)进行曲线拟合,拟合度r2分别为0.9957,n=6,制备的sflt-1校准曲线如图6所示,t/c值与校准品在浓度为10-10000pg/ml的范围内具有良好的相关性。表8检测数据标准浓度pg/ml01050400200010000t/c值0.19340.68340.96631.42562.08562.59242)定量限定量限(limitofquantitation,loq),参照clsi发布的ep17-a2文件。依据临床要求和室间质量评价的允许误差,设定本试剂sflt-1的总误差目标为30%。在不考虑分析偏差的情况下,允许总误差(tea)=2cv,即cv=1/2tea。sflt-1浓度在10.00pg/ml时检测的cv为13.19%,小于15%,符合质量目标要求,因此loq=10.00pg/ml,表明sflt-1荧光微球免疫层析检测卡的具有较高的灵敏度。3)精密度抽取三个批次的sflt-1免疫层析检测卡,分别检测浓度为50、400、2000pg/ml的样本进行检测,每个浓度点平行测定10次,计算三个批号检测试纸条的批内变异系数和批间变异系数,从表9中可以看出批间和批内变异系数均小于14.37%,说明sflt-1荧光免疫层析检测卡的精密度较高。表9检测数据4)回收率取三批次浓度为10000pg/ml的sflt-1校准品,分别加入到浓度接近于0的阴性样本中,其中所加入的sflt-1校准品与阴性样本的体积比为1:9,重复测定3次,计算回收率。三批样本校准品回收率的结果分别为97.45%、103.43%、95.34%,回收率均在90%-110%之间,说明测定结果符合标准。附:所需溶液配置(1)0.2m磷酸盐缓冲溶液nah2po4.h2o5.24g;na2hpo4.2h2o28.83g;纯化水定容至1000ml;(2)0.2m硼酸-硼砂缓冲溶液硼砂19.07g;硼酸12.37g;peg20005~30g;纯化水定容至1000ml。以上所述实施例仅是为充分说明本发明而所举的实施例,本发明的保护范围不限于此。本
技术领域:
的技术人员在本发明基础上所作的等同替代或变换,均在本发明的保护范围之内。本发明的保护范围以权利要求书为准。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1