一种同步快速检测维生素A、维生素D3和维生素E的方法与流程
本发明属于分析检测
技术领域:
,具体涉及一种同步快速检测维生素a、维生素d3和维生素e的方法。
背景技术:
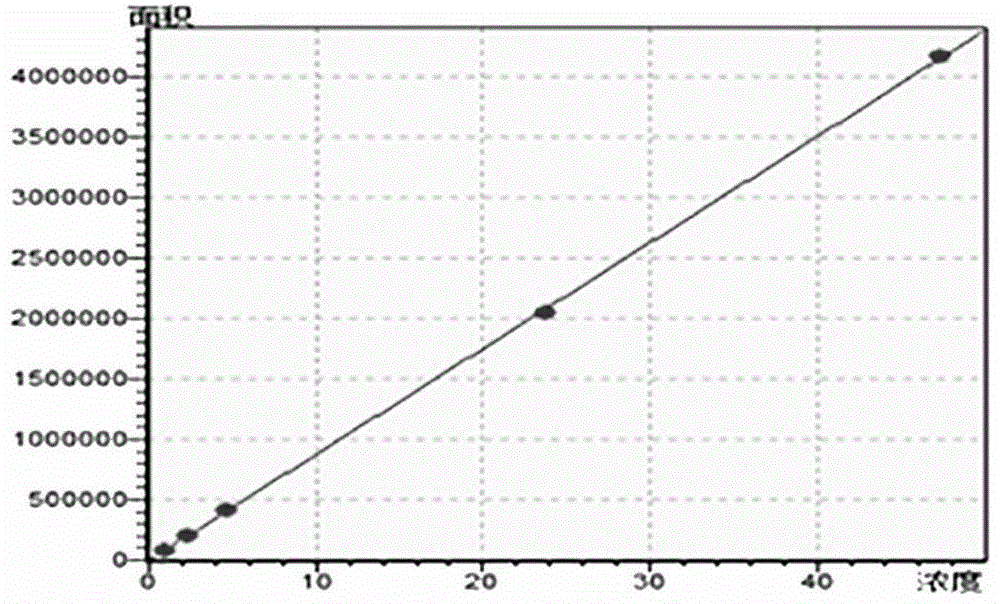
:维生素a、d和e为脂溶性维生素,脂溶性维生素是由长的碳氢链或稠环组成的聚戊二烯化合物。维生素a(维生素a乙酸酯)、维生素d3(胆钙化醇)和维生素e(维生素e乙酸酯)对于人类的健康至关重要,其中,维生素d3是哺乳动物重要的营养成分,具有促进哺乳动物钙磷代谢和成骨的作用,因此,维生素a、维生素d3和维生素e是婴幼儿奶粉和米粉的主要营养成分,也是各种保健食品的重要组成成分。维生素a和维生素e紫外吸收较强并且在食品中的含量较高,一维色谱即可实现这两种化合物的准确定量,但维生素d3含量较低、紫外吸收不强、易受基质干扰,难以通过一维色谱实现其与基质的分离和准确定量,因此,同时定量食品中维生素a、维生素d3和维生素e难以实现。美国分析化学家协会(aoac)采用皂化萃取后lc-ms/ms技术定量奶粉中维生素d3,欧盟采用两套方法定量维生素a、维生素d3和维生素e,即皂化萃取后反相色谱(一维色谱)定量维生素a和维生素e,皂化萃取后离线二维法(正相色谱制备+反相色谱分析)定量维生素d3,而我国的国标gb5009.82-2016囊括以上三种检测方法。目前,普遍采用国标gb5009.82-2016皂化法进行维生素a、d3、e的含量检测,但该检测方法存在检测步骤繁琐、检测前处理复杂、检测专属性不强、测试周期长的问题,并且无法同步检测三种维生素,检测种类不全,无法准确反映被检测样品中维生素的真实含量。另外由于维生素a、d3、e本身不稳定、易氧化、易分解的性质,导致检测难度大,冗长的流程会导致不同实验室间的测试误差加大,数据测试误差导致不必要的复测,从而导致检测成本的提高。技术实现要素:本发明的目的在于解决现有技术中存在的无法同时进行维生素a、维生素d3和维生素e含量检测的问题,提出了一种同步快速检测维生素a、维生素d3和维生素e的方法,可实现维生素a、d3、e的同步检测,能够大幅缩短样品前处理时间,提高工作效率,同时提高了检测精度,降低实验室成本。为了实现本发明的目的,本发明采用如下技术方案:一种同步快速检测维生素a、维生素d3和维生素e的方法,包括如下步骤:(1)采用二甲基亚砜提取待测样品中的维生素a、维生素d3和维生素e,得到的提取液经正己烷震荡萃取、浓缩、复溶后得到样品溶液;(2)配制维生素a、维生素d3、维生素e的标准溶液,按照浓度梯度配制多份标准系列溶液;(3)采用高效液相色谱法对所述样品溶液和标准品溶液进行检测分析,利用外标法得到维生素a、d3、e的含量。进一步的,所述样品溶液的配制包括如下步骤:准确称取待测样品1-3g(准确至0.1mg),置于500ml棕色平底烧瓶中,向待测样品中加入30ml的dmso,在超声波水浴中进行超声提取,水浴温度不超过35度,超声过程中旋摇2-3次以防样品附着瓶底;超声一段时间后取出烧瓶,放置冷却至室温,准确加入100ml正己烷,加盖,设置300次/min的频率剧烈振摇15min,静置分层后再次准确加入100ml正己烷,重复提取一次,静置;待正己烷层变澄清透明,且中间乳化层消失以后,将全部正己烷层萃取液经析相分离纸过滤,备用;依据样品标示量、称样量和提取液用量确定分取量,准确移取一定体积的滤液,置于旋转蒸发器烧瓶中,在不超过40℃条件下缓慢真空蒸发至近干或直接用氮气吹干;残渣用甲醇溶解,并稀释至10ml,过0.22μm微孔滤膜,待测。进一步的,所述超声提取的水浴温度为30-35℃,所述超声提取的时间为20-30min。进一步的,所述高效液相色谱法的色谱条件为:色谱柱:c18色谱柱,规格为柱长250mm,内径4.6mm,粒径5μm;柱温:30±5℃;进样量:10μl;流动相包括流动相a和流动相b,所述流动相a为甲醇,所述流动相b为水,二者体积比为甲醇:水=97:3;流速:1.0ml/min;检测波长:采用多波长检测,波长设置为维生素a325nm,维生素d3264nm,维生素e285nm。进一步的,所述高效液相色谱法采用等度洗脱。进一步的,所述维生素a标准溶液由维生素a标准储备溶液稀释得到,所述维生素d3标准溶液由维生素d3标准储备溶液稀释得到,所述维生素e标准溶液直接采用维生素e标准储备溶液。进一步的,所述标准储备溶液的制备过程为:维生素a标准储备溶液:准确称取50mg(准确至0.01mg)维生素a乙酸酯标准品于50ml棕色容量瓶中,用甲醇溶解定容;置-18℃冰箱保存,有效期3个月。临用前利用紫外分光光度计检测其吸光度值,计算其准确浓度。维生素d3标准储备溶液:准确称取50mg(准确至0.01mg)维生素d3标准品于50ml棕色容量瓶中,用甲醇溶解定容;置-18℃冰箱保存,有效期3个月。临用前利用紫外分光光度计检测其吸光度值,计算其准确浓度。维生素e标准储备溶液:准确称取dl-а-生育酚乙酸酯标准品50mg(准确至0.01mg)于50ml棕色容量瓶中,用甲醇溶解定容;置-18℃冰箱保存,有效期3个月。临用前利用紫外分光光度计检测其吸光度值,计算其准确浓度。进一步的,所述标准系列溶液的配制方法为:准确移取适量所述标准溶液,用甲醇稀释定容配成标准系列溶液,其浓度分别为维生素a标准系列溶液:0.50μg/ml、1.0μg/ml、2.0μg/ml、5.0μg/ml、8.0μg/ml、10.0μg/ml、20.0μg/ml;维生素d3标准系列溶液:0.20μg/ml、0.50μg/ml、1.0μg/ml、2.0μg/ml、5.0μg/ml、8.0μg/ml、10.0μg/ml;维生素e标准系列溶液:20.0μg/ml、40.0μg/ml、80.0μg/ml、100.0μg/ml、200.0μg/ml、300.0μg/ml、500.0μg/ml。进一步的,所述待测样品包括保健食品、婴幼儿奶粉或者米粉。本发明的有益效果:本发明提供的检测方法以二甲亚砜超声溶解取代国标中的皂化过程,以正己烷震荡萃取取代国标中的石油醚反复萃取,且本方法无需用水反复清洗,前处理操作简单,能够大幅缩短前处理时间,并且可实现维生素a、d3、e的同步检测,提高工作效率,同时避免了冗长的操作流程所导致的不同实验室间测试误差的加大,提高了检测精度,避免了因测试数据差异导致的复测,降低实验室成本。附图说明图1为维生素a乙酸酯标准系列溶液的线性响应曲线图;图2为维生素d3标准系列溶液的线性响应曲线图;图3为维生素e乙酸酯标准系列溶液的线性响应曲线图。具体实施方式下面将结合具体实施例对本发明的技术方案进行清楚、完整的描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下,所获得的所有其他实施例,都属于本发明保护的范围。为了进一步理解本发明,下面结合实施例对本发明进行详细说明。实施例1保健食品中维生素a、维生素d3和维生素e的含量检测1、试剂和材料:甲醇:色谱纯;二甲基亚砜:色谱纯;正己烷:色谱纯或分析纯;维生素a乙酸酯标准品:cas:127-47-9,纯度不低于99.0%;维生素d3标准品:cas:67-97-0,纯度不低于99.0%;dl-а-生育酚乙酸酯标准品:cas:7695-91-2,纯度不低于99.0%。2、标准储备溶液:维生素a标准储备溶液(1mg/ml)的制备:准确称取50mg(准确至0.01mg)维生素a乙酸酯标准品于50ml棕色容量瓶中,用甲醇溶解定容;维生素d3标准储备溶液(1mg/ml)的制备:准确称取50mg(准确至0.01mg)维生素d3标准品于50ml棕色容量瓶中,用甲醇溶解定容;维生素e标准储备溶液(1mg/ml)的制备:准确称取dl-а-生育酚乙酸酯标准品50mg(准确至0.01mg)于50ml棕色容量瓶中,用甲醇溶解定容;三份储备溶液均放置于-18℃冰箱保存,有效期3个月;临用前利用紫外分光光度计检测其吸光度值,计算其准确浓度。3、标准溶液:维生素a标准溶液:准确移取1.00ml的维生素a标准储备液于10ml棕色容量瓶中,用甲醇稀释至刻度,摇匀;维生素a标准浓度为100μg/ml,于-18℃保存,有效期为半个月。维生素d3标准溶液:准确移取0.50ml的维生素d3标准储备液于10ml棕色容量瓶中,用甲醇稀释至刻度,摇匀;维生素d3标准浓度为100μg/ml,于-18℃保存,有效期为半个月。维生素e标准溶液:直接采用维生素e标准储备溶液。4、标准系列溶液:准确移取一定体积的维生素a标准溶液、维生素d3标准溶液、维生素e标准溶液置于棕色容量瓶中,加入甲醇稀释定容,摇匀即得混合标准系列溶液,其浓度分别为:维生素a标准系列溶液:0.50μg/ml、1.0μg/ml、2.0μg/ml、5.0μg/ml、8.0μg/ml、10.0μg/ml、20.0μg/ml;维生素d3标准系列溶液:0.20μg/ml、0.50μg/ml、1.0μg/ml、2.0μg/ml、5.0μg/ml、8.0μg/ml、10.0μg/ml;维生素e标准系列溶液:20.0μg/ml、40.0μg/ml、80.0μg/ml、100.0μg/ml、200.0μg/ml、300.0μg/ml、500.0μg/ml。5、样品溶液:准确称取待测样品1-3g(准确至0.1mg),置于500ml棕色平底烧瓶中,向待测样品中加入30-50ml的dmso,置于35℃水浴温度的超声仪中超声提取30min,超声过程中旋摇2-3次以防样品附着瓶底;取出放置冷却至室温,准确加入70-120ml正己烷,加盖,设置300次/min的频率剧烈振摇15min,静置分层后再次准确加入70-120ml正己烷,重复提取一次,静置;待正己烷层变澄清透明,且中间乳化层消失以后,将全部正己烷层萃取液经析相分离纸过滤,备用。依据样品标示量、称样量和提取液用量确定分取量,准确移取一定体积的滤液,置于旋转蒸发器烧瓶中,在不超过40℃条件下缓慢真空蒸发至近干或直接用氮气吹干;残渣用甲醇溶解,并稀释至10ml,过0.22μm微孔滤膜,待测。样品溶液进行液相色谱检测的色谱条件如下:选用规格为柱长250mm,内径4.6mm,粒径5μm的c18色谱柱,或性能相当的色谱柱;柱温为30℃;进样量为10μl;流动相为甲醇和水,二者体积比为甲醇:水=97:3;流动相的流速为1.0ml/min;采用等度洗脱;检测波长设置为325nm,264nm以及285nm三个波长同时检测。采用外标法计算样品溶液中维生素a、维生素d3、维生素e的含量。6、标准系列溶液的线性测定将上述配制好的混合标准系列溶液进样到高效液相仪器中,采用同上述样品溶液一致的色谱条件进行检测分析。混合标准系列溶液进样后,记录相应的色谱数据并绘制线性相关工作曲线,得到图1、图2和图3;并对其数据进行分析,得到如下表1-3所示的结果。表1维生素a乙酸酯标准系列溶液的线性相应浓度(μg/ml)峰面积响应值0.948746962.3701979844.7414089129.48173689123.704205159447.4074175937189.62817191352回归方程y=90416.4x+0相关系数r2=0.9999629注:y为标准系列溶液浓度,x为峰面积响应值。表2维生素d3标准系列溶液的线性相应注:y为标准系列溶液浓度,x为峰面积响应值。表3维生素e乙酸酯标准系列溶液的线性相应浓度(μg/ml)峰面积响应值5.01562959410.031241975920.062484529250.1562104313100.3124214453401.2496859334回归方程y=2140.67x+0相关系数r2=0.9999848注:y为标准系列溶液浓度,x为峰面积响应值。由上述表格数据分析可知,维生素a、维生素d3、维生素e的相关系数分别为0.9999629、0.9998945、0.9999848,曲线线性关系良好,说明利用该检测方法进样的维生素a、维生素d3、维生素e在高效液相色谱仪器上的响应较好,标准曲线范围较宽,可满足保健食品行业不同产品检测的需求。7、准确度试验由于保健食品中维生素含量较高,加标实验操作难度较大,因此针对未加标的保健食品样品进行回收率测定,测得维生素a、维生素d3、维生素e的回收率如表4-6。表4保健食品空白样品维生素a回收率测定结果表5保健食品空白样品维生素d3回收率测定结果表6保健食品空白样品维生素e回收率测定结果上述说明仅为本发明的优选实施例,并非是对本发明的限制,凡在本发明的内容范围内所做出的任何修改、等同替换、改型等,均应包含在本发明的专利保护范围之内。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1