一种检测PIK3CA基因H1047R位点突变的电化学传感器及其制备与应用的制作方法
本发明涉及dna点突变检测技术领域,特别是涉及一种检测pik3ca基因h1047r位点突变的电化学传感器及其制备与应用。
背景技术:
磷酸肌醇3-激酶(pi3k)信号传导途径是许多重要细胞功能的关键调节因子。在癌症和其他病理中之所以能观察到pi3k信号传导的激活,是由于该途径的pi3k催化亚基α(pik3ca)突变的结果。有报道显示,激活pik3ca基因突变也表明人类表皮生长因子受体2(her2)阳性乳腺癌模型中曲妥珠单抗治疗效果不佳。此外,具有不同pik3ca突变的患者亚组可能呈现不同的结果或对特定治疗显示出不同的敏感性。
在cosmic(癌症中的体细胞突变目录)数据库中,pik3cah1047r和pik3cae545k代表了人类肿瘤中两种最常见的pik3ca突变,分别占乳腺癌中检测到的所有pik3ca突变的55%和24%,占所有癌症中pik3ca突变的百分比分别为38%和27%。
目前有一些研究表明,患者携带pik3ca突变受益于pi3k/akt/mtor途径抑制剂,并且pik3ca突变已被提议作为转移性结直肠癌患者中抗egfr治疗的阴性预测生物标志物。
因此,解决癌症患者中的pik3cah1047r突变状态可以提供更准确的分子诊断,从而实现定制的治疗方法。
目前,已有应用sangerdna测序对来自组织的样本进行检测的方法。然而,该方法对低丰度突变的敏感性差(约为20%)。而新一代测序(ngs)技术虽然实现了对肿瘤dna样品的高通量、高灵敏度分析,但由于ngs技术的复杂性和高成本,它们在现行的资源有限的医疗保健环境中难以开展临床常规检测。此外,临床上使用最广泛的pcr方法具有灵敏度特异性高、重复性好、检测快速、操作简单等优点,但操作过程需要不断的温度循环和专门的pcr实验室及荧光pcr仪,从而也限制了该方法在检测pik3cah1047r基因突变上的使用。
技术实现要素:
鉴于以上所述现有技术的缺点,本发明的目的在于提供一种检测pik3cah1047r基因突变的电化学传感器及其制备与应用,用于解决现有技术中pik3cah1047r基因突变检测的灵敏度低、特异性低、操作复杂及成本高等问题。
为实现上述目的及其他相关目的,本发明第一方面提供一种检测pik3ca基因h1047r位点突变的电化学传感器的制备方法,所述方法包括以下步骤:
(1)靶物质的识别和切割:将靶物质互补探针(h)和靶物质(pik3cah1047r基因)溶解,混合,恒温孵育;然后加入核酸内切酶,进行切割,得到切割反应产物;
(2)将步骤(1)所得切割反应产物,加入聚合酶、剪切酶和扩增模板,进行聚合剪切扩增反应,得到扩增产物;
(3)将步骤(2)所得的扩增产物滴加到修饰有捕获探针的工作电极上,孵育反应;
(4)向步骤(3)所得的工作电极上滴加dna自组装结构,孵育反应;
(5)将步骤(4)中所得的工作电极与参比电极及对电极连接到电化学工作站上,加入反应基底液,即得所述电化学传感器。
可选地,步骤(3)中,所述工作电极的制备方法包括以下步骤:
①金电极表面处理:将裸电极表面进行抛光处理,使其表面光洁;
②固定捕获探针:将捕获探针滴涂在处理干净的金电极表面,并孵育;
③封闭电极:用6-巯基乙醇封闭非特异性吸附位点,即得探针修饰的工作电极。
优选地,步骤①中,采用氧化铝粉对所述金电极进行抛光处理。
优选地,步骤②中,所述捕获探针的核苷酸序列如seqidno.9所示,具体为:5’-caaatccatgatgcgcatcattcaccac-3’;更优选地,所述捕获探针为巯基修饰的捕获探针,核苷酸序列为:5′-hs-(ch2)6-aaaaaaaaaacctcaactcacctaacc-3′。
优选地,步骤②中,所述捕获探针的浓度为100~1000nmol/l,优选为200nmol/l。
可选地,步骤(1)中,所述靶物质为突变型pik3cah1047r基因,所述靶物质互补探针(h)与突变型pik3cah1047r基因之间有28个碱基互补配对。
可选地,步骤(1)中,所述靶物质为野生型pik3cah1047r基因,所述靶物质互补探针(h)与野生型pik3cah1047r基因之间有27个碱基互补配对。
可选地,步骤(1)中,所述靶物质互补探针(h)的核苷酸序列如seqidno.2或seqidno.6所示;优选地,所述靶物质互补探针(h)的如seqidno.2所示,核苷酸序列为:5’-caaatccatgatgcgcatcattcaccac-3’。
可选地,步骤(2)中,所述靶物质切割反应产物与扩增模板之间有14个碱基互补配对。
可选地,步骤(2)中,所述扩增模板的核苷酸序列为seqidno.3~5或seqidno.7中的任一种所示;优选地,所述扩增模板的核苷酸序列为:
5’-acctcaactcacctaaccccataaactgctaacacacctcagcgcatcattcatttg-3’。
可选地,步骤(3)中,所述扩增产物与捕获探针之间有18个碱基互补配对。
可选地,步骤(4)中,所述dna自组装结构为h1、h2、h3和d这4条序列的混合物。
可选地,所述dna自组装结构中的序列d的核苷酸序列如seqidno.3~5所示;优选地,所述dna自组装结构中的的序列d的核苷酸序列为:
5’-ccataaactgctaacacatggatggaatgaacggtggaagagtt-3’。
优选地,所述dna自组装结构中,每条序列的终浓度为300nm。
可选地,步骤(1)中,所述核酸内切酶为nsbi核酸内切酶。
可选地,步骤(2)中,所述聚合酶为klenowfragment聚合酶,所述剪切酶为nb.bbvci剪切酶。
可选地,步骤(1)中,所述靶物质互补探针(h)的浓度为100nm,所述nsbi核酸内切酶的浓度为0.2u/l。
可选地,步骤(2)中,所述扩增模板的浓度为100nm。
可选地,步骤(2)中,所述klenowfragment聚合酶和nb.bbvci剪切酶的浓度均为0.2u/l。
可选地,步骤(1)中,所述切割反应时间为15~90min,优选为30~60min,更优选为60min。
可选地,步骤(2)中,所述扩增反应时间为30~180min,优选为100~150min,更优选为120min。
可选地,步骤(3)中,所述孵育反应时间为90min。
可选地,步骤(4)中,孵育时间为15~90min,优选为30~60min,更优选为60min。
可选地,步骤(1)、(3)、(4)中,孵育温度均为37℃。
可选地,步骤(5)中,所述电化学传感器还包括反应基底液,所述反应基底液为1×pbs溶液。
可选地,所述参比电极选自饱和甘汞电极或银氯化银电极(ag/agcl)中的任意一种;优选地,所述参比电极为饱和甘汞电极。
可选地,步骤(5)中,所述对电极为铂丝电极。
本发明第二方面提供一种采用上述方法制备的电化学传感器。
本发明第三方面提供一种采用上述电化学传感器检测样品中的pik3ca基因h1047r位点突变的方法,将上述的工作电极与参比电极、对电极连接到电化学工作站上,以1×pbs溶液为电化学测量的反应基底液,用差分脉冲伏安法(dpv)测定样品中pik3cah1047r基因的含量。
可选地,所述样品选自人血清。上述方法可以是非疾病诊断目的方法,例如用于科研目的,研究pik3cah1047r的致病机理,或者与其他疾病之间的关联等等。
本发明的检测原理阐述如下:
首先,在均相反应体系中,靶物质互补探针可以与突变型pik3cah1047r序列完全互补结合形成双链dna,这条双链中含有一个nsbi酶的特异性的识别位点
如上所述,本发明的检测pik3ca基因h1047r位点突变的电化学传感器及其制备与应用,具有以下有益效果:
(1)本发明构建了一种基于nsbi酶和四联体dna自组装结构的电化学传感器,所述电化学传感器可以灵敏、特异地检测pik3cah1047r基因突变,其线性范围为0.001%-50.0%,线性方程式为i=0.98×lgc+6.77,检测低限为0.001%,线性相关系数为0.9976。
(2)本发明的电化学传感器特异性好、灵敏度高:本发明首先制得靶物质互补探针(h)和扩增模板(template),两条探针的设计增加了对靶物质突变的检测的特异性灵敏度。
(3)本发明首次将nsbi酶和聚合剪切扩增相结合并且用于pik3cah1047r基因突变的检测。
(4)综上所述,本发明成功构建了可用于检测pik3cah1047r基因突变的电化学传感器,应用本发明的传感器,对pik3cah1047r基因突变的测定显示了灵敏度高、稳定性强、重现性好的能力。与现有技术比较,本发明的传感器成本低,灵敏度高,特异性好,操作简便,成本低,有望应用于实际样品和临床标本的测定,发展成为具有临床应用价值的传感器。
附图说明
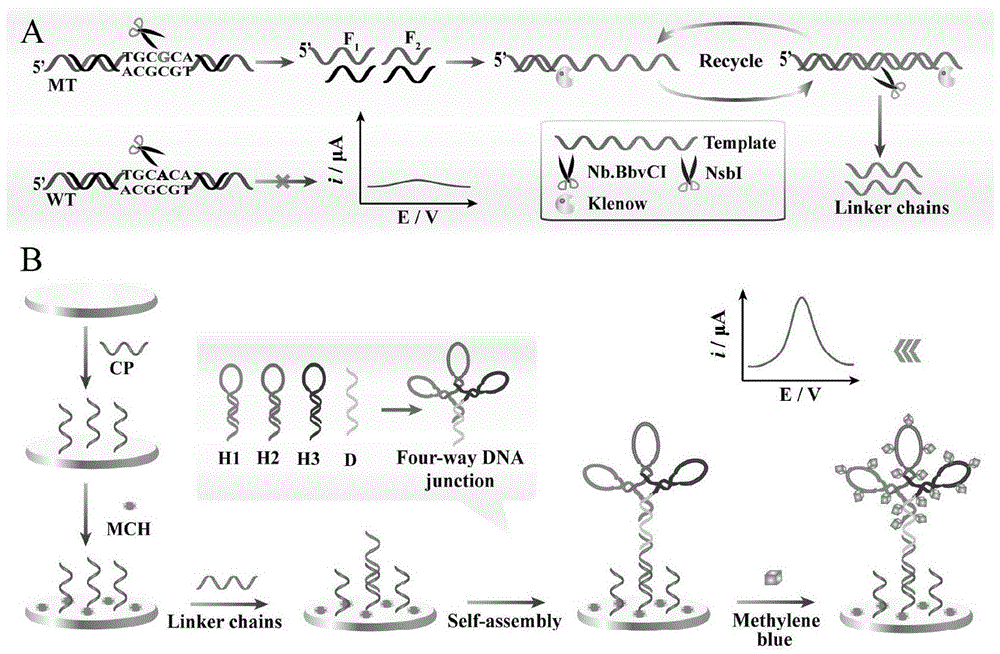
图1为本发明的检测原理图。
图2为本发明中各种探针在工作电极表面逐步组装的过程的eis和cv验证图。
图3为本发明实施例2中nbsi酶介导的聚合剪切反应和四联体dna结构自组装的可行性的电泳验证图。
图4为本发明实施例2中整体可行性的电化学dpv响应曲线图。
图5为本发明实施例3中nbsi酶切割反应时间优化的电化学dpv响应曲线图。
图6为本发明实施例3中聚合剪切反应时间优化的电化学dpv响应曲线图。
图7为本发明实施例3中电极表面自组装反应时间优化的电化学dpv响应曲线图。
图8为本发明中实施例线性范围图。
具体实施方式
以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。
本发明的电化学传感器检测方法的原理为:基于nsbi酶和四联体dna自组装结构用于pik3cah1047r基因突变的检测。
具体实施过程如下:
实施例1
制备电化学传感器并检测pik3cah1047r基因突变
1.材料与方法
1.1材料
nsbi限制酶、klenowfragment(3′→5′exo-)和nb.bbvci及其配套的缓冲液购于上海生工;dntpmixturesolution和亚甲蓝溶液购于上海生工;6-mercapto-1-hexanol(mch)购于sigma-aldrich(中国,上海);hplc纯化的寡核苷酸由上海生工合成;人血清来源于重庆医科大学附属第一医院。
1.2检测仪器
上海辰华chi660d电化学工作站,检测系统为三电极系统,其中,参比电极为ag/agcl电极、对电极为铂丝电极、工作电极为直径3mm的金电极。
1.3检测原理
结合图1和图2所示。
首先,在均相反应体系中,靶物质互补探针可以与突变型pik3cah1047r序列完全互补结合形成双链dna,这条双链中含有一个nsbi酶的特异性的识别位点
1.工作电极的制备
(1)金电极表面处理:
用0.05μm氧化铝粉对金电极进行抛光处理至“镜面状”,去离子水超声清洗3次,每次3min;然后,用食人鱼溶液(h2so4∶h2o2=3∶1)处理金电极10min,去离子水冲洗干净后用洗耳球吹干电极表面。
(2)固定捕获探针:将10μl0.2μmol/l巯基标记的捕获探针滴加在处理好的金电极表面,置于4℃过夜;所述捕获探针为巯基修饰的捕获探针,具体序列为:
5′-sh-aaaaaaaaaacctcaactcacctaacc-3′。
(3)采用mch封闭电极:将捕获探针组装好的金电极表面用1×pbs缓冲液冲洗电极三次后,滴加10μl1mmmch封闭1h;重复冲洗电极得到探针修饰的工作电极备用。
2.采用靶物质互补探针和扩增模板对pik3cah1047r基因突变进行特异性识别、切割和聚合剪切扩增。
(1)特异性识别和切割:将靶物质互补探针(h)和待测靶物质(pik3cah1047r基因)分别溶解于1×剪切缓冲溶液中,37℃条件下恒温孵育30min,然后加入nsbi限制酶,在37℃条件下进行60min酶切反应,在75℃条件下灭活10min,得到切割反应产物。
(2)聚合剪切扩增
将步骤(1)所得切割反应产物,加入聚合酶、剪切酶和扩增模板(template),进行聚合剪切扩增反应;
构建聚合剪切扩增反应体系:
将上述聚合剪切扩增反应体系在37℃下反应2h,获得扩增产物。
(3)将步骤(2)得到的扩增产物滴加到步骤1中制备好的含有捕获探针的工作电极上,在37℃下反应90min。
(4)用1×pbs缓冲液冲洗电极3次后,在电极表面滴加10μl包含终浓度均为300nm的h1,h2,h3和d的混合溶液,37℃条件下反应60min。
(5)向工作电极表面滴加10μl含有0.5mmmb的1×pbs溶液,并室温孵育30min以获得待测的工作电极。
(6)以1xpbs溶液作为电化学测量的反应基底液,将经步骤(5)处理后的待测的工作电极置于其中,以ag/agcl电极为参比电极,以铂丝电极为对电极,在室温下,用差分脉冲伏安法(dpv)测定样品中靶物质的含量。
实施例2
验证pik3cah1047r基因突变电化学传感器的可行性
1.对nsbi介导的切割反应和聚合剪切反应的验证
对实施例1中所得的nsbi识别靶物质和切割靶物质、聚合剪切扩增和整体检测过程用琼脂糖凝胶电泳和电化学过程进行验证,结果如图3和图4所示。
图3中a图显示为nbsi酶介导的聚合剪切反应的电泳验证图,其中:
泳道m为20bpdnamarker;
泳道1为野生型pik3cah1047r基因片段;
泳道2为突变型pik3cah1047r基因片段;
泳道3为靶物质互补探针;
泳道4为nsbi酶不能切割野生型pik3cah1047r基因片段;
泳道5为nsbi酶能切割突变型pik3cah1047r基因片段所得的反应产物;
泳道6为野生型pik3cah1047r基因片段所得的聚合剪切扩增产物;
泳道7为突变型pik3cah1047r基因片段所得的聚合剪切扩增产物。图3中b图显示为四联体dna结构的自组装电泳验证图,其中:
泳道m为50bp的dnamarker;
泳道1为h1;
泳道2为h2;
泳道3为h3;
泳道4为d;
泳道5为h1,h2,h3和d的自组装产物(即四联体dna结构)。
图4显示为本发明整体可行性的电化学响应验证图,其中:
曲线a为空白对照组;
曲线b为野生型pik3cah1047r基因组;
曲线c为突变型pik3cah1047r基因组。
如图3a中第4、5泳道显示,nsbi酶能够识别并切割突变的pik3cah1047r基因,而突变的靶物质则不能被切割。图3-a中第6、7泳道显示,在klenowfragment酶和nb.bbvci酶的作用下能够扩增突变型靶物质的切割产物而不能扩增野生型靶物质。在3a中第7泳道中,能观察到大约40bp的扩增产物。图3b中第5泳道则表示四联体dna结构的成功组装。图4中,当存在野生型的pik3cah1047r基因或者空白组时没有明显的电化学信号;只在存在突变的pik3cah1047r基因时,才能够得到明显的电化学响应。
实施例3
pik3cah1047r基因突变电化学传感器及其使用条件的优化
为进一步优化实验过程中对本发明实验测定影响较大几个的测定条件,即nsbi酶切割时间、聚合剪切扩增反应时间和自组装时间,本实施例对每一个优化条件都由低值到高值分别选取至少五个点进行了一系列实验。
1.为考察nsbi酶切割时间对pik3cah1047r基因突变电化学传感器检测结果的影响,本实验采用了不同的nsbi酶切割反应时间构建电化学传感器。
结果如图5所示,dpv信号强度随反应时间的变化而变化,当nsbi酶切割时间为60min时,信号强度达到平台期,而后续继续增加反应时间信号强度并不明显增加,说明60min为nsbi酶的最佳反应时间。
2.为考察聚合剪切扩增反应时间对pik3cah1047r基因突变电化学传感器检测结果的影响,本实验采用了不同的聚合剪切扩增反应时间构建电化学传感器。
结果如图6所示,在时间少于90min时,dpv信号强度随反应时间的延长而增强,当聚合剪切反应时间大于90min时,信号强度无明显增强,说明90min为聚合剪切扩增的最佳反应时间。
3.为考察自组装时间反应时间对pik3cah1047r基因突变检测结果的影响,本实验采用了不同的自组装时间反应时间构建电化学传感器。
结果如图7所示,随着自组装时间的增加,电极表面四联体dna结构的形成更加完整,dpv信号强度也随反应时间的延长而增强;当自组装反应时间为60min时,信号强度达到最高,其后随着时间的延长信号强度不再增加,说明此时四联体dna结构已经完全形成。因此,选择60min作为自组装反应的最佳时间。
实施例4
制备的pik3cah1047r基因突变电化学传感器的性能分析
为了评估本发明的电化学传感器的性能,在最佳实验条件下,探索所提出的电化学传感器检测的动态范围和灵敏度。
采用实施例1中的电化学传感器,在室温下,用差分脉冲伏安法(dpv)测定样品中(人血清)的电化学信号的变化,绘制标准曲线,结果如图8所示。
从图8可以看出,当pik3cah1047r基因突变率在0.001%到50%之间时,得到的电化学信号与pik3cah1047r基因突变率浓度的对数呈线性相关,线性方程为i=0.98×lgc+6.77,检测限为0.001%,线性相关系数为0.9976。
将传感器在空白溶液中重复检测3次,并重复检测3次,计算平均值和标准差。
实施例5
制备的pik3cah1047r基因突变电化学传感器的稳定性和重现性分析
在最优实验条件下,采用实施例1所构建的电化学传感器分别对0.01%、1.0%和45.0%的生物靶物质(人血清)进行检测,进行三次测定(结果如表1所示),变异系数分别为4.34%、4.70%和5.87%,表明本发明所构建的电化学传感器具有良好的重现性和稳定性。
表1
上述实施例仅例示性说明本发明的原理及其功效,而非用于限制本发明。任何熟悉此技术的人士皆可在不违背本发明的精神及范畴下,对上述实施例进行修饰或改变。因此,举凡所属技术领域中具有通常知识者在未脱离本发明所揭示的精神与技术思想下所完成的一切等效修饰或改变,仍应由本发明的权利要求所涵盖。
sequencelisting
<110>重庆医科大学
<120>一种检测pik3cah1047r基因突变的电化学传感器及其制备与应用
<130>pcqyk197588
<160>9
<170>patentinversion3.5
<210>1
<211>68
<212>dna
<213>artificial
<220>
<223>野生型pik3cah1047r基因
<400>1
ggagtatttcatgaaacaaatgaatgatgcacatcatggtggctggacaacaaaaatgga60
ttggatct68
<210>2
<211>68
<212>dna
<213>artificial
<220>
<223>突变型pik3cah1047r基因
<400>2
ggagtatttcatgaaacaaatgaatgatgcgcatcatggtggctggacaacaaaaatgga60
ttggatct68
<210>3
<211>28
<212>dna
<213>artificial
<220>
<223>靶物质互补探针(h)
<400>3
caaatccatgatgcgcatcattcaccac28
<210>4
<211>57
<212>dna
<213>artificial
<220>
<223>扩增模板
<400>4
acctcaactcacctaaccccataaactgctaacacacctcagcgcatcattcatttg57
<210>5
<211>31
<212>dna
<213>artificial
<220>
<223>捕获探针
<400>5
shchaaaaaaaaaacctcaactcacctaacc31
<210>6
<211>67
<212>dna
<213>artificial
<220>
<223>序列h1
<400>6
ggaggcgttatgaggttgggtggtggtgtcataacgcctccaactcttccaccgtcccac60
tctatca67
<210>7
<211>67
<212>dna
<213>artificial
<220>
<223>序列h2
<400>7
ggaggcgttatgaggttgggtggtggtgtcataacgcctcctgatagagtgggatagtgt60
tgatgaa67
<210>8
<211>67
<212>dna
<213>artificial
<220>
<223>序列h3
<400>8
ggaggcgttatgaggttgggtggtggtgtcataacgcctccttcatcaacactattcatt60
ccatcca67
<210>9
<211>44
<212>dna
<213>artificial
<220>
<223>序列d
<400>9
ccataaactgctaacacatggatggaatgaacggtggaagagtt44
- 还没有人留言评论。精彩留言会获得点赞!