一种激光显微切割获取抗体标记组织单细胞的方法与流程
本发明涉及生物组织单细胞获取技术领域,尤其涉及一种激光显微切割获取抗体标记组织单细胞的方法。
背景技术:
单细胞测序法可以较好地应用于组织中不同细胞的作用机制研究。目前获取单个细胞的方法主要有显微吸取法、流式分选法、显微切割法、微流控分选等。现有的方法大多存在获取细胞较为耗时(三、四个小时以上)、分选中对细胞大小及组织占比等要求限制较多、不能大量精准获取目标细胞、细胞在体位置信息丢失等问题。显微切割技术具有可定位获取细胞的优势,但目前应用于单细胞研究很少,现有的研究报道大多采用固定方式处理组织细胞,切割获得的单细胞主要用于pcr扩增,难以大量获得有效细胞用于单细胞测序。
技术实现要素:
有鉴于此,本发明提供了一种激光显微切割获取抗体标记组织单细胞的方法,该方法可以快速、较大量、在原位精准获取目标单细胞。
为解决以上问题,本发明提供了一种激光显微切割获取抗体标记组织单细胞的方法,包括以下步骤:
s1.将动物麻醉后,取目标动物组织置于干冰上速冻,所述目标动物组织中含有目标单细胞;
s2.将所述目标动物组织在冰冻切片机中进行冰冻切片,得到组织切片,将所述组织切片贴于显微切割专用膜片上,得到贴有组织切片的膜片;
s3.根据所述目标单细胞的类型选择携带有荧光标记物的特异性抗体溶液,将所述贴有组织切片的膜片放入干燥盒中低温干燥10分钟,然后放置在0~4℃冰箱中用携带有荧光标记物的特异性抗体溶液孵育10~15分钟对所述组织切片中的目标单细胞进行原位快速标记,然后在0~4℃温度条件下以depc水溶液浸泡洗涤1分钟;
s4.将步骤s3处理得到的贴有组织切片的膜片低温干燥后,采用激光显微切割获取目标单细胞,置于裂解液中,快速离心,得到单细胞样本并置于干冰中保存。
优选的,所述组织切片的厚度略大于所述目标单细胞的胞体直径。
优选的,步骤s4中所述采用激光显微切割获取目标单细胞具体为:在明场模式下找到组织,切换到荧光模式定位荧光标记的细胞;利用软件圈出目标细胞,激发激光自动按圈出的形状切割获得目标细胞。
优选的,所述动物为大鼠或小鼠。
优选的,所述荧光标记物为绿色荧光标记物。
优选的,所述特异性抗体溶液为特异性抗体稀释溶液,所述特异性抗体稀释溶液中特异性抗体与抗体稀释液的体积比为1:50~100。
优选的,所述目标单细胞为动物神经细胞。
本发明还提供了一种上述方法在pcr扩增或者单细胞测序分析中的应用。
与现有技术相比,本方法采用低温法处理动物组织,不对动物组织进行固定,在较短时间(0.5-1小时)内,在动物组织原位通过优化的免疫组化法快速标记识别目标细胞,采用激光显微切割法,可快速、较大量、精准获取目标细胞,可用于组织占比较低、细胞体积较大、细胞形态不规则、难以分离培养获得的特殊细胞(如在脊髓中仅占5%的成年大鼠脊髓前角运动神经元),获得的单细胞所在位置信息清晰,采用低温法可以较好的保持细胞rna活性,rna降解少,可用于pcr扩增及要求较高的单细胞测序研究。
附图说明
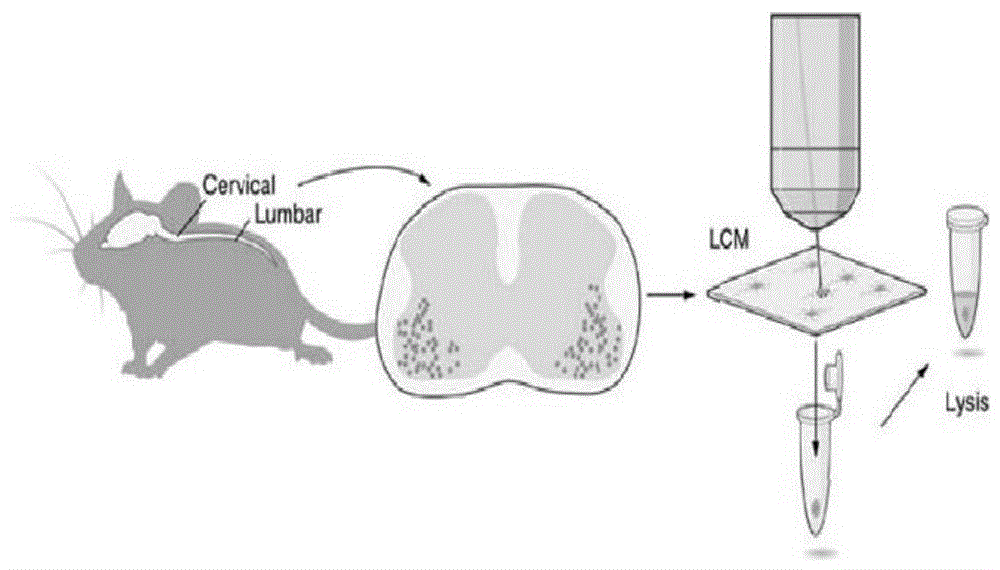
图1本发明实施例1提供的激光显微切割获取抗体标记组织单细胞方法流程示意图;
图2本发明实施例1中激光显微切割前后大鼠脊髓前角运动神经元示意图,a图为显微切割前脊髓前角,图中箭头所指绿色荧光细胞即为显微切割目标神经元;b图为显微切割后脊髓前角,图中圆圈即为显微切割轨迹,圈内黑色区域为已经切割去除目标神经元;c图为明场拍摄的显微切割收集管盖,箭头所指即为切割后从膜上掉落到收集管盖的运动神经元;d图为荧光场拍摄的显微切割收集管盖,箭头所指即为切割后从膜上掉落到收集管盖的具有绿色荧光的运动神经元。
具体实施方式
为了进一步理解本发明,下面结合实施例对本发明优选实施方案进行描述,但是应当理解,这些描述只是为了进一步说明本发明的特征和优点,而不是对本发明权利要求的限制。
本发明所有原料,对其来源没有特别限制,在市场上购买的或按照本领域技术人员熟知的常规方法制备的即可。
实施例1:获取成年大鼠脊髓神经元
如图1所示,获取成年大鼠脊髓神经元单细胞的具体步骤如下:
(1)成年大鼠麻醉后,快速取脊椎置于干冰上速冻;(从此步开始,全程低温操作保持组织细胞活性,防止rna降解)
(2)截取腰膨大部位,冰冻切片机中切片(片厚30微米),贴于显微切割专用膜片上;
(3)将贴有切片的显微切割专用膜片放入干燥盒中干燥10分钟,0-4℃用特异性标记运动神经元的chat抗体孵育10分钟(脊髓运动神经元的标记采用特异标记抗体chat,以1:100高浓度稀释,抗体携带绿色荧光标记神经元细胞),0-4℃以depc水溶液浸泡洗涤1分钟;本步骤的目的在于通过免疫组化法抗体快速标记目标细胞。
(4)将贴有荧光标记后的切片的显微切割专用膜片干燥后用激光显微切割获取脊髓神经元细胞,置于裂解液中,快速离心,干冰中保存所获得的单细胞样品;
具体切割过程为:启动激光显微切割系统;将膜片凸面朝下放于样品板上,装入显微镜载物台;在明场模式下找到组织,切换到荧光模式定位荧光标记的细胞,利用软件圈出目标细胞,激发激光自动按圈出的形状进行切割,切割圈内部位由于重力作用落入下方收集管中。图2显示了激光显微切割前后大鼠脊髓前角运动神经元示意图。
(5)对所获得的单细胞抽提rna,以smart-seq2方法对单细胞rna进行逆转录扩增,agilent2100(highsensitivitydnaassay)检测扩增产物浓度和片段大小,检测结果显示样本合格率可以达到60%以上,合格样本可以进一步建库测序或用作pcr扩增模板。
实施例2:获取成年小鼠黑质多巴胺能神经元
(1)成年小鼠麻醉后,快速取脑置于干冰上速冻;(从此步开始,全程低温操作保持组织细胞活性,防止rna降解)
(2)截取脑黑质部位,冰冻切片机中切片(片厚12微米),贴于显微切割专用膜片上;
(3)切好的片子放入干燥盒中干燥10分钟,0-4℃用特异性标记运动神经元的th抗体孵育10分钟(黑质多巴胺能神经元的标记采用特异标记抗体th,以1:100高浓度稀释,抗体携带绿色荧光标记神经元细胞),0-4℃以depc水溶液浸泡洗涤1分钟;(免疫组化法抗体快速标记目标细胞)
(4)干燥后激光显微切割获取脊髓神经元细胞,置于裂解液中,快速离心,干冰中保存所获得的单细胞样品;本步骤中具体切割过程同实施例1.
(5)对所获得的单细胞抽提rna,以smart-seq2方法对单细胞rna进行逆转录扩增,agilent2100(highsensitivitydnaassay)检测扩增产物浓度和片段大小,检测结果显示样本合格率可以达到60%以上,合格样本可以进一步建库测序或用作pcr扩增模板。
以上显示和描述了本发明的基本原理和主要特征和本发明的优点,对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
- 还没有人留言评论。精彩留言会获得点赞!