非洲猪瘟病毒的检测试纸、试剂盒及其制备方法与流程
本发明属于动物疫病检测技术领域,具体涉及非洲猪瘟病毒的检测试纸、试剂盒及其制备方法。
背景技术:
非洲猪瘟(asf)是由非洲猪瘟病毒(asfv)所引起的猪的一种出血性、高致死率、病毒性传染病。所有的日龄的猪都易感染。asf自然感染的潜伏期长,自然感染为4~19天。感染后平均死亡时间为2-10天,临床上表现形式有高热、食欲废绝、皮肤和内脏器官出血等,其临床症状与猪瘟、猪丹青病毒相似。猪或者野猪感染非洲猪瘟病毒后,其潜伏期通常为3-15d,强毒株感染的死亡率可达到100%,世界动物卫生组织(oie)认为,在asf流行疫区和低毒力asfv感染初期地区进行调查、诊断,血清学方法是首推的诊断方法,而以纯化获得的重组蛋白作为检测原,优势明显。
非洲猪瘟病毒属于非洲猪瘟病毒属,是双链dna病毒,也是唯一的虫媒dna病毒。asfv基因组为末端共价闭合的双股线状dna,长度为170kb~190kb,具有末端交联和反转重复区,其编码151-167种蛋白,成熟的病毒粒子包含有约50多种结构蛋白。其中由p72结构蛋白组成的核衣壳蛋白含量占到全部病毒蛋白的1/3,是结构蛋白中含量最多的。p72存在于病毒衣壳的表面,具有较好的免疫原性和抗原性,能够诱导机体产生中和抗体,因而是血清学检测的主要抗原区,也是用于asfv诊断检测的主要蛋白,为建立无感染性的、快速、灵敏的血清学检测方法奠定了基础。在抗原抗体的结合反应中,抗原参与结合的部位称为抗原的表位,抗原表位是蛋白质抗原性的基础,目前技术中普遍采用的抗原表位肽,免疫原性仍较弱、特异性较差,因此亟需一种免疫原性强、特异性好的非洲猪瘟病毒p72重组抗原蛋白,并可依此重组抗原蛋白制备与其结合的单克隆抗体或多克隆抗体,还可进一步利用得到的抗体对非洲猪瘟病毒进行检测。
此外,传统的诊断检测非洲猪瘟病毒的方法有分子生物学方法、酶联免疫试剂盒方法,其中分子生物学方法以聚合酶链式反应(pcr)为代表,通过检测病毒分子来确认动物是否被感染,其操作繁琐,试剂和设备昂贵,对于猪场来说难以操作;酶联免疫法利用96孔酶标板为载体,以抗原抗体特异性反应为原理检测动物是否感染asf病毒,具有灵敏度高、特异性好等特点,美中不足的是操作过程较为繁琐,加样精准度要求高,且需要酶标仪、恒温箱等实验设备来确保反应环境,基层养殖场、特别是现场检测时难以开展;以上方法均不能达到快速检测的目的。目前使用最广泛的是胶体金检测试纸条,同样利用抗原抗体反应原理,检测非洲猪瘟病毒抗原,其操作简便、反应时间短,但缺陷是灵敏度不够高,可能存在假阴性或者假阳性,特别针对asfv的快速检测时,由于样品多是全血、组织样本等,样本成分复杂,无法进行长时间前处理,使得试纸条可能出现干扰、特异性差等问题,难以满足快速检测asfv的要求。
技术实现要素:
本发明解决的技术问题是提供非洲猪瘟病毒的检测试纸、试剂盒及其制备方法,检测试纸可用于非洲猪瘟病毒的快速、高特异性、高灵敏度检测。
为了解决上述问题,本发明提供一种非洲猪瘟病毒的检测试纸,包括背板,背板上依次排列设置样品垫、乳胶微球垫、硝酸纤维素膜和吸水垫;乳胶微球垫上包被有乳胶微球标记的标记抗体;硝酸纤维素膜上设有检测线和质控线,检测线处包被有捕获抗体,检测线靠近乳胶微球垫一侧设置;质控线处包被有羊抗鼠抗抗体,质控线靠近吸水垫一侧设置;标记抗体为由保藏编号为cgmccno.18540的杂交瘤细胞7a7分泌产生的单克隆抗体或由保藏编号为cgmccno.18539的杂交瘤细胞3e5分泌产生的单克隆抗体,捕获抗体为非洲猪瘟病毒抗体。
其中,捕获抗体可以是非洲猪瘟病毒单克隆抗体或多克隆抗体中的一种或多种的混合;更具体的,可以是非洲猪瘟病毒抗体、非洲猪瘟病毒p72蛋白抗体、非洲猪瘟病毒p72重组蛋白抗体中的一种或多种的混合;优选地,捕获抗体为前述的非洲猪瘟病毒p72重组蛋白抗体;进一步优选的,捕获抗体为非洲猪瘟病毒p72重组蛋白单克隆抗体。并且,捕获抗体与标记抗体不同。
优选地,标记抗体为由保藏编号为cgmccno.18540的杂交瘤细胞7a7分泌产生的单克隆抗体,捕获抗体为由保藏编号为cgmccno.18539的杂交瘤细胞3e5分泌产生的单克隆抗体。
优选地,标记抗体为由保藏编号为cgmccno.18539的杂交瘤细胞3e5分泌产生的单克隆抗体,捕获抗体为由保藏编号为cgmccno.18540的杂交瘤细胞7a7分泌产生的单克隆抗体。
优选地,样品垫包括第一样品垫、第二样品垫和第三样品垫,第一样品垫、第二样品垫和第三样品垫上分别浸润不同的缓冲液,按照第三样品垫、第二样品垫、乳胶微球垫、第一样品垫的顺序依次交错设置。
优选地,非洲猪瘟病毒的检测试纸还包括滤血膜,滤血膜设于第二样品垫与乳胶微球垫之间。
优选地,第一样品垫的靠近硝酸纤维素膜的一端与检测线的距离为4-10mm。
优选地,第一样品垫与硝酸纤维素膜的重叠部分长度为1.5-2.0mm。
优选地,乳胶微球垫与第一样品垫的重叠部分长度为1-1.5mm。
优选地,滤血膜与乳胶微球垫的重叠部分长度为2.5-3.0mm。
优选地,第二样品垫与滤血膜的重叠部分长度为9.0-9.5mm。
具体地,第一样品垫、第二样品垫和第三样品垫可为玻璃纤维垫或纤维素垫或者纺织聚合物垫。
具体地,吸水垫为玻璃纤维垫。
具体地,背板为pvc背板。
本发明还提供了一种制备上述的非洲猪瘟病毒的检测试纸的方法,包括以下步骤:
s1.非洲猪瘟病毒p72重组蛋白单克隆抗体的制备:使用非洲猪瘟病毒p72重组蛋白免疫动物通过杂交瘤技术得到上述的非洲猪瘟病毒p72重组蛋白单克隆抗体;
s2.乳胶微球垫的制备:使用乳胶微球标记步骤s1得到的非洲猪瘟病毒p72重组蛋白单克隆抗体,然后将得到的乳胶微球标记的标记抗体包被于玻璃纤维垫中,得到乳胶微球垫;
s3.硝酸纤维素膜的制备:在硝酸纤维素膜上喷涂捕获抗体得到检测线,然后喷涂羊抗鼠抗抗体得到质控线;
s4.试纸的组装:在背板上依次相互交错的设置样品垫、乳胶微球垫、硝酸纤维素膜和吸水垫,得到非洲猪瘟病毒的乳胶微球检测试纸。
具体地,步骤s1非洲猪瘟病毒p72重组蛋白单克隆抗体的制备具体包括以下步骤:
s11.非洲猪瘟病毒p72重组基因的合成:通过dnastar及iedb数据库对非洲猪瘟病毒p72蛋白的优势表位进行分析,将其优势经b细胞表位预测进行串联表达,得到seqidno.4序列并进行基因合成,将得到的非洲猪瘟病毒p72重组基因插入puc载体,得到puc-p72;
s12.基因克隆及载体构建:根据seqidno.4基因序列设计引物,分别在上下游引物的近5’端添加bamhi和sali酶切位点,以puc-p72基因为模板扩增目标片段,双酶切后,扩增产物经琼脂糖凝胶电泳鉴定,与表达载体pfastbacht-b连接得到重组表达载体pfastbacht-p72,构建成功后测序鉴定;
s13.重组基因工程菌的构建、诱导表达及纯化:将阳性重组质粒pfastbacht-p72转座dh10bac感受态细胞,通过卡那霉素-四环素-庆大霉素和蓝白斑筛选阳性克隆,提取杆状病毒质粒,转染sf9昆虫细胞,收集重组杆状病毒,将重组杆状病毒以moi0.1感染sf9昆虫细胞,离心收集上清,得到非洲猪瘟病毒p72重组蛋白;
s14.免疫动物及p72单克隆抗体制备、筛选:使用非洲猪瘟病毒p72重组蛋白免疫动物,得到非洲猪瘟病毒p72重组蛋白多克隆抗体,或使用非洲猪瘟病毒p72重组蛋白免疫动物,将动物免疫后脾细胞与瘤细胞杂交,经筛选得到杂交瘤细胞,然后利用非洲猪瘟病毒p72重组蛋白筛选特异性抗体,并用猪瘟病毒活疫苗、猪伪狂犬活疫苗、猪繁殖与呼吸综合征活疫苗、猪细小病毒培养液、猪圆环病毒2型细胞培养液等猪易感染病毒做交叉筛选,获得非洲猪瘟病毒p72重组蛋白单克隆抗体。
具体地,步骤s2乳胶微球垫的制备具体包括以下步骤:
s21.制备乳胶微球标记的标记抗体;
s22.使用乳胶微球标记的检测抗体浸润玻璃纤维垫,得到乳胶微球垫。
具体地,步骤s2中制备乳胶微球标记的标记抗体的方法包括以下步骤:
s211.乳胶微球的清洗:使用标记缓冲液清洗乳胶微球至少两遍;
s212.乳胶微球的活化:将nhs和edc加入标记缓冲液中,然后加入清洗后的乳胶微球,室温孵育活化,得到乳胶微球缓冲液;
s213.乳胶微球的标记:将步骤s1得到的非洲猪瘟病毒p72重组蛋白单克隆抗体加入步骤s212得到的乳胶微球缓冲液中,室温孵育;然后加入封闭液,室温孵育;将得到的产物离心,弃上清,并加入标记缓冲液重悬乳胶微球,得到乳胶微球标记的标记抗体。
具体地,步骤s3硝酸纤维素膜的制备具体包括以下步骤:
s31.捕获抗体的制备:利用非洲猪瘟病毒或非洲猪瘟病毒p72蛋白或非洲猪瘟病毒p72重组蛋白多次免疫动物,纯化后得到非洲猪瘟病毒多克隆抗体或非洲猪瘟病毒p72蛋白多克隆抗体或非洲猪瘟病毒p72重组蛋白多克隆抗体,或采用前述方法制备非洲猪瘟病毒单克隆抗体、非洲猪瘟病毒p72蛋白单克隆抗体或非洲猪瘟病毒p72重组蛋白单克隆抗体;
s32.划膜:用划膜仪将捕获抗体和羊抗鼠抗抗体分别喷涂在硝酸纤维素膜上,形成检测线和质控线。
本发明与现有技术相比,具有以下有益效果:
1.本发明通过dnastar及iedb数据库对非洲猪瘟病毒p72蛋白的优势表位进行分析,为使蛋白n端和c端抗原表位更容易暴露出来,给抗体库的筛选提供更多的选择,对该两个主要抗原表位区域进行串联表达,以柔性氨基酸片段为linker,在保留了较多的氨基酸的同时尽量减小其空间位阻的影响,获得了免疫原性强的重组蛋白,并以此重组蛋白免疫动物,通过杂交瘤细胞技术筛选得到保藏编号为cgmccno.18540的杂交瘤细胞7a7、保藏编号为cgmccno.18539的杂交瘤细胞3e5分泌的特异性强的单克隆抗体,以此单克隆抗体制备得到的非洲猪瘟病毒检测试纸对非洲猪瘟病毒p72蛋白具有高特异性和高灵敏性;
2.本发明提供的非洲猪瘟病毒的乳胶微球检测试纸,乳胶微球具有均一度高,单分散性好、稳定性好等优点,用乳胶微球作为标记物,制得的检测试纸具有批次差异小,检测灵敏度高的优势,利用其制成的非洲猪瘟病毒的乳胶微球检测试纸,检测时无需有机试剂,无需恒温箱和酶标仪等设备,无需专门的场地,只要有采集好的样本和操作台面即可完成检测,操作简便、快速,整体耗时短,无需特殊培训,检测灵敏度高,特异性好特别适合用于现场、基层实验室等领域的检测,且检测结果可定性定量,在有读数仪的情况下,可以通过测定检测线和质控线的显色值并绘制校准曲线,定量检测抗原浓度;
3.本发明提供的非洲猪瘟病毒的乳胶微球检测试纸的制备方法,操作简便、所需原料简单,可以在较短时间内制备成功,能产生较大经济效益。
生物保藏信息说明
杂交瘤细胞7a7于2019年10月24日保藏于中国微生物菌种保藏管理委员会普通微生物中心,地址为北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所,邮编为100101,保藏编号为cgmccno.18540。
杂交瘤细胞3e5于2019年10月24日保藏于中国微生物菌种保藏管理委员会普通微生物中心,地址为北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所,邮编为100101,保藏编号为cgmccno.18539。
附图说明
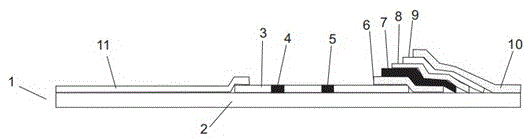
图1是本发明实施例所述的非洲猪瘟病毒的乳胶微球检测试纸的结构示意图;
图2是本发明实施例所述的非洲猪瘟病毒的乳胶微球检测试纸的剖面图;
图3是本发明实施例所述的非洲猪瘟病毒的乳胶微球检测试纸的俯视图;
图4是本发明实施例得到的非洲猪瘟病毒p72重组蛋白的抗原鉴定图;
图5是本发明实施例得到的非洲猪瘟病毒p72重组蛋白单克隆抗体与猪常见病毒交叉反应的鉴定结果图;
图6是本发明实施例得到的非洲猪瘟病毒乳胶微球检测试纸对p72蛋白浓度定量的标准曲线。
其中:1-非洲猪瘟病毒的乳胶微球检测试纸;2-背板;3-硝酸纤维素膜;4-质控线;5-检测线;6-第一样品垫;7-乳胶微球垫;8-滤血膜;9-第二样品垫;10-第三样品垫;11-吸水垫。
具体实施方式
下面将结合本发明的实施例,对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1非洲猪瘟病毒p72重组蛋白单克隆抗体的制备
1.非洲猪瘟病毒p72重组蛋白基因克隆及重组表达载体构建
根据genbank公布的非洲猪瘟病毒p72基因序列(序列号:aat84439.1)作为参考,设计优化基因序列,为使抗原的n/c端抗原表位更容易暴露出来,显现出更多的优势,从而筛选到比较合适的单克隆抗体,本发明通过dnastar及iedb数据库对该蛋白序列优势表位区域进行分析,以ggggs为linker对该两个主要抗原表位区域进行串联表达,两个抗原表位区域的氨基酸序列分别为seqidno.1和seqidno.2,在保留了较多的氨基酸的同时尽量减小其空间位阻的影响。优化后的非洲猪瘟病毒p72重组蛋白基因的核苷酸序列如seqidno.4,非洲猪瘟病毒p72重组蛋白的氨基酸序列如seqidno.3。
所述seqidno:1的序列结构如下:
lnsrisniknvnksygkpdpeptlsqieethlvhfnahfkpyvpvgfeynkvrphtgtptlgnkltfgipqygdffhdmvghhilgachsswqdapiqgtsqmgahgqlqtfprngydwdnqtplegavytlvdpfgrpivpgtknayrnlvyyceypgerlyenvrfdvngnsldeyssdvttlvrkfcipgdkmtgykhlvgqevsvegtsgpllcnihdlhkphqskpiltdendtqrtcshtnpkflsqhfpenshniqtagkqditpitdatyldirrnvhyscngpqtpkyyqp。
所述seqidno:2的序列结构如下:
twnisdqnphqhrdwhkfghvvnaimqpthhaeisfqdrdtalpdacssisdispvtypitlpiiknisvtahginlidkfpskfcssyipfhyggnaiktpddpgammitfalkpreeyqpsghinvsrarefyiswdtdyvgs。
所述seqidno:3的序列结构如下:
lnsrisniknvnksygkpdpeptlsqieethlvhfnahfkpyvpvgfeynkvrphtgtptlgnkltfgipqygdffhdmvghhilgachsswqdapiqgtsqmgahgqlqtfprngydwdnqtplegavytlvdpfgrpivpgtknayrnlvyyceypgerlyenvrfdvngnsldeyssdvttlvrkfcipgdkmtgykhlvgqevsvegtsgpllcnihdlhkphqskpiltdendtqrtcshtnpkflsqhfpenshniqtagkqditpitdatyldirrnvhyscngpqtpkyyqpggggstwnisdqnphqhrdwhkfghvvnaimqpthhaeisfqdrdtalpdacssisdispvtypitlpiiknisvtahginlidkfpskfcssyipfhyggnaiktpddpgammitfalkpreeyqpsghinvsrarefyiswdtdyvgs。
所述seqidno:4的序列结构如下:
ctgaatagcaggatctctaacattaaaaatgtgaacaaaagttatgggaaacccgatcccgaacccactttgagtcaaatcgaagaaacacatttggtgcattttaatgcgcattttaagccttatgttccagtagggtttgaatacaataaagtacgcccgcatacgggtacccccaccttgggaaacaagcttacctttggtattccccagtacggagactttttccatgatatggtgggccatcatatattgggtgcatgtcattcatcctggcaggatgctccgattcagggcacgtcccagatgggggcccatgggcagcttcaaacgtttcctcgcaacggatatgactgggacaaccaaacacccttagagggcgccgtttacacgcttgtagatccttttggaagacccattgtacccggcacaaagaatgcgtaccgaaacttggtttactactgcgaataccccggagaacgactttatgaaaacgtaagattcgatgtaaatggaaattccctagacgaatatagttcggatgtcacaacgcttgtgcgcaaattttgcatcccaggggataaaatgactggatataagcacttggttggccaggaggtatcggtggagggaaccagtggccctctcctatgcaacattcatgatttgcacaagccgcaccaaagcaaacctattcttaccgatgaaaatgatacgcagcgaacgtgtagccataccaacccgaaatttctttcacagcattttcccgagaactctcacaatatccaaacagcaggtaaacaagatattactcctatcacggacgcaacgtatctggacataagacgtaatgttcattacagctgtaatggacctcaaacccctaaatactatcagcccggaggaggaggttccacctggaacatctccgatcaaaatcctcatcaacaccgagattggcacaagttcggacatgttgttaacgccattatgcagcccactcaccacgcagagataagctttcaggatagagatacagctcttccagacgcatgttcatctatatctgatattagccccgttacgtatccgatcacattacctattattaaaaacatttccgtaactgctcatggtatcaatcttatcgataaatttccatcaaagttctgcagctcttacatacccttccactacggaggcaatgcgattaaaacccccgatgatccgggtgcgatgatgattacctttgctttgaagccacgggaggaataccaacccagtggtcatattaacgtatccagagcaagagaattttatattagttgggacacggattacgtggggtct。
用primer和dnastar设计扩增引物,其扩增序列如seqidno.4,并在引物中引入酶切位点bamhi和sali,引物序列由上海生工合成。设计的引物序列如下:
上游引物:ccggatccctgaatagcaggatctctaac
下游引物:acgcgtcgacctaagaccccacgtaatccgt
将得到的重组p72基因插入puc载体中(由北京擎科生物技术有限公司完成),以puc-p72质粒为模板,用pcr方法扩增。反应条件为:95℃预变性5min,95℃变性30s,退火条件为60℃30s,72℃延伸1min,27个循环后,再72℃延伸5min,4℃终止反应。纯化的pcr产物与表达载体pfastbachtb分别进行双酶切后,经琼脂糖凝胶电泳鉴定后,用t4dna连接酶4℃连接过夜,连接产物转化dh5α感受态细胞。阳性重组质粒命名为pfastbacht-p72。
2.非洲猪瘟病毒p72重组蛋白的诱导表达
将阳性重组质粒转座dh10bac感受态细胞,通过用ktg抗生素和蓝白斑筛选阳性克隆,提取杆状病毒质粒(bacmid),转染sf9昆虫细胞,观察转染后的细胞病变并收集重组杆状病毒。将重组杆状病毒以moi0.1感染sf9昆虫细胞,4d后5000r/min离心10min收集上清。而后进行sds-page电泳检测,结果表明在约50.3kda处出现特异性条带,即p72蛋白表达成功。
3.非洲猪瘟病毒p72重组蛋白的纯化及鉴定
目的蛋白的纯化参照ni-nta纯化系统说明书(ge公司)进行。纯化后的蛋白用bradford蛋白浓度测定试剂盒(北京康为世纪生物科技有限公司)测定蛋白含量,以sds-page鉴定纯度后分装,-80℃保存备用。
以westernblot鉴定非洲猪瘟病毒p72重组蛋白抗原性:
纯化蛋白煮样后进行sds-page电泳,通过湿法转印至nc膜上;经5%脱脂奶粉封闭后加入一抗(asfv阳性血清,由中国动物疫病预防控制中心提供),37℃孵育2h,tbst洗涤3次,10min/次;然后加入二抗(兔抗猪igghrp,1:3000稀释,sigma),37℃孵育1h,继续tbst洗涤3次,10min/次;最后加入二氨基联苯胺dab底物显色,以去离子水终止反应,拍照保存结果,在50.3kda处显示特异性条带,如图4所示,右侧条带即为非洲猪瘟病毒p72重组蛋白。
以elisa法鉴定非洲猪瘟病毒p72重组蛋白抗原性:
将纯化的非洲猪瘟病毒p72重组蛋白用0.05m碳酸盐缓冲液(ph9.6)稀释至2μg/ml按照每孔50μl包被酶标板,4℃过夜包被,然后以pbst洗板3次,250μl/孔,每次60s,然后以200μl1%明胶(1g明胶溶于100mlpbs,ph7.2~7.4,过滤除菌)封闭酶标板,37℃封闭2小时;继续pbst洗板1次;
再取非洲猪瘟asfv阳性血清、猪瘟病毒(csfv)阳性血清、猪伪狂犬病毒(prv)阳性血清、高致病性猪繁殖与呼吸综合征病毒(prrsv)阳性血清、猪细小病毒(ppv)阳性血清、猪圆环病毒2型(pcv-2)阳性血清、spf猪血清、空白pbs对照各50μl加入不同孔中(均已1:20稀释),37℃孵育30min;弃去孔中液体,洗板3次;
加入hrp酶标二抗50μl每孔,继续37℃孵育30min;弃去孔中液体,洗板3次;加入tmb底物,50μl每孔,37℃孵育10min,再以2m硫酸终止反应;酶标仪读取450nm吸光度值。
结果显示空白对照及阴性对照的od450nm值应均小于0.25,而阳性血清的od450nm值大于1.0,即所纯化的重组p72蛋白具有良好的抗原性,可与asfv阳性血清反应,而与csfv阳性血清、prv阳性血清、prrsv阳性血清、ppv阳性血清、pcv-2阳性血清及asfv阴性血清不反应。
4.非洲猪瘟病毒p72重组蛋白单克隆抗体的制备
将非洲猪瘟病毒p72重组蛋白按照20μg/次/只的剂量免疫balb/c小鼠,首次免疫时与等剂量的弗氏完全佐剂混合乳化,后续免疫时与等量的弗氏不完全佐剂混合乳化。多次免疫后采集血清测定效价,测定结果见表1,挑选血清效价较高的3#小鼠,利用40μg/只的剂量腹腔注射加强免疫,最后去脾脏细胞与sp2/0瘤细胞进行融合,按照常规方法以p72包被的酶标板筛选阳性克隆。
表1不同免疫小鼠血清效价测定结果
有限稀释至单克隆状态后测定细胞培养上清效价,并以猪瘟病毒活疫苗、猪伪狂犬活疫苗、猪繁殖与呼吸综合征活疫苗、猪细小病毒培养液、猪圆环病毒2型细胞培养液等病毒检测,筛选能与非洲猪瘟病毒p72重组蛋白反应,而与其它病毒无反应的抗体细胞株,得到7a7、3e5、2h3、3e1和5a3等多株细胞株,将筛选到的杂交瘤细胞株进行扩大培养后,于腹腔注射0.2ml(含2.5×106个细胞)经弗式不完全佐剂预处理的雌性balb/c小鼠,约10~15日后,待小鼠腹部明显肿大时,使用无菌注射器针头采集腹水。将收集到腹水以1000r/min离心10min,收集中间层。
将腹水以12000r/min离心5min,取上清液,并将上清液用结合缓冲液按照1:7比例进行稀释。稀释后的样品使用滤膜过滤,然后上柱(proteing事先先用结合缓冲液平衡)。上柱完成后,使用结合缓冲液冲洗大约5个柱体积;而后使用洗脱缓冲液(0.1m甘氨酸用盐酸调节ph2.7)洗脱,收集a280处的洗脱液。然后迅速使用1mtris-hcl(ph9.0)溶液中和甘氨酸,使ph处于中性范围。将纯化抗体透析至1xpbs中,期间多次换液。将检验合格的单克隆抗体定量分装,1ml/管,﹣80℃以下保存,避免反复冻融和污染。
5.非洲猪瘟病毒p72重组蛋白单克隆抗体免疫特异性鉴定
单克隆抗体7a7和3e1的特异性鉴定:
将asfv阳性脾脏研磨液、asfv阴性脾脏研磨液、prv、pcv2、prrsv、csfv等包被酶联反应板,分别与2株单克隆抗体进行反应,结果显示,单克隆抗体7a7株和3e1株与asfv阳性脾脏研磨液发生特异性反应,其od450nm值>1.0,而与阴性脾脏研磨液和其他病毒不发生反应,表明单克隆抗体7a7株和3e1株具有良好的特异性,详见图5。
6.两株单克隆抗体的配对
用ph9.6碳酸盐缓冲液将筛选得到的单克隆抗体稀释至1µg/ml,4℃包被过夜,用pbst洗板3次,然后使用含有1%bsa的封闭液37℃封闭两小时,加入非洲猪瘟病毒p72重组蛋白,37℃反应30min,洗板5次;加入hrp标记的酶标鼠单抗(1:10000倍稀释),37℃反应30min,洗板5次;加入tmb显色液显色10min,加入终止液,读取od450nm值,结果如表2。
表2不同抗体配对结果及od450nm值
选择od450nm值大于2.0的两对单克隆抗体,分别为7a7和3e5、2h3和3e1,将这两对单克隆抗体,用上述elisa方法对10-2、10-3、10-4、10-5三份不同稀释度的0.1mg/mlp72蛋白阳性质控品进行灵敏度检测,读取od450nm值,结果如表3。
表32对配对抗体灵敏度检测结果
从表3结果可以看出:对不同倍比稀释的p72蛋白阳性质控,7a7和3e5配对单抗检测od450nm值均高于2h3和3e1配对单抗,表明7a7和3e5的灵敏度更高,确定最佳配对单抗为7a7和3e5,用作本发明非洲猪瘟病毒抗原乳胶微球检测试纸条的标记抗体和捕获抗体。
实施例2乳胶微球标记的非洲猪瘟病毒p72重组蛋白单克隆抗体的制备
将制备好的非洲猪瘟病毒p72重组蛋白单克隆抗体(7a7)用稀释液稀释后用乳胶微球颗粒标记,具体操作如下:
1.乳胶微球的清洗:量取一定体积粒径为300nm的乳胶微球(购自苏州为度生物技术有限公司,货号dr05c),倒入洁净的离心管,按照每100μl乳胶微球加入900μl标记缓冲液(50mmmes,ph6.0)的比例加入标记缓冲液。17000r/min离心10min,去掉上清,再加入1000μl体积的标记缓冲液,17000r/min离心10min,去掉上清,加入1000μl体积的标记缓冲液重悬微球。
2.乳胶微球的活化:各称取20mgnhs和edc,用1ml标记缓冲液(50mmmes,ph6.0)溶解,现用现配,分别得到20mg/mlnhs溶液和edc溶液;取20μl配制好nhs溶液,加入到清洗后的微球中,快速混匀;然后再取5μl配制好的edc溶液加入到微球中,快速混匀;室温孵育20-30min。
3.乳胶微球的标记:将步骤2得到的活化后的乳胶微球17000r/min离心10min,加入1000μl体积的标记缓冲液重悬微球;17000r/min离心10min,弃上清,加入1000μl体积的标记缓冲液重悬微球;量取一定量的单克隆抗体(7a7),按每0.1mg抗体加入100μl微球缓冲液的比例加入活化后的微球缓冲液,快速混匀后,室温孵育3h。
再量取100μl体积的乳胶微球加入封闭液(20mg/ml的bsa,用终浓度100mm乙醇胺溶液充分溶解),室温孵育1小时;17000r/min离心10min,弃上清,再加入1000μl体积的缓冲液重悬微球,重复两次,去除未结合的抗体。最后一次用1000μl体积的标记缓冲液重悬微球,即为抗体-微球标记复合物,4℃放置备用,如长期保存需加入终浓度为0.2%bsa和0.02%nan3溶液。
实施例3乳胶微球垫的制备
1.从4℃冰箱里取出乳胶微球标记的非洲猪瘟病毒p72重组蛋白单克隆抗体溶液,恢复至室温。
2.取一张20cm×30cm的玻璃纤维并用辅料切条机裁切成0.6cm×30cm规格。
3.在桌上平铺一层保鲜膜,将切好的玻璃纤维放在保鲜膜上,用移液器吸取1ml乳胶微球标记的非洲猪瘟病毒p72重组蛋白单克隆抗体溶液均匀润湿一张切好的玻璃纤维。室温晾干12~16小时,再转移至40℃烘箱1h,然后置于装有干燥剂的密封袋中,密封,待用。
实施例4硝酸纤维素膜的制备
将捕获抗体(3e5)和质控线羊抗鼠抗抗体用ph7.20.01mpbs缓冲液稀释至0.5mg/ml,用划膜仪喷涂在硝酸纤维素膜上作为检测线5和质控线4。
实施例5滤血膜的制备及检验
1.滤血膜的制备:取滤血膜,检查并剔除有异物、折损及污渍的滤血膜,用辅料切条机裁切成生产要求的规格(30cm×12mm)。
2.滤血膜的检验:1)外观表面干净整洁无杂物;对着发光物观察,应看不出明显的透明度差异;2)水延展性剪取1cm滤血膜(0.5cm×2cm)平放在一支持物上,用移液器从一端慢慢滴加全血样品至整块滤血膜刚好饱和,滤血量可以达到120±5μl/cm2。
实施例6样品垫及吸水垫的处理
本发明的非洲猪瘟病毒的乳胶微球检测试纸适用于猪全血、血清、组织样品等的检测,无需复杂前处理。由于全血、组织样品等成分复杂,易对试验结果造成干扰,且特异性较差,本发明在使用滤血膜的同时,还使用了3层样品垫且用不同缓冲液进行处理,通过灵敏度、特异性、符合率检测,确定最优的处理方法如下:
1.第一样品垫6的处理:取30cm×6mm的玻璃纤维样品垫用0.02mpb(ph7.2)溶液以1ml/条浸润,烘箱干燥,干燥温度为40℃±2℃,时间为16h,备用。
2.第二样品垫9的处理:取30cm×15mm的玻璃纤维样品垫用含2%蔗糖的0.02mpb(ph7.2)溶液以2.5ml/条浸润,烘箱干燥,干燥温度为40℃±2℃,时间为16h,备用。
3.第三样品垫10的处理:取30cm×23mm的玻璃纤维样品用含2%蔗糖和0.5%tween20的0.02mpb(ph7.2)溶液以5ml/条浸润,烘箱干燥,干燥温度为40℃±2℃,时间为16h,备用。
4.吸水垫11的处理:用裁纸机将吸水纸裁切成30cm×18mm,备用。
实施例7试纸条的组装
试纸条具体组装方式如图1、2、3所示,在湿度30%一下、温度18~26℃的洁净环境下,将处理好的硝酸纤维素膜3、乳胶微球垫7、滤血膜8、样品垫6、9、10、吸水纸11及其它相关原料取出。将干燥固定后的硝酸纤维素膜3贴在pvc背板2上,粘贴好样品垫、乳胶微球垫和吸水纸,得到非洲猪瘟病毒的乳胶微球检测试纸1,具体粘贴方法如下:
1.贴第一样品垫6(30cm×6mm规格):第一样品垫6上沿需压硝酸纤维素膜3下沿,第一样品垫6与硝酸纤维素膜3重叠1.5~2.0mm。
2.贴乳胶微球垫7:乳胶微球垫7的上沿必须压着第一样品垫6的下沿,乳胶微球垫7与第一样品垫6重叠1~1.5mm。
3.贴滤血膜8:将滤血膜8贴在乳胶微球垫7的下方,并用手压平,要求滤血8与乳胶微球垫7重叠2.5~3.0mm。
4.贴第二样品垫9(30cm×15mm规格):将30cm×15mm规格的第二样品垫9贴在滤血膜8的下方,并用手压平,要求第二样品垫9与滤血膜8重叠9.0~9.5mm。
5.贴第三样品垫10(30cm×23mm规格):将30cm×23mm规格的第三样品垫10贴在第二样品垫9的下方,并用手压平,要求第三样品垫10下端对齐pcv底板2的下端,贴紧。
6.贴吸水垫11:将已贴好第三样品垫10的底板2的最上方的双面胶条揭开,把已经裁好的吸水垫11沿硝酸纤维素膜3贴在膜的上方,吸水纸的上端与pvc底板2的上端对齐,贴紧。
7.切条:将组装好的板子修剪整齐,送入切条机,切成宽为4.0±0.1mm的试纸条。
8.装卡:挑取无划痕、无污渍,边缘整齐的试纸条,放入卡的底卡中,盖上卡壳的盖,送入压盖机中压盖。
9.装袋:将压好的检测试纸条连同1粒干燥剂一起放入铝箔袋。
10.封口贴签:装好袋子的检测试纸条放入封口机,封口。在封口的铝箔袋中央贴上标签。
实施例8非洲猪瘟病毒的乳胶微球检测试纸使用方法及结果判定
1.全血、血浆和血清的处理:可采用未经处理的新鲜全血或加抗凝剂处理的全血作为检测样本,也可采集全血分离血浆或血清(5000~8000r/min离心2~5min或4℃过夜自然析出)作为检测样本。
2.组织脏器样品处理:分别从脾脏、淋巴结等组织的三个不同位置取样,称取样品约1g,用手术剪剪碎混匀,再取0.1g于研磨器中研磨,加入1.5ml生理盐水继续研磨,待匀浆后转至1.5ml灭菌离心管中,8000r/min离心2min,取上清液100µl于1.5ml灭菌离心管中,编号备用。
3.撕开试纸条铝箔袋包装,取出试纸条,放于平整、洁净的试验台面上。
4.用一次性塑料吸管吸取样本,滴加1滴(约30μl)至加样孔,随后垂直缓慢滴入3滴样本稀释液(约120μl)。
5.样本稀释液滴加操作完成后,等待10min判定结果,20min后的结果无效。
6.判定结果:当试纸条的c线显色,t线颜色不显色时,样本检测结果为阴性。当试纸条的c线显色,t线颜色显色时,样本检测结果为阳性,t线颜色越深,阳性越强。当试纸条的c线不显色,样本检测结果为无效,应更换试纸条重新检测。
实施例9非洲猪瘟病毒的乳胶微球检测试纸的敏感性、特异性、均一性和稳定性检测
1.敏感性检测:采用健康仔猪抗凝血(经非洲猪瘟病毒荧光pcr检测试剂盒(兽药生字010628858)检测为非洲猪瘟病毒阴性)作为阴性质控;采用体外表达的非洲猪瘟病毒p72重组蛋白,经超微量分光光度计测定蛋白浓度后,用健康仔猪抗凝血稀释至0.25mg/ml作为阳性质控。
对10-3、10-4、10-5共3份不同稀释度的阳性质控样品和1份阴性质控样品分别用本发明的非洲猪瘟病毒抗原乳胶微球检测试纸卡进行检测。检测结果如下表4所示。
表4
结果显示:本发明试纸卡对10-5阳性质控样品检测结果为阳性,表明试纸卡对非洲猪瘟病毒p72重组蛋白的检出限最低可达2.5ng/ml。
2.特异性检测:以猪繁殖与呼吸综合征活疫苗(购自中牧实业股份有限公司、jxa1-r株)、猪瘟病毒活疫苗(购自武汉科前生物股份有限公司、cvccav1412株)、猪伪狂犬活疫苗(购自武汉科前生物股份有限公司、hb-98株)、猪细小病毒(购自中国兽医微生物菌种保藏中心)培养液、猪圆环病毒2型细胞(北京市农林科学院畜牧兽医研究所提供)培养液为特异性质控品,对5份特异性质控样品进行检测,结果应均为阴性,说明本发明试纸卡不与猪其他病毒发生交叉反应,特异性良好。
均一性:取10-5阳性质控样品重复检测10次,结果均为阳性,显色均一;取阴性质控样品重复检测10次,结果均为阴性,显色均一。
稳定性:将试纸条于37℃放置7日,分别进行各项指标的检验,均符合要求。
实施例10非洲猪瘟病毒的乳胶微球检测试纸的定量检测
1.采用健康仔猪抗凝血(经非洲猪瘟病毒荧光pcr检测试剂盒【兽药生字010628858】检测为非洲猪瘟病毒阴性)作为阴性质控;采用体外表达的非洲猪瘟病毒p72重组蛋白,经超微量分光光度计测定蛋白浓度后,用健康仔猪抗凝血稀释至0.25mg/ml作为阳性质控。
2.将阳性质控品进行稀释,浓度分别为0ng/ml、2.5ng/ml、50ng/ml、100ng/ml、300ng/ml,用本发明的非洲猪瘟病毒乳胶微球检测试纸卡进行检测,10min后用nb读数仪读取检测线显色值,并绘制标准曲线,标准曲线如图6所示。
3.将阳性质控品稀释至浓度为2.5ng/ml、5ng/ml、10ng/ml、20ng/ml、40ng/ml分别用本发明试纸卡检测,并用读数仪读取显色值,根据标准曲线计算样品中p72蛋白浓度,并与实际浓度对比,对比结果如表5所示。
表5样品中p72浓度测定结果
从表5结果可以看出,使用本发明测定计算得到的样品中非洲猪瘟病毒p72蛋白浓度与实际浓度无明显差异,表明本发明试纸条可用于样品中非洲猪瘟病毒p72蛋白浓度进行定量检测,也可用来评价猪血液中非洲猪瘟病毒抗原的含量。
实施例11本发明的乳胶微球检测试纸与胶体金检测试纸的灵敏度对比
1.制备胶体金颗粒:用柠檬酸三钠还原剂将氯金酸还原制成20~40nm胶体金颗粒,取氯金酸水溶液500~1000ml用恒温电磁搅拌器加热至沸腾,持续搅拌的情况下加入16%柠檬酸三钠水0.5~1.5ml溶液,继续搅拌加热5~10min,溶液呈透亮的红色。室温冷却,用去离子水恢复到原体积,4℃保存。
2.非洲猪瘟病毒p72重组蛋白单克隆抗体-胶体金标记物的制备:取上步制备的1ml胶体金加入2.5~4.5μl浓度为0.1mol/l的k2co3溶液调节ph值,再加入0.8~1.5mg筛选纯化后的非洲猪瘟病毒p72重组蛋白单克隆抗体(7a7),混匀后静置5min,加入10μl10%聚乙二醇20000(peg,沃凯,货号20170615)溶液后12000rpm离心7min,弃上清,加入100μl复溶液(0.05m三羟甲基氨基甲烷+5%蔗糖),混合均匀。
3.试纸条组装:步骤同实施例6,将乳胶微球垫替换成胶体金垫。
4.乳胶微球试纸卡与胶体金试纸条灵敏度对比试验
对10-3、10-4、10-5共3份不同稀释度的阳性质控样品和1份阴性质控样品分别用本发明的非洲猪瘟病毒乳胶微球检测试纸与非洲猪瘟病毒胶体金试纸条进行检测,检测结果如下表6所示。
表6
由检测结果可以看出:本发明的非洲猪瘟病毒乳胶微球检测试纸与同样原料制成的胶体金试纸分别对不同浓度p72蛋白进行检测,乳胶微球试纸卡检测10-5稀释的p72蛋白时为阳性,灵敏度达到2.5ng/ml,胶体金试纸条检测10-4稀释的p72蛋白时为阳性,检测10-5稀释的p72蛋白时为阴性,灵敏度为25ng/ml,明显低于乳胶微球试纸。
实施例12乳胶微球检测试纸与胶体金检测试纸分别与荧光pcr试剂盒的符合率比较
采用非洲猪瘟病毒荧光pcr检测试剂盒【兽药生字010628858】、本发明自制的非洲猪瘟病毒乳胶微球检测试纸与胶体金试纸分别检测12只攻非洲猪瘟病毒的spf猪和12只对照组的spf猪的泄殖腔拭子以及临床样本共720份。
检测结果显示,荧光pcr检测试剂盒共检测出129份阳性、591份阴性,非洲猪瘟病毒特异性抗原检测试纸卡共检测出123份阳性、597份阴性,胶体金试纸条共检测出115份阳性、605份阴性,乳胶微球试纸卡与荧光pcr检测结果均为阳性的样品有117份,均为阴性的样品有585份,阳性符合率为90.70%,阴性符合率为98.98%,总符合率为97.50%。胶体金试纸条与荧光pcr检测结果均为阳性的样品有105份,均为阴性的样品有581份,阳性符合率为81.40%,阴性符合率为98.31%,总符合率为95.28%,具体结果见表7、表8。
表7本发明的乳胶微球试纸检测和荧光pcr检测总符合率结果
表8胶体金试纸条检测和荧光pcr检测总符合率结果
由检测结果可以看出:本发明的非洲猪瘟病毒乳胶微球检测试纸与荧光pcr试剂盒的符合率明显高于用同样单克隆抗体制成的胶体金试纸条,表明本发明试纸条的准确性更高。
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
序列表
<110>北京纳百生物科技有限公司
<120>非洲猪瘟病毒的检测试纸、试剂盒及其制备方法
<141>2019-11-26
<160>4
<170>siposequencelisting1.0
<210>1
<211>300
<212>prt
<213>非洲猪瘟病毒(africanswinefevervirus)
<400>1
leuasnserargileserasnilelysasnvalasnlyssertyrgly
151015
lysproaspprogluprothrleuserglnileglugluthrhisleu
202530
valhispheasnalahisphelysprotyrvalprovalglypheglu
354045
tyrasnlysvalargprohisthrglythrprothrleuglyasnlys
505560
leuthrpheglyileproglntyrglyaspphephehisaspmetval
65707580
glyhishisileleuglyalacyshissersertrpglnaspalapro
859095
ileglnglythrserglnmetglyalahisglyglnleuglnthrphe
100105110
proargasnglytyrasptrpaspasnglnthrproleugluglyala
115120125
valtyrthrleuvalasppropheglyargproilevalproglythr
130135140
lysasnalatyrargasnleuvaltyrtyrcysglutyrproglyglu
145150155160
argleutyrgluasnvalargpheaspvalasnglyasnserleuasp
165170175
glutyrserseraspvalthrthrleuvalarglysphecysilepro
180185190
glyasplysmetthrglytyrlyshisleuvalglyglngluvalser
195200205
valgluglythrserglyproleuleucysasnilehisaspleuhis
210215220
lysprohisglnserlysproileleuthraspgluasnaspthrgln
225230235240
argthrcysserhisthrasnprolyspheleuserglnhisphepro
245250255
gluasnserhisasnileglnthralaglylysglnaspilethrpro
260265270
ilethraspalathrtyrleuaspileargargasnvalhistyrser
275280285
cysasnglyproglnthrprolystyrtyrglnpro
290295300
<210>2
<211>145
<212>prt
<213>非洲猪瘟病毒(africanswinefevervirus)
<400>2
thrtrpasnileseraspglnasnprohisglnhisargasptrphis
151015
lyspheglyhisvalvalasnalailemetglnprothrhishisala
202530
gluileserpheglnaspargaspthralaleuproaspalacysser
354045
serileseraspileserprovalthrtyrproilethrleuproile
505560
ilelysasnileservalthralahisglyileasnleuileasplys
65707580
pheproserlysphecyssersertyrileprophehistyrglygly
859095
asnalailelysthrproaspaspproglyalametmetilethrphe
100105110
alaleulysproarggluglutyrglnproserglyhisileasnval
115120125
serargalaarggluphetyrilesertrpaspthrasptyrvalgly
130135140
ser
145
<210>3
<211>450
<212>prt
<213>非洲猪瘟病毒(africanswinefevervirus)
<400>3
leuasnserargileserasnilelysasnvalasnlyssertyrgly
151015
lysproaspprogluprothrleuserglnileglugluthrhisleu
202530
valhispheasnalahisphelysprotyrvalprovalglypheglu
354045
tyrasnlysvalargprohisthrglythrprothrleuglyasnlys
505560
leuthrpheglyileproglntyrglyaspphephehisaspmetval
65707580
glyhishisileleuglyalacyshissersertrpglnaspalapro
859095
ileglnglythrserglnmetglyalahisglyglnleuglnthrphe
100105110
proargasnglytyrasptrpaspasnglnthrproleugluglyala
115120125
valtyrthrleuvalasppropheglyargproilevalproglythr
130135140
lysasnalatyrargasnleuvaltyrtyrcysglutyrproglyglu
145150155160
argleutyrgluasnvalargpheaspvalasnglyasnserleuasp
165170175
glutyrserseraspvalthrthrleuvalarglysphecysilepro
180185190
glyasplysmetthrglytyrlyshisleuvalglyglngluvalser
195200205
valgluglythrserglyproleuleucysasnilehisaspleuhis
210215220
lysprohisglnserlysproileleuthraspgluasnaspthrgln
225230235240
argthrcysserhisthrasnprolyspheleuserglnhisphepro
245250255
gluasnserhisasnileglnthralaglylysglnaspilethrpro
260265270
ilethraspalathrtyrleuaspileargargasnvalhistyrser
275280285
cysasnglyproglnthrprolystyrtyrglnproglyglyglygly
290295300
serthrtrpasnileseraspglnasnprohisglnhisargasptrp
305310315320
hislyspheglyhisvalvalasnalailemetglnprothrhishis
325330335
alagluileserpheglnaspargaspthralaleuproaspalacys
340345350
serserileseraspileserprovalthrtyrproilethrleupro
355360365
ileilelysasnileservalthralahisglyileasnleuileasp
370375380
lyspheproserlysphecyssersertyrileprophehistyrgly
385390395400
glyasnalailelysthrproaspaspproglyalametmetilethr
405410415
phealaleulysproarggluglutyrglnproserglyhisileasn
420425430
valserargalaarggluphetyrilesertrpaspthrasptyrval
435440445
glyser
450
<210>4
<211>1350
<212>dna
<213>非洲猪瘟病毒(africanswinefevervirus)
<400>4
ctgaatagcaggatctctaacattaaaaatgtgaacaaaagttatgggaaacccgatccc60
gaacccactttgagtcaaatcgaagaaacacatttggtgcattttaatgcgcattttaag120
ccttatgttccagtagggtttgaatacaataaagtacgcccgcatacgggtacccccacc180
ttgggaaacaagcttacctttggtattccccagtacggagactttttccatgatatggtg240
ggccatcatatattgggtgcatgtcattcatcctggcaggatgctccgattcagggcacg300
tcccagatgggggcccatgggcagcttcaaacgtttcctcgcaacggatatgactgggac360
aaccaaacacccttagagggcgccgtttacacgcttgtagatccttttggaagacccatt420
gtacccggcacaaagaatgcgtaccgaaacttggtttactactgcgaataccccggagaa480
cgactttatgaaaacgtaagattcgatgtaaatggaaattccctagacgaatatagttcg540
gatgtcacaacgcttgtgcgcaaattttgcatcccaggggataaaatgactggatataag600
cacttggttggccaggaggtatcggtggagggaaccagtggccctctcctatgcaacatt660
catgatttgcacaagccgcaccaaagcaaacctattcttaccgatgaaaatgatacgcag720
cgaacgtgtagccataccaacccgaaatttctttcacagcattttcccgagaactctcac780
aatatccaaacagcaggtaaacaagatattactcctatcacggacgcaacgtatctggac840
ataagacgtaatgttcattacagctgtaatggacctcaaacccctaaatactatcagccc900
ggaggaggaggttccacctggaacatctccgatcaaaatcctcatcaacaccgagattgg960
cacaagttcggacatgttgttaacgccattatgcagcccactcaccacgcagagataagc1020
tttcaggatagagatacagctcttccagacgcatgttcatctatatctgatattagcccc1080
gttacgtatccgatcacattacctattattaaaaacatttccgtaactgctcatggtatc1140
aatcttatcgataaatttccatcaaagttctgcagctcttacatacccttccactacgga1200
ggcaatgcgattaaaacccccgatgatccgggtgcgatgatgattacctttgctttgaag1260
ccacgggaggaataccaacccagtggtcatattaacgtatccagagcaagagaattttat1320
attagttgggacacggattacgtggggtct1350
- 还没有人留言评论。精彩留言会获得点赞!