用于细胞AQP功能无标记评估的太赫兹超材料检测装置的制作方法
本实用新型属于太赫兹测量技术领域,涉及用于细胞aqp功能无标记评估的太赫兹超材料检测装置。
背景技术:
水是生命之源。水通道蛋白(aquaporin,aqp)是位于细胞膜上的跨膜蛋白,选择性高效转运水分子的通道。自1991年首次报道第一个水通道蛋白(aqp1)以来,研究者相继发现广泛分布于不同器官的13种水通道蛋白,对于维持器官正常生理功能发挥至关重要的作用。aqp表达量和功能状态与肿瘤、脑血管疾病、肾脏疾病等多种疾病密切相关。特别是aqp在肿瘤组织中表达上调,通过快速转运水分子进入肿瘤细胞介导其迁移、增殖和侵袭,并参与肿瘤新生血管的形成。因此准确评估细胞aqp功能状态、用于研发靶向aqp的阻断剂、抑制剂乃至激动剂是当前肿瘤靶向治疗和成像的热点所在。
细胞aqp功能评估主要通过测量水分子在胞外渗透压变化情况下透过胞膜的转运情况,宏观表现为细胞的体积和水含量改变。基于此目前评估细胞aqp功能方法有光散射法、显微图像测量法、光干涉法、离子浓度敏感型荧光标记等方法。光散射法受限于伪影信号产生,已较少应用;显微图像测量仅应用于表达aqp的非洲蟾蜍卵母细胞在细胞溶胀过程体积改变的分析,数据变异性较大、可靠度较低;激光干涉对仪器的光束对准及振动要求较高,实用性不强。荧光标记法对生长在固体支持物上的细胞层进行胞质钙黄绿素染色或转染绿色荧光蛋白,基于全内反射荧光平台测定渗透梯度改变时荧光信号的变化获得细胞容量动力学改变参数,具有应用广泛、伪影误差小、防止光漂白及结果可靠性高的优点,但其实质仍为有标记检测,且由于倏逝波穿透深度限制,仅能获得亚微米尺度的细胞层信息。综上,目前尚缺乏一种无标记、可靠的细胞aqp功能评估方法。
太赫兹(terahertz,thz)波技术是一种新型无标记检测技术。它是频率在0.1~10thz(对应波长范围为30μm-3mm)的电磁波,处于微波向红外过渡的波段,具备无标记检测的频谱优势:1thz振荡频率对应0.16皮秒转动,相较磁共振、准弹性中子散射和非相干中子散射等传统方法,thz技术无需氢氘置换或低温冷却,可将检测胞内水分子运动尺度从飞秒水平提升至皮秒及亚皮秒水平,从而实现精确、实时分析细胞内自由水和结合水的水化动力学,具备应用于细胞aqp功能实时评估的潜能。thz超材料芯片是指在硅、石英等衬底上加工形成亚波长尺度的周期排布金属结构,具有微米尺度的局域增强电场,可显著提升thz波与细胞层的相互作用,从而无标记、高灵敏获取整个细胞层的介电响应信息。同时,thz超材料芯片体积小巧,易于整合,是研发高灵敏细胞无标记检测芯片的有效途径。目前尚无将thz波技术应用于细胞aqp功能无标记评估领域的相关报道。
技术实现要素:
有鉴于此,本实用新型的目的在于提供一种用于细胞aqp功能无标记评估的太赫兹超材料检测装置。
为达到上述目的,本实用新型提供如下技术方案:
用于细胞aqp功能无标记评估的太赫兹超材料检测装置,由上而下包括夹具本体ⅰ、微流道反应腔隙盖层、太赫兹超材料芯片和夹具本体ⅱ,夹具本体ⅰ与夹具本体ⅱ均为正方形中空结构,微流道反应腔隙盖层嵌入夹具本体ⅰ的底部,并与夹具本体ⅰ的底部表面平齐,太赫兹超材料芯片嵌入夹具本体ⅱ的顶部,并与夹具本体ⅱ的顶部表面平齐,夹具本体ⅰ与夹具本体ⅱ磁吸式贴合;所述微流道反应腔隙盖层包括紧密贴合的方形基底和覆盖层两部分,覆盖层的中央开设圆形孔,所述圆形孔与基底构成反应槽。
作为优选的技术方案之一,所述夹具本体ⅰ与夹具本体ⅱ的贴合面处分别埋设磁铁和相应的吸合部件,为保证强吸合力,所述磁铁和相应的吸合部件进一步优选直径为6mm、厚度为1mm钕铁硼磁铁。
作为进一步优选的技术方案之一,在夹具本体ⅰ与夹具本体ⅱ的贴合面四条边中点处开设圆柱形预埋孔,在各个预埋孔中分别对应放入磁铁和相应的吸合部件并粘结固定,使磁铁和相应吸合部件的外部暴露表面与夹具本体ⅰ和夹具本体ⅱ的贴合面在磁吸压紧时平齐无空隙。
作为优选的技术方案之一,在夹具本体ⅰ的四个顶角处各开设一个定位销孔,并在夹具本体ⅱ的贴合面对应位置设置与定位销孔对应的定位销,用于所述检测装置的快速、准确组装;所述定位销孔、定位销的直径进一步优选为3mm。
作为优选的技术方案之一,在夹具本体ⅰ的底部和顶部分别开设内部连通的方形凹槽ⅰ和方形凹槽ⅱ,两者之间形成隔板ⅰ,方形凹槽ⅰ的边长大于方形凹槽ⅱ,所述微流道反应腔隙盖层嵌入方形凹槽ⅰ,并与夹具本体ⅰ的底部平面平齐;夹具本体ⅱ的顶部和底部分别开设方形凹槽ⅲ和方形凹槽ⅳ,两者之间形成隔板ⅱ,方形凹槽ⅲ的边长大于方形凹槽ⅳ,所述太赫兹超材料芯片嵌入方形凹槽ⅲ,并与夹具本体ⅱ的顶部平面平齐;方形凹槽ⅰ、方形凹槽ⅲ的边长相同,进一步优选为2cm,方形凹槽ⅱ、方形凹槽ⅳ的边长相同,进一步优选为1.5cm。
作为进一步优选的技术方案之一,所述检测装置还包括缓冲垫圈层ⅰ和缓冲垫圈层ⅱ,它们均为方形环状,缓冲垫圈层ⅰ设置于微流道反应腔隙盖层与夹具本体ⅰ之间;缓冲垫圈层ⅱ位于太赫兹超材料芯片与夹具本体ⅱ之间;缓冲垫圈层ⅰ、缓冲垫圈层ⅱ的环宽分别与隔板ⅰ、隔板ⅱ一致,用于保持夹具本体ⅰ、夹具本体ⅱ与微微流道反应腔隙盖层和超材料芯片层间的均匀压力和良好密封,应选择生物相容性佳、弹性优良及耐用的橡胶材质,进一步优选为硅橡胶材质,以保证测量时微流道反应腔隙盖层与太赫兹超材料芯片的表面紧密贴合。
作为优选的技术方案之一,基底和覆盖层的边长为2cm;基底的材质要求透光度优良、硬度好,进一步优选为石英、k9玻璃或cop塑料,更进一步优选为红外石英玻璃,其尺寸进一步优选为边长2cm、厚度1mm;覆盖层的材质进一步优选为pdms精密薄膜材质,其透光率大于95%,对细胞无毒性,厚度为500μm,圆形孔的直径优选为1cm。
作为优选的技术方案之一,所述基底靠近夹具本体ⅰ,覆盖层靠近夹具本体ⅱ,在反应槽对应位置处的基底上开设两个孔,分别作为进样孔和流出孔,在孔上连接软管,用于缓冲液的注入和流出;孔的直径进一步优选为2mm。
作为更进一步优选的技术方案之一,在孔上粘结直通型聚丙烯转接头,所述转接头上套接硅胶软管,硅胶软管的内径优选为2mm,外径优选为4mm。
作为优选的技术方案之一,所述太赫兹超材料芯片包括非金属基底以及在其表面溅镀的金属膜,在金属膜上刻蚀出周期性排布的圆环形狭缝,所述狭缝的底部为非金属基底。
作为进一步优选的技术方案之一,所述非金属基底的材质为双面抛光的高阻硅(厚度为500μm,电阻率大于10000ω.cm);所述金属膜的材质选自金、钛、银、铜、铝或镍中的任一种。
作为更进一步优选的技术方案之一,所述太赫兹超材料芯片包括双面抛光的高阻硅基底以及在其表面依次溅镀的钛膜和金膜,在金属膜上紫外光刻蚀出周期性排布的圆环形狭缝,所述狭缝的底部为高阻硅基底;钛膜的厚度进一步优选为20nm,金膜的厚度进一步优选为200nm,圆环的外直径为80μm,内直径为72μm,环宽(缝隙)为4μm,周期为120μm。
本实用新型的有益效果在于:
本实用新型由上而下包括夹具本体ⅰ、微流道反应腔隙盖层、太赫兹超材料芯片和夹具本体ⅱ,夹具本体ⅰ与夹具本体ⅱ均为正方形中空结构,微流道反应腔隙盖层嵌入夹具本体ⅰ的底部,并与夹具本体ⅰ的底部表面平齐,太赫兹超材料芯片嵌入夹具本体ⅱ的顶部,并与夹具本体ⅱ的顶部表面平齐,夹具本体ⅰ与夹具本体ⅱ磁吸式贴合;微流道反应腔隙盖层包括紧密贴合的方形基底和覆盖层两部分,覆盖层的中央开设圆形孔,圆形孔与基底构成反应槽。本实用新型可利用thz反射光谱可对水分子透过超材料芯片表面细胞层的状态进行实时、无标记检测,从而有效评估细胞aqp的功能状态;具备以下突出优势:
1.无标记检测,不需借助任何荧光染色或荧光蛋白转染的方法可有效评估细胞aqp功能;
2.全细胞尺度检测,超材料的局域增强电场在z轴方向分布近10μm,可完整获取全细胞范围的thz介电响应信息;
3.高灵敏性,超材料局域增强电场可显著提升thz波与细胞层的相互作用,有效解决thz波液相传感中水强吸收干扰的问题;
4.快速、便捷,夹具盖层选用光学透明性好的石英材质,加样过程全程可视,夹具本体采用磁吸式吸附方式,可实现快速闭合、拆卸,重复使用性好。
附图说明
为了使本实用新型的目的、技术方案和有益效果更加清楚,本实用新型提供如下附图进行说明:
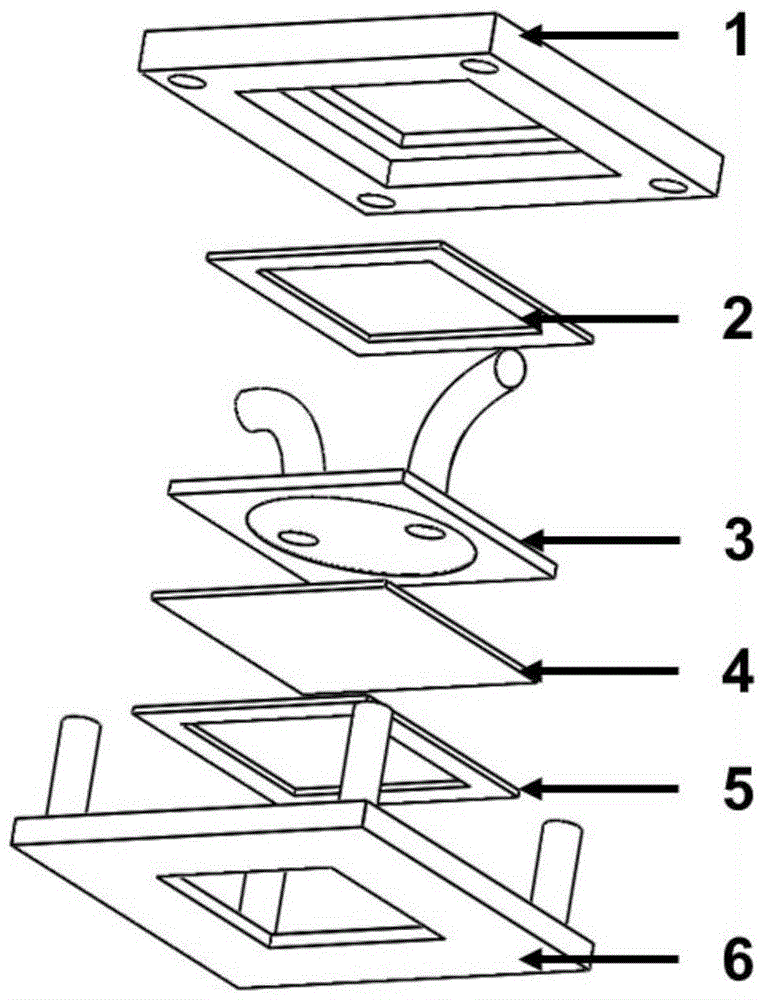
图1为本实用新型结构示意图;
其中,1为夹具本体ⅰ,2为缓冲垫圈层ⅰ,3为微流道反应腔隙盖层,4为太赫兹超材料芯片,5为缓冲垫圈层ⅱ,6为夹具本体ⅱ。
具体实施方式
下面将结合附图,对本实用新型的优选实施例进行详细的描述。
实施例:
如图1所示的一种用于细胞aqp功能无标记评估的太赫兹超材料检测装置,由上而下包括夹具本体ⅰ1、微流道反应腔隙盖层3、太赫兹超材料芯片4和夹具本体ⅱ6,夹具本体ⅰ1与夹具本体ⅱ6均为正方形中空结构,微流道反应腔隙盖层3嵌入夹具本体ⅰ1的底部,并与夹具本体ⅰ1的底部表面平齐,太赫兹超材料芯片4嵌入夹具本体ⅱ6的顶部,并与夹具本体ⅱ6的顶部表面平齐,夹具本体ⅰ1与夹具本体ⅱ6磁吸式贴合;微流道反应腔隙盖层3包括紧密贴合的方形基底和覆盖层两部分,覆盖层的中央开设圆形孔,圆形孔与基底构成反应槽。
夹具本体ⅰ1与夹具本体ⅱ6的贴合面处分别埋设磁铁和相应的吸合部件,为保证强吸合力,磁铁和相应的吸合部件选择直径为6mm、厚度为1mm钕铁硼磁铁。在夹具本体ⅰ1与夹具本体ⅱ6的贴合面四条边中点处开设圆柱形预埋孔,在各个预埋孔中分别对应放入磁铁和相应的吸合部件并粘结固定,使磁铁和相应吸合部件的外部暴露表面与夹具本体ⅰ1和夹具本体ⅱ6的贴合面在磁吸压紧时平齐无空隙。
在夹具本体ⅰ1的四个顶角处各开设一个定位销孔,并在夹具本体ⅱ6的贴合面对应位置设置与定位销孔对应的定位销,用于所述检测装置的快速、准确组装;定位销孔、定位销的直径为3mm。
在夹具本体ⅰ1的底部和顶部分别开设内部连通的方形凹槽ⅰ和方形凹槽ⅱ,两者之间形成隔板ⅰ,方形凹槽ⅰ的边长大于方形凹槽ⅱ,微流道反应腔隙盖层1嵌入方形凹槽ⅰ,并与夹具本体ⅰ1的底部平面平齐;夹具本体ⅱ6的顶部和底部分别开设方形凹槽ⅲ和方形凹槽ⅳ,两者之间形成隔板ⅱ,方形凹槽ⅲ的边长大于方形凹槽ⅳ,太赫兹超材料芯片4嵌入方形凹槽ⅲ,并与夹具本体ⅱ6的顶部平面平齐;方形凹槽ⅰ、方形凹槽ⅲ的边长相同,为2cm,方形凹槽ⅱ、方形凹槽ⅳ的边长相同,为1.5cm。
检测装置还包括缓冲垫圈层ⅰ2和缓冲垫圈层ⅱ5,它们均为方形环状,缓冲垫圈层ⅰ2设置于微流道反应腔隙盖层3与夹具本体ⅰ1之间;缓冲垫圈层ⅱ5位于太赫兹超材料芯片4与夹具本体ⅱ6之间;缓冲垫圈层ⅰ2、缓冲垫圈层ⅱ5的环宽分别与隔板ⅰ、隔板ⅱ一致,用于保持夹具本体ⅰ1、夹具本体ⅱ6与微微流道反应腔隙盖层3和太赫兹超材料芯片4层间的均匀压力和良好密封,应选择生物相容性佳、弹性优良及耐用的橡胶材质,选择硅橡胶材质,以保证测量时微流道反应腔隙盖层3与太赫兹超材料芯片4的表面紧密贴合。
基底和覆盖层的边长为2cm;基底的材质要求透光度优良、硬度好,选择红外石英玻璃,其尺寸为边长2cm、厚度1mm;覆盖层的材质为pdms精密薄膜材质,其透光率大于95%,对细胞无毒性,厚度为500μm,圆形孔的直径优选为1cm。
基底靠近夹具本体ⅰ1,覆盖层靠近夹具本体ⅱ6,在反应槽对应位置处的基底上开设两个孔,分别作为进样孔和流出孔,在孔上连接软管,用于缓冲液的注入和流出;孔的直径进一步优选为2mm。
在孔上粘结直通型聚丙烯转接头,转接头上套接硅胶软管,硅胶软管的内径为2mm,外径为4mm。
太赫兹超材料芯片4包括双面抛光的高阻硅基底以及在其表面依次溅镀的钛膜和金膜,在金属膜上紫外光刻蚀出周期性排布的圆环形狭缝,狭缝的底部为高阻硅基底;钛膜的厚度为20nm,金膜的厚度为200nm,圆环的外直径为80μm,内直径为72μm,环宽(缝隙)为4μm,周期为120μm。
以人乳腺癌细胞(mcf-7)的aqp功能检测为例,说明本实用新型的使用方法:
1、细胞培养:在高糖型dmem培养基中加入体积百分数10%胎牛血清、并加入体积百分数1%的青霉素链霉素双抗工作液(gibco,货号15140163)形成完全培养基,细胞培养箱温度设定为37℃、二氧化碳体积分数为5%,待培养瓶中mcf-7细胞(上海生工生物工程股份有限公司,货号d611026-0001)融合度达到85%左右时,以胰蛋白酶-edta消化液(其中胰酶质量浓度为0.25%,edta质量浓度为0.02%)在培养箱中消化2分钟,待细胞逐渐脱落(培养瓶呈毛玻璃样)时,加入以上所使用的完全培养基终止消化,并反复吹打获取细胞悬液,离心重悬后配置成浓度为1×106个细胞/ml悬液备用。
2、接种细胞:使用无水乙醇清洗太赫兹超材料芯片表面,并使用美国harrick等离子清洗机处理3分钟(功率为100w,真空度为0.3mbar,在超纯水中浸泡10分钟后,使用氮气吹干超材料芯片。将配置好的mcf-7细胞悬液滴加在超材料表面,并向细胞培养皿中加入3ml完全培养基后,放置于细胞培养箱中生长。待细胞贴壁生长并完全融合成单细胞层后,从培养箱中取出两块超材料芯片,将其分别放入使用pbs(其中nacl136.89mm,kcl2.67mm,na2hpo48.1mm,kh2po41.76mm;ph为7.4)配置的1mmaqp阻断剂-磺胺嘧啶银(silversulphadiazine)溶液中作用15分钟后取出,用pbs缓冲液清洗两次备用,按照图1的安装顺序固定好检测装置。将进样孔处软管连接驱动泵后,采用均匀流速向流道反应槽中加入pbs缓冲液,并确保反应槽检测区域无任何气泡产生。
3、thz检测:选用thz时域光谱的反射模块进行检测,提前1小时开机并充入干燥空气,维持光路中湿度在3%以下;将液相检测夹具模块水平放入thz检测光路使thz光斑对准中央检测区域,平均128次采集并保存初始细胞的thz光谱信号。使用驱动泵向液相反应槽中加入渗透压为150mosm/l的pbs缓冲液,并立即开始thz光谱测量,平均128次,时间间隔1秒,连续采集50次反射时域光谱信号,并使用同样方法获取pbs处理组的光谱信号
4、结果分析:提取不同反应时相点的时域光谱信号中来自超材料芯片表面反射的第二个峰信息,进行快速傅里叶变换分析,获得不同时相点的超材料芯片谐振峰强度值信号,以初始细胞的谐振峰强度值为参考,计算不同时相点谐振峰强度值的变化率。人乳腺癌mcf-7细胞高度表达aqp,而磺胺嘧啶银可以靶向抑制aqp的水转运功能。因此经过磺胺嘧啶银处理后mcf-7细胞在低渗透压环境下由水分子转运导致的细胞溶胀程度显著减弱,相对超材料谐振峰幅值信号变化远低于pbs溶液对照组信号。综上,本实用新型的检测装置可无标记、实时评估细胞aqp功能状态,其配套芯片检测夹具具备组装拆卸快速、便捷,可重复使用的优点。
最后说明的是,以上优选实施例仅用以说明本实用新型的技术方案而非限制,尽管通过上述优选实施例已经对本实用新型进行了详细的描述,但本领域技术人员应当理解,可以在形式上和细节上对其作出各种各样的改变,而不偏离本实用新型权利要求书所限定的范围。
- 还没有人留言评论。精彩留言会获得点赞!