鉴定结构的方法
1.本披露内容涉及显微术、组织学和病理学领域。在一种形式中,本披露内容提供了使用光学显微镜和增强的样品支架执行组织学的系统和方法。
背景技术:
2.以拉筹伯大学名义的pct/au2018/050496(其全部内容通过引用并入本文)披露了光学显微术的系统和方法,这些系统和方法通过使用具有等离子体层的样品支架提供了增强的图像对比度,该等离子体层包括周期性亚微米结构阵列。在本披露内容中,提及纳米载玻片是指根据pct/au2018/050496或申请人于2018年11月29日提交的发明名称为“microscopy method and system[显微术方法和系统]”的共同未决澳大利亚专利申请2018904553以及要求与本技术同一天提交的au2018904553的优先权的国际专利申请的教导的样品支架,这两个申请的内容出于所有目的通过引用并入本文。使用这种样品支架的显微术方法在本文中称为组织等离子体(histoplasmonics)或颜色对比度显微术,缩写为ccm。样品被放置在该样品支架上、邻近等离子体层。在使用中,用光(通常是宽带白光)照射样品和样品支架并产生样品的图像。发明人已经观察到,通过光与样品和等离子体层的相互作用,在生成的图像中可能会表现出颜色对比度。特别地,样品中具有不同介电常数的区域以不同颜色显现在图像中。还实现了强度对比度。与此相反,使用染色样品从常规光学显微术获得的图像通常仅表现出与所使用的染色相对应的单一颜色的强度对比度。
[0003]
使用这种类型的纳米载玻片的一个好处是,可以在不染色的情况下和/或通过相对薄的样品显示颜色对比度。
技术实现要素:
[0004]
本发明人已经意识到,纳米载玻片的使用能够对显微技术进行有效的改进,这些显微技术利用了这些独特优点中的一个或两个独特优点。
[0005]
在第一方面,提供了一种选择样品的关注区域用于后续分析过程的方法。该方法可以包括:
[0006]
提供具有上表面面和下表面的样品支架,该上表面具有与其相关联的等离子体层,该等离子体层包括周期性亚微米结构阵列;
[0007]
将待确定关注区域的样品施加到该样品支架的上表面;
[0008]
用光照射该样品,使得所述光与该样品和该样品支架相互作用;
[0009]
使用所述光在与所述样品和样品支架相互作用之后形成图像,其中,基于接收到的光的颜色,该样品的至少一个局部结构性质在该图像中是可见的;以及
[0010]
至少部分地基于该样品的至少一部分的颜色,选择施加到该样品支架的所述样品的关注区域。
[0011]
该局部结构性质优选地是该样品在某一位置处的介电常数。
[0012]
该方法可以包括对与所选有关区域相对应的后续分析样品执行后续分析。
[0013]
选择关注区域可以包括对该样品的包括该关注区域的部分进行切片,以产生与所选关注区域相对应的后续分析样品。
[0014]
在另一个方面,本发明提供了一种样品分析方法,该方法包括:
[0015]
提供具有上表面和下表面的样品支架,该上表面具有与其相关联的等离子体层,该等离子体层包括周期性亚微米结构阵列;
[0016]
将该样品施加到该样品支架的上表面;
[0017]
用光照射该样品,使得所述光与该样品和该样品支架相互作用;
[0018]
使用所述光在与所述样品和样品支架相互作用之后形成图像,其中,基于所接收到的光的颜色,该样品的至少一个局部结构性质在该图像中是可见的;以及
[0019]
使用所形成的图像来控制后续分析过程。
[0020]
使用所形成的图像来控制后续分析过程可以包括以下中的一项或多项:
[0021]
定义该后续分析中使用的一个或多个基准点和/或坐标系,
[0022]
选择样品的区域用于进一步分析;以及
[0023]
确定所述后续分析的顺序或时间表。
[0024]
在上述任一方面的一些实施例中,该方法可以包括选择施加到该样品支架的所述样品的关注区域,以及对与所选关注区域相对应的后续分析样品执行后续分析。选择该样品的关注区域可以包括对该样品的包括所选关注区域的部分进行切片,以产生与所选关注区域相对应的后续分析样品。
[0025]
在第一方面或第二方面的一些实施例中,与所选关注区域相对应的后续分析样品能够是在空间上与所选关注区域相对应的、从同一组织样品获取的不同样品。例如,后续分析样品可以是在平面视图中基本上在空间上与所选关注区域相对应的、源自同一组织样品的、其邻近的或接近邻近的切片中的样品。
[0026]
该样品可以用作该后续分析样品。
[0027]
在上述方面的一些实施例中,该后续分析过程是后续成像过程。在优选实施例中,该后续分析过程是后续显微术过程。
[0028]
在一些实施例中,该后续显微术过程是光学显微术过程。
[0029]
在一些实施例中,该后续显微术过程是电子显微术过程。
[0030]
在一些实施例中,该后续显微术过程是扫描探针显微术过程。
[0031]
在一些实施例中,该后续显微术过程是x射线显微术过程。
[0032]
该后续分析过程可以是tem过程。
[0033]
在第一方面或第二方面的一些实施例中,该方法包括确定所述后续分析的顺序或时间表。该方法可以包括优先地在关注区域上执行该后续分析。该方法可以包括仅在关注区域上执行该后续分析。替代性地,该方法包括在不是关注区域的其他区域之前对关注区域执行该后续分析。
[0034]
在第一方面或第二方面的一些实施例中,该方法可以包括从该样品传递一个或多个基准点和/或坐标系,用于在该后续分析中使用。该方法可以包括物理标记出一个或多个基准点。替代性地,该方法可以包括在使用所述光形成图像时使用的参考系与执行该后续分析时使用的参考系之间对齐现有基准点或坐标系。例如,可以相对于与样品支架相关的一个或多个基准点或坐标系来确定样品的取向。
[0035]
在另一个方面,提供了一种分析样品的方法,所述方法包括提供包括关注区域的样品;其中,在基于关注区域的后续分析之前,根据本披露内容的第一方面的实施例选择关注区域。
[0036]
该分析过程可以是后续成像过程。该成像过程可以是显微术过程。
[0037]
在一些实施例中,该后续显微术过程是光学显微术过程。
[0038]
在一些实施例中,该后续显微术过程是电子显微术过程。
[0039]
在一些实施例中,该后续显微术过程是扫描探针显微术过程。
[0040]
在一些实施例中,该后续显微术过程是x射线显微术过程。
[0041]
该后续显微术过程可以是tem过程。
[0042]
在另一方面,提供了一种使用上述任一方面的实施例来形成图像的系统。该系统可以包括显微镜,该显微镜具有图像形成系统、照射系统、以及样品支架,该样品支架具有上表面和下表面,该上表面具有与其相关联的等离子体层,该等离子体层包括周期性亚微米结构阵列。该系统可以包括图像捕获系统以用于产生该样品的图像。
[0043]
该系统可以包括用于后续分析的系统。
[0044]
在本披露内容的上述方面,该样品可以是生物样品。
[0045]
在本文所披露的方面的实施例中的结构或关注区域的鉴定可以根据以下任何一个的实施例来执行:
[0046]
申请人于2018年11月29日提交的发明名称为“method of identifying a structure[鉴定结构的方法]”的共同未决澳大利亚专利申请2018904550以及要求与本技术同一天提交的au 2018904550的优先权的国际专利申请;
[0047]
申请人于2018年11月29日提交的发明名称为“automated method of identifying a structure[鉴定结构的自动化方法]”的共同未决澳大利亚专利申请2018904551以及要求与本技术同一天提交的au2018904551的优先权的国际专利申请;
[0048]
每个申请的内容出于所有目的通过援引并入本文。
[0049]
在本说明书中,“形成图像”包括形成人类可感知的图像,例如通过聚焦光使得用户可以感知样品(或其一部分)的图像;或者生成样品(或其一部分)的数字或照片图像,用于存储、传输、显示或其他下游处理。
[0050]
应当注意的是,术语上表面和下表面并不旨在指代在样品制备或使用期间样品支架的特定取向。
附图说明
[0051]
本发明的说明性实施例将参照附图以非限制性示例的方式进行描述。与本国际申请一起提交的附图包括在本发明的实施例中使用的和因使用本发明的实施例而产生的彩色图像。颜色信息构成了实施例的披露内容的一部分。如果出现图像的黑白或灰度复制品,则可以从最初提交的文件中获得彩色披露内容。在附图中:
[0052]
图1a至图1c展示了在本披露内容的实施例中使用的示例性样品支架的细节。本发明不应被认为仅限于使用具有这些图中所展示的特定微结构阵列的样品支架。
[0053]
图2a和图2b展示了图1a的示例性样品支架,在该样品支架上放置了用于在本发明的实施例中使用的样品。
[0054]
图3是可用于执行本发明的实施例的系统的示意图。
[0055]
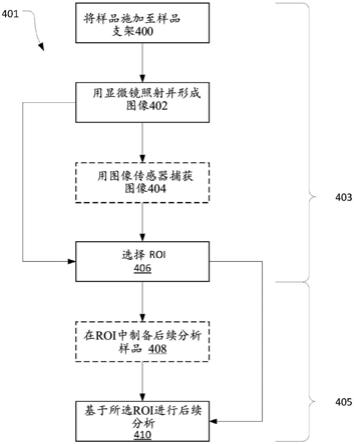
图4是展示了在本发明的实施例中执行的一种方法中的步骤的流程图。
[0056]
图5展示了使用以下样品形成的图像:在常规显微镜载玻片上的未染色样品(顶部);使用第一偏振光的纳米载玻片上的未染色样品,示出了可以用于鉴定样品结构的第一颜色对比度图像(中间);使用与第一偏振成90
°
的第二偏振光的纳米载玻片上的未染色样品,示出了可以用于鉴定样品结构的第二颜色对比度图像(第三个);在后续分析过程中捕获的对应样品的sem图像(底部)。
[0057]
图6a至图6e展示了在若干实施例中可用于基于鉴定的roi制备后续分析样品的步骤。
[0058]
图7展示了纳米载玻片样品支架的示例,在该纳米载玻片样品支架上放置了若干样品,使得能够鉴定一个或多个roi用于后续分析。
具体实施方式
[0059]
本发明人已经意识到,纳米载玻片的使用能够对分析技术进行有效的改进,这些分析技术利用了纳米载玻片的一个或多个独特优点。
[0060]
在特定实施例中,纳米载玻片的使用增强了快速鉴定样品中结构的能力,因为结构差异以对比色呈现,通常不需要对样品进行染色。在其他实施例中,纳米载玻片的使用可以通过在样品的一部分中选择性地表现出颜色对比度来增强看到样品中的结构的能力,样品的选择性地表现出颜色对比度的部分是在距样品支架的特征衰减距离内的那部分(例如平面区域)。相比之下,当样品被照射时,使用染色剂或染料来增强或引起样品中的强度对比度的常规光学显微术在样品的整个宽度上显示出这种对比度。这存在的缺点是,样品的视图(或拍摄的样品的图像)实际上是穿过样品整个厚度的总光吸收的二维投影。这会具有对观察者来说使样品中的细节模糊的作用。相比之下,使用纳米载玻片的组织学仅在样品中最靠近样品支架的部分产生颜色对比度,因此与仅依靠染色在接收到的光中产生强度对比度的常规显微术相比,可以有效地示出更小的结构。此外,染色可能需要几分钟或更长时间才能产生可用的样品。
[0061]
在优选的形式中,纳米载玻片可以用作分析过程中的初期。使用纳米载玻片的成像阶段可以在后续样品分析之前提供有效的分类过程。分类过程可以用来鉴定样品中的关注区域,以用于后续分析。例如给定结构或结构特征(例如细胞、细胞的一部分、组织等)的存在或不存在可以用于定义后续分析过程的关注区域。
[0062]
例如,纳米载玻片在无需染色且通常无需专门的样品制备的情况下,使用常规光学显微镜在样品中提供有效的对比度外观的能力,能够快速鉴定需要后续分析的样品或样品部分。此外,纳米载玻片能够在样品中进行视觉成像,否则可能无法提供显著的视觉对比度。
[0063]
由于一些分析技术的样品制备要求,经受了使用纳米载玻片的成像的样品在后续分析过程中使用是不切实际的。在这种情况下,或者如果需要额外的样品用于分析,则对应的样品可以用于后续分析,例如同一组织的邻近或附近切片可以用在后续分析中。在纳米载玻片上被成像的样品和对应的后续分析样品可以是同一组织样品的重叠薄片(优选地,但不一定相邻),使得当在平面视图中(即,在垂直于薄片面的方向上)观察时,这些薄片具
有相同或相似的结构构成。
[0064]
图1a示出了在本披露内容的示例中使用的样品支架的实施例。图1a示出了适用于本发明的样品支架的截面。样品支架100包括衬底,其上沉积有等离子体层102。图1b和图1c示出了两种类型的等离子体层102,其亚微米阵列已经被制造并且可以在实施例中使用。在其他实施例中可以使用其他阵列,包括1维线阵列。等离子体层均是150nm厚的银膜,但是也可以使用其他合适的材料。图1a的亚微米阵列采用圆形纳米孔形式,周期为450nm,以六边形图案排列。图1c在矩形图案上具有十字形纳米孔。十字形纳米孔在一个方向(此处定义为0
°
方向)上具有450nm的周期,在正交方向(定义为90
°
方向)上具有400nm的周期。这些阵列在470
‑
550nm范围内(在电磁谱的可见区域内)具有spp共振模式。为了保护等离子体层102的表面,在等离子体层102制造之后沉积氢倍半硅氧烷(hsq)(一种玻璃状材料)层104(10nm
±
1nm)。用hsq封盖后,样品支架100的上表面类似于可以在其上支撑样品的常规显微镜载玻片的上表面。在其他实施例中,可以使用金属氧化物封盖层(例如sio2)来代替hsq。
[0065]
将待成像的样品制备好并放置在根据以澳大利亚拉筹伯大学的名义提交的pct/au2018/050496或申请人于2018年11月29日提交的发明名称为“microscopy method and system[显微术方法和系统]”的共同未决澳大利亚专利申请2018904553以及要求与本技术同一天提交的au2018904553的优先权的国际专利申请的实施例的样品支架上。将样品106(通常是生物组织薄片,其在本发明的优选实施例中不需要被染色)放置在样品支架上、邻近等离子体层,如图2a所示。
[0066]
图3是被配置为执行根据本披露内容的方法的系统300的示意图。总体上,系统300包括适于接纳样品支架100的显微镜310。样品支架100是具有等离子体层的纳米载玻片(根据pct/au2018/050496的一方面制造的样品支架)。待成像的样品106被定位在样品支架上。在一些实施例中,显微镜是具有供用户观察的目镜的常规光学显微镜,然而,显微镜可以替代性地或附加地包括图像捕获系统,以用于生成用于显示、存储或供其他后续使用的数字图像。在一些形式中,显微镜310可以形成自动载玻片扫描仪的一部分。所展示的示例性系统300包括用于显示捕获的样品数字图像的用户终端312和用于存储捕获的图像的数据存储系统314。系统300进一步包括后续分析系统316。在使用中,如果使用纳米载玻片成像过程来选择样品106中的关注区域,则可以使用后续分析系统316来执行进一步的分析。取决于系统316的要求,后续分析样品106a可以与样品106相同。替代性地,可以对样品106进行处理和/或切片以形成样品106a。在另一示例中,不同的但对应的样品106s(未示出)可以在使用系统316的后续分析过程中使用。
[0067]
后续分析过程可以是后续成像过程。例如,后续分析过程可以是后续显微术过程,比如光学、电子、扫描探针或x射线显微术。在示例性实施例中,分析系统316是透射电子显微镜。图4是展示了本披露内容的各方面的步骤的流程图,这些步骤可以用来选择关注区域用于后续分析。在初始阶段,方法401包括用于选择403样品的关注区域以用于后续分析过程405的过程。在这种情况下,样品可以是图2a、图2b等的样品106。方法401从将样品106施加到样品支架100(此时是纳米载玻片)的步骤400开始。在402,载玻片和样品支架100如本文所阐述的被照射,并且形成图像。可选地,图像在步骤404以数字形式被捕获。随后,分析由用户直接感知的或在步骤404中捕获的图像,并且在408可以将样品中的一个或多个结构特征鉴定为关注区域(roi),在该关注区域上将执行后续分析。在步骤406中roi的选择可以
由人或者以自动化方式来执行,该自动化方式如申请人于2018年11月29日提交的发明名称为“automated method of identifying a structure[鉴定结构的自动化方法]”的共同未决澳大利亚专利申请2018904551以及要求与本技术同一天提交的au2018904551的优先权的国际专利申请中所阐述的,这两个申请的内容出于所有目的通过援引并入本文。
[0068]
roi的鉴定步骤406至少使用样品图像中表现出的颜色来执行。图像中特定位置的颜色代表样品的局部物理性质。特别地,通过使用具有包括周期性亚微米结构阵列的等离子体层的样品支架(纳米载玻片),表现出颜色对比度,其对样品中局部介电常数进行了编码。从图像中选择roi寻求鉴定和选择样品中的一个或多个关注结构,在关注结构上需要进一步的分析。关注结构可以例如包括细胞、细胞群、细胞的一部分、细胞之间的胞间隙、细胞中的空隙、或上述任一者的形态。最优选地,有关特征和/或结构指示样品或其一部分的健康状况。
[0069]
图像中非凡的光学对比度的基本机制是光与样品支架的等离子体层中的金属表面的自由电子的集体振荡的共振作用,被称为表面等离极化激元(spp)。透过与电介质标本接触的亚波长孔阵列的透射光的光谱变化是spp共振模式λ
θspp,d
,的波长偏移δλ的函数,其中,上标θ表示入射偏振角(对于未偏振光,符号被删除),并且下标指示介电常数对应于样品(d=s)还是空气(d=a)。spp模式由透射光谱中的峰值来表征,当厚度为t的样品放置在纳米孔之上时,相对于空气的对应波长偏移由下式给出:
[0070]
δλ≈(λ
θsp,s
‑
λ
θspp,a
)(1
‑
exp(
‑
2t/l
d
)),
ꢀꢀꢀ
(1)
[0071]
其中,l
d
~λ/2√ε
d
是spp电磁场的特征衰减长度,其本身是样品的介电常数ε
d
的函数。在样品比图2b的示例中所展示的样品的特征衰减长度更厚的情况下。在此示例中,特征衰减长度l
d
由附图标记110指示。如可以看出的,样品支架100上的样品108比衰减长度110厚。随着膜厚度的增加,透射spp共振峰越来越多地被红移,直到它等于λ
θspp
,此后不再发生颜色变化。因此,当使用标准透射明场显微镜时,将导致空间分辨的颜色分布,这与样品中局部介电常数的变化直接相关。通过在光谱中编码的局部介电常数,产生了显著的色度对比效果。这意味着以前由于缺乏对比度而难以检测到的光学透明样品中的任何结构都可以借助于图像中捕获的颜色对比度而在可见光透射图像中检测到。此外,与当样品被照射时使用染色剂或染料在样品中引起或增强强度对比度的常规光学显微术相比,优选的实施例产生代表样品内的窄层(小于约200nm)的可辨别的颜色对比度。常规显微术示出了贯穿样品整个厚度的强度对比度。这具有的缺点是(在常规显微术中),样品的图像实际上是样品整个厚度(可能明显厚于200nm)的总光吸收的二维投影。这可能具有对于对观察者而言使样品细节模糊的作用。视觉上,这可能会使图像中可见的结构模糊不清或模糊。相比之下,使用纳米载玻片的组织学仅在样品最靠近样品支架的部分产生颜色对比度,因此可以有效地示出大小比仅依靠染色的常规显微术更小的结构。如常规光学显微术领域的技术人员所理解的,较薄的薄片可以在某种程度上改善模糊不清或模糊问题,但是会导致伴随的缺点,即薄的薄片无法示出与薄的薄片明显的强度对比度。
[0072]
使用具有上表面面和下表面(上表面具有与其相关联的等离子体层,等离子体层包括周期性亚微米结构阵列)的纳米载玻片样品支架的光学显微术在(与大多数显微技术相比)不需要长时间制备样品的情况下使结构可见的能力意味着它非常适合鉴定样品的关注区域用于后续分析的快速且潜在的无损过程。步骤410中的后续分析可以使用不同的分
析模式进行,其方式为利用关注区域的优先选择,例如:
[0073]
可以基于从过程403确定的一个或多个基准点和/或坐标系来定向或映射对其执行后续分析的样品;
[0074]
可以进行样品的一部分的物理选择,例如通过对样品的包括关注区域的部分进行切片来产生后续分析样品,从而可以更有效或高效地分析roi,例如无需分析原始样品的剩余部分;或
[0075]
可以执行所述后续分析的顺序或时间表来优先处理roi,例如首先分析它,或者更详细地分析它等。
[0076]
图5展示了使用过程403捕获的图像的若干示例,并且展示了鉴定示例性样品中的结构的能力。图像出现在显微镜下显现,没有染色或标记。
[0077]
对于这些组织学样品,通过显微注射由1.3kb mbp 58序列和3.4kb c
‑
myc基因组dna组成的4.7kb dna片段(包括内含子1的一部分、外显子2至3和38个非翻译序列19中的316bp)来产生转基因小鼠。2
‑
50系谱在9号染色体上携带了大约10个构建体副本,并且是基于单独在该系谱中(在最初产生的七个系谱中)明显的颤抖表型的基础上分离出来的。转基因小鼠和非转基因的同窝小鼠在37℃时通过左心室灌注磷酸盐缓冲盐水2min,然后灌注磷酸盐缓冲液(ph 7.4、含200iu肝素/100ml)中的4%多聚甲醛/2.5%戊二醛。对于图5b,在经由切片法从视神经上切下切片之前,将组织置于4℃原位放置1小时。将组织固定在10%缓冲福尔马林中,石蜡包埋并切片到载玻片或纳米载玻片上。
[0078]
图5示出了从70nm米厚的视神经薄片收集的图像。这种切片通常只能使用透射电子显微术(tem)来观察,而使用常规光学显微术基本上是看不到的,如在显示未染色样品的顶部图片中所看到的那样。中间和下部的图片示出了图像(左)及其特写细节(右)。中间的图片示出了用0
°
入射偏振照射样品时捕获的图像。下部的图片示出了同一样品,但是用具有90
°
入射偏振的光照射。
[0079]
所使用的纳米载玻片包括周期性纳米孔阵列,这些纳米孔阵列是使用聚焦离子束(fib)光刻技术(helios nanolab 600 dual beam fib
‑
sem,fei)或光刻法(用于大面积)制造的。在阵列制造之后,旋涂氢倍半硅氧烷(hsq)保护层。经由暴露于电子,hsq被转化为无定形氧化硅。在图5的示例中,周期性阵列具有结合图1c阐述的结构,其在矩形图案上具有十字形纳米孔。十字形纳米孔在一个方向(此处定义为0
°
方向)上具有450nm的周期,在正交方向(定义为90
°
方向)上具有400nm的周期。
[0080]
明场和dic数据是使用尼康(nikon)ti
‑
u显微镜系统收集的,其中物镜为60
×
(na=0.7);使用isoplane sct 320(美国普林斯顿仪器公司)以1200光栅/mm的速度收集光谱数据。光谱数据相对于裸衬底被归一化。这里呈现的所有图像都是通过显微镜“观察”的,丝毫没有应用任何图像处理。bruker dimension icon afm(原子力显微镜)用于收集形貌数据和线扫描。
[0081]
从第二和第三图像中可以很容易地看出,使用纳米载玻片,由于图像中表现出的颜色对比度,样品中的结构可以很容易地可视化。样品内的不同结构的颜色反映了不同介电常数的区域。此外,同一类型的结构也往往在整个样品中以同一颜色显现,使得能够可靠地鉴定这种结构,
[0082]
发明人已经观察到,改变入射偏振方向(对常规明场图像没有影响)能够选择性地
增强组织(比如对于大范围的病理来说至关重要的髓鞘)的亚细胞结构。这被认为是由于亚微米阵列在平行于每个偏振角的方向上的周期性不同。不同的周期性被认为调谐了透射光谱,使得给定介电常数的结构显现的颜色发生变化。这使得能够选择性地增强或着色具有某些性质的结构。因此,典型靶结构(例如细胞类型)的颜色调谐可以通过选择亚微米周期结构的参数(例如周期、大小、形状、阵列几何形状中的一个或多个)来执行,使得靶结构显现在特征颜色或色带中。如将了解的,这极大地增强了靶结构的快速检测或其特征的确定。
[0083]
通过在选择过程403中使用纳米载玻片进行可视化,可以确定关注区域并用于后续成像。例如,可以确定在右侧图像中放大并由左侧图像中的方形指示的区域是要在后续分析过程405中分析的关注区域。
[0084]
如将了解的,癌症和其他疾病的鉴定可以基于细胞形态的细微变化,比如细胞骨架和细胞核的改变。这包括细胞对称性、形状、核多形性/组织。可以基于细胞大小、形状和组织纹理区分细胞类型。使用本发明的实施例允许通过使用纳米载玻片来定义后续分析过程的关注区域,从而增强这些特征和结构的可见性。此外,当形态减小/受影响时(由于组织保存/制备技术或当仅存在很少的难以发现的癌症载玻片时),仅基于形态很难做出癌症的准确诊断。在这种情况下,本发明的实施例提供颜色作为区分特征。即,当更大尺度的形态受到影响时,颜色对比度仍然是可见的,从而能够定义roi。取决于步骤410中的后续分析过程的性质,可能需要执行合适的样品制备步骤408来产生合适的后续分析样品。在一些实施例中,这可以包括对过程404中使用的包括所选关注区域的样品的一部分进行切片,以产生与所选关注区域相对应的后续分析样品。
[0085]
然而,在其他实施例中,与所选关注区域相对应的后续分析样品可以是在空间上与所选关注区域相对应的、从同一组织样品获取的不同样品。例如,后续分析样品可以是在平面视图中基本上在空间上与所选关注区域相对应的、源自同一组织样品的、其邻近的或接近邻近的切片中的样品。
[0086]
图5的底部图片展示了由扫描电子显微镜捕获的所选关注区域的图像(即,在右侧展示并由整个样品图像上的框所指示的放大部分)。此时,sem成像是在所使用的同一样品上执行的或者是纳米载玻片光学显微术,但是也可以在在空间上与成像在图5的顶部三个图片中的样品相对应的后续分析样品上执行执行。
[0087]
在步骤410中,因为roi是最重要的,所以sem过程可以限于任一roi。替代性地,roi可以在样品的其他部分之前成像。在一些实施例中,后续分析过程可以由roi引导,例如,可以选择用于后续分析的分析参数来优化关注区域的分析。
[0088]
如将在图5的sem图像中观察到的,样品支架的等离子体层中的亚微米结构在sem图像中显现为一系列黑点。
[0089]
图6示出了这些情况中的每种情况的示例。在此示例中,从组织样品600中切下第一样品108。样品108被如图2b所展示的那样施加到纳米载玻片上,并且如上所述被成像。此时,纳米载玻片上的样品中有两个结构602和604可见。然而,由于结构相较于彼此和/或周围组织的相对颜色,部分602被确定为需要进一步分析,并被选择为关注区域。由于样品108的厚度,需要将其切成更薄的薄片和更小的部分以用于tem分析,例如,需要切割成直径约3mm、厚度为70nm的圆片。还需要适当的固定、树脂浸润和固化以及tem显微术领域技术人员已知的其他方法。虽然这是可能的,但是这可能是不切实际的,例如,如果样品108的制备需
要不相容的处理。因此,在一些实施例中,可以产生与关注区域相对应的不同的后续分析样品。例如,可以使用从与样品108相同的组织样品被切片的组织切片。这在图6a中被示出。切片606是覆盖组织样品600中的样品108的薄片。如可以看出的,在平面视图中,切片606将具有与样品108相似的特征(602a和604a),特别是在平面视图中(即,当在垂直于薄片方向的方向上观察时),它们可以紧密对应。如将了解的,尽管薄片606直接邻近样品108,但在实践中,后续分析样品606可以源自与样品108分离的位置,只要预期与样品108中的roi在很大程度上共享结构特征以便后续分析具有价值即可。
[0090]
可以对样品606进行进一步的切片,使得样品的与关注区域602相对应的部分为后续分析做好准备。
[0091]
如将理解的,对于tem示例,这通常意味着将制备好的样品放置在tep网格600上,比如在图6d中所示出的网格。tem网格可能具有在其上定义的可鉴定的基准612或轴线。这可以与后续分析样品对齐,使得在纳米载玻片成像过程中定义的任何基准或坐标轴以与tem网格的基准612或坐标轴的已知的关系定位。图6e展示了施加至网格610的图6c的样品,使得关注区域602a可以在tem过程中被成像。
[0092]
图7展示了本方法的替代性实施例。在此实施例中,提供了纳米载玻片100。一系列tem网格和相关联的样品,例如网格610和样品602a,被放置在该纳米载玻片上。然后,可以使用如结合选择过程403所述的纳米载玻片将该系列样品一起成像,并且可以选择一个或多个tem网格和相关联的样品作为后续分析的关注区域。在此示例中,这可能只需要将所选样品在其tem网格上加载到tem中进行成像。此时,不需要对在初始成像过程中没有表现出任何关注的样品执行不必要的tem成像。在此实施例中,纳米载玻片100的上表面可以设置有释放层,或者用于促进从纳米载玻片移除tem网格以使得能够执行tem分析的其他技术。例如,tem网格可以浮离纳米载玻片,或者通过施加静电或声能来释放。
[0093]
例如,此时,样品602a和700的蓝色着色可以指示它们是关注区域,而绿色样品702和704可以指示不需要进一步分析的健康组织。
[0094]
虽然已经在此实施例中描述了tem,但是本披露内容不应被认为是如此限制。实施例可以使用其他后续分析技术。应当了解,通过仅选择合适的roi进行分析来代替费力地分析整个初始样品,可以提高后续分析系统的实际效率和有效吞吐量。
[0095]
应当理解的是,在本说明书中披露和限定的本发明可扩展至所提及的或者从文本部分和附图部分显而易见的单个特征的两个或更多个的所有替代性组合。所有这些不同组合构成本发明的多个替代性方面。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1