一种镇静安神保健品中违法添加药物的同时检测方法与流程
本发明属于涉及保健品检测领域,提供了一种镇静安神保健品中违法添加药物的同时检测方法。
背景技术:
睡眠是人体重要且必须的生理需求。然而随着社会生活节奏的加快,不规律,压力的与日俱增,失眠现象日趋严重。现代医学对失眠进行了深入的研究,也逐渐找到了一系列的用于治疗失眠的药物,主要有巴比妥类(第一类),苯二氮卓类(第二类)和非典型苯二氮卓类(新型)等,这些药物具有较强的镇静催眠作用,但长期使用会产生依赖性甚至毒副作用。因此,一些以中药、中成药为主要成分的保健品因为不良反应小,受到了市场的青睐。但是,也出现在保健品中违法添加镇静催眠药物来提高改善睡眠的功效,欺骗消费者的现象,给保健品市场带来了恶劣影响,阻碍了中医药和保健品事业的健康长远发展。
目前,保健食品中镇静催眠药物的检测方法主要有薄层色谱法、高效液相色谱法、气相色谱-质谱法和液相色谱-串联质谱法。其中薄层色谱法和高效液相色谱法检测分辨率较弱,由于保健食品杂质较多,常出现假阳性现象;气相色谱质谱法灵敏度较差;由于液相色谱-串联质谱法具有灵敏度高、抗干扰能力强的优势,是目前鉴别保健品非法添加化学药物最有效的方法。
国家食品药品监督管理局《药品检验补充检验方法和检验项目批准件编号2009024》采用薄层色谱法初筛,液相色谱定性,阳性样品液相色谱串联质谱全扫描确证的方法较为繁琐,文献检索的采用液相色谱串联质谱检测的项目较为单一,覆盖面不足。
技术实现要素:
本发明的一个目的是提供一种镇静安神保健品中违法添加药物的同时检测方法,以改进的液相色谱串联质谱法对保健品中苯二氮卓类(地西泮、劳拉西泮、氯硝西泮、硝西泮、奥沙西泮、氯氮卓、三唑仑、艾司唑仑、阿普唑仑、氯丙嗪)、巴比妥类(巴比妥、异戊巴比妥、司可巴比妥、苯巴比妥)和非典型苯二氮卓类(扎来普隆)等镇静催眠药物进行同时分析检测,具有快速简便,灵敏准确等特点,对保健品中违法物质添加检测工作具有实际指导意义。
本发明采用以下的技术方案,
一种镇静安神保健品中违法添加药物的同时检测方法,包括以下步骤流程,
s1、配制标准品:分别准确称取10mg标准品置于10ml容量瓶中,用甲醇溶解稀释定容,获得标准品溶液;再分别准确移取各所述标准品溶液,用甲醇稀释成各标准品浓度均为100ng/ml的混合标准溶液;本步骤是将所要测定的每种违法添加药物的标准品配制成标准品溶液后,再混合到甲醇中配制成每种违法添加药物标准品的浓度都为100ng/ml的混合标准溶液;
s2、标准工作曲线配置:分别准确吸取步骤s1中所述混合标准溶液5μl、10μl、25μl、50μl、100μl于50ml离心管中,加入甲醇溶解均匀后体积为5ml,超声提取20min,4000r/min离心5min,取上清液1ml,氮吹浓缩至近干,再用体积比2:8的甲醇水溶液定容至1.0ml,过滤,上机分析;
s3、样品前处理和测试;取固体样品0.5g或液体样品0.5ml,置于50ml洁净的离心管中,加入甲醇溶解均匀后体积为5ml,超声提取20min,4000r/min离心5min,取上清液1ml,氮吹浓缩至近干,再用体积比2:8的甲醇水溶液定容至1.0ml,过滤,上机分析;
步骤s2和步骤s3中所述上机分析的仪器参数为,
(1)液相色谱条件
色谱柱:acquityuplcbehc18柱(2.1mm×100mm,1.7μm);柱温:35℃;流速:0.3ml/min;进样量:5μl;流动相a:超纯水;流动相b:乙腈;
(2)质谱条件
离子源:esi;离子源温度:325℃;毛细管电压:4000v(+),3500v(-);鞘气压力:30psi;辅助气压力:10psi;蒸发气温度:350℃。
优选的,步骤s1中所述标准品选自巴比妥类、苯二氮卓类和非典型苯二氮卓类镇静催眠药物。
更优选的,所述巴比妥类镇静催眠药物选自巴比妥、异戊巴比妥、司可巴比妥和苯巴比妥。
更优选的,所述苯二氮卓类镇静催眠药物选自地西泮、三唑仑、劳拉西泮、氯硝西泮、硝西泮、奥沙西泮、氯氮卓、艾司唑仑、阿普唑仑和氯丙嗪。
更优选的,所述非典型苯二氮卓类镇静催眠药物为扎来普隆。
优选的,步骤s3中所述固体样品为片剂时预先除去包衣,固体样品为胶囊时预先取出内容物,固体样品为丸剂时预先剪碎研磨成粉。
优选的,步骤s2和s3中所述过滤为采用孔径0.22μm滤膜。更优选的,滤膜为尼龙滤膜。
优选的,所述液相色谱洗脱条件为:第0分钟,流动相a:流动相b=75:25(体积比);第1分钟,流动相a:流动相b=65:35(体积比);第4分钟,流动相a:流动相b=55:45(体积比);第5分钟,流动相a:流动相b=55:45(体积比);第6分钟,流动相a:流动相b=10:90(体积比);第7分钟,流动相a:流动相b=10:90(体积比);第7.01分钟,流动相a:流动相b=75:25(体积比);第9分钟,流动相a:流动相b=75:25(体积比)。
质谱扫描离子信息见表1。
表1质谱扫描离子信息
注:*为定量离子
步骤s3中如果检测结果高出标准曲线范围,待测液溶液再稀释10~100倍后进样分析。
本发明的有益效果:
(1)采用外标法定量,巴比妥、苯巴比妥、异戊巴比妥和司可巴比妥四种项目在10~200ng/ml,其余项目在1~20ng/ml浓度范围内的曲线方程相关系数r2都>0.99,具有良好的线性关系。以3倍信噪比时相应浓度确定检测低限,以10倍信噪比时相应浓度确定定量低限。本发明对镇静剂类药物的检测限为5.97×10-5~3.77μg/kg,定量限为1.99×10-4~12.6μg/kg,显著优于《药品检验补充检验方法和检验项目批准件编号2009024》的检测水平,说明该方法灵敏度高。
(2)以片剂、胶囊、液态保健食品为基底,分别进行低浓度和高浓度两种水平的加标,同时做平行试验(n=6),其中测定回收率及rsd。结果显示,在两个加标浓度条件下镇静剂检测项目的回收率在71.8%~116.7%,相对标准偏差rsd(n=6),在0.2%~4.4%,测定结果符合药物残留检测分析的要求。
附图说明
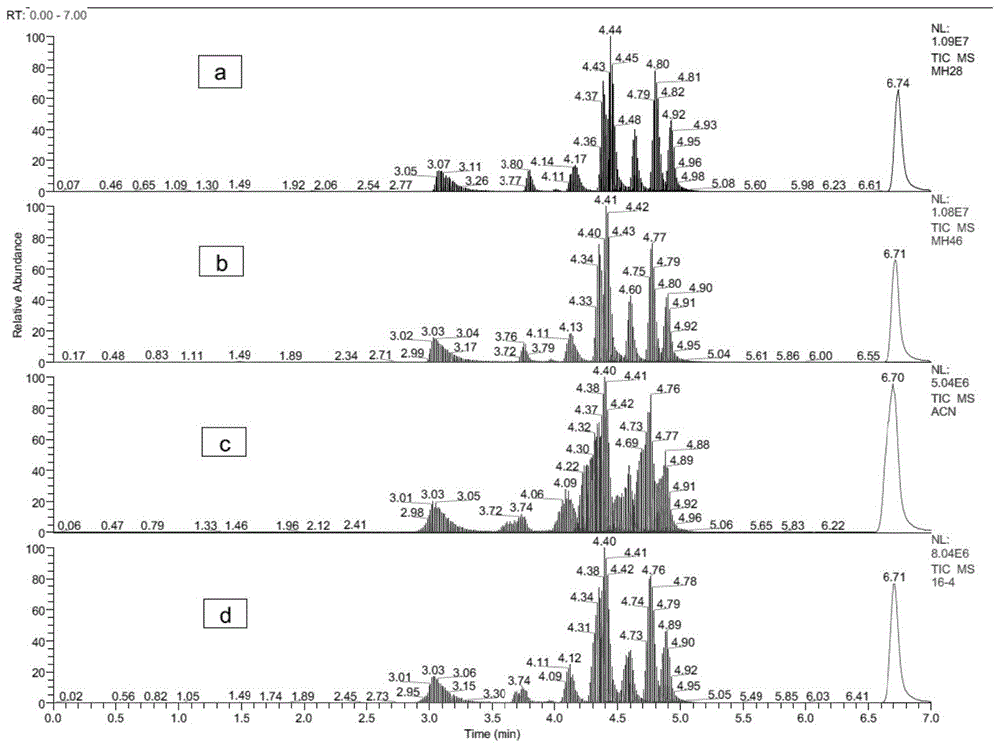
图1为本发明实施例中不同定容溶剂的tic谱图,
其中,(a)为甲醇水(2:8,v/v)定容的tic谱图;
(b)甲醇水(4:6,v/v)定容的tic谱图;
(c)乙腈定容的tic谱图;
(d)甲醇定容的tic谱图。
具体实施方式
以下藉由特定的具体实施例说明本发明的实施方式,熟悉此技艺的人士可由本说明书所揭示的内容轻易地了解本发明的其他优点及功效。
须知,本说明书所附图式所绘示的结构、比例、大小等,均仅用以配合说明书所揭示的内容,以供熟悉此技艺的人士的了解与阅读,并非用以限定本发明可实施的限定条件,故不具技术上的实质意义,任何结构的修饰、比例关系的改变或大小的调整,在不影响本发明所能产生的功效及所能达成的目的下,均应落在本发明所揭示的技术内容得能涵盖的范围内。同时,本说明书中所引用的如「上」、「内」、「外」、「底」、「一」、「中」等用语,也仅为便于叙述的明了,而非用以限定本发明可实施的范围,其相对关系的改变或调整,在无实质变更技术内容下,当也视为本发明可实施的范畴。如无特别指明,以下实施例中的份数都为重量份数。
实施例
配制标准品:分别准确称取10mg标准品(标准品分别为巴比妥、异戊巴比妥、司可巴比妥、苯巴比妥、地西泮、三唑仑、劳拉西泮、氯硝西泮、硝西泮、奥沙西泮、氯氮卓、艾司唑仑、阿普唑仑、氯丙嗪和扎来普隆)置于10ml容量瓶中,用甲醇溶解稀释定容,获得各标准品溶液;再准确移取上述各标准品溶液,加入到10ml容量瓶中,用甲醇稀释成各标准品浓度均为100ng/ml的混合标准溶液;
标准工作曲线配置:分别准确吸取上述混合标准溶液5μl、10μl、25μl、50μl、100μl于50ml离心管中,加入甲醇旋涡混匀后体积为5ml,超声提取20min,4000r/min离心5min,取上清液1ml,氮吹浓缩至近干,再用体积比2:8的甲醇水溶液定容至1.0ml,0.22μm尼龙滤膜过滤,上机分析;
样品前处理和测试;市售镇静安神保健品为测试对象,取0.5固体测试对象(固体测试对象为片剂时预先除去包衣,固体测试对象为胶囊时预先取出内容物,固体测试对象为丸剂时预先剪碎研磨成粉)或0.5ml液体测试对象,置于50ml洁净的离心管中,加入甲醇旋涡混匀后体积为5ml,超声提取20min,4000r/min离心5min,取上清液1ml,氮吹浓缩至近干,再用体积比2:8的甲醇水溶液定容至1.0ml,0.22μm尼龙滤膜过滤,上机分析;
上述上机分析的仪器参数为,
(1)液相色谱条件
色谱柱:acquityuplcbehc18柱(2.1mm×100mm,1.7μm);柱温:35℃;流速:0.3ml/min;进样量:5μl;流动相a:超纯水;流动相b:乙腈;
液相色谱洗脱条件为:第0分钟,流动相a:流动相b=75:25(体积比);第1分钟,流动相a:流动相b=65:35(体积比);第4分钟,流动相a:流动相b=55:45(体积比);第5分钟,流动相a:流动相b=55:45(体积比);第6分钟,流动相a:流动相b=10:90(体积比);第7分钟,流动相a:流动相b=10:90(体积比);第7.01分钟,流动相a:流动相b=75:25(体积比);第9分钟,流动相a:流动相b=75:25(体积比)。
分别将上述标准工作曲线配置和样品前处理和测试步骤中的定容溶剂调整为甲醇、甲醇水(4:6,v/v)和乙腈,tic图谱对比如图1所示。结果表明,甲醇水(2:8,v/v)能够显著改善峰型,并提高响应。
(2)质谱条件
离子源:esi;离子源温度:325℃;毛细管电压:4000v(+),3500v(-);鞘气压力:30psi;辅助气压力:10psi;蒸发气温度:350℃。质谱扫描离子信息见表1。
样品前处理和测试中测试巴比妥、苯巴比妥、异戊巴比妥和司可巴比妥时无需稀释,测试地西泮、三唑仑、劳拉西泮、氯硝西泮、硝西泮、奥沙西泮、氯氮卓、艾司唑仑、阿普唑仑、氯丙嗪和扎来普隆时待测样品稀释10倍。
分别以片剂(预先除去包衣)、胶囊(预先取出内容物)、液态市售保健品为测试对象,分别进行低浓度和高浓度(测试巴比妥、苯巴比妥、异戊巴比妥和司可巴比妥,低浓度和高浓度分别为20μg/kg和100μg/kg;测试地西泮、三唑仑、劳拉西泮、氯硝西泮、硝西泮、奥沙西泮、氯氮卓、艾司唑仑、阿普唑仑、氯丙嗪和扎来普隆,低浓度和高浓度分别为2μg/kg和10μg/kg)两种水平的加标,同时做平行试验(n=6),其中测定回收率及rsd,结果见表2。结果显示,在两个加标浓度条件下镇静剂检测项目的回收率在71.8%~116.7%,相对标准偏差rsd(n=6)在0.2%~4.4%。测定结果符合药物残留检测分析的要求。
表2加标回收率
以3倍信噪比时相应浓度确定检测低限,以10倍信噪比时相应浓度确定定量低限,结果见表3。各检测项目曲线方程相关系数r2都>0.99,具有良好的线性关系。因此,本发明对镇静剂类药物的检测限为5.97×10-5~3.77μg/kg,定量限为1.99×10-4~12.6μg/kg。
表3检测项目线性相关系数、检测低限与定量限
- 还没有人留言评论。精彩留言会获得点赞!