一种用于分析一种或多种待分析物的检测系统及其方法与流程
1.本发明涉及生物芯片检测技术领域,具体涉及一种用于分析一种或多种待分析物的检测系统及其方法。
背景技术:
2.目前市场上使用的液相悬浮芯片检测仪主要基于流式细胞术和荧光成像术的原理实现检测,有半自动和全自动两种。其中半自动化设备除了检测等基本控制由机器完成外,其它比如加样、加试剂、孵育等过程需要人工参与才能完成,这不仅增加了人力劳动成本,而且人工操作容易造成误差,影响检测结果的准确性。全自动化液相悬浮芯片检测仪实现了整个分析过程的自动化,包括加样、加试剂、孵育及检测等过程都由机器来完成,无需人工参与,自动化程度高,但是全自动化设备采用试管盛装样本,采用反应杯作为样本与试剂的反应容器,导致需要采集大量样本才能满足检测;而且试管的运输需要样本架、轨道以及驱动样本架在轨道上移动的驱动装置,样本和试剂的吸取需要探针、输送需要各种管路以及清洗装置,这些造成了目前的全自动化设备体积庞大、结构复杂、造价较高,仅适合样本量较大的大型医院和大型体检中心。
技术实现要素:
3.本技术提供一种用于分析一种或多种待分析物的检测系统及其方法,以促进设备的小型化。
4.根据第一方面,本技术提供一种用于分析一种或多种待分析物的检测系统,包括:
5.收容装置,用于容纳并固定微流控芯片;所述微流控芯片包括加样口、反应区和微流检测通道,所述加样口与所述反应区通过微流体通道和/或微阀连通,所述反应区与所述微流检测通道通过微流体通道和/或微阀连通;所述加样口用于加样;所述反应区用于为样本和试剂的反应提供反应场所;反应后的一种或多种待分析粒子被约束成单列或单层通过所述微流检测通道;
6.光源,用于照射所述微流检测通道内的待分析粒子,以使待分析粒子受照射后发出与待分析粒子本身特性相关的光信号;
7.检测装置,用于检测待分析粒子受照射后发出的光信号,将光信号转换成光信号数据;所述光信号数据为经过处理能得到光信号所指代的待分析物和/或待分析物含量的数据。
8.根据第二方面,本技术提供一种液相芯片检测系统,包括:
9.收容装置,用于容纳并固定微流控芯片;所述微流控芯片包括加样口和反应检测区,所述加样口和反应检测区通过微流体通道和/或微阀连通;所述加样口用于加样;所述反应检测区用于为样本和试剂的反应提供反应场所,为反应后的一种或多种待分析粒子提供检测场所;所述待分析粒子在所述反应检测区成单层排列;
10.光源,用于照射反应检测区内的待分析粒子,以使待分析粒子受照射后发出与待
分析粒子本身特性相关的光信号;
11.检测装置,用于检测待分析粒子受照射后发出的光信号,将光信号转换成光信号数据;所述光信号数据为经过处理能得到光信号所指代的待分析物和/或待分析物含量的数据。
12.所述的检测系统中,还包括粒子约束装置;所述粒子约束装置用于将所述反应检测区中的所述待分析粒子约束成单层排列,以便于检测。
13.所述的检测系统中,所述光信号包括编码光信号和报告光信号;所述检测装置检测待分析粒子受照射后发出的光信号,将光信号转换成光信号数据包括:
14.检测待分析粒子受照射后发出的光信号,得到各种待分析粒子的编码光信号和报告光信号;将编码光信号转换成编码光信号数据,将报告光信号转换成报告光信号数据;所述编码光信号数据为经过处理能得到编码光信号所指代的待分析物的数据;所述报告光信号数据为经过处理能得到报告光信号所指代的待分析物含量的数据。
15.所述的检测系统中,还包括处理器,所述处理器用于对所述编码光信号数据进行处理,得到编码光信号所指代的待分析物;对同种待分析粒子的每个待分析粒子的报告光信号数据进行处理,得到该种待分析粒子中待分析物的含量。
16.所述的检测系统中,还包括储气腔,所述储气腔设置在微流控芯片内部或外部,用于驱动微流控芯片中的样本和/或液体移动以实现样本的反应和/或检测。
17.所述的检测系统中,还包括样本过滤器,用于过滤样本中对检测造成干扰的物质。
18.所述的检测系统中,所述待分析粒子在磁场中具有磁性,所述粒子约束装置通过磁力将所述反应检测区中的待分析粒子约束成单层排列,并通过磁力将所述待分析粒子固定在所述反应检测区。
19.所述的检测系统中,还包括设置在所述微流控芯片内部和/或外部的试剂存储区;所述试剂存储区包括粒子包被试剂和/或发光标记试剂;所述粒子包被试剂干燥在所述试剂存储区,或者凝胶态存储在所述试剂存储区,或者液态存储在所述试剂存储区;所述发光标记试剂干燥在所述试剂存储区,或者凝胶态存储在所述试剂存储区,或者液态存储在所述试剂存储区;所述试剂存储区与所述反应区或反应检测区为同一区域或不同区域或共同使用部分区域。
20.所述的检测系统中,所述待分析粒子为结合有样本中的待分析物的磁性粒子;所述检测系统还包括粒子驱动装置;所述粒子驱动装置用于在样本与试剂的反应结束之前驱动磁性粒子运动,以加速样本中的待分析物与试剂中的磁性粒子反应,和/或,用于驱动待分析粒子运动,以转移待分析粒子。
21.所述的检测系统中,还包括用于控制样本与试剂反应温度的温度控制装置。
22.根据第三方面,本技术提供一种分析一种或多种待分析物的方法,包括如下步骤:
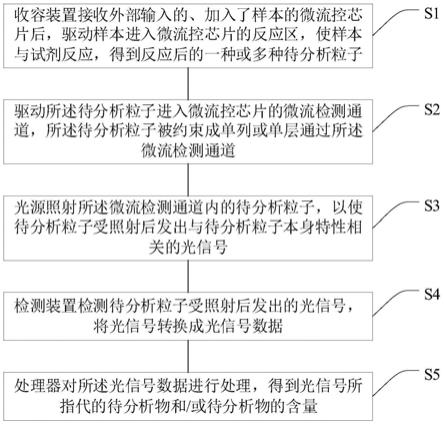
23.收容装置接收外部输入的、加入了样本的微流控芯片后,驱动样本进入微流控芯片的反应区,使样本与试剂反应,得到反应后的一种或多种待分析粒子;
24.驱动所述待分析粒子进入微流控芯片的微流检测通道,所述待分析粒子被约束成单列或单层通过所述微流检测通道;
25.光源照射所述微流检测通道内的待分析粒子,以使待分析粒子受照射后发出与待分析粒子本身特性相关的光信号;
26.检测装置检测待分析粒子受照射后发出的光信号,将光信号转换成光信号数据;
27.处理器对所述光信号数据进行处理,得到光信号所指代的待分析物和/或待分析物的含量。
28.根据第四方面,本技术提供一种分析一种或多种待分析物的方法,包括如下步骤:
29.收容装置接收外部输入的、加入了样本的微流控芯片后,驱动样本进入微流控芯片的反应检测区,使样本与试剂反应,得到反应后的一种或多种待分析粒子;
30.将所述反应检测区中的所述待分析粒子约束成单层排列,以便于检测;
31.光源照射反应检测区内的待分析粒子,以使待分析粒子受照射后发出与待分析粒子本身特性相关的光信号;
32.检测装置检测待分析粒子受照射后发出的光信号,将光信号转换成光信号数据;
33.处理器对所述光信号数据进行处理,得到光信号所指代的待分析物和/或待分析物的含量。
34.依据上述实施例的用于分析一种或多种待分析物的检测系统及其方法,样本和试剂在微流控芯片中反应,由于微流控芯片集成了样本和试剂反应及检测所需的相关液路,故无需试管、反应杯以及相关的装置,不仅需要采集的样本量变少,而且极大的节省了检测系统的体积,有利于设备的小型化。
附图说明
35.图1为本发明提供的用于分析一种或多种待分析物的检测系统一实施例的结构框图;
36.图2为本发明提供的用于分析一种或多种待分析物的检测系统一实施例的原理图;
37.图3为本发明提供的用于分析一种或多种待分析物的检测系统另一实施例的原理图;
38.图4为本发明提供的用于分析一种或多种待分析物的检测系统中,一实施例的液路示意图;
39.图5为试剂存储区一实施例的示意图;
40.图6为本发明提供的分析一种或多种待分析物的检测方法一实施例的流程图;
41.图7为本发明提供的用于分析一种或多种待分析物的检测系统一实施例中,检测装置的示意图;
42.图8为本发明提供的用于分析一种或多种待分析物的检测系统中,另一实施例的液路示意图;
43.图9为本发明提供的分析一种或多种待分析物的检测方法另一实施例的流程图;
44.图10为本发明提供的用于分析一种或多种待分析物的检测系统另一实施例中,检测装置的示意图。
具体实施方式
45.下面通过具体实施方式结合附图对本发明作进一步详细说明。
46.本发明提供的用于分析一种或多种待分析物的检测系统,可适用于各类检测设
备,例如:液相芯片检测仪,从功能是可用于体外诊断、免疫分析等。该检测系统包括检测设备本体(图中未示出),检测设备本体采用液相芯片技术检测外部输入的微流控芯片,从而实现一种或多种待分析物的分析检测。
47.检测设备本体上设置有收容装置(图中未示出),用于容纳并固定微流控芯片。微流控芯片通常是板卡的形式,故收容装置可以具有供微流控芯片插入或放置的入口,还可以具有将微流控芯片推送到检测设备本体内部、以及在检测后将微流控芯片推出的推送机构,以及具有在微流控芯片进入检测设备本体内部后将微流控芯片固定的固定机构或限位结构。
48.微流控芯片是一种通过微米级管道及腔体结构对微量液体进行操纵和分析的载体,能把生物、化学、医学分析过程的样品制备、反应、分离、检测等基本操作单元集成到一块芯片上。微流控芯片的材质可为硅、石英、玻璃、高分子聚合物等,其通常是一次性的。微流控芯片中粒子检测方式有多种,本发明提供两种(分别对应图2和图3)进行阐述。
49.第一种方式如图2所示,微流控芯片包括加样口11、反应区121和微流检测通道13。加样口11与反应区121通过微流体通道和/或微阀连通,反应区与微流检测通道13通过微流体通道和/或微阀连通。微流体通道和微阀就是设置在微流控芯片中的管道(通常是沟槽)和阀门。微流体通道的横截面的尺寸可以是厘米级或厘米级以下,通常是微米级、毫米级的。微阀在尺寸上与微流体通道适配,微流体通道和微阀具体采用常规方式,不做赘述。
50.加样口11用于加样(即加入样本)。加样口11可以设置加样塞,用来封闭加样口11。
51.反应区121用于为样本和试剂的反应提供反应场所。加样口11与反应区121之间的微流体通道可以是竖直的,即反应区121位于加样口11的下方,加样后即可反应。当然,加样口11与反应区121之间的微流体通道也可以是水平的,如图2所示,样本加样后在外力的推动下进入反应区121反应。
52.样本与试剂反应后得到一种或多种待分析粒子,待分析粒子结合有待分析物。反应后的一种或多种待分析粒子被约束成单列或单层通过微流检测通道13,以便于检测。即本方式可以采用类似于流式细胞术的方式对待分析粒子进行检测。
53.如图1所示,所述检测系统还包括处理器21、光源22和检测装置23。光源22和检测装置23设置在检测设备本体内,处理器21可以设置在检测设备本体内,即对检测设备本体的控制、粒子的检测和后续的数据处理分析都可以由检测设备本体完成。当然,处理器21也可以设置在检测设备本体外,例如,检测系统还包括电脑,处理器21为电脑中的处理器,换而言之,可以由电脑控制检测设备本体完成粒子的检测,由电脑对后续的数据进行处理分析。
54.光源22,用于照射微流检测通道13内的待分析粒子,以使待分析粒子受照射后发出与待分析粒子本身特性相关的光信号。光源22可以是静态光源,也可以是点扫描、线扫描光源等。光信号可以是荧光,也可以是散射光等。与待分析粒子本身特性相关的光信号可以包括编码光信号,编码光信号能指代粒子的编码,从而能得到编码对应的待分析物。待分析物可以是核酸、抗原、抗体、激素、糖类、抗生素、细菌或病毒等各类生化标志物等。与待分析粒子本身特性相关的光信号也可以包括报告光信号,报告光信号的强弱能反映出待分析物的含量。与待分析粒子本身特性相关的光信号还可以包括编码光信号和报告光信号,本实施例以包括这两种光信号为例进行说明。
55.检测装置23,用于检测待分析粒子受照射后发出的光信号,将光信号转换成光信号数据;光信号数据为经过处理能得到光信号所指代的待分析物和/或待分析物含量的数据。检测装置23可以包括:单点的光敏检测器(光电探测器),线阵列的光敏检测器和面阵列的光敏检测器中的至少一种。本实施例中,所述待分析粒子排成单列或单层通过所述微流检测通道。检测装置23检测待分析粒子受照射后发出的光信号,得到各种待分析粒子的编码光信号和报告光信号。检测装置23可以对待分析粒子受照射后发出的光信号进行滤光,从而分离出编码光信号和报告光信号。例如,检测装置23分别对每个待分析粒子受照射后发出的光信号,采用分光装置进行分光、采用对应的滤光片滤光,从而分离出编码光信号和报告光信号。分光装置可采用二向色镜。检测装置23对分离得到的编码光信号和报告光信号进行探测,将编码光信号转换成编码光信号数据,将报告光信号转换成报告光信号数据。编码光信号数据为经过处理能得到编码光信号所指代的待分析物的数据;报告光信号数据为经过处理能得到报告光信号所指代的待分析物含量的数据。处理光信号数据即可得到对应的待分析物及其含量。例如,检测装置23根据编码光信号数据中光的种类(按波长分类,如颜色)、种类的数量、粒子的大小和/或形状等得到粒子的编码,即得到待分析物;根据报告光信号数据中的光强等得到待分析物的含量。当然,也可以获取待分析粒子受照射后发出的光信号但不分离。例如,检测装置23检测待分析粒子受照射后发出的光信号的光谱,得到光谱数据,从而可以从光谱数据中识别出编码光光谱数据和报告光光谱数据,从而对光谱数据进行分析即可得到待分析物及其含量。可见检测装置23检测光信号并将其转换成光信号数据、进而得到检测结果的方式有多种,与粒子的编码、标识方式对应即可。
56.本发明的这种检测方式为流式细胞术的检测方式,可以同时检测多种待分析物及其含量,而传统的化学发光检测只能检测一种待分析物及其含量,故本发明的检测效率高。
57.处理器21用于对所述编码光信号数据进行处理,得到编码光信号所指代的待分析物。由于本发明采用液相芯片技术,各种粒子都有其对应的编码,一个编码就对应一待分析物。例如,根据不同的发光物质(例如荧光物质)组合进行编码,根据粒子的不同形状、大小进行编码等,处理器21对编码光信号数据进行解码即可得到该种待分析粒子包含何种待分析物。进而,处理器21对同种待分析粒子的每个待分析粒子的报告光信号数据进行处理,得到该种待分析粒子中待分析物的含量。通常含量越高,报告光信号的光强越大。对每个待分析粒子的报告光信号数据都进行处理,使得最终得到的含量具有统计学意义,含量准确可靠。
58.图4所示为微流控芯片上的一种微液路,所述检测系统还包括储气腔14。储气腔14设置在微流控芯片内部或外部,用于驱动微流控芯片中的样本和/或液体移动以实现样本的反应和/或检测。这种驱动液体流动的方式属于压力推动式微流控,当然,还可以采用离心力推动式微流控、液滴微流控、数字化微流控(如电润湿微流控)、毛细力驱动微流控等一种或多种方式,本发明不做限制。
59.微流控芯片还设置有样本过滤器15,用于过滤样本中对检测造成干扰的物质。样本过滤器15可设置在加样口11与反应区121之间,图4所示实施例中,样本过滤器15设置在加样口11处,加样后即过滤,例如,样本为血液,血液经加样口11进入微流控芯片的微液路后,样本过滤器15将其血细胞等对检测造成干扰的物质滤除,便于后续检测。废液池17和17’上分别设置有一个或多个透气孔,其将微液路(图2-图4中样本或试剂能流过的区域)与
大气连通,使得微液路中的流体在运动过程中内压不变,基本与大气压接近。
60.在加样口11与反应区121之间还可以设置稀释液存储区16,稀释液存储区16存储有用于稀释样本和/或试剂的稀释液。稀释液可以包含有蛋白质和表面活性剂等。稀释液存储区16可以设置在微流控芯片内部,也可以设置在微流控芯片外部,通过微流控芯片上设置在接口连通到微流控芯片的微液路中。
61.所述检测系统还包括设置在微流控芯片内部和/或外部的试剂存储区。试剂存储区包括粒子包被试剂和/或发光标记试剂等,还可以包括抗体试剂、缓冲液试剂(如调整ph值或离子浓度等的试剂)等,本发明不做限制。粒子包被试剂中用作包被的物质、发光标记试剂中用来结合待分析物的物质可以是核酸、抗原、抗体、激素、糖类、抗生素等各类生化分子。粒子包被试剂可以干燥或凝胶存储在试剂存储区,如此,试剂存储区与反应区121可为同一区域或共同使用部分区域。当然,粒子包被试剂也可以以液态或凝胶态的形式存储在试剂存储区,如图5所示,如此,试剂存储区与反应区121可为不同区域,试剂存储区可位于进样口11与反应区121之间;为应对多种待分析物的检测,试剂存储区可将多种粒子包被试剂存储在同一区域(如图5所示)。当然,试剂存储区也可对多种粒子包被试剂分别存储。待分析粒子可以为结合有待分析物并具有发光物质标识的粒子,通常待分析物不同则粒子的种类就不同,本发明能检测一种或多种待分析物。发光物质可以是荧光染料、荧光基团、荧光微粒、量子点、时间分辨发光材料、或拉曼光谱特征分子等。发光物质在光的激发下能够发射出特征光谱。本实施例以荧光物质为例进行说明,荧光物质在光的激发下能够发射出荧光。不论是干燥的粒子包被试剂、凝胶态的粒子包被试剂还是液态的粒子包被试剂,其主要包括已编码并能结合待分析物的粒子,待分析物可以是生物分子等。粒子可以通过粒子形状、粒子图案(比如可以在粒子表面刻蚀任意图案)、粒子大小、发光物质等进行编码。粒子的尺寸可以在纳米至微米范围内,可以是各种形状的微粒,例如,粒子可以是一种微球,粒径可以在纳米至微米范围内。待分析物通常与荧光物质是关联的,例如,荧光物质用来标识待分析物的有无或多少(含量)。当然,有的实施例中,一种发光物质可以关联一种待分析物,通过其特有的光谱特征来识别其对应的待分析物,一种发光物质也可以关联多种待分析物,通过其特有的光谱特征以及粒子大小/形状等识别出关联的多种待分析物。
62.同样的,发光标记试剂可以干燥或凝胶存储在试剂存储区,如此,试剂存储区与反应区121可为同一区域或共同使用部分区域。当然,发光标记试剂也可以以液态或凝胶态的形式存储在试剂存储区,如图5所示,如此,试剂存储区与反应区121可为不同区域,为应对多种待分析物的检测,试剂存储区可将多种发光标记试剂存储在同一区域(如图5所示)。当然,试剂存储区也可对多种发光标记试剂分别存储。
63.同一微流控芯片中,粒子包被试剂和发光标记试剂的状态(干燥态、凝胶态还是液态)可以相同也可以不同,状态不同时,比如一个为干燥态一个为液态时,试剂存储区中存储粒子包被试剂的区域和存储发光标记试剂的区域不同。
64.所述检测系统还包括设置在微流控芯片内部和/或外部的:废液池17和鞘液/清洗液存储区19。检测系统还包括设置在微流控芯片内部的清洗区18。反应区121、废液池17、清洗区18和鞘液/清洗液存储区19、微流检测通道13等可依次沿待分析粒子移动的方向设置。废液池17用于存储废液。清洗区18为清洗反应后待分析粒子的区域。鞘液/清洗液存储区19存储有鞘液和/或清洗液。其中鞘液主要起到驱动作用,凡是能起到驱动作用的液体均可;
清洗液主要起到洗涤的作用,凡是能起到洗涤作用的液体均可。鞘液和清洗液可以是同一种液体,也可以是不同的液体,例如,鞘液和/或清洗液可以包括磷酸盐缓冲液、碳酸盐缓冲液、铵盐缓冲液、去离子水、纯净水等液体,本发明不做限定。
65.本实施例中,待分析粒子为结合有样本中的待分析物的磁性粒子。检测设备本体内还设置有粒子驱动装置25和温度控制装置26。粒子驱动装置25用于在样本与试剂的反应结束之前驱动磁性粒子运动,以加速样本中的待分析物与试剂中的磁性粒子反应,和/或,用于驱动待分析粒子运动,以转移待分析粒子。温度控制装置26用于对温度有要求的区域进行温度的精确控制,比如反应时将反应区121的温度控制在样本与试剂反应所需的温度。
66.请参阅图6,检测系统分析一种或多种待分析物的过程如下:
67.步骤s1、收容装置接收外部输入的、加入了样本的微流控芯片。通常,用户采集样本,打开加样塞并将样本滴入微流控芯片的加样口11,重新盖上加样塞后,将该微流控芯片放在收容装置中。检测系统还包括芯片控制装置、扫描装置27和打印装置28。芯片控制装置用于控制微流控芯片以实现样本与试剂的移动、反应、清洗等。微流控芯片上还设置有用于标识芯片唯一性的标签,其可以是条形码、二维码或者射频标签等。扫描装置27通过扫描标签,得到微流控芯片的信息,如微流控芯片的检测项目、批号、定标信息、出厂信息等。储气腔14可通过微流体通道和/或微阀与加样口11连通,芯片控制装置按压储气腔14,使储气腔14中的气体,驱动样本进入微流控芯片的反应区121,使样本与试剂反应,得到反应后的一种或多种待分析粒子。
68.具体的,以图4为例,芯片控制装置按压储气腔14,储气腔14中的气体驱动样本经过样本过滤器,释放稀释液到样本中,稀释后的样本进入反应区121。反应区121中干燥有粒子包被试剂和发光标记试剂,样本中的待分析物与粒子包被试剂和发光标记试剂反应。反应区121可以是一段管道,例如一段弯曲的长管道,样本和试剂混合流动的时间长、反应更充分。储气腔14不仅能将液体往远处推,而且也能将液体往回拉,例如,储气腔14具有一定的弹性,其排出部分气体后,芯片控制装置撤掉或减小按压在储气腔14上的力,储气腔14回弹从而能将液体往回吸,如此往复推拉液体,可以使反应更加充分。温度控制装置26控制反应区121的温度。由于粒子通常含有顺磁性物质,周围有磁场存在时粒子带有磁性,周围没有磁场存在时粒子没有磁性;粒子驱动装置25通常为电磁线圈或永磁铁,或者套有电磁线圈的永磁铁或套有电磁线圈的铁芯等,都可以具有磁性,粒子驱动装置25通过翻转磁极或改变磁场强度或移动磁场来移动粒子,起到搅拌的作用,从而促进反应的进行。
69.反应后,粒子驱动装置25通过磁力将待分析粒子转移到清洗区18,有的实施例中清洗区18与反应区121是同一个区域,所以可以不用转移,反应后直接清洗。
70.鞘液/清洗液存储区通常有两个(19、19’),设置在微流控芯片内部或外部,对称的设置在微流体通道两侧,并与微流体通道连通,微流体通道就是微流控芯片上的管道,用来连通芯片上的各个功能区域。芯片控制装置可以通过按压鞘液/清洗液存储区(19、19’)中的鞘液和/或清洗液进入清洗区18对待分析粒子进行清洗,清洗后的液体排入废液池17。可通过设置微阀让清洗后的液体顺利排入废液池17。
71.步骤s2、清洗待分析粒子后,芯片控制装置通过按压储气腔14、鞘液/清洗液存储区19,有的实施例中粒子驱动装置25也参与进来,共同驱动待分析粒子进入微流控芯片的微流检测通道13,待分析粒子在微流检测通道13、储气腔和鞘液的约束下排成单列或单层
通过微流检测通道13。微流检测通道13的末端连通有废液池17’。废液池17和废液池17’可以是同一个废液池,也可以是两个不同的废液池。
72.步骤s3、光源22照射微流检测通道13内的待分析粒子,以使待分析粒子受照射后发出与待分析粒子本身特性相关的光信号。本实施例以光信号为荧光,包括编码荧光和报告荧光为例进行说明。如图7所示,光源22照射待分析粒子f,使待分析粒子f内部或表面耦合的荧光物质受到激发,从而发出荧光。检测装置23包括光敏检测器(光电探测器)231和分光装置233,两者的数量通常是多个,以应对多种待分析物的检测要求。分光装置233用于分光,各个分光装置233可采用串并联的形式,对原始的光信号(光源22的光、待分析粒子受照射后发出的光信号)进行分光,得到编码光信号和报告光信号。分光装置233可采用二向色镜。分光装置233和光敏检测器231之间还可以设置滤光片234,以滤除其他光信号(如光源的光)的干扰。
73.步骤s4、检测装置23检测待分析粒子受照射后发出的光信号,将光信号转换成光信号数据。本实施例中,光源22开启时,或者,在光源22照射待分析粒子f之后,光敏检测器231对接收的光信号进行检测,得到光信号数据。
74.步骤s5、处理器21对所述光信号数据进行处理,得到光信号所指代的待分析物和/或待分析物的含量。本实施例中,光信号数据包括编码光信号数据和报告光信号数据。处理器21对编码光信号数据和报告光信号数据进行处理,得到待分析粒子f的编码以及荧光强度,从而可以确定该待分析粒子f包含何种待分析物,以及待分析物的含量。根据所有待分析粒子f的检测结果,可得到样本中一种或多种待分析物的含量。之后,可通过打印装置28将待分析物及其含量等分析结果以报告单的形式打印出来。
75.综上所述,本发明提供的用于分析一种或多种待分析物的检测系统及其方法,在微流控芯片上实现样本和试剂的反应过程,使得液相悬浮芯片检测设备能够实现小型化、自动化、便携化,推动其更加广泛的应用,以及促进poct(point care of testing,即时检测)产品的推广。
76.上述实施例中,给出了采用流式细胞术检测方式来检测微流控芯片中的粒子,下面结合图3给出另一种检测粒子的方式。
77.图2所示的实施例待分析粒子排成单列或单层通过微流检测通道13时进行检测,而本实施例中,如图3所示,待分析粒子在反应检测区12成单层排列后进行检测。本实施例检测待分析粒子时待分析粒子是不动的。因此,微流控芯片会有所差异。本实施例的微流控芯片包括加样口11和反应检测区12,加样口11和反应检测区12通过微流体通道和/或微阀连通。反应检测区12用于为样本和试剂的反应提供反应场所,为反应后的一种或多种待分析粒子提供检测场所。本实施例中,待分析粒子在反应检测区12成单层排列,且通常是静止不动的,可一次性完成检测,效率高。待分析粒子在反应检测区12单层排列可通过重力实现,如沉淀,也可以由电场或磁场等约束来实现。
78.加样口11同上述实施例,故不做赘述。加样口11同样可以设置加样塞。
79.反应检测区12包括:用于为样本和试剂的反应提供反应场所的反应区121,以及用于为反应后的一种或多种待分析粒子提供检测场所的检测区122。反应区121和检测区122可以是同一个区域,也可以是不同的区域(如图3所示),本实施例以后者为例进行说明。
80.同样的,加样口11与反应区121之间的微流体通道可以是竖直的,即反应区121位
于加样口11的下方,加样后即可反应。当然,加样口11与反应区121之间的微流体通道也可以是水平的,如图3所示,样本加样后在外力的推动下进入反应区121反应。
81.如图1所示,所述检测系统还包括处理器21、光源22、检测装置23和粒子约束装置24。光源22、检测装置23和粒子约束装置24设置在检测设备本体内。
82.光源22,用于照射反应检测区具体是检测区122内的待分析粒子,以使待分析粒子受照射后发出与待分析粒子本身特性相关的光信号。同样的,光信号可以是荧光,也可以是散射光等;可以包括上述实施例的编码光信号,和/或包括上述实施例的报告光信号。本实施例以包括这两种光信号为例进行说明。
83.粒子约束装置24用于将检测区122中的待分析粒子约束成单层排列,以便于检测。约束的方式有多种,如粒子带电,通过电场将其约束成单层,本实施例中,待分析粒子为结合有样本中的待分析物的磁性粒子,粒子约束装置24通过磁力将检测区122中的待分析粒子约束成单层排列,并通过磁力将待分析粒子固定在检测区122。
84.检测装置23,用于检测待分析粒子受照射后发出的光信号,将光信号转换成光信号数据;光信号数据为经过处理能得到光信号所指代的待分析物和/或待分析物含量的数据。检测装置23可以包括:单点的光敏检测器(光电探测器),线阵列的光敏检测器和面阵列的光敏检测器中的至少一种。本实施例中,检测装置23检测待分析粒子受照射后发出的光信号,得到各种待分析粒子的编码光信号和报告光信号。例如,检测装置23可以对待分析粒子受照射后发出的光信号进行滤光,从而分离出编码光信号和报告光信号。当然,也可以获取待分析粒子受照射后发出的光信号但不分离。检测装置23将编码光信号转换成编码光信号数据,将报告光信号转换成报告光信号数据。编码光信号数据为经过处理能得到编码光信号所指代的待分析物的数据;报告光信号数据为经过处理能得到报告光信号所指代的待分析物含量的数据。例如,检测装置23分别对分离出的编码光信号和报告光信号进行成像,将光信号转换成图像数据,进而处理图像数据即可得到对应的待分析物及其含量。又例如,检测装置23对待分析粒子受照射后发出的光信号进行成像,得到成像数据,根据成像数据中粒子的大小、形状等得到待分析物,根据粒子的光强等得到待分析物的含量。还例如,检测装置23检测待分析粒子受照射后发出的光信号的光谱,得到光谱数据,从而可以从光谱数据中识别出编码光光谱数据和报告光光谱数据,从而对光谱数据进行分析即可得到待分析物及其含量。可见检测装置23检测光信号并将其转换成光信号数据、进而得到检测结果的方式有多种,与粒子的编码、标识方式对应即可。
85.本发明的这种检测方式为液相芯片的检测方式,可以同时检测多种待分析物及其含量,而传统的化学发光检测只能检测一种待分析物及其含量,故本发明的检测效率高。
86.本实施例的处理器21与上述实施例相同,故不做赘述。
87.图8所示为微流控芯片上的另一种微液路,所述检测系统还包括储气腔14,其特点在上述实施例中已叙述,故不做赘述。
88.本实施例的微流控芯片还设置有如上所述的样本过滤器15。废液池17上设置有一个或多个透气孔,其将微液路(图8中样本或试剂能流过的区域)与大气连通,使得微液路中的流体在运动过程中内压不变,基本与大气压接近。
89.在加样口11与反应区121之间还可以设置稀释液存储区16。
90.所述检测系统还包括设置在微流控芯片内部和/或外部的试剂存储区。试剂存储
区包括粒子包被试剂和/或发光标记试剂等,还可以包括抗体试剂、缓冲液试剂(如调整ph值或离子浓度等的试剂)等,本发明不做限制。粒子包被试剂可以干燥或凝胶存储在试剂存储区,如此,试剂存储区与反应区121可为同一区域或共同使用部分区域。当然,粒子包被试剂也可以以液态或凝胶态的形式存储在试剂存储区,如图5所示,如此,试剂存储区与反应区121可为不同区域,试剂存储区可位于进样口11与反应区121之间;为应对多种待分析物的检测,试剂存储区可将多种粒子包被试剂存储在同一区域(如图5所示)。当然,试剂存储区也可对多种粒子包被试剂分别存储。
91.同样的,发光标记试剂可以干燥或凝胶存储在试剂存储区,如此,试剂存储区与反应区121可为同一区域或共同使用部分区域。当然,发光标记试剂也可以以液态或凝胶态的形式存储在试剂存储区,如图5所示,如此,试剂存储区与反应区121可为不同区域,为应对多种待分析物的检测,试剂存储区可将多种发光标记试剂存储在同一区域(如图5所示)。当然,试剂存储区也可对多种发光标记试剂分别存储。
92.同一微流控芯片中,粒子包被试剂和发光标记试剂的状态(干燥态、凝胶态还是液态)可以相同也可以不同,状态不同时,比如一个为干燥态一个为液态时,试剂存储区中存储粒子包被试剂的区域和存储发光标记试剂的区域不同。
93.所述检测系统还包括设置在微流控芯片内部和/或外部的:废液池17和清洗液存储区30。检测系统还包括设置在微流控芯片内部的清洗区18。反应区121、废液池17、清洗区18、检测区122、清洗液存储区30等可依次沿待分析粒子移动的方向设置。废液池17用于存储废液。清洗区18为清洗反应后待分析粒子的区域。清洗液存储区30存储有清洗液。
94.本实施例中,检测设备本体内还设置有粒子驱动装置25和温度控制装置26。粒子驱动装置25用于在样本与试剂的反应结束之前驱动磁性粒子运动,以加速样本中的待分析物与试剂中的磁性粒子反应,和/或,用于驱动待分析粒子运动,以转移待分析粒子。粒子驱动装置25和粒子约束装置24都具有磁性,通过磁力驱动或约束粒子,故粒子约束装置24和粒子驱动装置25可以是同一装置,当然也可以是两个独立的装置。
95.温度控制装置26用于对温度有要求的区域进行温度的精确控制,比如反应时将反应区121的温度控制在样本与试剂反应所需的温度。
96.请参阅图9,本实施例中,检测系统分析一种或多种待分析物的过程如下:
97.步骤s1’、收容装置接收外部输入的、加入了样本的微流控芯片。通常,用户采集样本,打开加样塞并将样本滴入微流控芯片的加样口11,重新盖上加样塞后,将该微流控芯片放在收容装置中。检测系统还包括芯片控制装置、扫描装置27和打印装置28。芯片控制装置用于控制微流控芯片以实现样本与试剂的移动、反应、清洗等。微流控芯片上还设置有用于标识芯片唯一性的标签,其可以是条形码、二维码或者射频标签等。扫描装置27通过扫描标签,得到微流控芯片的信息,如微流控芯片的检测项目、批号、定标信息、出厂信息等。储气腔14可通过微流体通道和/或微阀与加样口11连通,芯片控制装置按压储气腔14,使储气腔14中的气体,驱动样本进入微流控芯片的反应检测区12,具体是进入反应区121,使样本与试剂反应,得到反应后的一种或多种待分析粒子。
98.具体的,以图8为例,芯片控制装置按压储气腔14,储气腔14中的气体驱动样本经过样本过滤器15,释放稀释液存储区16中的稀释液到样本中,稀释后的样本进入反应区121。本实施例中,反应区121中干燥有粒子包被试剂和发光标记试剂,样本中的待分析物与
粒子包被试剂和发光标记试剂反应。反应区121可以是一段管道,例如一段弯曲的长管道,样本和试剂混合流动的时间长、反应更充分。储气腔14不仅能将液体往远处推,而且也能将液体往回拉,例如,储气腔14具有一定的弹性,其排出部分气体后,芯片控制装置撤掉或减小按压在储气腔14上的力,储气腔14回弹从而能将液体往回吸,如此往复推拉液体,可以使反应更加充分。温度控制装置26控制反应区121的温度。由于粒子和粒子驱动装置25都具有磁性,粒子驱动装置25通过翻转磁极或改变磁场强度或移动磁场来移动粒子,起到搅拌的作用,从而促进反应的进行。
99.反应后,粒子驱动装置25通过磁力将待分析粒子转移到清洗区18,有的实施例中清洗区18与反应区121是同一个区域,所以可以不用转移,反应后直接清洗。
100.清洗液存储区30用于存储清洗液,清洗液存储区30与微流体通道连通,微流体通道就是微流控芯片上的管道,用来连通芯片上的各个功能区域。清洗液存储区设置在微流控芯片内部或外部。芯片控制装置按压清洗液存储区30中的清洗液进入清洗区18对待分析粒子进行清洗,清洗后的液体排入废液池17。可通过设置微阀让清洗后的液体顺利排入废液池17。
101.步骤s2’、清洗待分析粒子后,粒子驱动装置25驱动待分析粒子转移到检测区122,有的实施例中还可以同时按压储气腔14以促进粒子的转移。待分析粒子转移到检测区122后,粒子约束装置24将待分析粒子吸附固定在检测区122,检测区122是一具有预设面积的区域,待分析粒子被吸附后单层排列,如图10所示。
102.步骤s3’、光源22照射检测区122内的待分析粒子,以使待分析粒子受照射后发出与待分析粒子本身特性相关的光信号。本实施例以光信号为荧光,包括编码荧光和报告荧光为例进行说明。如图10所示,光源22照射待分析粒子f,使待分析粒子f内部和/或表面耦合的荧光物质受到激发,从而发出荧光。检测装置23包括光敏检测器(光电探测器)231和滤光片切换装置232。滤光片切换装置232用于让不同波长的光通过,其包括多个成像滤光片2321,其中一个成像滤光片2321设置在检测区122与光敏检测器231之间的光路上,从而实现让一种波长的光进入。通过切换光路中的成像滤光片,实现不同波长的光分别进入光敏检测器231。例如,滤光片切换装置232可以是滤光片转轮,其包括转轮以及圆周阵列在转轮上的多个成像滤光片,其中一个成像滤光片位于检测区122与光敏检测器231之间的光路上。成像滤光片用于对待分析粒子f的荧光进行滤光,例如只让一种荧光通过,从而检测一种荧光信号;转轮转动以切换成像滤光片2321,则能检测另一种荧光信号。
103.步骤s4’、检测装置23检测待分析粒子受照射后发出的光信号,将光信号转换成光信号数据。本实施例中,光源22开启时,或者,在光源22照射待分析粒子f之后,光敏检测器231启动对待分析粒子f的荧光进行检测。检测可以是对待分析粒子f进行拍照,得到待分析粒子f的照片。由于有成像滤光片2321的作用,光源22发出的光被滤除,照片质量高。检测装置23包括的光敏检测器231可以是单点的光敏检测器,线阵列的光敏检测器和面阵列的光敏检测器中的至少一种。面阵列的光敏检测器优选的可以采用相机。另外,检测装置23包括的每种光敏检测器可以是一个也可以是多个。
104.步骤s5’、处理器21对所述光信号数据进行处理,得到光信号所指代的待分析物和/或待分析物的含量。本实施例中,处理器21得到待分析粒子f的照片后,对照片进行图像处理等,得到待分析粒子f的编码以及荧光强度,从而可以确定该待分析粒子f包含何种待
分析物,以及待分析物的含量。根据照片上所有待分析粒子f的检测结果,可得到样本中一种或多种待分析物的含量。之后,可通过打印装置28将待分析物及其含量等分析结果以报告单的形式打印出来。
105.可见,本发明将微流控技术与液相悬浮芯片技术结合,可以把生化分析中所涉及的样品预处理、反应、分离、检测等基本操作单元集成到一块几平方厘米大小的芯片上,进而采用液相悬浮芯片技术进行检测,能够一次分析一种或多种待分析物,检测通量高、所需样品用量少、分析速度快、体积小、集成度高,而且成本低、污染少,非常适用于即时、现场分析,便于制成便携式仪器,应用前景广阔。
106.以上应用了具体个例对本发明进行阐述,只是用于帮助理解本发明,并不用以限制本发明。对于本发明所属技术领域的技术人员,依据本发明的思想,还可以做出若干简单推演、变形或替换。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1