一种检测牛奶中雌激素的方法与流程
本发明涉及水食品检测
技术领域:
,具体涉及一种检测牛奶中雌激素的方法。
背景技术:
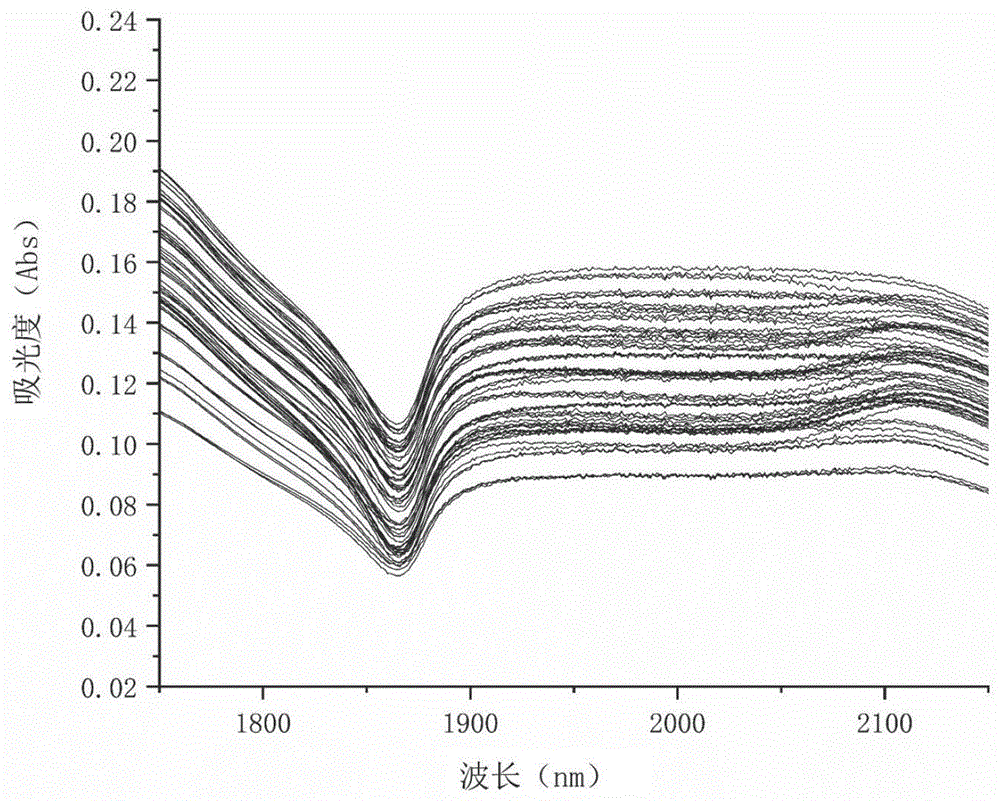
:食用动物饲养加工过程中存在滥用激素现象,其导致了水产品、肉类、蛋类及乳类中激素残留污染。雌激素可使女性幼儿提前发育,男性儿童乳腺发育呈女性化,使男性生殖系统发育异常与病变,使女性乳腺癌和子宫内膜异位症发生率上升。国内外测定牛奶中激素的方法很多,其中放射免疫法和酶联免疫法等生物技术仅能测定少数几种激素而且测定方法较为单一;目前国标中所规定的关于牛奶中雌激素残留的检测方法有气相色谱-负化学电离质谱和液相色谱-串联质谱,所需仪器昂贵,而且操作繁琐,耗时较长。技术实现要素:本发明旨在至少在一定程度上解决相关技术中的技术问题之一。为此,本发明的目的在于提供一种检测牛奶中雌激素的方法。该方法解决了现有技术中对牛奶中雌激素残留量进行测定时,只能对某几种雌激素进行检测,而无法对多种雌激素进行测定的问题;现有技术对样品前处理耗时长,步骤繁琐,操作复杂,不仅成本花费高而且在检测过程中容易因为操作不当产生误差;现阶段检测所得数据报告不及时,容易影响生产过程中决策的及时性和有效性;而本发提供的一种检测牛奶中雌激素的方法,可对多种雌激素进行检测,能够立即获得结果,而且无需进行样品前处理,操作方便快捷,节约成本,也减少时间,检测结果重现性好,准确率高。为此,在本发明的一方面,本发明提出了一种检测牛奶中雌激素的方法,其包括以下步骤:s1、配制具有不同雌激素浓度的样品作为校正集;s2、测定校正集样品的近红外光谱,用化学计量学软件制作雌激素浓度校正模型;s3、配制具有不同雌激素浓度的样品作为验证集;其中,校正集样品中雌激素浓度变化范围大于验证集样品中雌激素浓度变化范围;s4、测定验证集样品的近红外光谱,用已建立的雌激素浓度校正模型计算验证集样品的雌激素浓度,并验证上述雌激素浓度校正模型的准确性与有效性;s5、测定待测样品的近红外光谱,用已建立的雌激素浓度校正模型计算待测样品的雌激素浓度。根据本发明实施例的检测牛奶中雌激素的方法,采用近红外光谱技术可使样品预处理简便或无需处理;分析速度快,效率高;纯物理光学检测不破坏检测样品化学品质,而且不需要使用试剂,分析成本极低;不破坏样品,可对样品反复检测,测试重现性很好;可迅速得到样品成分信息,对样品进行定性分析或定量分析;基于化学计量学方法制作的校正模型,对样品进行检测,所得结果相对误差小;对同一样品进行多次检测,重现性好;在同一模式下,可以测定多种组分,简化了操作的流程。另外,根据本发明上述实施例提出的检测牛奶中雌激素的方法,还可以具有如下附加的技术特征:根据本发明的实施例,s1中,校正集样品由不含雌激素的纯牛奶与雌激素分析纯混合配制,混合温度为60~80℃。根据本发明的实施例,近红外光谱的检测波长为1750~2150nm,光谱分辨率为10nm。根据本发明的实施例,近红外光谱检测时,样品的温度为30~38℃,检测所需环境温度为5~40℃。根据本发明的实施例,s2中,化学计量学软件制作雌激素浓度校正模型包括:s21,在matlab软件中,导入已转化为txt文本格式的校正集中所有数据的近红外光谱信息,输入每个近红外光谱信息所对应的雌激素浓度值;s22,使用savitzky-golay卷积求导方法平滑、变量标准化、数据微分对上述近红外光谱信息进行预处理,获得建模所需的光谱数据;s23,使用偏最小二乘法pls,利用上述的光谱数据,构建雌激素浓度校正模型。根据本发明的实施例,s4中,当雌激素浓度校正模型的准确性与有效性不足时,增加s1中校正集样品的抽取数量,直到雌激素浓度校正模型的准确性达到相对误差<5%,有效性达到相对标准偏差<1%。本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。附图说明图1为根据本发明实施例中校正集样品的近红外光谱图;图2为根据本发明实施例中验证集样品的近红外光谱图;图3为根据本发明实施例中建立的醋酸美仑孕酮浓度校正模型。具体实施方式以下通过特定的具体实例说明本发明的技术方案。应理解,本发明提到的一个或多个方法步骤并不排斥在所述组合步骤前后还存在其他方法步骤或在这些明确提到的步骤之间还可以插入其他方法步骤;还应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。而且,除非另有说明,各方法步骤的编号仅为鉴别各方法步骤的便利工具,而非为限制各方法步骤的排列次序或限定本发明可实施的范围,其相对关系的改变或调整,在无实质变更技术内容的情况下,当亦视为本发明可实施的范畴。为了更好的理解上述技术方案,下面更详细地描述本发明的示例性实施例。虽然显示了本发明的示例性实施例,然而应当理解,可以以各种形式实现本发明而不应被这里阐述的实施例所限制。相反,提供这些实施例是为了能够更透彻地理解本发明,并且能够将本发明的范围完整的传达给本领域的技术人员。本发明采用的试材皆为普通市售品,皆可于市场购得。下面参考具体实施例,对本发明进行描述,需要说明的是,这些实施例仅仅是描述性的,而不以任何方式限制本发明。实施例以醋酸美仑孕酮为例建立近红外校正模型1、配制具有不同醋酸美仑孕酮浓度的样品作为校正集:选择符合生产要求的新鲜灭菌纯牛乳。实验前,先按照国家标准方法(gb/t22973-2008)牛奶和奶粉中醋酸美仑孕酮的检测方案对所购买的牛奶进行醋酸美仑孕酮检测,检测结果证明该灭菌纯牛乳中不含有醋酸美仑孕酮。利用购买的醋酸美仑孕酮分析纯(纯度99.7%),称取50组质量不同的醋酸美仑孕酮分析纯与所购纯牛乳充分混合,配制成共50个浓度均匀分布在0mg/l-10mg/l变化范围内的醋酸美仑孕酮牛奶作为校正集样品并进行振荡。其中,0mg/l-1mg/l浓度变化范围的有5个,1mg/l-2mg/l浓度变化范围的有5个,2mg/l-3mg/l浓度变化范围的有5个,3mg/l-4mg/l浓度变化范围的有5个,4mg/l-5mg/l浓度变化范围的有5个,5mg/l-6mg/l浓度变化范围的有5个,6mg/l-7mg/l浓度变化范围的有5个,7mg/l-8mg/l浓度变化范围的有5个,8mg/l-9mg/l浓度变化范围的有5个,9mg/l-10mg/l浓度变化范围的有5个,各样品浓度如表1所示。表1各样品浓度真实值2、测定上述校正集样品的近红外光谱,用化学计量学软件制作醋酸美仑孕酮浓度校正模型:在35℃下对校正集样品于1750nm-2150nm波长范围进行测定,每个样品进行三次信号测定取平均值作为近红外光谱信息,结果如图1所示。为提高模型测量精度,减小基线漂移和图谱的不稳定性导致的测量误差,首先对光谱进行预处理。使用化学计量学软件matlab的建立模型功能,对图谱进行savitzky-golay卷积求导方法平滑,去除高频信号;然后图谱进行变量标准化消除量纲、数据来源和量纲单位不同带来的偏差;最后图谱进行数据微分消除光谱基线漂移。再使用偏最小二乘法pls建立牛奶中雌激素含量预测模型,相关系数r2为0.97;相对误差re<5%;相对标准偏差rsd<1%。具体地,利用matlab软件建立牛奶中醋酸美仑孕酮浓度校正模型的步骤如下所示:1)在matlab软件中,导入已转化为txt文本格式的校正集中所有数据的光谱信息,输入每个光谱信息所对应的醋酸美仑孕酮浓度的真实值。2)使用savitzky-golay卷积求导方法平滑、变量标准化、数据微分对光谱进行预处理,获得建模所需的光谱数据。3)选择的交叉验证方法为偏最小二乘法pls,使用上述预处理后的光谱数据进行校正模型的建立。建模过程和统计检验方法符合astme1655-2017标准。4)输出校正模型,选择mat格式保存文件。最终校正模型如图2所示。3、按步骤1中所述方法,制备15个不同醋酸美仑孕酮浓度的样品作为验证集(其具体浓度如表2中的真实值所示)。其中,验证集选择的样品浓度变化范围是小于校正集样品浓度范围)4、测定上述验证集样品的近红外光谱,用步骤2已建立的校正模型对其进行浓度测量,其中,验证模型的准确性与有效性:将测定完成的验证集所有光谱信息导入到上述校正模型中,利用醋酸美仑孕酮浓度校正模型计算,得到验证集的醋酸美仑孕酮浓度预测值,所得验证结果如表2所示。表2:验证集样品的验证数据样品编号平均值(mg/l)真实值(mg/l)差值re(%)rsd(%)11.6121.5930.0191.190.09921.1431.167-0.0242.050.10633.0393.131-0.0922.940.53948.1948.1720.0220.270.02355.3485.368-0.0200.370.27768.6478.4750.1722.090.48077.2777.357-0.0801.080.04886.3276.433-0.1061.650.02499.2489.316-0.0680.720.287105.9895.8640.1252.130.203116.2976.435-0.1382.140.583121.5671.588-0.0211.320.521137.1517.324-0.1732.360.109144.6914.5670.1242.710.045155.2345.1230.1112.160.044上述表中:平均值:验证集样品5次测定结果的平均值;差值:平均值与真实值之间的差值;re(相对误差):差值/真实值×100%;rsd(相对标准偏差):由此可知,该实施例建立的醋酸美仑孕酮浓度校正模型检测牛奶中醋酸美仑孕酮浓度时重现性好,相对误差re<3%,相对标准偏差rsd<1%,因此可以使用该模型检测牛奶中醋酸美仑孕酮残留情况。称取醋酸美仑孕酮分析纯,与水充分混合制备醋酸美仑孕酮标准液,其中,醋酸美仑标准液ⅰ的浓度为2mg/l,醋酸美仑孕酮标准液ⅱ的浓度为4mg/l,醋酸美仑孕酮标准液ⅲ的浓度为6mg/l,醋酸美仑孕酮标准液ⅳ的浓度为8mg/l,醋酸美仑孕酮标准液ⅴ的浓度为10mg/l,通过酶联免疫法进行检测并制作醋酸美仑孕酮标准曲线,酶联免疫法具体步骤如下:1)将步骤一中的醋酸美仑孕酮标准液依次加入96孔板,每孔10μl。0)每孔加入100μl的0.01mol/l磷酸缓冲液作为包被液,置于4℃下包被过夜后用含0.5%bsa的磷酸缓冲液洗涤5次,每次3分钟,并拍干。3)每孔中加100μl封闭液(含5%bsa的磷酸缓冲液),37℃封闭2小时。4)用含0.5%bsa的磷酸缓冲液洗涤5次,每次三分钟,并拍干,每孔加入100μl封闭液稀释的抗血清,37℃孵育1小时。5)用含0.5%bsa的磷酸缓冲液洗涤5次,每次三分钟,并拍干,加封闭液稀释的酶标二抗,37℃孵育孵育1小时。6)用含0.5%bsa的磷酸缓冲液洗涤5次,每次三分钟,并拍干,每孔加显色剂tmedm100μl,37℃孵育30分钟。7)每孔加50μl的2m硫酸溶液终止,最后使用酶标仪在450nm处测定od值并自动生成标准曲线。7.使用上述酶联免疫法对验证集样品进行检测,所得结果如表3所示;使用酶联免疫法检测过程中的参数与本发明的检测过程中的参数对比如表4所示:表3:酶联免疫法对验证集检测样品编号平均值(mg/l)真实值(mg/l)差值re(%)11.6091.5930.0161.0021.1451.167-0.0221.8933.0463.131-0.0852.7148.1818.1720.0080.1055.3585.368-0.0100.1968.6378.4750.1621.9177.2937.357-0.0640.8786.3416.433-0.0931.4599.2679.316-0.0490.53105.9785.8640.1141.94116.3096.435-0.1261.96121.5691.588-0.0191.20137.1707.324-0.1542.10144.6824.5670.1152.52155.2265.1230.1032.01表4:酶联免疫分析和近红外光谱检测过程对比:由此可知,与常用的牛奶中雌激素残留检测方法相比,近红外光谱检测有如下的优点:灵敏度高,检出限为0.01mg/l;近红外光线具有很强的穿透能力,在检测样品时,不需要进行任何前处理;近红外技术能够及时快捷的对样品进行检测,扫描一次样品仅需5s左右,2min之内可以通过样品的一张光谱计算出样品的各种组成或性质数据;在同一模式下,可以同时测定多种组分,节约了检测的时间,简化了操作的流程。在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不应理解为必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任何的一个或多个实施例或示例中以合适的方式结合。此外,本领域的技术人员可以将本说明书中描述的不同实施例或示例进行接合和组合。尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1