祛湿和调整体脂的药食同源组合物的鉴定方法与流程
本发明涉及药物成分分析技术领域,涉及药物质量控制方法,尤其是涉及一种祛湿和调整体脂的药食同源组合物的鉴定方法。
背景技术:
从中医上来看,“春困夏乏”是“湿邪”所致,“湿邪”是最为常见的一种中医病症。中医认为脾主运化,湿气过重而不祛会妨碍脾的运化,导致脾胃失调而表现为体型肥胖、面部皮肤油脂较多、易困倦、舌苔滑腻、便溏等。所以说人体内湿气不祛会严重影响我们的健康,直接饮用祛湿产品的方式历来被认为是一种实现消暑祛湿最为简单快捷的方法。因此,选用质量佳、效果好的祛湿产品尤为重要,但是现有的祛湿产品的质量标准不涉及药效作用的活性成分变化,无法对其生产工艺过程中质量作出科学评价。
中药指纹图谱是指对中药材或中药制剂进行适当处理后,采用一定的分析手段,得到能够标示其化学特征的色谱图或光谱图。中药指纹图谱是一种可以对中药制剂的质量进行全面、客观、科学的评价和控制的有效方法。但是现有技术中尚无较好的质量控制方法来鉴定祛湿产品的质量品质,无法保证其药用价值。因此,通过指纹图谱来科学的评价和控制祛湿产品的质量有非常重要的意义。
技术实现要素:
本发明的目的是提供一种祛湿和调整体脂的药食同源组合物的鉴定方法,本方法的优点是:稳定性、重复性好,可对药食同源组合物的质量进行全面、客观、科学的评价和控制。
为了实现本发明的上述目的,特采用以下技术方案:
本发明涉及一种祛湿和调整体脂的药食同源组合物的鉴定方法,所述祛湿和调整体脂的药食同源组合物以重量份计,包括以下组分:决明子2~30份、荷叶2~30份、干姜片1~10份、代代花1~10份、绿茶1~10份、橘皮1~10份、薏苡仁0.5~5份、茯苓0.5~5份以及甘草0.2~3份;所述鉴定方法包括:
1)通过高效液相色谱法测定待检测物溶液的指纹图谱:
所述高效液相色谱法测定以流动相a和流动相b进行梯度洗脱;
所述流动相a为乙腈,流动相b为0.05(v/v)%~0.5(v/v)%的磷酸水溶液;
2)若所述指纹图谱具有如下所示的标准峰,则待检测物为所述祛湿和调整体脂的药食同源组合物;
所述标准峰包含11个特征峰,各峰的相对保留时间分别为:(1)0.265~0.270、(2)0.309~0.313、(3)0.462~0.469、(4)0.677~0.687、(5)0.815~0.826、(6)0.877~0.889、(7)0.937~0.947、(8)0.956~0.966、(9)0.961~0.971、(10)1.000~1.000、(11)1.033~1.044。
与现有技术相比,本发明的有益效果为:
本发明提供的祛湿和调整体脂的药食同源组合物指纹图谱鉴定方法中,建立的指纹图谱具有稳定性高和重复性好的优点。本发明通过对9批祛湿和调整体脂的药食同源组合物样品的图谱分析,得到了丰富的色谱峰信息,9批样品均出现了11个共有峰,说明所述指纹图谱能够准确有效的鉴定药食同源组合物产品的质量。本发明还考察了共有峰的相对保留时间,发现相对保留时间的rsd均在2.0%以内,且各色谱相似度均在0.99以上,说明该方法具有很好的重复性,对药食同源组合物质量的控制提供了可靠的鉴定方法。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
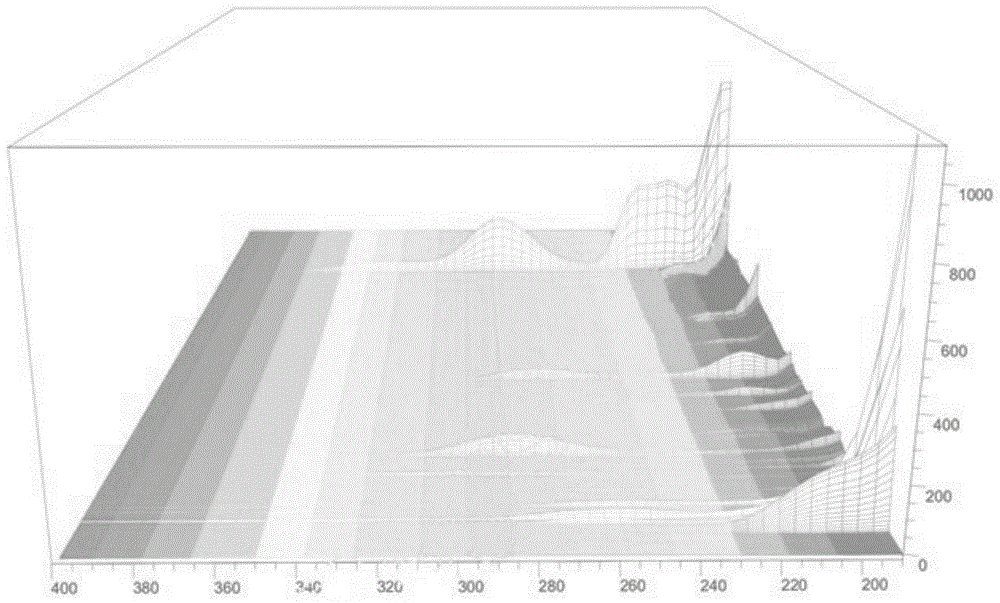
图1为本发明一个实施例中乙腈-水3d指纹图谱;
图2为本发明一个实施例中乙腈-0.1(v/v)%磷酸水溶液3d指纹图谱;
图3为本发明一个实施例中不同波长下的色谱图;
图4为本发明一个实施例中不同梯度优化下的色谱图;
图5为本发明一个实施例中精密度实验指纹图谱;
图6为本发明一个实施例中重复性实验指纹图谱;
图7为本发明一个实施例中稳定性实验指纹图谱;
图8为本发明一个实施例中9批祛湿和调整体脂的药食同源组合物的指纹图谱;
图9为本发明一个实施例中祛湿和调整体脂的药食同源组合物的标准高效液相指纹图谱。
具体实施方式
本发明涉及一种祛湿和调整体脂的药食同源组合物的鉴定方法,所述祛湿和调整体脂的药食同源组合物以重量份计,包括以下组分:决明子2~30份、荷叶2~30份、干姜片1~10份、代代花1~10份、绿茶1~10份、橘皮1~10份、薏苡仁0.5~5份、茯苓0.5~5份以及甘草0.2~3份;所述鉴定方法包括:
1)通过高效液相色谱法测定待检测物溶液的指纹图谱:
所述高效液相色谱法测定以流动相a和流动相b进行梯度洗脱;
所述流动相a为乙腈,流动相b为体积分数为0.05(v/v)%~0.5(v/v)%的磷酸水溶液;
2)若所述指纹图谱具有如下所示的标准峰,则待检测物为所述祛湿和调整体脂的药食同源组合物;
所述标准峰包含11个特征峰,各峰的相对保留时间分别为:(1)0.265~0.270、(2)0.309~0.313、(3)0.462~0.469、(4)0.677~0.687、(5)0.815~0.826、(6)0.877~0.889、(7)0.937~0.947、(8)0.956~0.966、(9)0.961~0.971、(10)1.000~1.000、(11)1.033~1.044。
本发明通过对9批药食同源组合物样品的图谱分析,得到了丰富的色谱峰信息,9批样品均出现了11个共有峰,说明所述指纹图谱能够准确有效的鉴定药食同源组合物产品的质量。并且考察了11个特征峰的相对保留时间,发现相对保留时间均在2.0%以内,且相似度均在0.99以上,说明本发明提供的药食同源组合物的鉴定方法具有很好的重复性,用于对药食同源组合物质量的评价和控制是可靠的。
在一些实施方式中,祛湿和调整体脂的药食同源组合物的制备方法,包括以下步骤:将各原料进行单方或复方提取、浓缩,混合在一起。
在一些实施方式中,所述浓缩为低温高压差连续提取浓缩得到浓缩液。
在一些实施方式中,对所述浓缩液进行喷雾干燥得到浓缩粉。
在一些实施方式中,所述低温高压差连续提取的温度为20℃~40℃,压强为10mpa~60mpa。
在一些实施方式中,所述制备方法还包括,将混合后的组分经过高温瞬时灭菌后分装。
在一些实施方式中,所述高效液相色谱法测定的洗脱方式为梯度洗脱;所述梯度洗脱程序包括:0min~10min,流动相a:5%~8%;10min~45min,流动相a:8%~15%;45min~65min,流动相a:15%;65min~75min,流动相a:15%~25%;75min~90min,流动相a:25%~70%。
在一些实施方式中,所述流动相b为体积分数0.1(v/v)%的磷酸水溶液。
在一些实施方式中,所述高效液相色谱法测定所用到的色谱柱为反相色谱柱。
在一些实施方式中,所述高效液相色谱法测定所用到的色谱柱为安装保护柱的反相色谱柱。
在一些实施方式中,所述高效液相色谱测定中色谱柱规格为250nm×4.6nm,5μm。
在一些实施方式中,所述高效液相色谱测定中色谱柱的填料为十八烷基硅烷键合硅胶。
在一些实施方式中,所述高效液相色谱法测定的进样体积为15μl~25μl,还可以选择20μl。
在一些实施方式中,所述高效液相色谱法测定的流速为0.5ml/min~1.5ml/min,还可以选择1.0ml/min。
在一些实施方式中,所述高效液相色谱法测定的波长为200nm~300nm,还可以选择220nm。
在一些实施方式中,所述高效液相色谱测定中色谱柱的柱温为25℃~40℃,还可以选择35℃。
在一些实施方式中,所述祛湿和调整体脂的药食同源组合物供试液的制备方法包括以下步骤:称取所述祛湿和调整体脂的药食同源组合物样品,超声溶解后定容、过滤;所述过滤膜的孔径为0.2μm~0.5μm;所述过滤膜的孔径还可以选择0.45μm。
在一些实施方式中,所述祛湿和调整体脂的药食同源组合物供试液的浓度为60mg/ml~80mg/ml,还可以选择45mg/ml。
现将详细地提供本发明实施方式的参考,其一个或多个实例描述于下文。提供每一实例作为解释而非限制本发明。实际上,对本领域技术人员而言,显而易见的是,可以对本发明进行多种修改和变化而不背离本发明的范围或精神。例如,作为一个实施方式的部分而说明或描述的特征可以用于另一实施方式中,来产生更进一步的实施方式。
因此,旨在本发明覆盖落入所附权利要求的范围及其等同范围中的此类修改和变化。本发明的其它对象、特征和方面公开于以下详细描述中或从中是显而易见的。本领域普通技术人员应理解本讨论仅是示例性实施方式的描述,而非意在限制本发明更广阔的方面。
下面将结合实施例对本发明的实施方案进行详细描述。
实施例1
(1)称取:
按照原料重量份,称取药食同源组合物60份,即荷叶12份、决明子12份、干姜8份、代代花6份、绿茶6份、橘皮6份、薏苡仁4份、茯苓4份以及甘草2份;
(2)粉碎:
将上述药食同源组合物中各组分分别进行湿法粉碎,得到细碎物;
(3)提取:
在步骤(2)所得到的各细碎物中加水浸泡30min,将得到的药食同源组合物溶液在温度为25℃以及压强为40mpa的条件下,在低温高压差连续提取设备上进行提取;
(4)纯化:
将上述提取液置于孔径为500nm的陶瓷微滤膜上进行分离提纯,收集滤液;
(5)浓缩:
将步骤(4)中所得滤液通过反渗透装置以及真空浓缩装置进行浓缩,得到浓缩液;
(6)将上述浓缩液进行喷雾干燥得到浓缩粉;
(7)配制:
将药食同源组合物提取粉混合均匀、制粒。
(8)灭菌、包装:
将上述配制好的组合物进行灭菌包装即得最终产品。
实施例2
祛湿和调整体脂的药食同源组合物供试液的制备:精密称取350mg祛湿和调整体脂的药食同源组合物样品,置于5ml容量瓶中,加入超纯水超声溶解、定容;经过孔径为0.45μm微孔过滤膜过滤至进样瓶中即得祛湿和调整体脂的药食同源组合物供试液。
对照品溶液的制备:精密称取决明子苷c对照品,以甲醇为溶剂,配置浓度为65.8μg/ml的对照品溶液。
(1)流动相系统的选择
高效液相色谱测定条件:
色谱柱:intertsilods-3(250nm×4.6nm,5μm)
检测波长:3d
进样体积:20μl
流速:1.0ml/min
色谱柱柱温:35℃
液相梯度:乙腈(a相)-水(b相)
梯度洗脱程序:0min~50min:乙腈:5%~35%;
乙腈(a相)-0.1(v/v)%磷酸水溶液(b相)
梯度洗脱程序:0min~14min:乙腈:5%~12%;14min~50min:乙腈:10%~25%。
如图1和图2所示,从所得的图谱中发现,乙腈(a相)-0.1(v/v)%磷酸水溶液(b相)系统所得到的的图谱信息更丰富,按照指纹图谱建立中的信息丰富原则,选用乙腈(a相)-0.1(v/v)%磷酸水溶液(b相)系统作为流动相。
(2)波长的选择
高效液相色谱测定条件:
色谱柱:intertsilods-3(250nm×4.6nm,5μm)
进样体积:20μl
流速:1.0ml/min
色谱柱柱温:35℃
液相梯度:
梯度洗脱程序:0min~10min:a相:5%~8%;10min~50min:a相:8%~15%;50min~70min:a相:15%~40%;70min~80min:a相:40%~90%
检测波长:根据(1)中3d指纹图谱检测结果,祛湿和调整体脂的药食同源组合物样品在205nm(s1)、215nm(s2)、220nm(s3)、225nm(s4)、235nm(s5)、255nm(s6)、265nm(s7)、275nm(s8)、285nm(s9)以及295nm(s10)波长处得到的图谱信息较为丰富,因此从上述波长中选择最优波长。如图3所示,图谱结果表明,祛湿和调整体脂的药食同源组合物样品在220nm波长下的图谱信息最为丰富,因此本实验选取220nm作为最佳扫描波长。
(3)梯度洗脱程序优化
系统:乙腈(a相)-0.1(v/v)%磷酸水溶液(b相)
具体梯度程序:
s1:0min~14min:a相:5%~12%;14min~50min:a相:12%~25%;50min~65min:a相:25%~90%。
s2:0min~15min:a相:5%~10%;15min~50min:a相:10%~20%;50min~70min:a相:20%~90%。
s3:0min~15min:a相:5%~10%;15min~50min:a相:10%~15%;50min~70min:a相:15%~90%。
s4:0min~10min:a相:5%~8%;10min~50min:a相:8%~15%;50min~70min:a相:15%~40%;70min~90min:a相:40%~90%。
s5:0min~10min:a相:5%~8%;10min~45min:a相:8%~15%;45min~70min:a相:15%~40%;70min~90min:a相:40%~90%。
s6:0min~10min:a相:5%~8%;10min~45min:a相:8%~15%;45min~70min:a相:15%~25%;70min~90min:a相:25%~90%。
s7:0min~10min:a相:5%~8%;10min~45min:a相:8%~15%;45min~60min:a相:15%~18%;60min~70min:a相:18%~25%;70min~90min:a相:25%~90%。
s8:0min~10min:a相:5%~8%;10min~45min:a相:8%~15%;45min~65min:a相:15%~15%;65min~75min:a相:15%~25%;75min~90min:a相:25%~70%。
如图4所示,图谱结果表明,s8优化程序的图谱信息最为丰富,且分离度良好,因此确定s8梯度洗脱程序为最优的流动相梯度。
(4)精密度实验
高效液相色谱测定条件:
色谱柱:intertsilods-3(250nm×4.6nm,5μm)
流动相:;流动相a为乙腈,流动相b为体积分数0.1(v/v)%的磷酸水溶液检测波长:220nm
进样体积:20μl
流速:1.0ml/min
色谱柱柱温:35℃
洗脱方式为梯度洗脱,洗脱程序如下:
0min~10min,流动相a:5%~8%;10min~45min,流动相a:8%~15%;45min~65min,流动相a:15%;65min~75min,流动相a:15%~25%;75min~90min,流动相a:25%~70%
按照如上设定好的高效液相色谱测定程序,连续进样6次,记录各色谱图,如图5所示。考察共有峰的相对保留时间和相对峰面积,分别列于表1和表2,且计算了rsd值。
表1精密度实验(共有峰相对保留时间)
表2精密度实验(相对峰面积)
通过表1和表2可知,相对保留时间的rsd均在2.0%以内,相对峰面积均在5.0%以内,且各色谱图相似度均在0.99以上,表明仪器精密度良好,符合指纹图谱的技术要求。
(5)重复性实验
按照上述设定好的高效液相色谱测定程序,连续进样6次,记录各色谱图,如图6所示。考察共有峰的相对保留时间和相对峰面积,分别列于表3和表4,且计算了rsd值。
表3重复性实验(共有峰相对保留时间)
表4重复性实验(相对峰面积)
通过表3和表4可知,相对保留时间的rsd均在2.0%以内,相对峰面积均在5.0%以内,且各色谱图相似度均在0.99以上,表明此法的重复性良好,符合指纹图谱的技术要求。
(6)稳定性实验
按照上述设定好的高效液相色谱测定程序,分别与0h(s1)、2h(s2)、4h(s3)、6h(s4)、8h(s5)、12h(s6)、18h(s7)、24h(s8)进样,记录各色谱图,如图7所示。考察共有峰的相对保留时间和相对峰面积,分别列于表5和表6,且计算了rsd值。
表5稳定性实验(共有峰相对保留时间)
表6稳定性实验(相对峰面积)
通过表5和表6可知,相对保留时间的rsd均在2.0%以内,相对峰面积均在5.0%以内,且各色谱图相似度均在0.99以上,表明供试液在24h内稳定性良好,符合指纹图谱的技术要求。
(7)多批次祛湿和调整体脂的药食同源组合物产品相似度评价
通过对9批祛湿和调整体脂的药食同源组合物产品进行指纹图谱分析,如图8所示。计算了相对保留时间和相对峰面积,分别如表7和表8所示。
表7多批次祛湿和调整体脂的药食同源组合物产品相似度评价(相对峰保留时间)
表8多批次祛湿和调整体脂的药食同源组合物产品相似度评价(相对峰面积)
通过表7和表8可知,相对保留时间的rsd均在2.0%以内,相对峰面积均在5.0%以内,且各色谱图相似度均在0.99以上,说明本产品在生产过程中工艺稳定,产品质量控制良好,也说明使用指纹图谱可以实现对祛湿和调整体脂的药食同源组合物的质量进行快捷、准确的鉴定。
根据上述鉴定方法得到的祛湿和调整体脂的药食同源组合物的标准高效液相指纹图谱如图9所示。
最后应说明的是:以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!