一种含有脒基类化合物的溶血剂及其血液分析试剂盒的制作方法
1.本发明涉及血液检测技术领域,具体涉及一种含有脒基类化合物的溶血剂及其血液分析试剂盒。
背景技术:
2.国际血液学委员会指定血红蛋白测定标准试剂是将血红蛋白与氰化物反应成为氰化血红蛋白,是很精确的测量方法,但是氰化物有剧毒,对环境以及人体有危害,因此氰化物的替代是目前研究的重点。
3.申请号为03140211.9的中国专利提出无氰化物溶血素,包含至少一种非离子表面活性剂,至少一种阳离子表面活性剂,至少一种阴离子表面活性剂。实现了不适用氰化物,无毒性的溶血素来测定血红蛋白,并且能将白细胞至少分成两个亚群。
4.申请号为201710031822.x的中国专利提出一种乳糜血溶血效果更好的血红蛋白溶血剂。
5.包括上述专利在内的现有技术只关注了常温下血红蛋白等血液组分的测试稳定性,在温度过高或者低温条件下不能保证测试的稳定性和准确性。
技术实现要素:
6.本发明提供一种含有脒基类化合物的溶血剂及其血液分析试剂盒。
7.第一方面,在一实施例中,提供一种溶血剂,含有至少一种脒基类化合物或其盐;
8.所述脒基类化合物具有式(a)所示结构:
[0009][0010]
式(a)中,r1、r2、r3、r4独立地为氢、烃基、取代的烃基、羟基或氨基。
[0011]
第二方面,在一实施例中,提供一种用于血液分析的试剂盒,包括脒基类化合物或其盐,或第一方面所述溶血剂。
[0012]
第三方面,在一实施例中,提供一种血红蛋白检测试剂盒,包括至少一种脒基类化合物或其盐,或第一方面所述溶血剂。该试剂盒可用于检测血红蛋白在血液样本中的浓度。
[0013]
第四方面,在一实施例中,提供一种白细胞检测试剂盒,包括至少一种脒基类化合物或其盐,或第一方面所述溶血剂。
[0014]
第五方面,在一实施例中,提供一种血小板检测试剂盒,包括至少一种脒基类化合物或其盐,或第一方面所述溶血剂。
[0015]
第六方面,在一实施例中,提供一种血液分析设备,其包括第二方面所述试剂盒、或第三方面所述血红蛋白检测试剂盒、或第四方面所述白细胞检测试剂盒、或第五方面所述血小板检测试剂盒。
[0016]
第七方面,在一实施例中,提供脒基类化合物或第一方面所述溶血剂在制备血液
分析试剂盒中的应用。
[0017]
依据上述实施例的溶血剂,脒基类化合物可以与血红蛋白及其衍生物牢固地结合,提高血液分析的温度适应范围,不仅可在常温下进行血液分析,而且可在低温或高温下进行血液分析。
附图说明
[0018]
图1显示为实施例1的溶血剂所处理血样的血红蛋白浓度检测结果与氰化血红蛋白法所测得的血红蛋白浓度检测结果关系曲线图;
[0019]
图2显示为实施例2的溶血剂所处理血样的血红蛋白浓度检测结果与氰化血红蛋白法所测得的血红蛋白浓度检测结果关系曲线图;
[0020]
图3显示为实施例3的溶血剂所处理血样的血红蛋白浓度检测结果与氰化血红蛋白法所测得的血红蛋白浓度检测结果关系曲线图;
[0021]
图4显示为实施例4的溶血剂所处理血样的血红蛋白浓度检测结果与氰化血红蛋白法所测得的血红蛋白浓度检测结果关系曲线图;
[0022]
图5显示为实施例5的溶血剂所处理血样的血红蛋白浓度检测结果与氰化血红蛋白法所测得的血红蛋白浓度检测结果关系曲线图;
[0023]
图6显示为实施例1的溶血剂所处理血样的分光光度计测试图谱;
[0024]
图7显示为实施例2的溶血剂所处理血样的分光光度计测试图谱;
[0025]
图8显示为实施例3的溶血剂所处理血样的分光光度计测试图谱;
[0026]
图9显示为实施例4的溶血剂所处理血样的分光光度计测试图谱;
[0027]
图10显示为实施例5的溶血剂所处理血样的分光光度计测试图谱。
具体实施方式
[0028]
下面通过具体实施方式结合附图对本发明作进一步详细说明。其中不同实施方式中类似元件采用了相关联的类似的元件标号。在以下的实施方式中,很多细节描述是为了使得本技术能被更好的理解。然而,本领域技术人员可以毫不费力的认识到,其中部分特征在不同情况下是可以省略的,或者可以由其他元件、材料、方法所替代。在某些情况下,本技术相关的一些操作并没有在说明书中显示或者描述,这是为了避免本技术的核心部分被过多的描述所淹没,而对于本领域技术人员而言,详细描述这些相关操作并不是必要的,他们根据说明书中的描述以及本领域的一般技术知识即可完整了解相关操作。
[0029]
另外,说明书中所描述的特点、操作或者特征可以以任意适当的方式结合形成各种实施方式。同时,方法描述中的各步骤或者动作也可以按照本领域技术人员所能显而易见的方式进行顺序调换或调整。因此,说明书和附图中的各种顺序只是为了清楚描述某一个实施例,并不意味着是必须的顺序,除非另有说明其中某个顺序是必须遵循的。
[0030]
本文中所编序号本身,例如“第一”、“第二”等,仅用于区分所描述的对象,不具有任何顺序或技术含义。
[0031]
本文中,试剂盒通常是指将各试剂独立存放于不同的试剂瓶等容器中,然后将各容器成套包装形成的产品。
[0032]
第一方面,在一实施例中,提供一种溶血剂,含有至少一种脒基类化合物或其盐;
[0033]
所述脒基类化合物具有式(a)所示结构:
[0034][0035]
式(a)中,r1、r2、r3、r4独立地为氢、烃基、取代的烃基、羟基或氨基。
[0036]
该溶血剂属于一种新的非氰化物的溶血剂,价格低,用量少,无毒性,溶血效果更好,而且准确性、稳定性相对现有技术更好,温度适应性强。
[0037]
现有试剂在低温或者高温下都会造成测试结果不稳定,可能的原因有:1、表面活性剂在低温下溶血不足,或者存在盐离子析出现象;2、高温的时候会导致部分血红蛋白变性,无法测出。
[0038]
在一实施例中,采用本发明的溶血剂时,形成的蛋白质-脒基复合物可以增强血红蛋白抵抗高温能力,此处的高温一般指40℃以下。
[0039]
本发明实施例的实验证实,所述脒基类物质可以与血红蛋白及其衍生物结合,大多以氢键形式结合,并且结合牢固,能适应4-37℃的温度变化,吸光值无显著变化,使hgb测量值稳定。
[0040]
在一实施例中,所述溶血剂用于检测血红蛋白浓度时,在4℃-37℃条件下,测试结果依然准确。本发明首次使用脒基类化合物作为血红蛋白稳定剂,降低了试剂对环境温度的高要求。
[0041]
在一实施例中,所述烃基包括但不限于链状烃基、环状烃基中的至少一种。
[0042]
在一实施例中,所述链状烃基包括但不限于所述c
1-c
10
烷基、c
2-c
10
烯基、c
2-c
10
炔基中的任一种。
[0043]
在一实施例中,所述环状烃基包括但不限于环丙基、环丁基、环戊基、环己基、环丙烯基、苄基、芳基、杂芳基、芳烷基、三苯甲基中的任一种。
[0044]
在一实施例中,所述r1、r2、r3、r4独立地为烷基、取代的烷基、羟基烷基、芳基、芳烷基、环烷基、杂环基、醚、硫醚、卤素、多亚乙基多胺、硝基、酮基、酯、或碳酰胺。
[0045]
在一实施例中,所述r1、r2、r3、r4独立地为甲基、乙基、丙基、异丙基、丁基、异丁基。
[0046]
在一实施例中,所述r1、r2、r3、r4独立地为c
1-c
36
烷基、被氧或硫中断的c
2-c
25
烷基、c
2-c
24
烯基、未取代的或被c
1-c4烷基、和/或羧基取代的c
4-c
15
环烷基、未取代的或被c
1-c4烷基和/或羧基取代的c
5-c
15
环烯基、c
13-c
26
多环烷基、未取代的或在苯环上被c
1-c4烷基取代的c
7-c9苯基烷基、任选被取代的胺基团、或任选用具有至多8个碳原子的烃基醚化的羟基。
[0047]
在一实施例中,所述脒基类化合物包括但不限于(甲醚)、(n-羟基丙酸脒)、(带苯环的脒基类化合物)中的至少一种,r1、r2、r3独立地选自氢、c
1-c5烷基、c
2-c5烯基或c
2-c5炔基。
[0048]
在一实施例中,所述脒基类化合物的盐包括但不限于(苄脒盐酸盐)、(4-氯苯甲脒盐酸盐)中的至少一种。
[0049]
在一实施例中,所述脒基类化合物或其盐在所述溶血剂中的浓度为0.5-2g/l,相当于0.05%-0.2%(v/v)。脒基类化合物或其盐在0.2%(v/v)浓度下几乎无毒,对人类无害。高浓度的脒基类化合物或其盐对生物体有杀伤作用,例如,脒基类杀虫剂是对节肢动物有杀伤作用。当脒基类化合物或其盐在所述溶血剂中的浓度大于0.2%(v/v)浓度时,会导致试剂产生低毒性,当脒基类化合物或其盐与所有血红蛋白结合之后,会达到饱和,过量的该试剂也不会造成结果的改变,反而造成试剂浪费;少于0.05%(v/v)会导致与血红蛋白结合不充分,导致测试结果偏小。脒基类化合物或其盐可以特异性与血红蛋白结合,与血红蛋白形成稳定的复合物,在4-37℃范围内使用依然保持稳定,4℃为血液冰箱储存的最适温度,在测试的时候,不用等到常温,也避免了血液反复改变温度对血细胞的破坏,37℃是公认的人体的正常体温,环境温度也几乎不会超过37℃,4℃及37℃下的血红蛋白浓度测试结果与常温(25℃)下的血红蛋白浓度测试结果偏差保持在1.5%以内。
[0050]
在一实施例中,所述溶血剂还含有至少一种表面活性剂。表面活性剂可以溶解红细胞,使得血红蛋白及其衍生物从红细胞中释放出来。在一实施例中,表面活性剂也可以造成白细胞的细胞膜部分损失,因此,制得的溶血剂可用于白细胞分类检测等。溶血剂中的表面活性剂足以溶解红细胞,使得血红蛋白及其衍生物充分释放。
[0051]
在一实施例中,所述表面活性剂包括但不限于阳离子表面活性剂、非离子表面活性剂、阴离子表面活性剂中的至少一种。
[0052]
在一实施例中,所述阳离子表面活性剂包括但不限于季铵盐型阳离子表面活性剂、胺盐型阳离子表面活性剂、杂环型阳离子表面活性剂、啰盐型阳离子表面活性剂中的至少一种。阳离子表面活性剂可以实现红细胞的快速溶血,将血红蛋白释放。在一实施例中,当溶血剂用于血红蛋白检测时,溶血剂中阳离子表面活性剂的用量足以溶解红细胞膜而使血红细胞从中释放。在一实施例中,当用于白细胞检测时,溶血剂中阳离子表面活性剂的用量足以溶解红细胞膜而使血红细胞从中释放,同时保留白细胞以便测定其大小和体积。在一实施例中,阳离子表面活性剂在一定浓度范围内,可快速溶解红细胞,排除计数时红细胞对白细胞的干扰,同时与血红蛋白结合形成络合物,可根据比色原理测定血红蛋白的浓度。
[0053]
在一实施例中,所述季铵盐型阳离子表面活性剂包括但不限于十二烷基三甲基溴化铵、十二烷基三甲基氯化铵、十六烷基三甲基氯化铵、十六烷基三甲基溴化铵、十八烷基三甲基氯化铵、十八烷基三甲基溴化铵中的至少一种。
[0054]
在一实施例中,所述胺盐型阳离子表面活性剂包括但不限于伯胺盐、仲胺盐和叔胺盐表面活性剂中的至少一种。
[0055]
在一实施例中,所述杂环型阳离子表面活性剂中含有的杂环包括但不限于含氮的吗啉环、吡啶环、咪唑环、哌嗪环、喹啉环中的至少一种。
[0056]
在一实施例中,所述阳离子表面活性剂在所述溶血剂中的浓度为4-8g/l。
[0057]
在一实施例中,所述非离子表面活性剂包括但不限于聚氧乙烯型、多元醇型、烷醇酰胺型、聚醚型、氧化胺型非离子表面活性剂中的至少一种。非离子表面活性剂用量应足以使高血脂样本中的脂质在分析体系中被溶解,从而降低对血红蛋白吸光度的干扰。在一实施例中,当溶血剂用于白细胞分析时,非离子表面活性剂的亲水基团的位于脂质层的一侧,而有小亲水基团的表面活性剂则能穿透过脂质层,当非离子表面活性剂浓度加大时,亲水基团的表面活性剂能与脂质膜上的磷脂形成胶质粒子,溶解了脂质,进而溶解红细胞,为白细胞膜打孔。在一实施例中,非离子表面活性剂可显著改善溶血速率,并且诱导血红蛋白的β链n端暴露在血红蛋白分子的外侧,从而加快血红蛋白检测的反应速率。
[0058]
在一实施例中,所述非离子表面活性剂包括但不限于脂肪胺聚氧乙烯醚、烷基酚聚氧乙烯醚、聚氧乙烯-8-辛基苯基醚中的至少一种。
[0059]
聚氧乙烯-8-辛基苯基醚又称为聚乙二醇对异辛基苯基醚、曲拉通x-100、triton x-100,cas号:9002-93-1。
[0060]
在一实施例中,聚氧乙烯醚类的非离子表面活性剂能快速溶解红细胞,使红细胞膜碎片收缩成更小的微粒,不影响血红蛋白的检测,此外,如果溶血剂是用于白细胞分析检测,红细胞膜碎片收缩成更小的微粒,就不会影响到白细胞分类。
[0061]
在一实施例中,所述非离子表面活性剂在所述溶血剂中的浓度为0.5-5g/l,包括但不限于0.5g/l、1g/l、1.5g/l、2g/l、2.5g/l、3g/l、3.5g/l、4g/l、4.5g/l、5g/l等等。
[0062]
在一实施例中,所述阴离子表面活性剂包括但不限于十二烷基磺酸钠、十二烷基苯磺酸钠和十二烷基硫酸钠中的至少一种。阴离子表面活性剂既有破裂细胞和溶解红细胞的作用,又可以与血红蛋白结合形成稳定的复合物,利于血红蛋白检测,也利于白细胞分类、计数等。
[0063]
在一实施例中,所述阴离子表面活性剂在所述溶血剂中的浓度为0.5-10g/l,包括但不限于0.5、1g/l、1.5g/l、2g/l、2.5g/l、3g/l、3.5g/l、4g/l、4.5g/l、5g/l、5.5g/l、6g/l、6.5g/l、7g/l、7.5g/l、8g/l、8.5g/l、9g/l、9.5g/l、10g/l等等。
[0064]
在一实施例中,所述溶血剂还含有至少一种醇类。醇类可在一定程度上改变血红蛋白及其衍生物的结构,促进血红蛋白及其衍生物结合至脒基类化合物。在一实施例中,溶血剂中也可以不加醇类。
[0065]
在一实施例中,所述醇类包括但不限于甲醇、乙醇、丁醇、苯氧乙醇中的至少一种。
[0066]
在一实施例中,所述醇类在所述溶血剂中的浓度为0.3-1.0ml/l,包括但不限于0.3ml/l、0.4ml/l、0.5ml/l、0.6ml/l、0.7ml/l、0.8ml/l、0.9ml/l、1.0ml/l。
[0067]
在一实施例中,所述溶血剂还含有金属盐。少部分脒基类化合物或者盐可以与溶血剂中的金属盐反应,形成脒基金属盐,此类脒基金属盐可以作为环保催化剂,催化其他的脒基与血红蛋白充分结合,通常在4℃-37℃下有一定的催化作用。在一实施例中,溶血剂中也可以不加金属盐。
[0068]
在一实施例中,所述金属盐包括但不限于氯化钠、氯化钾、碳酸钠、碳酸钾中的至少一种。
[0069]
在一实施例中,所述溶血剂的ph为6-8。具体可以通过加入缓冲液来稳定溶血剂的ph。通常可以采用酸或盐调节溶血剂的ph,调节ph所用的试剂包括但不限于柠檬酸、盐酸、硼酸、硫酸氢钠、氢氧化钠中的至少一种。
[0070]
在一实施例中,所述溶血剂还含有缓冲液。缓冲液可以使得溶液的ph保持稳定。
[0071]
在一实施例中,所述缓冲液包括但不限于柠檬酸-柠檬酸钠缓冲液、柠檬酸-柠檬酸盐缓冲液、pbs缓冲液、醋酸-醋酸钠缓冲液、tris-hcl缓冲液、硼酸-硼砂缓冲液、britton-robison缓冲液、碳酸盐缓冲液、磷酸盐缓冲液、甲酸-甲酸钠缓冲液、丁二酸-丁二酸钠缓冲液、甘氨酸钠-盐酸缓冲液中的至少一种。
[0072]
在一实施例中,碳酸盐缓冲液可以是碳酸钠-碳酸氢钠缓冲液,磷酸盐缓冲液可以是磷酸二氢钠-磷酸氢二钠缓冲液。
[0073]
第一方面所述溶血剂可以封装于试剂瓶等容器中,形成产品。或者与其他套装试剂组合成试剂盒。试剂盒可以是具有多个腔室的盒体,溶血剂以及其他配套试剂封装于盒体内的不同腔室中,形成产品。
[0074]
第二方面,在一实施例中,提供一种用于血液分析的试剂盒,包括脒基类化合物或其盐,或第一方面所述溶血剂。
[0075]
在一实施例中,所述脒基类化合物具有式(a)所示结构:
[0076][0077]
式(a)中,r1、r2、r3、r4独立地为氢、烃基、取代的烃基、羟基或氨基。
[0078]
在一实施例中,所述用于血液分析的试剂是用于分析血液中的血红蛋白的试剂。
[0079]
在一实施例中,所述用于血液分析的试剂是用于分析血液中的白细胞的试剂。
[0080]
第三方面,在一实施例中,提供一种血红蛋白检测试剂盒,包括至少一种脒基类化合物或其盐,或第一方面所述溶血剂。该试剂盒可用于检测血红蛋白在血液样本中的浓度。
[0081]
在一实施例中,还包括用于稀释血液样本的稀释剂。第一方面所述溶血剂或其试剂盒也可应用于糖化血红蛋白检测等其他用途。
[0082]
第四方面,在一实施例中,提供一种白细胞检测试剂盒,包括至少一种脒基类化合物或其盐,或第一方面所述溶血剂。
[0083]
在一实施例中,还包括用于抑制溶血剂对血液中的白细胞进一步损害的抑制剂。白细胞检测试剂盒可以用于白细胞分类计数,例如可用于白细胞三分类、四分类、五分类的分析等等。例如,用于五分类计数时,可将白细胞分成五个细胞群,分别为中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞和嗜碱性细胞。也可用于检测白细胞体积等等。
[0084]
第五方面,在一实施例中,提供一种血小板检测试剂盒,包括至少一种脒基类化合物或其盐,或第一方面所述溶血剂。血小板检测试剂盒可用于检测血小板的数量或体积等等。
[0085]
在一实施例中,还包括用于选择性着色血液样本中的血小板的着色剂。
[0086]
第六方面,在一实施例中,提供一种血液分析设备,其包括第一方面所述溶血剂,或第二方面所述试剂盒,或第三方面所述血红蛋白检测试剂盒,或第四方面所述白细胞检
测试剂盒,或第五方面所述血小板检测试剂盒。通常,血液分析设备可设有容纳溶血剂的腔室,溶血剂随检测设备售卖,或者将溶血剂以及其他套装试剂单独封装于各容器中,再成套封装,形成试剂盒,并与检测设备组合为成套产品。
[0087]
第七方面,在一实施例中,提供脒基类化合物或第一方面所述溶血剂在制备血液分析试剂盒中的应用。脒基类化合物或其盐可应用于各种血液分析,示例但非限制性的,如用于分析血液中的血红蛋白、白细胞、血小板等等。在一实施例中,可以是用于检测血液中血红蛋白的浓度、用于血液白细胞分群计数、血小板计数等等。
[0088]
以下实施例中检测所得的血红蛋白浓度为换算得到的血红蛋白在原始血样中的浓度。
[0089]
以下实施例中,ph调节剂包括柠檬酸、浓盐酸、氢氧化钠。
[0090]
以下实施例中,如无特别说明,室温(或称为常温)均为25℃。
[0091]
实施例1
[0092]
本实施例的溶血剂含有如下浓度的组分:
[0093]
十六烷基三甲基溴化铵4g/l;
[0094]
曲拉通x-100 1ml/l;
[0095]
无水乙醇0.5ml/l;
[0096]
柠檬酸2g/l;
[0097]
苄脒盐酸盐1g/l;
[0098]
氯化钠0.5g/l,
[0099]
柠檬酸钠0.8g/l;
[0100]
加水补足至1l。
[0101]
调节溶血剂的ph,使其达到6.8。
[0102]
使用日本sysmex(希森美康)株式会社生产的sysmex xn-1000血液细胞分析仪,使用xn-1000配套的cellpack dcl全血稀释液,并使用本实施例的溶血剂进行手动测试分析。
[0103]
sysmex xn-1000血液细胞分析仪检测血红蛋白的主要原理是通过测试吸光度来计算血红蛋白的量。
[0104]
按照稀释液:血样=1250μl:3μl进行稀释,再加入250μl溶血剂,用于血红蛋白浓度测试。分别在4℃、室温(25℃)、37℃条件下测试8组血样,记录每个温度下的血红蛋白浓度值。本实施例的8组血样分别来源于8个受试者,分别在4℃、室温(25℃)、37℃条件下测试每组血样的血红蛋白(hgb)的浓度。
[0105]
使用该仪器cbc模式试剂测试得到血红蛋白(hgb)的浓度值,取8组血样进行测试,血红蛋白浓度结果(g/l)如表1所示。
[0106]
表1
[0107][0108][0109]
从表1可以看出,4℃相对于25℃血红蛋白测试结果偏差约0.80%;37℃相对于25℃血红蛋白hgb测试结果偏差约0.50%。
[0110]
实施例2
[0111]
本实施例的溶血剂含有如下浓度的组分:
[0112]
十六烷基三甲基氯化铵4g/l;
[0113]
曲拉通x-100 1ml/l;
[0114]
无水乙醇0.5ml/l;
[0115]
甲脒2g/l;
[0116]
氯化钠0.5g/l;
[0117]
柠檬酸2g/l;
[0118]
柠檬酸钠0.8g/l;
[0119]
加水补足至1l。
[0120]
调节溶血剂的ph,使其达到7.5。
[0121]
另取8组血样,本实施例的8组血样分别来源于8个受试者,分别在4℃、室温(25℃)、37℃条件下测试每组血样的血红蛋白(hgb)的浓度。测试方法同实施例1,血红蛋白浓度结果(g/l)如表2所示。
[0122]
表2
[0123]
序号4℃室温37℃11341351342122122122314814914941331351375141140140615415615571371371388107110118均值134.5135.5136.625
[0124]
从表2可以看出,4℃相对于25℃血红蛋白测试结果偏差约0.74%;37℃相对于25℃血红蛋白浓度测试结果偏差约0.83%。
[0125]
实施例3
[0126]
本实施例的溶血剂含有如下浓度的组分:
[0127]
十二烷基三甲基溴化铵6g/l;
[0128]
曲拉通x-100 1ml/l;
[0129]
无水乙醇0.5ml/l;
[0130]
4-氯苯甲脒盐酸盐0.7g/l;
[0131]
氯化钠0.5g/l;
[0132]
柠檬酸2g/l;
[0133]
柠檬酸钠0.8g/l;
[0134]
加水补足至1l。
[0135]
调节溶血剂的ph,使其达到7.0。
[0136]
另取8组血样,本实施例的8组血样分别来源于8个受试者,分别在4℃、室温(25℃)、37℃条件下测试每组血样的血红蛋白(hgb)的浓度。测试方法同实施例1,血红蛋白浓度结果(g/l)如表3所示。
[0137]
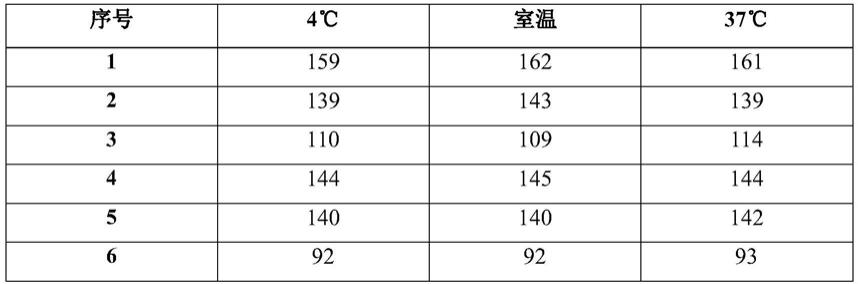
表3
[0138]
温度4℃室温37℃11591601622139139143311010910941441441455140141140692939271281291298164162163均值134.5134.625135.375
[0139]
从表3可以看出,4℃相对于25℃血红蛋白测试结果偏差约0.09%;37℃相对于25℃血红蛋白浓度测试结果偏差约0.56%。
[0140]
实施例4
[0141]
本实施例的溶血剂含有如下浓度的组分:
[0142]
十二烷基苯磺酸钠5g/l;
[0143]
脂肪胺聚氧乙烯醚1ml/l;
[0144]
n-羟基丙酸脒0.9g/l;
[0145]
氯化钾0.5g/l;
[0146]
盐酸2g/l;
[0147]
tris-hcl缓冲液0.8g/l;
[0148]
加水补足至1l。
[0149]
调节溶血剂的ph,使其达到7.0。
[0150]
另取8组血样,本实施例的8组血样分别来源于8个受试者,分别在4℃、室温(25℃)、37℃条件下测试每组血样的血红蛋白(hgb)的浓度。测试方法同实施例1,血红蛋白浓度结果(g/l)如表4所示。
[0151]
表4
[0152]
温度4℃室温37℃11571561572969998314013813841591591585139140137611511611671181201178147147149均值133.9134.4133.8
[0153]
从表4可以看出,4℃相对于25℃血红蛋白测试结果偏差约0.37%;37℃相对于25℃血红蛋白浓度测试结果偏差约0.45%。
[0154]
实施例5
[0155]
本实施例的溶血剂含有如下浓度的组分:
[0156]
十八烷基三甲基氯化铵6g/l;
[0157]
烷基酚聚氧乙烯醚1ml/l;
[0158]
无水丁醇0.5ml/l;
[0159]
氨基乙脒二氢溴酸盐0.5g/l;
[0160]
盐酸2g/l;
[0161]
tris-hcl缓冲液0.8g/l;
[0162]
加水补足至1l。
[0163]
调节溶血剂的ph,使其达到7.0。
[0164]
另取8组血样,本实施例的8组血样分别来源于8个受试者,分别在4℃、室温(25℃)、37℃条件下测试每组血样的血红蛋白(hgb)的浓度。测试方法同实施例1,血红蛋白浓度结果(g/l)如表5所示。
[0165]
表5
[0166]
[0167][0168]
从表5可以看出,4℃相对于25℃血红蛋白测试结果偏差约0.45%;37℃相对于25℃血红蛋白浓度测试结果偏差约0.15%。
[0169]
氰化血红蛋白法测定及关系曲线绘制:
[0170]
氰化血红蛋白法具体参照文献“邓文桤,张志雄.用氰化高铁血红蛋白测定法调查广东省正常人群hb水平的分析.数理医药学杂志,1995”进行。
[0171]
图1至图5中,各曲线的横坐标、纵坐标的单位均为g/l。
[0172]
共采集了40个受试者的血样,在常温(25℃)下,分别采用实施例1的溶血剂与方法、氰化血红蛋白法对每个受试者的血样进行血红蛋白浓度检测,图1显示为采用实施例1的溶血剂与方法的检测结果与氰化血红蛋白法的检测结果关系曲线图,x坐标轴是使用氰化血红蛋白法测得的血样中血红蛋白浓度(g/l),y坐标轴是实施例1自制溶血剂测得的血样中血红蛋白浓度(g/l),r2=0.9916,相关性非常好,说明本实施例的测试结果高度接近。
[0173]
共采集了另外40个受试者的血样,在常温(25℃)下,分别采用实施例2的溶血剂与方法、氰化血红蛋白法对每个受试者的血样进行血红蛋白浓度检测,图2显示为采用实施例2的溶血剂与方法的检测结果与氰化血红蛋白法的检测结果关系曲线图,x坐标轴是使用氰化血红蛋白法测得的血样中血红蛋白浓度,y坐标轴是实施例2自制溶血剂测得的血样中血红蛋白浓度,r2=0.9936,相关性非常好,说明本实施例的测试结果高度接近。
[0174]
共采集了另外40个受试者的血样,在常温(25℃)下,分别采用实施例3的溶血剂与方法、氰化血红蛋白法对每个受试者的血样进行血红蛋白浓度检测,图3显示为采用实施例3的溶血剂与方法的检测结果与氰化血红蛋白法的检测结果关系曲线图,x坐标轴是使用氰化血红蛋白法测得的血样中血红蛋白浓度,y坐标轴是实施例3自制溶血剂测得的血样中血红蛋白浓度,r2=0.9904,相关性非常好,说明本实施例的测试结果高度接近。
[0175]
共采集了另外40个受试者的血样,在常温(25℃)下,分别采用实施例4的溶血剂与方法、氰化血红蛋白法对每个受试者的血样进行血红蛋白浓度检测,图4显示为采用实施例4的溶血剂与方法的检测结果与氰化血红蛋白法的检测结果关系曲线图,x坐标轴是使用氰化血红蛋白法测得的血样中血红蛋白浓度,y坐标轴是实施例4自制溶血剂测得的血样中血红蛋白浓度,r2=0.9936,相关性非常好,说明本实施例的测试结果高度接近。
[0176]
共采集了另外40个受试者的血样,在常温(25℃)下,分别采用实施例5的溶血剂与方法、氰化血红蛋白法对每个受试者的血样进行血红蛋白浓度检测,图5显示为采用实施例5的溶血剂与方法的检测结果与氰化血红蛋白法的检测结果关系曲线图,x坐标轴是使用氰
化血红蛋白法测得的血样中血红蛋白浓度,y坐标轴是实施例5自制溶血剂测得的血样中血红蛋白浓度,r2=0.9947,相关性非常好,说明本实施例的测试结果高度接近。
[0177]
分光光度计(岛津紫外分光光度计uv-1780,扫描范围:500-800nm)测试图谱实验:
[0178]
正常情况下,血红蛋白在540纳米左右有波峰,在570纳米左右有一个峰肩。
[0179]
图6为实施例1的溶血剂及其所处理血样(从实施例1所测血样中任取一个)的分光光度计测试图谱,按照xn-1000稀释液:实施例1溶血剂:血样=1250:250:3(体积比)对血液进行稀释溶血,混匀后,静置30s,然后使用紫外分光光度计,在500-800nm波段进行扫描,得到图6所示图谱,在539nm光波处有吸收峰,577nm光波处有一个小的吸收峰。
[0180]
图7为实施例2的溶血剂及其所处理血样(从实施例2所测血样中任取一个)的分光光度计测试图谱,按照xn-1000稀释液:实施例2溶血剂:血样=1250:250:3(体积比)对血液进行稀释溶血,然后使用紫外分光光度计,在500-800nm波段进行扫描,得到图7所示图谱,在542nm光波处有吸收峰,575nm光波处有一个小的吸收峰。
[0181]
图8为实施例3的溶血剂及其所处理血样(从实施例3所测血样中任取一个)的分光光度计测试图谱,按照xn-1000稀释液:实施例3溶血剂:血样=1250:250:3(体积比)对血液进行稀释溶血,然后使用紫外分光光度计,在500-800nm波段进行扫描,得到图8所示图谱,在540nm光波处有吸收峰,569nm光波处有一个小的吸收峰。
[0182]
图9为实施例4的溶血剂及其所处理血样(从实施例4所测血样中任取一个)的分光光度计测试图谱,按照xn-1000稀释液:实施例4溶血剂:血样=1250:250:3(体积比)对血液进行稀释溶血,然后使用紫外分光光度计,在500-800nm波段进行扫描,得到图9所示图谱,在538nm光波处有吸收峰,567nm光波处有一个小的吸收峰。
[0183]
图10为实施例5的溶血剂及其所处理血样(从实施例5所测血样中任取一个)的分光光度计测试图谱,按照xn-1000稀释液:实施例5溶血剂:血样=1250:250:3(体积比)对血液进行稀释溶血,然后使用紫外分光光度计,在500-800nm波段进行扫描,得到图10所示图谱,在538nm光波处有吸收峰,568nm光波处有一个小的吸收峰。
[0184]
上述图谱实验结果证实各实施例的溶血剂处理后的样品中存在血红蛋白,脒基类化合物能够结合至血红蛋白及其衍生物,形成稳定的复合物。
[0185]
以上应用了具体个例对本发明进行阐述,只是用于帮助理解本发明,并不用以限制本发明。对于本发明所属技术领域的技术人员,依据本发明的思想,还可以做出若干简单推演、变形或替换。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1