一种土壤中有效磷的测定方法与流程
本发明属于土壤成份测定方法技术领域,具体涉及一种土壤中有效磷的测定方法。
背景技术:
有效磷是指土壤中可被植物吸收和利用的磷的总称,在土壤中没有固定的形态,包括土壤溶液中的磷、弱吸附态磷、交换性磷和易溶性固体磷酸盐等。土壤有效磷是土壤中可被植物吸收的磷组份,是土壤肥力的重要指标之一,测定有效磷含量可用于了解土壤的供磷能力,对合理施肥,改良土壤,提高作物产量和品质具有重要参考价值。
目前土壤有效磷的测定方法主要有3种,分别是olsen法(0.5mol/lnahco3,ph=8.5)、bray-kurtzl法(0.025mol/lhcl+0.03mol/lnh4f)和mehlich法(ph=2.5,0.2mol/lch3cooh+0.25mol/lnh4no3+0.015mol/lnh4f+0.001mol/ledta),bray-kurtzl法可以容易的测定酸性土壤有效磷,包括大部分磷酸钙和一部分磷酸铝和磷酸铁,此方法为目前国际通用的测定酸性土壤有效磷的方法;mehlich法能够提取多种有效养分,并广泛适用于中性、酸性土壤;olsen法既适合于石灰性土壤,也适合于中、酸性土壤,但olsen浸提剂容易将土壤中的腐殖质溶解出来似的浸提液呈现黄色或黄褐色,需要对浸提液进行脱色。
不同测定方法对有效磷的提取机理不同,针对中性和碱性土壤,常按照中华人民共和国环境保护部2014-09-15发布,2014-12-01实施的hj704-2014《土壤有效磷的测定碳酸氢钠浸提-钼锑抗分光光度法》进行检测,即采用0.5mol/l碳酸氢钠溶液(ph=8.5)浸提。但此种方法存在一定的弊端,即所用碳酸氢钠浸提剂在配制完成后应在4h内使用,每次检测时需重新配制浸提剂,绘制校准曲线,操作繁琐,耗费时间,降低了测定效率。
因此,需要提供一种针对上述现有技术不足的改进技术方案。
技术实现要素:
本发明的目的是一种土壤中有效磷的测定方法,用以克服上述现有技术中每次检测时需重新配制浸提剂,绘制校准曲线,测定效率低的问题。
为了实现上述目的,本发明提供如下技术方案:
一种土壤中有效磷的测定方法,所述测定方法包括以下步骤:
步骤s1、将土壤进行采集并自然风干,经过研磨、过筛,取筛下物作为待测土样;
步骤s2、称取步骤s1中的所述待测土样加入浸提剂中,经恒温振荡后过滤,得到滤液;
步骤s3、取步骤s2中的所述滤液于容量瓶中,然后加入抗坏血酸溶液,混合后再加入钼酸盐溶液,再用水定容并混合,得到待测液或称为试料,体积为v1;
步骤s4、将步骤s3中得到的所述待测液静置,然后吸取v2体积的所述试料测定样品吸光度值a和空白试验的吸光度值a0;所述空白对照是按照与步骤s2、步骤s3和步骤s4的操作设置的与待测土样试验平行的对照试验,所述空白对照试验中不加入所述待测土样;
步骤s5、利用磷标准使用液和浸提剂的混合液替代步骤s3中的滤液,并按照步骤s3和步骤s4的操作获得磷质量与通过空白试验校正的吸光度值的关系,由此绘制以磷质量为纵坐标、空白试验校正的吸光度值为横坐标的校准曲线;
步骤s6、根据所述校准曲线以及经过空白试验校正的测定样品吸光度值计算土壤中有效磷的含量。
如上所述的土壤中有效磷的测定方法,作为优选方案,所述浸提剂为nahco3溶液,所述nahco3溶液的物质的量浓度为0.5mol/l;所述浸提剂的ph值为8.5;
优选地,所述浸提剂的配制时间距离使用时间不超过5d,当所述浸提剂的配制时间距离使用时间超过4h,所述浸提剂在使用前采用无机酸重新调节ph值至8.5;所述无机酸为硫酸,更优选为2mol/l的硫酸。
如上所述的土壤中有效磷的测定方法,作为优选方案,所述钼酸盐溶液中,钼酸铵浓度为10g/l,硫酸浓度为3.76mol/l;
优选地,以配制1l钼酸盐溶液为基础,所述钼酸盐溶液的配制方法包括以下步骤:
a、将10.0g钼酸铵在60℃下溶解于300ml的水中,冷却,得到钼酸铵溶液;
b、量取浓硫酸在不断搅拌下注入水中,冷却得到硫酸溶液;
c、取400ml步骤b中得到的所述硫酸溶液,在搅拌条件下加入步骤a中得到的所述钼酸铵溶液中,再加入100ml5g/l的酒石酸锑钾溶液,最后用水定容至1l,得到钼酸盐溶液;
优选地,步骤b中所述浓硫酸与水的体积比为1:1;
所述浓硫酸的密度为1.84g/ml,浓度为98%。
如上所述的土壤中有效磷的测定方法,作为优选方案,步骤s1中所述过筛为过0.25mm筛孔的筛子;
优选地,步骤s1中所述土壤进行采集的深度为地表以下20~30cm。
如上所述的土壤中有效磷的测定方法,作为优选方案,步骤s2中所述待测土样的质量与浸提剂的体积比为1:(15~25),其中,待测土样的质量的单位为g,浸提剂的体积的单位为ml;
优选地,步骤s2中所述待测土样的质量与浸提剂的体积比为1:20,其中,待测土样的质量的单位为g,浸提剂的体积的单位为ml;
更优选地,步骤s2中所述待测土样的质量为2.50g,所述浸提剂的体积为50.0ml。
如上所述的土壤中有效磷的测定方法,作为优选方案,步骤s2中,所述恒温振荡是指置于恒温振荡器中振荡25~35min;所述恒温振荡器的温度为25℃,所述恒温振荡器的振荡频率为180~200r/min;
优选地,所述过滤为采用无磷滤纸过滤。
如上任一项所述的土壤中有效磷的测定方法,作为优选方案,步骤s3中,所述抗坏血酸溶液的浓度为100g/l,用量为0.75ml;
所述滤液的用量为10ml;
所述混合的时间为30s;
所述钼酸盐溶液的用量为5ml;
用水定容至50ml并混合均匀,得到待测液。
如上任一项所述的土壤中有效磷的测定方法,作为优选方案,步骤s4中,所述静置是指置于25℃恒温箱中静置30min;
以水做参比,采用10mm比色皿于波长880nm处,测定样品吸光度值a和空白试验的吸光度值a0。
如上所述的土壤中有效磷的测定方法,作为优选方案,步骤s5中绘制校准曲线的具体步骤为:
s51、配制质量浓度为5.00mg/l的磷标准使用液;
s52、分别量取0.00ml,1.00ml,2.00ml,3.00ml,4.00ml,5.00ml,6.00ml步骤s51中的所述磷标准使用液于50ml的具塞比色管中,加入0.5mol/l的nahco3溶液至10.00ml,加水至25.00ml,再加入100g/l抗坏血酸溶液0.75ml,混合30s,然后再加入5ml钼酸盐溶液,用水定容至50ml并混合均匀,得到一系列标准液;
s53、将步骤s52中得到的一系列所述标准液置于25℃恒温箱中静置30min,以水做参比,采用10mm比色皿于波长880nm处,分别测定吸光度和空白试验吸光度;
s54、以磷质量为纵坐标,对应扣除空白的校正后的系列标准液的吸光度为横坐标,绘制校准曲线。
如上所述的土壤中有效磷的测定方法,作为优选方案,步骤s6中,以干重计,土壤中有效磷的含量,根据下述公式计算:
式中:ω---土壤中有效磷的含量,mg/kg;
a---样品吸光度值;
a0---空白试验的吸光度值;
a---校准曲线的斜率;
b---校准曲线的截距;
v1---试料体积,ml;
v2---吸取试料体积,ml;
wdm---土壤样品的干物质含量,%;
m---称取待测土样的质量,kg。
与最接近的现有技术相比,本发明提供的技术方案具有如下优异效果:
本发明中的测定方法适用于多次样品有效磷的测定,检验人员一次性配制碳酸氢钠浸提剂后,可多次使用,在多次测定过程中无需重复配制浸提剂和重复绘制校准曲线,使得操作过程更加简便,大大提高了测定效率。
本发明中将放置时间超过4h的0.5mol/l碳酸氢钠浸提剂用于土壤有效磷测定时,使用前调节其ph至8.5,浸提剂的放置时间可延长至5d,土壤中有效磷含量的实测值与真实值之差<1.0mg/kg,在允许的误差范围之内;且采用碳酸氢钠作为浸提剂,并对浸提后的显色反应进行了改进,可快速方便的测出土壤中有效磷,同时解决了显色试剂配制复杂、需现配现用的问题。
附图说明
构成本申请的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。其中:
图1为本发明具体实施例中的校准曲线图。
具体实施方式
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员所获得的所有其他实施例,都属于本发明保护的范围。
本发明提供的土壤有效磷的测定方法中,采用放置时间超过4h的0.5mol/l碳酸氢钠作为浸提剂用于土壤有效磷测定,使用前调节其ph至8.5,然后再用于土壤有效磷的测定,使得浸提剂的放置时间可延长至5d,土壤中有效磷含量的实测值与真实值之差<1.0mg/kg,在允许的误差范围之内;该方法适用于多次样品有效磷的测定,检验人员一次性配制碳酸氢钠浸提剂后,可多次使用,在多次测定过程中无需重复配制浸提剂和重复绘制校准曲线,使得操作过程更加简便,大大提高了测定效率。
本发明具体实施例中提供一种土壤中有效磷的测定方法,测定方法包括以下步骤:
步骤s1、将土壤进行采集并自然风干,经过研磨、过筛,取筛下物作为待测土样;
在本发明具体实施例中,步骤s1中过筛为过0.25mm筛孔的筛子;先过2mm筛,经过研磨后再过0.25mm筛。
优选地,土壤进行采集的深度为地表以下20~30cm(比如20cm、22cm、24cm、25cm、26cm、28cm、30cm)。
步骤s2、称取步骤s1中的待测土样加入装有浸提剂的具塞瓶中,塞紧,经恒温振荡后过滤,得到滤液。
在本发明具体实施例中,步骤s2中,恒温振荡是指置于恒温振荡器中振荡25~35min(比如25min、26min、27min、28min、29min、30min、31min、32min、33min、34min、35min);恒温振荡器的温度为25℃,恒温振荡器的振荡频率为180~200r/min(比如180r/min、185r/min、190r/min、195r/min、200r/min)。
优选地,过滤为采用无磷滤纸过滤。
在本发明具体实施例中,步骤s2中浸提剂为nahco3溶液,nahco3溶液的物质的量浓度为0.5mol/l;浸提剂的ph值为8.5。
优选地,浸提剂的配制时间距离使用时间不超过5d(比如0d、1d、2d、3d、4d、5d),当浸提剂的配制时间距离使用时间超过4h,浸提剂在使用前采用无机酸重新调节ph值至8.5;无机酸为硫酸,更优选为2mol/l的硫酸。
其中,nahco3溶液的ph值为8.5时对土壤中有效磷的浸提效果最好,但是nahco3浸提剂在放置过程中可因失去co2而使ph增高,浸提效果变差,当浸提剂放置时间超过4h,ph有所升高,滴加c(1/2h2so4)=2mol/l硫酸溶液调节其ph至8.5,这时浸提剂浸提效果最好,可用于土壤有效磷测定。
在本发明具体实施例中,步骤s2中待测土样的质量与浸提剂的体积比为1:(15~25)(比如1:15、1:16、1:17、1:18、1:19、1:20、1:21、1:22、1:23、1:24、1:25),其中,待测土样的质量的单位为g,浸提剂的体积的单位为ml。
优选地,步骤s2中所述待测土样的质量与浸提剂的体积比为1:20,其中,待测土样的质量的单位为g,浸提剂的体积的单位为ml;
更优选地,步骤s2中待测土样的质量为2.50g,浸提剂的体积为50.0ml。
步骤s3、取步骤s2中的所述滤液于容量瓶中,加入抗坏血酸溶液,混合后再加入钼酸盐溶液,用水定容并混合均匀,得到待测液或称为试料,体积为v1。
在本发明具体实施例中,步骤s3中,抗坏血酸溶液的浓度为100g/l,用量为0.75ml;滤液的用量为10ml;混合的时间为30s;钼酸盐溶液的用量为5ml;用水定容至50ml并混合均匀,得到待测液。
在本发明具体实施例中,钼酸盐溶液中,钼酸铵浓度为10g/l,硫酸浓度为3.76mol/l;
优选地,以配制1l钼酸盐溶液为基础,所述钼酸盐溶液的配制方法包括以下步骤:
a、将10.0g钼酸铵在60℃下溶解于300ml的水中,冷却,得到钼酸铵溶液;
b、量取浓硫酸在不断搅拌下注入水中,冷却得到硫酸溶液;
在本发明具体实施例中,步骤b中浓硫酸与水的体积比为1:1;浓硫酸的密度为1.84g/ml,浓度为98%。即将1体积的浓硫酸缓缓加入1体积水的容器中,并不断搅拌。
c、取400ml步骤b中得到的硫酸溶液,在搅拌条件下加入步骤a中得到的钼酸铵溶液中,再加入100ml酒石酸锑钾溶液,最后用水定容至1l,得到钼酸盐溶液。
按照中华人民共和国环境保护部2014-09-15发布,2014-12-01实施的hj704-2014《土壤有效磷的测定碳酸氢钠浸提-钼锑抗分光光度法》中的显色过程是先采用硫酸溶液中和碳酸氢钠,然后进行显色,在实际操作过程中,当土壤中有效磷含量较低时,滴加硫酸时,溶液变色较难判断,所以,与该标准相比,本发明具体实施例中,在钼酸盐溶液配制过程中,增加了硫酸用量,简化了显色的操作过程,可快速方便的测出土壤中有效磷,同时解决了显色试剂配制复杂、需现配现用的问题。
步骤s4、将步骤s3中得到的待测液静置,然后吸取v2体积的所述试料测定样品吸光度值a和空白试验的吸光度值a0;空白对照是按照与步骤s2、步骤s3和步骤s4的操作设置的与待测土样试验平行的对照试验,空白对照试验中不加入待测土样;
在本发明具体实施例中,步骤s4中,静置是指置于25℃恒温箱中静置30min;
以水做参比,采用10mm比色皿于波长880nm处,测定样品吸光度值a和空白试验的吸光度值a0。
步骤s5、利用磷标准使用液和浸提剂的混合液替代步骤s3中的滤液,并按照步骤s3和步骤s4的操作获得磷质量与通过空白试验校正的吸光度值的关系,由此绘制以磷质量为纵坐标、空白试验校正的吸光度值为横坐标的校准曲线。
在本发明具体实施例中,步骤s5中绘制校准曲线的具体步骤为:
s51、配制质量浓度为5.00mg/l的磷标准使用液;
s52、分别量取0.00,1.00,2.00,3.00,4.00,5.00,6.00ml步骤s51中的所述磷标准使用液于50ml的具塞比色管中,其对应的磷质量分别为0.00、5.00、10.0、15.0、20.0、25.0、30.0μg,加入0.5mol/l的nahco3溶液至10.00ml,加水至25.00ml,再加入100g/l抗坏血酸溶液0.75ml,混合30s,然后再加入5ml钼酸盐溶液,用水定容至50ml并混合均匀,得到一系列标准液;
s53、将步骤s52中得到的一系列标准液置于25℃恒温箱中净置30min,以水做参比,采用10mm比色皿于波长880nm处,分别测定吸光度和空白试验吸光度;
s54、以磷质量(mg)为纵坐标,对应扣除空白的校正后的系列标准液的吸光度为横坐标,绘制校准曲线。对应扣除空白的校正后的标准液的吸光度为标准液相对应测得的吸光度与空白试验吸光度的差值。
步骤s6、根据校准曲线以及经过空白试验校正的测定样品吸光度值a计算土壤中有效磷的含量。
在本发明具体实施例中,步骤s6中,以干重计,土壤中有效磷的含量,根据下述公式计算:
式中:ω---土壤中有效磷的含量,mg/kg;
a---样品吸光度值;
a0---空白试验的吸光度值;
a---校准曲线的斜率;
b---校准曲线的截距;
v1---试料体积,ml;
v2---吸取试料体积,ml;
wdm---土壤样品的干物质含量,%;
m---称取待测土样的质量,kg。
其中,土壤样品的干物质含量是按照hj613-2011《土壤干物质和水分的测定重量法》进行土壤干物质测定而得到的,具体为,将土壤样品在105±5℃下烘干至恒重,以烘干前后的土壤样品质量差值计算干物质的含量。
本发明中未详细描述的溶液的配制方法参照中华人民共和国环境保护部2014-09-15发布,2014-12-01实施的hj704-2014《土壤有效磷的测定碳酸氢钠浸提-钼锑抗分光光度法》中记载的相应溶液的配制。
实施例1
本发明实施例提供一种某苗圃土壤有效磷的测定方法,测定方法包括以下步骤:
步骤s1、在苗圃中选取5个样点,每个样点均设5个采样点,每个采样点采集地表以下20~30cm土层的土壤,然后将每个样点的5个土样分别混合,并自然风干,采用四分法,取其中两份过2mm筛,经过研磨后再过0.25mm筛,得到待测土样,对5个样点的样品分别编号为s-1、s-2、s-3、s-4、s-5。
步骤s2、称取步骤s1中编号为s-1、s-2、s-3、s-4、s-5的待测土样2.50g加入装有50.0ml0.5mol/l的nahco3溶液浸提剂的具塞瓶中,塞紧,置于25℃的振荡器中以180~200r/min的频率振荡30min,用无磷滤纸过滤,得到滤液;
其中,所用浸提剂的放置时间分别为0d、1d、3d、5d、7d,且使用前,滴加c(1/2h2so4)=2mol/l硫酸溶液调节其ph至8.5。
步骤s3、分别取10.0ml步骤s2中的滤液于容量瓶中,加入100g/l抗坏血酸溶液0.75ml,混合30s,然后再加入5ml钼酸盐溶液,用水定容至50ml并混合均匀,得到待测液或称为试料,体积为v1。
步骤s3中钼酸盐溶液的配制方法包括以下步骤:
a、将10.0g钼酸铵在60℃下溶解于300ml的水中,冷却,得到钼酸铵溶液;
b、量取200ml密度为1.84g/ml,浓度为98%的浓硫酸,在不断搅拌下注入装有200ml水的容器中,冷却得到硫酸溶液;
c、取400ml步骤b中得到的硫酸溶液,在搅拌条件下加入步骤a中得到的钼酸铵溶液中,再加入100ml酒石酸锑钾溶液,最后用水定容至1l,得到钼酸盐溶液。
步骤s4、将步骤s3中得到的待测液置于25℃恒温箱中净置30min,然后吸取v2体积的试料以水做参比,采用10mm比色皿于波长880nm处,分别测定样品吸光度值a和空白试验的吸光度值a0。空白对照是按照与步骤s2、步骤s3和步骤s4的操作设置的与待测土样试验平行的对照试验,空白对照试验中不加入待测土样;
步骤s5、利用磷标准使用液和浸提剂的混合液替代步骤s3中的滤液,并按照步骤s3和步骤s4的操作获得磷质量与通过空白试验校正的吸光度值的关系,由此绘制以磷质量为纵坐标、空白试验校正的吸光度值为横坐标的校准曲线。该校准曲线绘制过程中所用的物质的量浓度为0.5mol/l的nahco3浸提剂的放置时间为0d。
步骤s5中绘制校准曲线的具体步骤为:
s51、量取5.00ml质量浓度为100mg/l的磷标准贮备溶液于100ml容量瓶中,用浸提剂稀释至刻度,配制质量浓度为5.00mg/l的磷标准使用液;
s52、分别量取0.00,1.00,2.00,3.00,4.00,5.00,6.00ml步骤s51中的所述磷标准使用液于50ml的具塞比色管中,其对应的磷质量分别为0.00、5.00、10.0、15.0、20.0、25.0、30.0μg,加入0.5mol/l的nahco3浸提剂至10.00ml,加水至25.00ml,再加入100g/l抗坏血酸溶液0.75ml,混合30s,然后再加入5ml钼酸盐溶液,用水定容至50ml并混合均匀,得到一系列标准液;
s53、将步骤s52中得到的一系列标准液置于25℃恒温箱中净置30min,以水做参比,采用10mm比色皿于波长880nm处,分别测定吸光度和空白试验吸光度;
s54、以磷质量(mg)为纵坐标,对应扣除空白的校正后的一系列标准液的吸光度为横坐标,绘制校准曲线。对应扣除空白的校正后的标准液的吸光度为标准液相对应测得的吸光度与空白试验吸光度的差值。
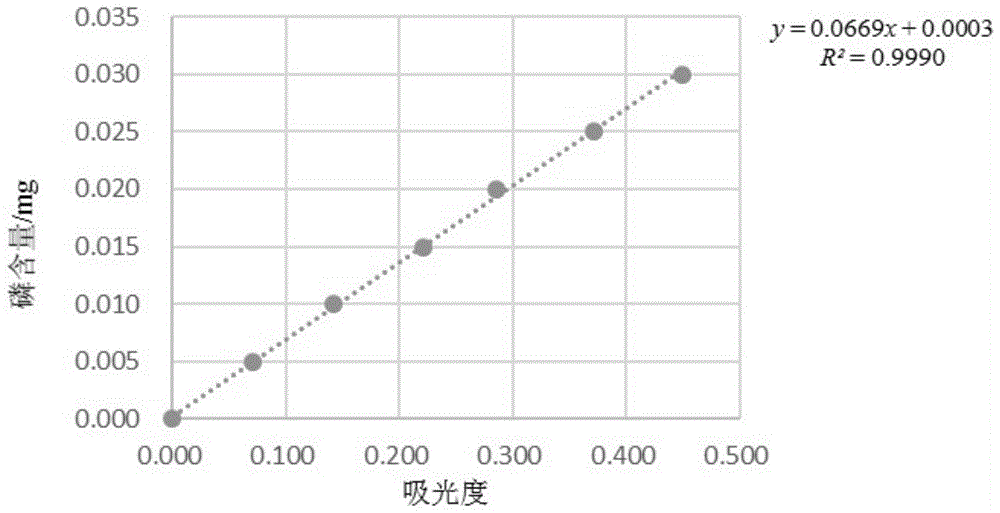
所得校准曲线如图1所示,图1表明校准曲线的相关系数为0.9990,校准曲线方程为y=0.0669x+0.0003,其中x为扣除空白的校正吸光度a,y为磷质量(mg)。
步骤s6、根据校准曲线以及经过空白试验校正的测定样品吸光度值a计算土壤中有效磷的含量。
在本发明实施例中,步骤s6中,以干重计,土壤中有效磷的含量,根据下述公式计算:
式中:ω---土壤中有效磷的含量,mg/kg;
a---样品吸光度值;
a0---空白试验的吸光度值;
a---校准曲线的斜率;
b---校准曲线的截距;
v1---试料体积,ml;
v2---吸取试料体积,ml;
wdm---土壤样品的干物质含量,%;
m---称取待测土样的质量,kg。
其中,土壤样品的干物质含量是按照hj613-2011《土壤干物质和水分的测定重量法》进行土壤干物质测定而得到的。
对5个土壤样品s-1、s-2、s-3、s-4、s-5分别进行有效磷的测定,按照步骤s6中的公式计算得出各土样中有效磷的测定结果,如下表1所示为使用前调节浸提剂的ph值至8.5时,浸提剂放置时间对有效磷测定结果的影响。
表1浸提剂放置时间(使用前调节ph=8.5)对有效磷测定结果的影响
由表1可知,在使用浸提剂前调节ph值的情况下,所测0.015mg标样的实测值与真实值的相对误差不超过±5%,调节浸提剂的ph值对其吸光度值影响较小,可忽略不计,说明所用校准曲线符合要求,因此无需重新绘制校准曲线。
表1结果表明,在浸提剂使用前调节ph至8.5的情况下,当浸提剂放置5d时,土样有效磷的实测值与真实值之差在允许的误差范围之内(允许误差范围<1.0mg/kg),当浸提剂放置7d时,部分土样有效磷的实测值与真实值之差超出了允许的误差范围(允许误差范围<1.0mg/kg);在浸提剂的ph调节过程中,随着放置时间的增加,浸提剂中co32-逐渐减少,可能会对浸提效果有所影响,由表1中结果可知,碳酸氢钠浸提剂放置时间最长为5d。
对照例1
本对照例提供一种某苗圃土壤有效磷的测定方法,本对照例与实施例1的区别在于,步骤s2中所用浸提剂的放置时间分别为0d、1d、3d、5d、7d,且使用前未调节ph值,其他步骤与实施例1相同,在此不再赘述。
对5个土壤样品s-1、s-2、s-3、s-4、s-5分别进行有效磷的测定,按照步骤s6中的公式计算得出各土样中有效磷的测定结果,如下表2所示为使用前未调节浸提剂的ph值时,浸提剂放置时间对有效磷测定结果的影响。
表2浸提剂放置时间(使用前未调节ph)对有效磷测定结果的影响
由表2对比可知,在使用浸提剂前未调节ph值的情况下,所测0.015mg标样的实测值与真实值的相对误差不超过±5%,调节浸提剂的ph值对其吸光度值影响较小,可忽略不计,说明所用校准曲线符合要求,因此无需重新绘制校准曲线。
表2表明,当浸提剂放置1d时,部分土样有效磷的实测值与真实值之差超出了允许的误差范围(允许误差范围<1.0mg/kg)。
实施例2
本发明实施例提供一种某市公园土壤有效磷的测定方法,本实施例中的测定方法与实施例1的区别在于,步骤s1中,在公园中选取5个样点,每个样点均设5个采样点,每个采样点采集地表以下20~30cm土层的土壤,然后将每个样点的5个土样分别混合,并自然风干,采用四分法,取其中两份过2mm筛,经过研磨后再过0.25mm筛,得到待测土样,5个样点的土样分别编号为h-1、h-2、h-3、h-4、h-5;其他步骤与实施例1相同,再此不再赘述。
对5个土壤样品h-1、h-2、h-3、h-4、h-5分别进行有效磷的测定,按照与实施例1相同的公式计算得出各土样中有效磷的测定结果,如下表3所示为使用前调节浸提剂的ph值至8.5时,浸提剂放置时间对有效磷测定结果的影响。
表4浸提剂放置时间(使用前调节ph=8.5)对有效磷测定结果的影响
由表3可知,在使用浸提剂前调节ph值的情况下,所测0.015mg标样的实测值与真实值的相对误差不超过±5%,调节浸提剂的ph值对其吸光度值影响较小,可忽略不计,说明所用校准曲线符合要求,因此无需重新绘制校准曲线。
表3结果表明,在浸提剂使用前调节ph至8.5的情况下,当浸提剂放置5d时,土样有效磷的实测值与真实值之差在允许的误差范围之内(允许误差范围<1.0mg/kg),当浸提剂放置7d时,部分土样有效磷的实测值与真实值之差超出了允许的误差范围(允许误差范围<1.0mg/kg);由表3中结果可知,碳酸氢钠浸提剂放置时间最长为5d。
对照例2
本对照例提供一种某市公园土壤有效磷的测定方法,本对照例与实施例2的区别在于,步骤s2中所用浸提剂的放置时间分别为0d、1d、3d、5d、7d,且使用前未调节ph值,其他步骤与实施例2相同,再此不再赘述。
对5个土壤样品h-1、h-2、h-3、h-4、h-5分别进行有效磷的测定,按照与实施例1相同的公式计算得出各土样中有效磷的测定结果,如下表4所示为使用前未调节浸提剂的ph值,浸提剂放置时间对有效磷测定结果的影响。
表4浸提剂放置时间(使用前未调节ph)对有效磷测定结果的影响
由表4可知,在使用浸提剂前未调节ph值的情况下,所测0.015mg标样的实测值与真实值的相对误差不超过±5%,调节浸提剂的ph值对其吸光度值影响较小,可忽略不计,说明所用校准曲线符合要求,因此无需重新绘制校准曲线。
表4表明,在浸提剂使用前未调节ph的情况下,当浸提剂放置1d时,部分土样有效磷的实测值与真实值之差超出了允许的误差范围(允许误差范围<1.0mg/kg)。
综上,将放置一定时间的浸提剂(使用前调节ph至8.5)用于土壤有效磷的测定时,采用0.015mg标准样品对校准曲线进行校准时,见表1和表3可知,0.015mg标准样品的测量值与实际值在允许的误差范围内,调节浸提剂的ph值对其吸光度值影响较小,可忽略不计,因此无需重新绘制校准曲线。而按照中华人民共和国环境保护部2014-09-15发布,2014-12-01实施的hj704-2014《土壤有效磷的测定碳酸氢钠浸提-钼锑抗分光光度法》中规定,碳酸氢钠浸提剂应在4h内使用,按照此规定,当浸提剂放置时间超过4h就需重新配制碳酸氢钠浸提剂。不同的试剂其成分会有一些差异,即使是相同批号的同一试剂也会因开封时间、贮藏条件等因素的影响而有所差异,这些差异直接影响测量的吸光度值,校准曲线也会发生改变,因此更换试剂后一般要重新进行校准曲线的绘制。
在实际工作中可根据5d内的检测量,一次性配制完成所需的碳酸氢钠浸提剂,对土壤样品进行检测。由于调节碳酸氢钠浸提剂的ph对校准曲线影响较小,试验中调节ph后无需重复绘制校准曲线,当样品检测量较大时,本发明中的测定方法可减少浸提剂的配制次数和绘制标准曲线的次数,工作量明显减小。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均在本发明待批权利要求保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!