用于生化反应探测的立体微流控芯片量热计及制备方法
1.本发明涉及一种应用于生物化学反应过程检测的芯片量热计,具体地说,是涉及一种用于高灵敏度立体热电堆结构微流控芯片量热计及制备方法。
背景技术:
2.大部分的化学反应和生物过程都会产生热量信号,例如蛋白质折叠过程、促酶反应、蛋白质
‑
核酸相互作用和生物分子
‑
细胞相互作用。通过测量这些生化反应过程释放或吸收的热量,可以确定这些过程的热力学特性,这对蛋白质稳定性和其他生物化学研究剧有重要意义。量热计是基于量热法所制备的,用于描述化学反应或生物过程的有效工具。它可以检测蛋白质反应过程的相变温度和焓变,实时对反应的过程进行温度监控。通过测量这些生化反应过程释放或吸收的热量,可以确定这些过程的热力学特性,这对蛋白质稳定性和其他生物化学研究剧有重要意义。
3.传统量热计,尽管拥有很高的分辨率。但是传统量热计材料消耗量大,检测时间长和体积大,携带性差,量产率低等问题。在面对未来实验室外实验,以及便携性测量上都难以达到要求,制造微型化的量热计成为了迫切的需求。在生物化学科学研究和药物评价相关工业应用中,对快速响应,低功耗量热计的需求越来越大,近十年来,随着微机电系统(mems)技术的发展,使得小型量热计的低成本、大规模制造成为可能。与微流控系统相结合作为试剂容器的量热计称为微流控芯片量热计。微流控芯片量热计有许多优点。
4.但是现有的生物化学微流控芯片量热计,大多是在派瑞林聚合物或硅、氮化硅等刚性基底表面溅射单质金属的薄膜热电堆或者热电阻,然后在热电堆或者热电阻薄膜上采用开放式腔室制作微流控系统来检测样品热量变化。当生物液体产生代谢活动或者发生化学反应时,根据热电效应,在热电堆冷节点和热节点间会产生温度差,该温度差经由热电堆可以转换为热电动势信号输出,或者由热电阻经过惠斯通电桥也会转换成电压信号,从而实现对被测物表面热流的测量。但是目前用于生物化学微流控芯片量热计的热电堆都是平面的且是单质金属构成的,存在灵敏度低、所占面积大、样品消耗量多、制备成本高等问题,而且只适用于大热量的测量;而热电阻式热流传感器需要通过惠斯通电桥进行信号测量,测试方法较为复杂,并且由于热电阻的电热效应会产生自加热效应使测量的信号发生偏差。目前商用的量热计一般是在硅、氮化硅等刚性基底上制备,这些材料的拉伸能力较差,在使用过程中容易发生断裂现象。并且这两种材料的热导率太高,会加速热量流失,导致测量过程非常短且不够稳定。而目前现有的生物化学微流控芯片量热计的微流道系统一般使用的是开放式腔室,但基于微量生物液体样品的测量,开放型腔室所造成的蒸发热损失,会使得测量的溶液体积无法得到精确控制,在一定程度上会降低灵敏度。
5.所以,目前迫切需要一种可以精确控制生物液体容量、方便携带和能够高精度测量室温下生物化学热量变化的芯片量热计。
技术实现要素:
6.本发明的目的在于针对现有技术的不足之处,提供一种用于生化反应探测的立体微流控芯片量热计及制备方法。
7.本发明的一个方面,提供一种用于生化反应探测的立体微流控芯片量热计,包括:柔性聚酰亚胺基底,所述柔性聚酰亚胺基底上设置碲化铋n型半导体柱、碲化锑p型半导体柱、底层au连接电极和热电堆的两个au引线端;在所述碲化铋n型半导体柱和所述碲化锑p型半导体柱的顶部覆盖有顶层au连接电极,所述碲化铋n型半导体柱和所述碲化锑p型半导体柱的底部设置有底层au连接电极,其中:一个所述碲化铋n型半导体柱与一个所述碲化锑p型半导体柱在一个底层au连接电极、顶层au连接电极连接下形成一对热电偶,所述顶层au连接电极上覆盖有ni顶层保护电极;多对所述热电偶首尾搭接形成立体热电堆薄膜,所述立体热电堆薄膜的两端连接热电堆的两个au引线端、;
8.所述立体热电堆薄膜上设有所述聚酰亚胺保护层,所述聚酰亚胺保护层覆盖所述立体热电堆薄膜且仅露出热电堆的两个au引线端;所述聚酰亚胺保护层上部设置有顶层pdms微流道,所述聚酰亚胺保护层的下部设置有底层pdms微流道,形成一个封闭型腔室。
9.优选地,当所述顶层pdms微流道由外部注入生物或化学液体,所述底层pdms微流道中注入室温纯水时,所述生物或化学液体产生热反应,所述顶层pdms微流道和所述底层pdms微流道之间形成温度差,使得所述立体热电堆薄膜上表面成为热节点,而所述立体热电堆薄膜下表面成为冷节点,根据塞贝克效应则有相应的电势输出,从而实现对测量样品热反应的瞬态测量。
10.优选地,所述热电堆的两个au引线端,可以选择以下金属材料中一种:金、铝、铜丝等导电金属丝。而其引线采用两种相同的金属细线,所述金属细线的材料为铂丝或者铜丝或者铝丝。
11.优选地,所述顶层pdms微流道、所述底层pdms微流道键合在所述立体热电堆薄膜的上下部。
12.本发明的第二方面,提供一种用于生化反应探测的立体微流控芯片量热计的制备方法,包括:
13.第一步、在基片上形成pdms薄层,加热使pdms薄层固化;
14.第二步、在形成所述pdms薄层的基片上制备聚酰亚胺薄膜作为柔性聚酰亚胺基底;
15.第三步、在柔性聚酰亚胺基底沉积au种子层;
16.第四步、沉积半导体柱,图形化,在au种子层上形成碲化铋n型半导体柱;随后用同样的方法,在au种子层上形成碲化锑p型半导体柱;
17.第五步、采用旋涂正胶并固化后,使光刻胶、n型半导体材料柱、p型半导体材料柱齐平;
18.第六步、沉积au,图形化,在光刻胶、n型半导体材料柱、p型半导体材料柱上形成顶层au连接电极;
19.第七步、沉积ni薄膜,图形化,在顶层au连接电极上形成ni顶层保护电极;
20.第八步、使用掩膜刻蚀,将au种子层图形化,形成底层au连接电极以及热电堆的两个au引线端;
21.第九步、在整个热电堆上方旋涂聚酰亚胺薄膜,并全固化形成聚酰亚胺保护层;
22.第十步、在玻璃片或者硅片上旋涂su8正胶,使用热板固化su8薄层,图形化,形成微流道模具;
23.第十一步、在微流道模具上溅射铬铜薄膜,用以完整快速脱模;
24.第十二步、在模具上倒入配置的pdms溶液,常温真空静置去除气泡,随后固化,取下两个微流道,并在两个微流道上开孔作为腔室出入口,分别作为顶层pdms微流道、底层pdms微流道;
25.第十三步、将柔性聚酰亚胺基底从pdms薄层上剥离下来;
26.第十四步、将顶层pdms微流道、底层pdms微流道分别粘取pdms液体后,对准柔性聚酰亚胺基底上的热电偶节点进行键合,最终形成立体结构微流控芯片量热计。
27.优选地,所述第四步、第六步、第七步、第八步和第十步中,所述图形化,是利用掩膜电化学沉积方法、掩膜刻蚀或lift
‑
off工艺实现的。
28.优选地,所述酰亚胺保护层采用悬涂聚酰亚胺旋涂、固化形成。
29.优选地,所述底层au连接电极、顶层au连接电极、ni顶层保护电极均由磁控溅射的方式沉积而成。
30.优选地,所述顶层pdms微流道、底层pdms微流道均由pdms通过软刻蚀技术制成,并键合在热电堆的上下部。
31.优选地,所述对准柔性聚酰亚胺基底上的热电偶节点进行键合后,再放入烘箱,75度加热60分钟提高键合强度。
32.与现有技术相比较,本发明实施例至少具有以下一种有益效果:
33.本发明上述的微流控芯片量热计,能实现对测量的生物液体代谢反应、化学反应产生的热量进行瞬态测量,具有灵敏度高,柔性,应用范围广,结构简单,操作简单、样品体积小,对被测场的影响小,响应速度快,制备成本低的特点。
34.本发明上述的微流控芯片量热计,采用室温下,塞贝克系数差很大的碲化铋和碲化锑作为热电堆的两种材料,灵敏度非常高。
35.本发明上述的微流控芯片量热计中,封闭式pdms微流道腔室有效降低了样品的蒸发情况,且其良好的生物兼容性,可以保证在测试样品时,生物化学样品的稳定性,大大的增加了测量的准确度。
36.本发明上述的微流控芯片量热计,采用多对立体热电偶串联形成立体热电堆,这使得单位面积上热电偶数量大大增加,从而极大提高量热计的灵敏度,不需再进行信号放大处理。
37.本发明上述的微流控芯片量热计,通过5ms
‑
100ms的短时间直接测出热端与冷端温度变化产生的电压变化,来得到样品液体的热量变化,而不需要像传统的生物芯片量热计测出两点温度后,再求反应前后热量的变化。
38.本发明上述的微流控芯片量热计,采用柔性聚酰亚胺作为量热计的基底及保护层,延展性好,热导率低,绝热性能好,应用范围更广,制造成本更低。
附图说明
39.通过阅读参照以下附图对非限制性实施例所作的详细描述,本发明的其它特征、
目的和优点将会变得更明显:
40.图1是本发明一实施例的微流控芯片量热计的剖面示意图;
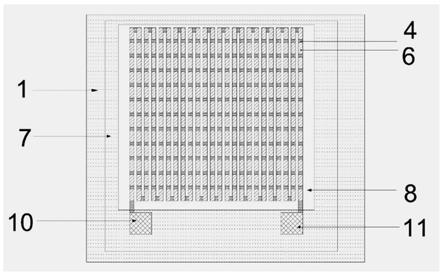
41.图2是本发明一实施例的微流控芯片量热计整体结构正面俯视示意图;
42.图3是本发明一实施例的微流控芯片量热计整体结构反面俯视示意图;
43.图中:1为柔性聚酰亚胺基底、2为碲化铋n型半导体柱、3为碲化锑p型半导体柱、4为底层au连接电极、5为顶层au连接电极、6为ni顶层保护电极、7为聚酰亚胺保护层、8为顶层pdms微流道、9为底层pdms微流道、10和11为热电堆的两个au引线端。
具体实施方式
44.下面结合具体实施例对本发明进行详细说明。以下实施例将有助于本领域的技术人员进一步理解本发明,但不以任何形式限制本发明。应当指出的是,对本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进。这些都属于本发明的保护范围。
45.图1是本发明一实施例的本发明上述的微流控芯片量热计的剖面示意图。
46.如图1所示,该实施例中的微流控芯片量热计,包括:柔性聚酰亚胺基底1、碲化铋n型半导体柱2、碲化锑p型半导体柱3、底层au连接电极4、顶层au连接电极5、ni顶层保护电极6、聚酰亚胺保护层7、顶层pdms微流道8、底层pdms微流道9。柔性聚酰亚胺基底1上设有碲化铋n型半导体柱2、碲化锑p型半导体柱3、底层au连接电极4,顶层au连接电极5覆盖在碲化铋n型半导体柱2与碲化锑p型半导体柱顶部;碲化铋n型半导体柱2和碲化锑p型半导体柱3的底部设置有底层au连接电极4,顶层au连接电极5上覆盖有ni顶层保护电极6;其中:一个碲化铋n型半导体柱2与一个碲化锑p型半导体柱3在一个底层au连接电极4、顶层au连接电极5连接下形成一对热电偶,多对热电偶首尾搭接形成立体热电堆薄膜。
47.参照图2所示,立体热电堆薄膜的两端连接热电堆的两个au引线端10、11;聚酰亚胺保护层7覆盖在热电堆薄膜上仅露出热电堆的两个au引线端10、11;顶层pdms微流道8制作在酰亚胺保护层5上部;底层pdms微流道9制作在柔性聚酰亚胺基底1下部。
48.上述实施例中的微流控芯片量热计,当从外部注入生物或化学液体在顶层pdms微流道8,并在底层pdms微流道9中注入室温纯水时,由于生物化学液体产生的热反应,两个微流道之间会形成温度差,使得立体热电堆薄膜上表面成为热节点,而立体热电堆薄膜下表面成为冷节点,根据塞贝克效应,就有相应的电势输出,多对热电偶首尾搭接形成薄膜热电堆,具有极高灵敏度,从而实现对测量样品热反应的瞬态测量。
49.本发明上述实施例在分析总结国内外众多用于生物化学反应探测的微流控芯片量热计的基础上,研究利用薄膜技术,制作出了基于立体热电堆的高灵敏度封闭腔室的生物化学微流控芯片量热计,这种芯片量热计,既继承了热电堆式芯片量热计简单的测量原理和方法,同时又将平面结构改造成了立体结构,极大提高了单位面积内热电偶数量,并使用了成本低而且在室温条件下塞贝克系数差非常大的碲化铋和碲化锑两种材料制备出超高灵敏度立体热电堆,解决了传统平面单质金属热电堆芯片量热计灵敏度低和成本高的问题。
50.本发明上述pdms制成的封闭型腔室结构,首先其良好的生物兼容性保证了实验时样品的稳定性,其次封闭结构也避免了实验样品在测量过程的挥发,保证了测试的准确性。
51.如图2所示,碲化铋n型半导体柱2与碲化锑p型半导体柱3使用底层au电极4和顶层au电极5对接形成热电偶。多对热电偶首尾相连形成立体热电堆,可放大热流传感器的输出信号,两个au热电堆的引线端10、11从热电堆的首尾引出。
52.在部分实施例中,使用了室温条件下,即温度在15
‑
40℃的区间内,塞贝克系数差可达501uv/k的超高灵敏度bi2te3
‑
sb2te3热电偶,除bi2te3
‑
sb2te3热电偶,根据使用的温度和环境要求的不同还可以采用铁
‑
康铜热电偶、铜
‑
康铜热电偶、铁
‑
铜镍热电偶、镍铬
‑
镍铝热电偶、铜
‑
铜镍热电偶、钯
‑
锑热电偶、铬
‑
铋热电偶、铬
‑
金热电偶等任一种的热电偶。另外,立体热电堆薄膜的两个au热电堆的引线端10、11的引线采用两种相同的金属细线,材料为金丝、铂丝、铜丝或者铝丝中的任一种。
53.在上述实施例基础上,作为优选,底层au电极4、顶层au电极5和顶层ni保护电极6采用磁控溅射方法沉积薄膜、利用掩膜溅射方法或liftoff方法实现图形化。在另实施例中,碲化铋n型半导体柱2和碲化锑p型半导体材料3采用电化学沉积方法沉积制成、利用掩膜方法或liftoff方法实现图形化。
54.在上述实施例基础上,作为优选,聚酰亚胺保护层7厚度可以根据需求制成1.5
‑
7μm,采用悬涂固化聚酰亚胺形成,再用刻蚀的方法使两个au热电堆的引线端10、11释放出来,不被热阻层覆盖。
55.在上述实施例基础上,作为优选,顶层pdms微流道8、底层pdms微流道9均由pdms在su8制成的模具中制成。pdms成本低,加工工艺简单,有良好的生物相容性,将会很好的防止样品液体的蒸发以实现精确测量。
56.上述实施例中的优选特征可以任一或任意多个组合使用,只要互不冲突即可,在此不再赘述。
57.在本发明另一实施例中,还提供一种上述微流控芯片量热计的制备方法,具体可以包括如下执行步骤:
58.第一步、在基片上形成pdms薄层,加热使pdms薄层固化;
59.第二步、在形成所述pdms薄层的基片上制备聚酰亚胺薄膜作为柔性聚酰亚胺基底1;
60.第三步、在柔性聚酰亚胺基底1沉积au种子层;
61.第四步、沉积半导体柱,图形化,在au种子层上形成碲化铋n型半导体柱2;随后用同样的方法,在au种子层上形成碲化锑p型半导体柱3;
62.第五步、采用旋涂正胶并固化后,使光刻胶、n型半导体材料柱2、p型半导体材料柱3齐平;
63.第六步、沉积au,图形化,在光刻胶、n型半导体材料柱2、p型半导体材料柱3上形成顶层au连接电极5;
64.第七步、沉积ni薄膜,图形化,在顶层au连接电极5上形成ni顶层保护电极6;
65.第八步、使用掩膜刻蚀,将au种子层图形化,形成底层au连接电极4以及热电堆的两个au引线端10、11;
66.第九步、在整个热电堆上方旋涂聚酰亚胺薄膜,并全固化形成聚酰亚胺保护层7;
67.第十步、在玻璃片或者硅片上旋涂su8正胶,使用热板固化su8薄层,图形化,形成微流道模具;
68.第十一步、在微流道模具上溅射铬铜薄膜,以便脱模;
69.第十二步、在模具上倒入配置的pdms溶液,常温真空静置去除气泡,随后固化,取下两个微流道,并在两个微流道上打孔作为腔室出入口,分别作为顶层pdms微流道8、底层pdms微流道9;
70.第十三步、将柔性聚酰亚胺基底从pdms薄层上剥离释放下来;
71.第十四步、将顶层pdms微流道8、底层pdms微流道9分别粘取pdms液体后,对准柔性聚酰亚胺基底1上的热电偶节点进行键合,最终形成立体结构微流控芯片量热计。
72.上述实施例能实现图1所示微流控芯片量热计的制备,另外,作为部分优选的实施例,上述的第四步、第六步、第七步、第八步和第十步中,可以利用掩膜电化学沉积方法、掩膜刻蚀或lift
‑
off工艺实现图形化。另外,上述制备方法中酰亚胺保护层7优选采用悬涂聚酰亚胺旋涂、固化形成。底层au连接电极4、顶层au连接电极5、ni顶层保护电极6均可以优选由磁控溅射的方式沉积而成。在其他实施例中,顶层pdms微流道8、底层pdms微流道9均可以优选由pdms通过软刻蚀技术制成,并键合在热电堆的上下部。
73.在本发明另一优选的具体实施例中,上述微流控芯片量热计的制备方法具体可以包括如下执行步骤:
74.第一步、采用旋涂的方法在玻璃片或者硅片上旋涂pdms薄层,使用热板或者烘箱加热使pdms薄层固化;
75.第二步、采用旋涂的方法或者直接贴pi薄膜的方法在旋涂了pdms薄层的基片上制备聚酰亚胺薄膜作为柔性聚酰亚胺基底1;
76.第三步、采用磁控溅射方法在柔性聚酰亚胺基底1沉积au种子层;
77.第四步、采用电化学沉积方法沉积半导体柱、利用掩膜电化学沉积方法实现图形化,在au种子层上形成碲化铋n型半导体柱2。随后用同样的方法,在au种子层上形成碲化锑p型半导体柱3。
78.第五步、采用旋涂正胶并固化后,使用机械抛光,使得光刻胶、n型半导体材料柱2、p型半导体材料柱3齐平。
79.第六步、采用磁控溅射方法沉积au、利用掩膜溅射方法实现图形化,在光刻胶、n型半导体材料柱2、p型半导体材料柱3上形成顶层au连接电极5。
80.第七步、采用磁控溅射方法沉积ni薄膜、利用掩膜溅射方法实现图形化,在顶层au连接电极5上形成ni顶层保护电极6。
81.第八步、使用掩膜刻蚀,将au种子层图形化,形成底层au连接电极4以及热电堆的两个au引线端10、11。
82.第九步、采用旋涂的方法在整个热电堆上方旋涂1
‑
5微米的聚酰亚胺薄膜,并全固化形成聚酰亚胺保护层7。
83.第十步、采用旋涂的方法在玻璃片或者硅片上旋涂su8正胶,使用热板固化su8薄层,并利用掩膜刻蚀方法实现图形化,形成微流道模具。
84.第十一步、采用磁控溅射方法微流道模具上溅射铬铜薄膜,以便脱模。
85.第十二步、在su8模具上倒入配置的pdms溶液,常温真空静置去除气泡。随后固化,取下两个微流道,并在两个微流道上打孔作为腔室出入口,分别作为顶层pdms微流道8、底层pdms微流道9。
86.第十三步、采用机械剥离的方法将柔性聚酰亚胺基底从pdms薄层上剥离释放下来。
87.第十四步、将顶层pdms微流道8、底层pdms微流道9分别粘取pdms液体后,对准柔性聚酰亚胺基底1上的热电偶节点进行键合。放入烘箱,75度加热60分钟提高键合强度。最终形成立体结构微流控芯片量热计。
88.本发明上述实施例制备得到的微流控芯片量热计,采用立体结构热电偶结构,极大提高了单位面积下热电偶数量,并使用了制备成本低而且塞贝克系数差非常高的碲化铋和碲化锑两种材料,制备出超高灵敏度立体热电堆,解决了传统平面单质金属热电堆芯片量热计灵敏度低和成本高的问题。
89.本发明上述实施例制备得到的微流控芯片量热计,是一种基于立体热电堆的封闭式腔室的高灵敏度生化化学微流控芯片量热计,可用于测量化学试剂反应、细胞代谢活动检测、生物分子间相互作用等功能。
90.以上对本发明的具体实施例进行了描述。需要理解的是,本发明并不局限于上述特定实施方式,本领域技术人员可以在权利要求的范围内做出各种变形或修改,这并不影响本发明的实质内容。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1