一种草甘膦的检测方法与流程
本发明涉及分析化学
技术领域:
,具体涉及一种草甘膦的检测方法。
背景技术:
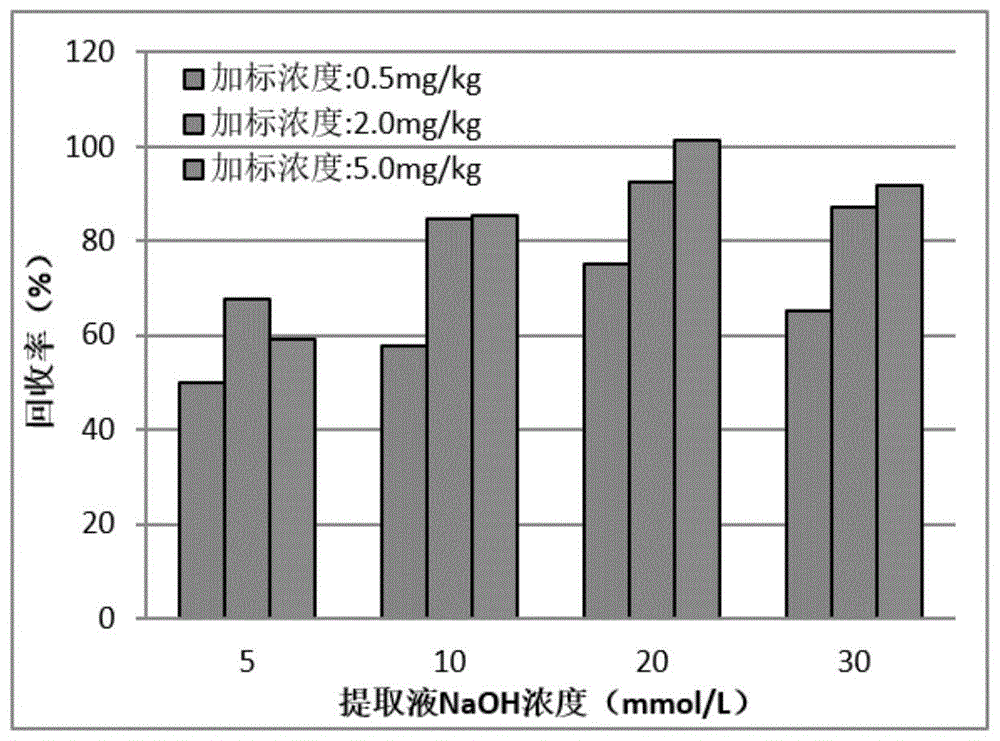
:草甘膦(glyphosate,gly)化学名称n-磷酰基甲基甘氨酸,是由美国孟山都公司开发的除草剂,又称镇草宁、农达(roundup)、草干膦、膦甘酸。草甘膦是一种内吸传导型非选择性广谱除草剂,主要抑制植物体内的烯醇丙酮基莽草素磷酸合成酶,从而抑制莽草素向苯丙氨酸、酪氨酸及色氨酸的转化,使蛋白质合成受到干扰,导致植物死亡,由于优异的除草性能及低廉的价格,广泛应用于农田各种杂草的防除,也常用于非农田杂草的治理。随着抗草甘膦作物的培育成功,草甘膦的用量逐年递增,目前已成为世界上应用最广、用量最大的除草剂之一。由于草甘膦的使用量越来越大,使用范围越来越广,其在土壤环境中行为越发受到关注。研究表明,残留的草甘膦已经对土壤化学过程和生态系统造成影响,而且给环境带来安全风险。随着草甘膦毒理学及生态效应研究的深入,逐渐有文献报道草甘膦具有广泛的生殖毒性、诱突变性等一些环境激素效应,对生态环境和人体健康的潜在危害极大。目前检测多菌草甘膦农药残留的传统方法主要有气相色谱法、高效液相色谱法,液质联用仪法、毛细管电泳等,虽然上述方法的灵敏度高、选择性好、结果精确可靠,但样品处理操作较为繁琐,并且对实验设备和实验操作人员的专业性要求也较高,检测耗时,不适合大规模样品的检测,并且需要大型且昂贵的设备,检测成本高等。因此,开发一种简单、快速、灵敏、可靠的方法实现对草甘膦的检测尤为重要。技术实现要素:草甘膦为强极性两性化合物、易溶于水、难溶于大多数有机溶剂、挥发性差、没有发色和荧光基团。在使用气相色谱法和高效液相色谱法测定前,必须进行衍生化处理,样品前处理过程比较复杂,不适合大量样品检测,准确度的干扰因素也较多。光度法存在的缺陷,而离子色谱法不需要衍生化,可以大体积进样分析,操作简便,对人体健康和环境没有危害。土壤中草甘膦测定的研究时有报道,但由于操作繁琐,通用性低,或者对仪器要求较高等因素都没有得到普遍推广。液相和气相色谱法均需要衍生化,气质或者液质联机对仪器要求较高,检测成本高。本发明的主要目的是对土壤中草甘膦的前处理方法进行优化,通过对草甘膦测定方法的研究,建立一种草甘膦的离子色谱分析方法,适用于实际土壤样品的分析,以及对实际土壤样品分析。一种草甘膦的检测方法,包括如下步骤:1)土壤样品制备与提取将采集的土壤样品,风干后过60-100目筛,混匀,密封保存。称取土壤样品于离心管中,加入碱性提取液,充分震荡,室温下超声提取20-40min,以4000-8000r/min离心6-10min,上清液经0.45μm滤膜过滤,待净化;2)提取液的净化采用onguardⅱag/h柱和ng1柱联合使用在线去除无机卤化物、高浓度金属离子和有机类物质,把ng1柱连接到离子色谱柱前端,即可以在线去除有机类物质;3)本发明采用了ionpacas19分析柱koh淋洗体系对土壤中草甘膦含量进行测定,通过实验对梯度洗脱和等度洗脱两种洗脱模式进行了比较。梯度洗脱程序为:0-15.0min,koh浓度由10mmol/l线性上升至30mmol/l;15.1-25.0min,koh浓度为30mmol/l;25.1-30.0min,koh浓度为10mmol/l。所述碱性提取液选自碱金属的氢氧化物,具体选自氢氧化钾、氢氧化钠,其浓度可以为10mmol/l到30mmol/l。附图说明图1不同浓度提取液的提取回收率(n=3)图210mmol/l到35mmol/l梯度洗脱混合标准溶液色谱图,从左向右8个色谱峰及保留时间分别为:1-f--4.920,2-cl--6.908,3-no2--8.047,4-br--9.153,5-no3--9.977,6-so42--12.207,7-po43--18.143,8-草甘膦-21.373图3三种浓度koh等度洗脱混合标准溶液色谱图比较图435mmol/lkoh等度洗脱混合标准溶液色谱图,从左向右7个色谱峰及保留时间分别为:1-f--3.650,2-cl--4.390,3-no2-+br--4.940,4-no3--5.447,5-so42--5.857,6-po43--6.847,7-草甘膦-8.250图5草甘膦工作曲线拟合图具体实施方式实施例1土壤中草甘膦检测方法的建立由于草甘膦的极性和水溶性,不利于使用有机溶剂对其进行提取,本发明拟采用水系溶剂对土壤中草甘膦进行提取,然后采用离子色谱法检测分析,不需要衍生化,方法前处理简便,无污染。仪器设备ics-5000+离子色谱仪(thermofisher),配有chromeleon7.10色谱工作站,as-ap自动进样器,koh淋洗液自动发生器,aers-500抑制器,ed50电导检测器,ionpacas19色谱分析柱,ag19保护柱。ag104电子天平,12通道固相萃取装置,离心机。试剂和材料氟离子(f-)、氯离子(cl-)、溴离子(br-)、亚硝酸盐氮(no2--n)、硝酸盐氮(no3--n)、硫酸盐(so42-)、标准物质购自国家标准物质中心;草甘膦(gly)标准品由农业部环境保护科研监测所研制accustandard,氢氧化钠(分析纯,国药)。on-guardⅱrp柱(thermofisher),0.45μm滤膜,50ml离心管,钕磁铁(ndfeb),实验用水为二次去离子水(milli-q纯水系统,电阻率18.2mω·cm)。实验方法土壤样品制备与提取将采集的土壤样品,风干后过60目筛,混匀,密封保存。称取1.0g土壤样品于50ml离心管中,加入10ml20mmol/lnaoh提取液,充分震荡,室温下超声提取30min,以6000r/min离心8min,上清液经0.45μm滤膜过滤,待净化。净化固相萃取柱净化①固相萃取柱活化:onguardⅱrp柱先用5ml甲醇溶液以4ml/min的流速通过,再用10ml去离子水以4ml/min的流速通过,将小柱平放20min,备用。onguardⅱag/h柱先用15ml去离子水以2ml/min的流速通过,将小柱平放20min,备用。②萃取液净化:取过滤后的萃取液以4ml/min的速度通过onguardⅱrp或onguardⅱag/h固相萃取柱,弃去前面3ml流出液后,收集滤液2ml,供离子色谱分析。onguardⅱag/h固相萃取柱和ng1柱组合净化取过滤后的萃取液以4ml/min的速度通过onguardⅱag/h固相萃取柱,弃去前面3ml流出液后,收集滤液2ml,进入离子色谱分析,离子色谱分析时使用ng1柱在线去除有机质。标准溶液的配制将草甘膦标准物质配制成浓度为10.0mg/l的标准使用液,然后分别取适量标准使用液,配制成浓度分别为0.02mg/l、0.05mg/l、0.1mg/l、0.2mg/l、0.5mg/l、1.0mg/l、2.0mg/l的草甘膦标准溶液系列。色谱条件色谱柱:ionpacas19分析柱,ag19保护柱;35mmol/lkoh等度洗脱;淋洗液流速:1.0ml/min;进样体积:100μl;柱温:30℃;抑制器电流:87ma;电导检测。结果与讨论土壤提取条件的选择草甘膦能以氢键和离子交换的形式吸附于土壤中的矿物质及有机质上。根据其理化性质分析,草甘膦是一种三元酸,其解离常数分别为pka1=2.27,pka2=5.58,pka3=10.25;在酸性条件下草甘膦大多以分子态形式存在,而在碱性条件下,大多以可溶态的阴离子形态存在(参见dukeso,lydonj,koskinenwc,etal.glyphosateeffectsonplantmineralnutrition,croprhizospheremicrobiota,andplantdiseaseinglyphosate-resistantcrops[j].j.agric.foodchem.2012,60(42):10375-10397)。考虑到土壤带负电荷的特性,所以采用水系溶液进行提取,通过借鉴国内外土壤检测的提取方法,首先比较了纯水和碱性溶液(30mmol/lnaoh)的提取效果,通过向土壤中加入相同量的草甘膦标准溶液,测定其回收率的方法,来表征不同提取溶剂的提取效率。实验结果表明,碱性溶液30mmol/lnaoh提取的回收率要明显高于纯水的回收率,因此采用碱性溶液进行提取,并且离子色谱检测阴离子时常用koh溶液和naoh溶液作为流动相。之后比较了不同浓度naoh溶液(5mmol/l、10mmol/l、20mmol/l和30mmol/l)的提取效率,每种提取液进行0.5mg/kg、2.0mg/kg、5.0mg/kg三个水平的土壤加标实验,通过离子色谱测定,得到12个加标回收率数值,加标回收率情况见图1,由此图可以看出,当20mmol/lnaoh溶液作为提取溶剂时,草甘膦的回收率高于其他3种提取溶剂,提取效果较好,因此确定提取溶剂为20mmol/lnaoh溶液。提取液的净化采用碱性水溶液作为提取剂,容易将土壤样品中的腐植酸、脂肪酸等极性化合物提取出来,若直接进样分析,离子型物质会对草甘膦的测定造成干扰;虽然有机物质不表现在离子色谱图谱中,但随着对提取样品分析次数的不断叠加,有机物累积在离子色谱柱越来越多,会严重损坏色谱柱,降低分离效率,对草甘膦检测产生较大干扰,因此要进行净化处理,降低对测定过程的干扰和对仪器设备的损害。(1)方法一:首先采用onguardⅱrp柱去除有机物,采用onguardⅱag/h柱去除无机卤化物以及高浓度金属离子的干扰,可以达到很好的去除效果,回收率得到提高,但是萃取液两次过柱,操作相对繁琐,不利于大量样品的测定。(2)方法二:使用ng1柱在线去除有机类物质,通过实验发现,把ng1柱连接到离子色谱柱前端,即可以在线去除有机类物质,达到onguardⅱrp柱同样的效果。所以本发明首先采用onguardⅱag/h柱去除提取物中无机卤化物以及高浓度金属离子的干扰,然后使用ng1柱在线去除有机类物质,简化了前处理步骤,提高工作效率。(3)两种净化方法净化效果比较表1两种方法比较色谱条件的优化本发明采用了ionpacas19分析柱,koh淋洗体系对土壤中草甘膦含量进行测定,通过实验对梯度洗脱和等度洗脱两种洗脱模式进行了比较。梯度洗脱程序为:0-15.0min,koh浓度由10mmol/l线性上升至30mmol/l;15.1-25.0min,koh浓度为30mmol/l;25.1-30.0min,koh浓度为10mmol/l。表2梯度洗脱程序时间(min)流速(ml/min)koh浓度(mmol/l)0.01.01015.01.03025.01.03025.11.01030.01.010在此梯度洗脱条件下,常规阴离子和草甘膦均可以达到很好的分离效果,草甘膦21.37min出峰,但分析时间较长(如图2)。等度洗脱不能将几种常规阴离子得到有效分离,但可与草甘膦分离,不影响草甘膦的测定,方法比较了30mmol/l、40mmol/l和35mmol/lkoh3种淋洗液浓度条件下的分离效果,如图3所示。在30mmol/lkoh等度洗脱时,草甘膦出峰时间为11.35min,时间较长;40mmol/lkoh等度洗脱时,草甘膦出峰时间为6.54min,与前面阴离子较近,容易受到其他阴离子干扰;而35mmol/lkoh等度洗脱时,草甘膦出峰时间为8.25min,峰形较好,与其他峰之间干扰较少且检测时间较短。综合考虑出峰时间和分离效果,35mmol/lkoh等度洗脱可以在相对较短的时间内对草甘膦进行定量分析,达到本研究采用离子色谱法测定草甘膦的目的,因此选择35mmol/lkoh等度洗脱(图4)。标准曲线与检出限按照色谱条件,将配制的草甘膦标准溶液系列分别进样分析,保留时间定性,峰面积定量,以草甘膦的浓度为横坐标,峰面积为纵坐标绘制标准曲线。工作曲线拟合图见图5称取1.0g土壤样品,加标浓度为0.5mg/kg,进行样品前处理及测定,按照公式mdl=t(n-1,0.99)×s计算检出限,s为7次测定的标准偏差,此时t(n-1,0.99)=3.143,7次平行实验的相对标准偏差为2.74%。工作曲线、相关系数和检出限结果见表3。表3工作曲线、相关系数和检出限精密度与回收率采用对某一实际土壤样品进行低、中、高3个浓度加标的方法进行精密度和回收率实验,加标浓度分别为0.5mg/kg、2.0mg/kg、5.0mg/kg,在给定的提取、净化方法和色谱条件下,每个加标浓度进行6次平行实验,计算加标回收率和6次实验的相对标准偏差rsd,实验结果见表4。结果表明,本方法回收率在73.2%~93.6%,准确度可靠,rsd在2.24%~6.49%,精密度良好。表4精密度和加标回收实验结果(n=6)结论本发明建立了一种测定土壤中草甘膦的离子色谱分析方法。与国家标准方法《土壤和沉积物草甘膦的测定高效液相色谱法》(hj1055-2019)相比,该方法更加简便,不需要进行衍生化,而且不使用有机溶剂,不对人员和环境产生危害,更加环保。该方法采用20mmnaoh提取土壤中草甘膦,固相萃取小柱净化,抑制型电导检测器检测。草甘膦在0.02~2.00mg/l范围内线型关系良好,相关系数r为0.9990,检出限为0.086mg/kg。在低、中、高三种加标水平下,草甘膦的平均回收率分别为81.5%、86.3%和88.3%,重复测定相对标准偏差(rsd%)分别为6.49%、5.0%和2.24%。该方法操作简单,线性良好,可以准确的测定土壤中草甘膦的含量。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1