孕妇外泌体LTF蛋白在制备胎儿先心病检测产品中的应用、试剂盒及检测方法与流程
孕妇外泌体ltf蛋白在制备胎儿先心病检测产品中的应用、试剂盒及检测方法
技术领域
1.本发明涉及生物医药技术领域,具体地,涉及孕妇外泌体ltf蛋白在制备胎儿先心病检测产品中的应用、试剂盒及检测方法。
背景技术:
2.先天性心脏病(congenital heart disease,chd)是最常见的先天性畸形,在所有的出生缺陷中,先心病一直处于我国出生缺陷的首位,据文献报道先心病在新生婴儿中的发病率8/1000,一直以来都是婴幼儿发病率和死亡率最重要的病因。而在产前chd发生率其实更高,在所有的先天畸形中,超过40%的产前胎儿死亡是由于先心病。然而超声确诊胎儿先心病时往往已经处于孕中晚期,给孕妇及其家属带来极大的身心伤害。
3.外泌体被认为是细胞之间的通讯工具,它的内容物(蛋白,rna等)已作为潜在生物标志物广泛用于疾病研究。外泌体存在于血清、血浆、尿液等几乎所有的体液中。越来越多研究表明外泌体蛋白是十分有潜力的诊断标志物或预后生存指标。
4.ltf作为一线免疫介质和抗细胞凋亡的重要分子,在维持孕期子宫内稳态中起到重要的作用。ltf可以和多种小分子或生物大分子结合,如dna、脂多糖、肝素、氨基葡聚糖以及两性电解质等。ltf能够与特定dna序列高效特异性结合,做为转录因子参与基因的转录调控,正向调节某些细胞因子(如白介素
‑
1)和生长因子(如转化生长因子tgf
‑
β)的表达。
5.蛋白质组的定义是指一个基因组、一个或多个细胞或某些组织所表达的所有蛋白质,无论是小到一个细胞还是大到一个生物体,都是从一个整体水平去研究参与生命活动的所有蛋白质。这些所有蛋白质并不是一个一成不变的集合,而是随时随地变化着的,因为随着生命活动的进行和稳态的调节总有不同的蛋白质在被表达或修饰。蛋白质是生命活动的承担者,也是大多数生物体结构的组成部分,蛋白质的形成要经过一系列的转录后修饰,因此,从基因组和转录组并不能直接推导出蛋白质组的情况。
6.目前先天性心脏病领域用孕妇血清外泌体为标本进行外泌体蛋白质组学的研究很少见,随着外泌体提取技术及tmt蛋白质谱技术等高通量蛋白组技术的出现和发展,使用外泌体蛋白或者外泌体mirna做为某种疾病的生物标志物的研究趋势越来越多。越来越多的证据表明胎儿先天性心脏病的发生和发展与母亲因素相关,与此同时,很多学者也试图寻找母体因素做为胎儿先心病的标志物未果。
技术实现要素:
7.针对现有技术中的缺陷,本发明的目的是提供孕妇外泌体ltf蛋白在制备胎儿先心病检测产品中的应用、试剂盒及检测方法。
8.本发明的目的是通过以下方案实现的:
9.本发明的第一方面提供一种孕妇血清外泌体蛋白在制备胎儿先心病检测产品中的应用,所述外泌体蛋白为ltf蛋白。
10.优选地,所述检测产品包括芯片或试剂盒。
11.优选地,所述ltf蛋白在孕妇血清中表达下调,检测的cut
‑
off值小于97ng/ml,可预测患有先心病。
12.优选地,所述试剂盒包括elisa检测试剂盒、胶体金检测试剂盒、免疫共沉淀试剂盒、化学发光试剂盒、免疫荧光试剂盒。
13.本发明的第二方面提供一种试剂盒,包括:包被ltf单克隆抗体的固相载体,酶标抗体,酶的底物,蛋白标准品(试剂盒里已有的已经确定含量的ltf蛋白),阴性对照品(蛋白含量为0的标准品),稀释液,酶反应终止液。
14.优选地,所述酶标抗体是试剂盒中的生物素化的乳铁蛋白抗体,酶的底物是试剂盒中的显色底物。
15.本发明的第三方面提供一种基于上述胎儿先心病检测试剂盒检测孕妇血清外泌体ltf蛋白浓度的方法,其特征在于,包括以下步骤:
16.(1)加样:分别取50μl待测血清样本和50μl梯度稀释的标准品加入酶标板孔中,贴上封膜,水平摇床轻轻摇动,室温孵育2hr;
17.(2)洗板:弃去板中液体,每孔加入200μl 1
×
wash buffer清洗5min
×
5次,彻底甩干洗涤液;
18.(3)加入酶标抗体,洗板:加入50μl 1
×
biotinylatedlactoferrin antibody(生物素化的乳铁蛋白抗体),贴上封膜,水平摇床轻轻摇动,室温孵育1小时;洗板同步骤(2);
19.(4)加入streptavidin
‑
peroxidase conjugate(抗生蛋白链菌素
‑
过氧化物酶偶联物),洗板:每孔加入50μl 1
×
sp conjugate(抗生蛋白链菌素
‑
过氧化物酶偶联物),贴上封膜,水平摇床轻轻摇动,室温孵育30min;洗板同步骤(2);
20.(5)显色:每孔加入50μlchromogen substrate(显色底物,四甲基联苯胺显色底物),水平摇床轻轻摇动,室温避光孵育10min;
21.(6)终止:每孔加入50μl酶反应终止液,轻轻混匀;
22.(7)检测:用酶标仪在波长450nm处依序测量各酶标板孔的od值,然后进行计算,得到孕妇血清外泌体ltf蛋白浓度。
23.与现有技术相比,本发明具有如下的有益效果:
24.本发明提供了一种与胎儿先天性室间隔缺损相关的外泌体蛋白ltf,并进一步证实该外泌体ltf蛋白在胎儿室间隔缺损的母体血清外泌体中表达下调。利用该蛋白检测胎儿室间隔缺损不仅能够快速有效的做到早期检测,而且为基因治疗、药物治疗和预防等临床应用提供了治疗靶点和重要依据。
附图说明
25.通过阅读参照以下附图对非限制性实施例所作的详细描述,本发明的其它特征、目的和优点将会变得更明显:
26.图1本发明实施例4中的外泌体ltf表达量标准曲线。
27.图2本发明实施例4中的外泌体ltf检测胎儿先天性心脏病(室间隔缺损)的roc曲线。
具体实施方式
28.下面结合具体实施例对本发明进行详细说明。以下实施例将有助于本领域的技术人员进一步理解本发明,但不以任何形式限制本发明。应当指出的是,对本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变化和改进。这些都属于本发明的保护范围。
29.实施例中未注明具体条件的实验方法,通常为本领域常规方法。
30.本发明的发明人对6例胎儿为先天性室间隔缺损的母体血清外泌体样本及6例健康胎儿母体血清外泌体对照样本进行tmt标记定量蛋白质组学分析,结合生物信息学方法进行筛选,挑选出候选外泌体蛋白ltf,现有研究中并没有外泌体ltf蛋白和胎儿先天性室间隔缺损相关的报道,进一步,发明人进行了分子生物学方法验证,证实了外泌体ltf蛋白在室间隔缺损胎儿的母体血清中表达下调,其相关产品可用于预测、诊断、治疗胎儿室间隔缺损。例如,缺乏乳铁蛋白造成胎儿室间隔缺损,可以通过外泌体包被乳铁蛋白注射入孕母体内或者直接尝试母体通过喝牛奶的方式补充乳铁蛋白观察疗效后再定。
31.本发明还采用elisa检测试剂盒检测上述蛋白在胎儿室间隔缺损母体血清外泌体和健康胎儿母体血清外泌体中的表达,并验证了该外泌体蛋白为胎儿室间隔缺损母体血清外泌体中表达下调。
32.本发明应用tmt联合质谱的方法鉴定胎儿为室间隔缺损的母体血清外泌体中的蛋白标志物。tmt
tm
(tandem mass tag
tm
)技术是由美国thermo scientific公司研发的一种多肽体外标记技术。该技术采用10种同位素的标签,标记多肽的氨基基团,经过lc
‑
ms/ms分析,可同时比较10组不同样品中蛋白质的相对含量。tmt技术是常用的差异蛋白质组学技术,一级质谱中,任何一种tmt试剂标记的不同样品中的同一肽段表现出相同的质荷比;二级质谱中,可切割键(箭头所指)断裂释放出tmt报告离子,在质谱低质量区产生了10个tmt报告离子峰,其强度反应了该肽段在不同样品中的相对表达量信息,另外二级质谱中的肽段碎片离子峰质荷比反应了该肽段的序列信息;这些质谱原始数据经过数据库检索,可得到蛋白质的定性和相对定量信息。
33.tmt试剂由三部分组成:质量报告基团、质量标准化基团和氨基反应基团。
34.质量报告基团有10种不同的分子量,质量标准化基团也有10种不同的分子量,与不同的报告基团搭配,能保证被标记的不同来源的同一肽段在一级质谱中具有相同的质荷比;氨基反应基团能与肽段n端及赖氨酸侧链氨基发生共价连接使肽段连上标记。tmt具有以下技术服务优势:(1)灵敏度高:低丰度蛋白也能检测出;(2)适用范围广:几乎可对任何物种的各类蛋白质进行分离鉴定;(3)高通量:能同时对10组样本中包含的蛋白进行鉴定及表达差异分析;(4)高效:液相色谱与串联质谱连用,自动化操作,分析速度快,分离效果好。
35.本发明的外泌体ltf基因的核苷酸全长序列或其片段通常可以用pcr扩增法、重组法或人工合成的方法获得。对于pcr扩增法,可根据已公开的有关核苷酸序列,尤其是开放阅读框序列来设计引物,并用市售的cdna库或按本领域技术人员已知的常规方法所制备的cdna作为模板,扩增而得到有关序列。当序列较长时,常常需要进行两次或多次扩增,然后再将多次扩增的片段按正确次序拼接在一起。
36.一旦获得了有关的序列,就可以用重组法来大批量地获得有关序列。这通常是将其克隆入载体,再转入细胞,然后通过常规方法从增殖后的宿主细胞中分离得到有关序列。
此外,还可用人工合成的方法来合成有关序列,尤其是片段长度较短时。通常,通过先合成多个小片段,然后再进行连接可获得序列很长的片段。
37.目前,已经可以完全通过化学合成来编码本发明的蛋白(或其片段,或其衍生物)的dna序列。然后可将该dna序列引入本领域中的各种dna分子(如载体)和细胞中。此外,还可通过化学合成将突变引入本发明蛋白序列中。
38.本发明蛋白的片段除了可用重组法产生之外,还可用固相技术通过直接合成肽而加以生成(conesa c等人,(2010)recombinant human lactoferrin:a vatuable protein for phannaceufical products and functional foods.biotechnol adv.2010.28:831
‑
838.)。在体外合成蛋白质可以用手工或自动进行。例如,可以用applied biosystems的431a型肽合成仪(foster city,ca)来自动合成肽。可以分别化学合成本发明蛋白的各片段,然后用化学方法加以连接以产生全长的分子。
39.本文使用的术语“表达下调”指对应于所表达基因的序列,其中序列量的测量证明,与从健康胎儿母体或从胎儿为室间隔缺损母体的已经确定胎儿为室间隔缺损的母体血清外泌体中分离的生物学样品中的同蛋白相比,所述基因在从胎儿患室间隔缺损的孕母血清中分离的生物学样品中的表达水平降低。根据本发明,“表达下调”是指通过本发明方法杂交强度测量的至少1%、2%、3%、4%、5%、6%、7%、8%、9%、10%或更多的表达降低,例如20%、30%、40%、50%、60%、70%、80%、90%或更低。
40.本文使用的术语“表达水平”指通过本领域技术人员已知和本文所述的方法测定的给定核酸或蛋白质的可测量。涉及本发明生物标志物对应的rna、hnrna、mrna或mrna剪接变体时,表达水平可以通过杂交或更多定量测量来测定,例如包括使用sybr green、taqman和分子信标技术的定量实时rt
‑
pcr。
41.本文使用的“对照”指超声未显示任何畸形并且出生后健康的胎儿的母体或母体组。优先地,所述对照个体早孕期未接触不良、有毒有害物质,并且孕期没有任何合并症。更优选地,对照个体具有与测试样本相比相似的年龄、孕周。根据本发明,“对照”还指分离自健康胎儿母体个体的样品,包括分离自健康胎儿母体个体的总rna或mrna。
42.ltf蛋白是存在多种体液或分泌物中,以人乳汁特别是初乳中含量最高,近年来的研究表明,它具有抗肿瘤、抗细菌、抗病毒等多种生理功能。研究表明ltf蛋白可以作为宫内稳态的生物标记物,与胎儿发育的指标相关。
43.实施例1、样本的收集
44.病例
‑
对照研究是本研究所采用的方法。实验组的研究对象为2018年度在嘉兴学院附属妇儿医院经过产前超声心动图诊断的胎儿为室间隔缺损的孕妇16例,对照组的研究对象为经过产前超声排除了胎儿畸形的正常胎儿的孕妇16例,实验组符合《中国胎儿超声心动图检查规范(2015)》(中华超声影像学杂志,2015年11月第24卷第11期,p921
‑
926)标准。实验组的年龄为29.7
±
3.5岁,对照组的年龄为29.6
±
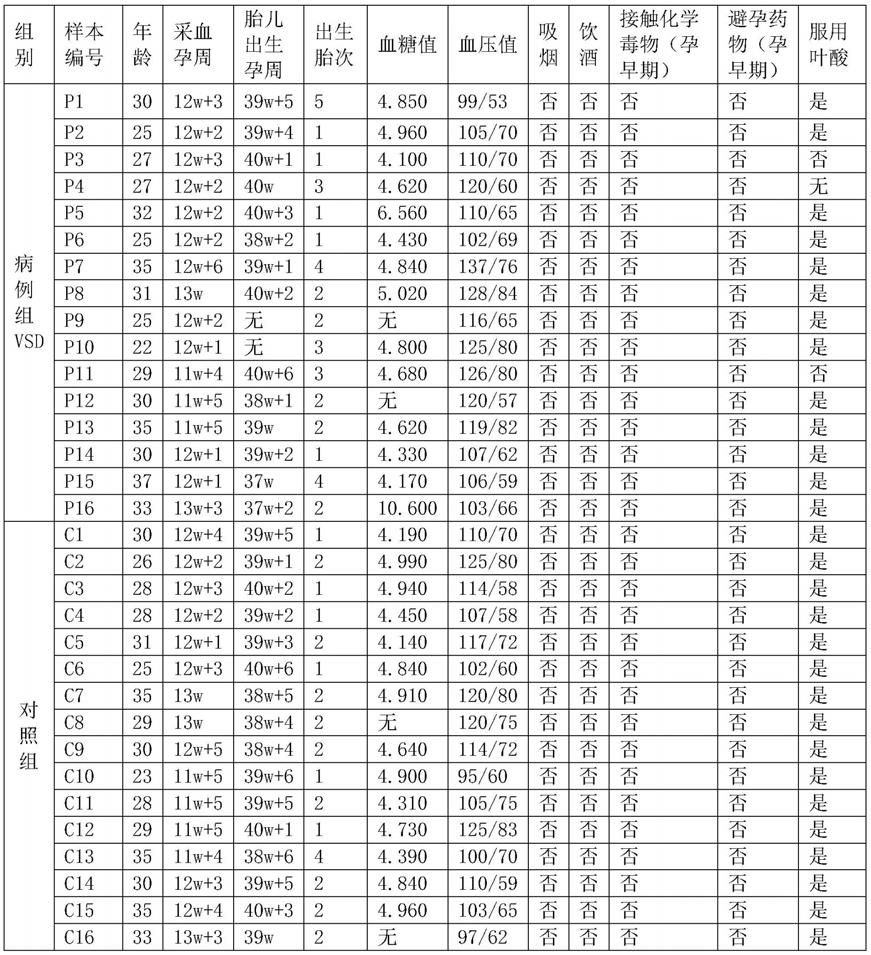
4.2岁。实验方案经嘉兴学院附属妇儿医院伦理委员会同意,并取得每位受试者的书面知情同意。实验组和对照组基本资料见表1。回顾性收集实验组和对照组的早孕期检测唐氏筛查剩余的血清,
‑
80℃保存备用。
45.表1、样本的基本资料
[0046][0047]
vsd病例组的纳入标准:
[0048]
①
在我院行胎儿超声心动图,确诊为单纯性先天性室间隔缺损的孕妇;
②
回顾性寻找并收集已确诊为胎儿先心病且进行了早中孕联合筛查的单胎妊娠的孕妇,孕期为11
‑
13+6周经唐氏筛查后剩余的血清;
③
在知情同意的基础上,愿意参与本课题研究的病例;
[0049]
vsd病例组的排除标准:
[0050]
①
患有妊娠合并症和并发症的孕妇;
②
胎儿确诊有染色体异常的孕妇;
③
胎儿确诊有多发畸形的孕妇。
[0051]
对照组的纳入标准:
[0052]
对照组选取的是在我院行胎儿超声心动图,胎儿心脏发育正常的孕妇,对照组的年龄、孕周与vsd病例组相匹配,并签署知情同意书。
[0053]
对照组的排除标准:
[0054]
①
患有妊娠合并症和并发症的孕妇;
②
胎儿确诊有染色体异常的孕妇;
③
胎儿确诊有任何其他畸形的孕妇。备注:对照组中如生后新生儿超声心动图显示存在chd则归为病
例组。
[0055]
实施例2、tmt实验筛选差异外泌体蛋白
[0056]
(一)样品制备所需材料和试剂
[0057]
tmt标记试剂盒(thermo)
[0058]
胰酶(trypsin,(1μg/μl,质谱级)(promega)
[0059]
乙腈(acetonitrile)(fisher chemical)
[0060]
三氟乙酸(trifluoroacetic acid)(sigma
‑
aldrich)
[0061]
甲酸(formic acid)(fluka)
[0062]
碘代乙酰胺(iodoacetamide,1m,用超纯水配制)(sigma)
[0063]
二硫苏糖醇(dithiothreitol,1m,用超纯水配制)(sigma)
[0064]
三乙基碳酸氢铵(teab)(sigma)
[0065]
超纯水(h2o)(fisher chemical)
[0066]
bca试剂盒(碧云天)。
[0067]
(二)tmt定量实验流程
[0068]
1、蛋白提取
[0069]
从实施例1中
‑
80℃保存备用的样品中取出300ul样品,4℃,12000g离心10分钟,去除细胞碎片,上清液转移至新的离心管,用thermo公司生产的试剂盒参照pierce
tm
top12abundant protein depletion spin columns kit说明书去除高丰度蛋白。利用bca试剂盒进行蛋白浓度测定。
[0070]
2、胰酶酶解
[0071]
蛋白溶液(蛋白总量达到800ug)中,用含8m尿素的pbs将浓度调至1mg/ml,然后加入二硫苏糖醇使其终浓度为5mm,56℃还原30min。之后加入碘代乙酰胺使其终浓度为11mm,室温避光孵育15min。最后将样品的尿素浓度稀释至低于2m(高浓度尿素对胰酶活性有影响,一般需要将尿素终浓度稀释到2m以下)。以1:50的质量比例(胰酶:蛋白)加入胰酶,37℃酶解过夜。再以1:100的质量比例(胰酶:蛋白)加入胰酶,继续酶解4h。
[0072]
3、tmt标记
[0073]
胰酶酶解的肽段用strata x c18(phenomenex,反相固相萃取柱)除盐后真空冷冻干燥。以0.5m teab溶解肽段,根据tmt试剂盒操作说明标记肽段。简单的操作如下:标记试剂解冻后用乙腈溶解,与肽段混合后室温孵育2h,标记后的肽段混合后除盐,真空冷冻干燥。
[0074]
4、hplc分级
[0075]
肽段用高ph反向hplc分级,色谱柱为agilent 300extend c18(5μm粒径,4.6mm内径,250mm长)。操作如下:肽段分级梯度为8%
‑
32%乙腈、ph 9,60min时间分离60个组分,随后肽段合并为18个组分,合并后的组分经真空冷冻干燥后进行后续操作。(先通过hplc分级降低每个组分样本的复杂度,最后将含不同亲疏水性肽段的60个组分合并成合适的组分数去进行质谱上机,如果不作合并,每个组分的肽段洗脱时间不均匀,实际上也会浪费质谱采集时间)。
[0076]
5、液相色谱
‑
质谱联用分析
[0077]
肽段用液相色谱流动相a相(0.1%(v/v)甲酸水溶液)溶解后使用easy
‑
nlc 1000
超高效液相系统进行分离。流动相a为含0.1%甲酸和2%乙腈的水溶液;流动相b为含0.1%甲酸和90%乙腈的水溶液。液相梯度设置:0~26min,9%
‑
25%b;26~34min,25%
‑
36%b;34~37min,36%
‑
80%b;37~40min,80%b(流动相b的比例,即这个时间点进入分析柱的流动相为20%a和80%b),流速维持在700纳升/min。
[0078]
肽段经由超高效液相系统分离后被注入nsi离子源中进行电离然后进q exactive
tm
质谱进行分析。离子源电压设置为2.2kv,肽段母离子及其二级碎片都使用高分辨的orbitrap进行检测和分析。一级质谱扫描范围设置为350
‑
1800m/z,扫描分辨率设置为70,000;二级质谱扫描范围则固定起点为100m/z,二级扫描分辨率设置为17,500。数据采集模式使用数据依赖型扫描(dda)程序,即在一级扫描后选择信号强度最高的前20肽段母离子依次进入hcd碰撞池使用28%的碎裂能量进行碎裂,同样依次进行二级质谱分析。为了提高质谱的有效利用率,自动增益控制(agc)设置为5e4,信号阈值设置为20000ions/s,最大注入时间设置为100ms,串联质谱扫描的动态排除时间设置为30秒避免母离子的重复扫描。
[0079]
6、数据库搜索
[0080]
二级质谱数据使用maxquant(v1.5.2.8)进行检索。检索参数设置:数据库为swissprot mouse(16839条序列),添加了反库以计算随机匹配造成的假阳性率(fdr),并且在数据库中加入了常见的污染库,用于消除鉴定结果中污染蛋白的影响;酶切方式设置为trypsin/p;漏切位点数设为2;肽段最小长度设置为7个氨基酸残基;肽段最大修饰数设为5;first search和main search的一级母离子质量误差容忍度分别设为20ppm和5ppm,二级碎片离子的质量误差容忍度为0.02da。将半胱氨酸烷基化设置为固定修饰,可变修饰为甲硫氨酸的氧化,蛋白n端的乙酰化。定量方法设置为tmt
‑
6plex,蛋白鉴定、psm鉴定的fdr都设置为1%。
[0081]
基于tmt技术,我们总共从实验组和对照组的血清外泌体中鉴定到了312种蛋白质,其中272个蛋白质包含定量信息,如果以1.2倍为变化阈值,t
‑
test p
‑
value<0.05为标准,那么在定量到的蛋白质中,6个蛋白表达在vsd组中发生上调,9个蛋白在vsd组中表达发生下调(如下表2所示)。
[0082]
表2、筛选出的孕妇血清外泌体中的15种差异蛋白信息
[0083]
[0084][0085]
为了更好的理解差异蛋白的功能,我们对差异蛋白进行了gene onlogy和信号通路分析,并对差异蛋白进行功能注释和蛋白质互相作用网络分析(以t
‑
test p
‑
value<0.05为标准,如果差异倍数值变化超过1.2倍作为显著上调、小于1/1.2作为显著下调),鉴于以上数据分析的结果,结合文献我们筛选了1个差异蛋白即ltf(lactoferrin,乳铁蛋白)在vsd胎儿孕母血清外泌体中呈现下调。本实施例中检测到的cut
‑
off=94.8255。
[0086]
实施例3、westernblot验证vsd胎儿孕母血清外泌体中ltf蛋白的表达
[0087]
(一)取样
[0088]
参照实施例1中挑选样本的标准,2018年在嘉兴学院附属妇儿医院经过产前超声诊断为胎儿室间隔缺损胎儿的孕妇,分别标号为vsd1
‑
vsd10,对照组的研究对象为胎儿心脏发育正常的孕妇10例分别标号为ctr1
‑
ctr10。回顾性收集实验组和对照组唐筛实验用剩下的血清,置于
‑
80℃保存备用。
[0089]
(二)实验过程
[0090]
1、主要试剂和仪器
[0091]
30%丙烯酰胺溶液(bio
‑
rad,货号:161
‑
0156);
[0092]
t
‑
per tissue protein extraction reagent(组织总蛋白提取试剂)(thermo pierce,货号:78510);
[0093]
halt protease and phosphatase inhibitor cocktail(100x)(抑制剂)(thermo pierce,货号:78440);
[0094]
bca蛋白浓度测定试剂盒(增强型)(碧云天,货号:p0010);
[0095]
pvdf转印膜(millipore,货号:ipvh00010);
[0096]
ecl dualvue wb marker(ge,货号:rpn810);
[0097]
supersignal west dura extended duration substrate(thermo pierce,货号:34075)
[0098]
x
‑
ray film华东医药;
[0099]
常规化学试剂华东医药;
[0100]
紫外分光光度计(美国beckman);
[0101]
低温高速离心机(德国eppendorf);
[0102]
mini
‑
protean电泳系统以及mini trans
‑
blot转印系统(美国bio
‑
rad);
[0103]
水平脱色摇床(国产华利达)。
[0104]
2、主要步骤
[0105]
2.1、样品制备和定量
[0106]
采用总蛋白提取试剂盒(含protease inhibitor cocktail)进行总蛋白的提取,然后采用bca定量试剂盒进行总蛋白定量。
[0107]
2.2、sds
‑
page电泳分析
[0108]
配制8
‑
12%分离胶和5%浓缩胶,每个孔60ug总蛋白进行上样,每孔10
‑
15ul,浓缩胶60v,分离胶80v进行电泳2hr左右。
[0109]
2.3、蛋白质转膜
[0110]
pvdf膜甲醇中浸泡20sec,然后转移到tris
‑
glycine转移缓冲液(含5%甲醇)中平衡至少5min;sds
‑
page凝胶在tris
‑
glycine转移缓冲液平衡至少30min;在冷却条件下以100v恒压全湿转膜2hr。
[0111]
2.4、转印膜封闭
[0112]
转膜结束后,放到t
‑
tbs(含5%脱脂奶粉或bsa),室温封闭1hr,然后t
‑
tbs漂洗,5min
×
3。
[0113]
2.5一抗杂交
[0114]
表3:western blotting实验中的一抗信息
[0115]
抗体名称品牌及货号稀释度分子量(kda)ltf(lactoferrin)abcam ab158111:50079mbd3abcam ab1574641:200033dcdabcam ab1755191:100012sbsnabcam ab2327711:50061β
‑
actin(c4)(内参)santa cruz sc
‑
477781:150043
[0116]
一抗按照表3中比例溶于t
‑
tbs(含3%脱脂奶粉或bsa),4℃孵育过夜;然后t
‑
tbs漂洗5min
×
4。
[0117]
2.6、二抗杂交
[0118]
二抗按照下表4中比例溶于t
‑
tbs(含2%脱脂奶粉),室温1hr;然后t
‑
tbs漂洗5min
×
5。
[0119]
表4:western blotting实验中的二抗信息
[0120]
二抗名称品牌及货号稀释度goat anti
‑
mouse igg(h+l)secondary antibodythermo pierce货号:311601:5000
goat anti
‑
rabbit igg(h+l)secondary antibodythermo pierce货号:312101:5000
[0121]
2.7、信号检测
[0122]
采用west dura extended duration substrate,按说明书操作,制备约1ml ecl工作液,室温孵育转印膜1min,然后去除多余ecl试剂,保鲜膜密封,暗盒中放上x
‑
ray film曝光5
‑
10min后进行显影和定影。
[0123]
2.8、数据分析
[0124]
采用image j软件分析条带的光密度值,每个条带重复3次,目的蛋白相对表达量={目的蛋白(光密度值)/内参(光密度值)}
×
10n进行表示,结果以平均数
±
标准差表示。n代表乘以倍数,为了比值的可视化。
[0125]
(三)实验结果
[0126]
实验得到了10个样本组合对照组的灰度值(如表5所示),计算样品中外泌体ltf的相对表达量,样品的灰度值为三个次读数值的平均值。统计学具有统计学意义(p<0.01),上述结果表明,外泌体ltf蛋白在胎儿为室间隔缺损的孕母血清外泌体中表达水平下调。(采用spss统计软件进行统计)。
[0127]
表5:ltf的灰度值
[0128]
样本组编号灰度值对照组编号灰度值vsd11.43ctr13.06vsd21.96ctr23.06vsd30.74ctr33.04vsd40.82ctr43.35vsd51.48ctr54.34vsd61.09ctr65.45vsd71.13ctr73.25vsd81.54ctr84.24vsd91.24ctr92.96vsd101.61ctr105.03
[0129]
实施例4、elisa验证vsd胎儿孕母血清外泌体中ltf蛋白的表达
[0130]
(一)取样
[0131]
参照实施例1中挑选样本的标准,2019年在嘉兴学院附属妇儿医院经过产前超声诊断为胎儿室间隔缺损胎儿的孕妇,分别标号为vsd1
‑
vsd27;对照组的研究对象为胎儿心脏发育正常的孕妇10例分别标号为ctr1
‑
ctr27。回顾性收集实验组和对照组唐筛实验用剩下的血清,置于
‑
80℃保存备用。
[0132]
(二)实验过程
[0133]
1、主要试剂和仪器
[0134]
human lactoferrin(hlf2)elisa kit(品牌:abcam,货号:ab108882规格:96t/盒),
[0135]
spectramax m5/m5e多功能酶标仪(molecular devices美国),
[0136]
离心机(sigma1
‑
14美国),
[0137]
移液枪(gilson法国),
[0138]
水平摇床(其林贝尔ts
‑
8中国),
[0139]
电热恒温培养箱(pyx
‑
dhs上海跃进医疗器械厂),
[0140]
漩涡混合器(xw
‑
80a上海青浦沪西仪器厂)。
[0141]
2、主要步骤
[0142]
2.1、样品处理
[0143]
血清样本:冰上溶解,离心(10,000g,1min,4℃),取上清100μl至新的1.5ml管,振荡混匀,简单离心备用。
[0144]
2.2、以下步骤按照试剂盒说明书进行:
[0145]
加样:取50μl待测血清样本或50μl系列稀释的标准品加入酶标板孔中,贴上封膜,水平摇床轻轻摇动,室温孵育2hr。系列稀释的标准品如下:1号标准品:40ng/ml,2号标准品:20ng/ml,3号标准品:10ng/ml,4号标准品:5ng/ml,5号标准品:2.5ng/ml,6号标准品:1.25ng/ml,7号标准品:0.625ng/ml,8号标准品:0.313ng/ml;
[0146]
洗板:弃去板中液体,每孔加入200μl 1
×
wash buffer清洗5min
×
5次,彻底甩干洗液;
[0147]
加入检测抗体和洗板:加入50μl 1
×
biotinylatedlactoferrin antibody,贴上封膜,水平摇床轻轻摇动,室温孵育1hr;洗板同步骤二;
[0148]
加入streptavidin
‑
peroxidase conjugate和洗板:每孔加入50μl 1
×
sp conjugate,贴上封膜,水平摇床轻轻摇动,室温孵育30min;洗板同步骤二;
[0149]
显色:每孔加入50μlchromogen substrate,水平摇床轻轻摇动,室温避光孵育10min;
[0150]
终止:每孔加入50μl stop solution,轻轻混匀;
[0151]
检测:在检测波长450nm处读出od值,最后导出数据进行统计分析。
[0152]
(三)实验结果
[0153]
获得8个标准品的od值(试剂盒中包含的标准品9个,其中有一个9号是0ng/ul,是空白对照,为了绘制标准曲线),如表6所示,制作的标准曲线如图1所示。
[0154]
表6、标准品的od值
[0155]
标准品cal
‑
1cal
‑
2cal
‑
3cal
‑
4cal
‑
5cal
‑
6cal
‑
7cal
‑
8cal
‑
9浓度(ng/ml)40201052.51.250.6250.3130od均值1.8651.3810.8830.4630.2420.1290.0560.0250.015
[0156]
测定实验得到了27个样本组和对照组的od值(将样品稀释3倍后测定od值,其中样本组和对照组每个样品的od值为两个复孔去背景后的od均值),结果如表7所示:
[0157]
表7、27个样本组和对照组的od值
[0158]
[0159][0160]
根据图1的标准曲线,计算稀释后的样本组和对照组中ltf的浓度(稀释3倍后的浓度),最后计算得到样本组和对照组中ltf的实际浓度,结果如表8所示:
[0161]
表8、27个样本组和对照组的浓度值
[0162]
[0163][0164]
由于样品本身存在个体差异,实验结果需综合分析和统计软件分析,得到总体的趋势,采用统计学分析表8中数据,可知27个样本的浓度均值范围为61.971ng/ml
‑
94.326ng/ml,对照组样本的浓度均值为107.16ng/ml。上述差异具有统计学意义(p<0.01),分析结果表明,外泌体ltf蛋白在胎儿为室间隔缺损的孕母血清外泌体中表达水平下调12%~36.6%。如图2所示,室间隔缺损胎儿的孕妇和健康胎儿的孕妇之间的roc曲线分析,auc=0.804,表明孕妇血清外泌体乳铁蛋白具有比较好的胎儿室间隔缺损预测价值。综上,通过t检验分析和roc曲线分析,该外泌体蛋白的表达水平具有比较好的预测胎儿室间隔缺损的价值。
[0165]
虽然,上文中已经用一般性说明及具体实施方案对本发明做了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
[0166]
以上对本发明的具体实施例进行了描述。需要理解的是,本发明并不局限于上述特定实施方式,本领域技术人员可以在权利要求的范围内做出各种变化或修改,这并不影响本发明的实质内容。在不冲突的情况下,本申请的实施例和实施例中的特征可以任意相互组合。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1