分离测定3-氨基-4-亚氨基利福霉素S及有关杂质的方法与流程
本发明属于分析化学领域,具体涉及到一种原料药利福布汀中间体3-氨基-4-亚氨基利福霉素s及有关物质的分离测定方法。
背景技术:
:3-氨基4亚氨基利福霉素s具有很高的抗菌活性,是许多利福霉素衍生物(如利福布汀)合成中的重要中间体。目前,主要的合成方法是以3-卤代利福霉素s或sv为原料合成,经卤代反应、硝化反应、还原反应、氧化反应、氨化反应得到。在这一系列反应过程中,会产生各种化合物,最终有一部分会残留于3-氨基4亚氨基利福霉素s中即杂质。因此,3-氨基4亚氨基利福霉素s的质量优劣是药物利福布汀质量保证的关键因素。在药物分析中,所称的“有关物质”是指特定药物中不是主要组成物,但与成份相关的物质。在药物合成过程中,起始原料、试剂、中间体、副产物和异构体等,都有可能产生有关的物质。国内外对药物的研究,可允许含有一定限量的无害或低毒性的有关物质,但对毒性较大,能危害人体健康的、无效的或者能影响药物稳定性的有关物质则必须严格控制。因此,有关物质检测是控制药品质量的重要指标。目前,美国药典usp版、欧洲药典ep、中国药典均未查询到3-氨基4-亚氨基利福霉素s的有关物质的测定方法。因此开发一种能够有效分离和测定3-氨基4-亚氨基利福霉素s及其有关杂质的方法,很有意义。技术实现要素:有鉴于此,本发明目的之一是提供一种分离3-氨基-4-亚氨基利福霉素s及有关杂质的方法,有效将主药和各有关物质进行分离。为了解决上述技术问题,本发明采用以下技术方案:分离3-氨基-4-亚氨基利福霉素s及有关杂质的方法,所述方法采用的色谱柱是以十八烷基硅烷键合硅胶为填料,采用流动相a、流动相b进行梯度洗脱,将所述3-氨基-4-亚氨基利福霉素s及其有关杂质进行分离;所述相关杂质为3-氨基利福霉素s、3-溴利福霉素s、利福霉素s、杂质a、杂质b、杂质c、杂质d中的一种或几种;所述3-氨基-4-亚氨基利福霉素s、相关杂质的结构式具体如下:在选定本发明流动相之前,还采用了其他流动相,甲醇-水,乙腈-水,乙腈-磷酸二氢钠,有保留,但有拖尾且与杂质分析效果不佳。采用乙腈-磷酸二氢钾(ph调为7.0),有保留,但是分离效果不理想。经过反复试验,综合考虑选用磷酸缓冲盐和有机溶剂的混合物作为流动相。所述流动相a为有机溶剂;所述流动相b为磷酸盐缓冲液与有机溶剂的混合物。进一步,所述的流动相a所选有机溶剂为甲醇、乙腈和乙醇中的一种或者两种,优选溶剂为乙腈和甲醇。进一步,所述的流动相a中乙腈和甲醇的体积比为500~950∶50~500,优选体积比为900∶100。进一步,所述的流动相b所选磷酸盐缓冲液为包括磷酸氢二钾、磷酸二氢钾、磷酸氢二钠、磷酸二氢钠、磷酸二氢铵、磷酸氢二铵中的一种或多种的溶液,优选磷酸盐为磷酸二氢铵。进一步,所述磷酸盐溶液的浓度为0.01mol/l~0.2mol/l,优选的磷酸盐溶液的浓度为0.1mol/l。进一步,所述磷酸盐溶液的ph值为2.5~10,优选ph值为5~9。进一步,所述磷酸盐溶液选用氢氧化钠溶液、氢氧化钾溶液、氨水中一种或者多种进行ph调节,优选为氢氧化钾溶液。进一步,所述的流动相b中所选有机溶剂为乙腈、甲醇和乙醇的一种或者两种,优选为乙腈。进一步,所述的流动相b中磷酸盐溶液与有机溶剂的体积比为700~950:50~500,优选体积比为800:200。进一步,所述的流动相a与流动相b的体积比为200~800:200~600,采用等度洗脱出峰有保留,时间相当长,且拖尾严重,杂质分离度不佳。进一步,所述梯度洗脱具体为:时间/min流动相a/%流动相b/%050~6040~505~1545~5545~5510~3060~7030~4020~3565~7525~3535~4550~6040~5040~6050~6040~50进一步,优选的流动相a和流动相b采用梯度洗脱方法洗脱设置如下:进一步,所述十八烷基键合硅胶色谱柱为填料的颗粒粒径为3~5μm。进一步,所述进样量为10μl~20μl。进一步,所述流动相a、b流速为0.5ml/min~1.5ml/min;所述色谱柱温度为15℃~50℃。本发明目的之二是提供一种鉴定3-氨基-4-亚氨基利福霉素s及有关杂质的方法,通过该方法可以有效鉴定检测物中是否存在3-氨基-4-亚氨基利福霉素s及有关杂质。为了解决上述技术问题,本发明采用以下技术方案:鉴定3-氨基-4-亚氨基利福霉素s及有关杂质的方法,利用目的一中所述方法将所述3-氨基-4-亚氨基利福霉素s及其有关杂质进行分离,通入检测器中进行检测,所述检测器检测波长为254nm±2nm;所述相关杂质为目的一中所述相关杂质;将检测得到的色谱图与已知对照品色谱图进行对比,鉴定检测物中是否含有所述3-氨基-4-亚氨基利福霉素s及其有关杂质。进一步,所述检测器选用紫外检测器。本发明目的之三是提供一种测定3-氨基-4-亚氨基利福霉素s及有关杂质的方法,通过该方法可以有效测量检测物中3-氨基-4-亚氨基利福霉素s及有关杂质的含量。为了解决上述技术问题,本发明采用以下技术方案:测定3-氨基-4-亚氨基利福霉素s及有关杂质的方法,利用目的一中所述方法将所述3-氨基-4-亚氨基利福霉素s及其有关杂质进行分离,在检测波长为254nm±2nm的检测器中进行检测得到色谱图,外标法计算所述3-氨基-4-亚氨基利福霉素s及其有关杂质的含量;所述相关杂质为目的一中所述相关杂质。进一步,所述方法具体步骤如下:s1:试剂配制取供试样品溶于稀释剂,得供试品溶液;取对照品溶于稀释剂,得对照品溶液;s2:分离利用目的一中所述方法,将所述3-氨基-4-亚氨基利福霉素s及其有关杂质分离;s3:鉴定利用目的二中所述方法,鉴定检测物中是否含有所述3-氨基-4-亚氨基利福霉素s及其有关杂质;s4:含量计算根据得到的色谱图,利用外标法计算所述3-氨基-4-亚氨基利福霉素s及其有关杂质的含量。所述稀释剂为水和乙腈的混合溶液,所述稀释剂ph为6.5,所述稀释剂中水与乙腈的体积比为40:60。所述供试品溶液浓度为0.1mg/ml~1mg/ml,优选所述供试品溶液浓度为0.4mg/ml。本发明目的之四是提供一种用于分离测定3-氨基-4-亚氨基利福霉素s及有关杂质的溶液,通过使用该溶液进行高效液相色谱法检测,可有效检测3-氨基-4-亚氨基利福霉素s及有关杂质。为了解决上述技术问题,本发明采用以下技术方案:一种用于分离测定3-氨基-4-亚氨基利福霉素s及有关杂质的溶液,所述有关杂质为权利要求1所述相关杂质;所述溶液为:溶液a:乙腈和甲醇混合溶液,体积比为9:1;溶液b:磷酸盐缓冲液和乙腈,体积比为8:2;溶液c:氢氧化钾溶液;所述磷酸盐缓冲液为磷酸二氢铵的溶液;所述缓冲盐中磷酸二氢铵的浓度为0.01mol/l~0.2mol/l。本发明的有益效果在于:1.本发本发明提供了一种有效分离测定3-氨基-4亚氨基利福霉素s及其有关物质的方法,杂质峰和主峰完全分离,方法有效、可靠、分离度大于1.5。2.该方法专属性强,灵明度高,操作简单。3.分析时间短,在55分钟内,能将多种已知杂质和主峰基线分离。4.能对3-氨基4亚氨基利福霉素s及有关物质进行定量,进而可严格控制最终产品利福布汀的质量。附图说明所举实施例是为了更好地对本发明进行说明,但并不是本发明的内容仅局限于所举实施例。所以熟悉本领域的技术人员根据上述
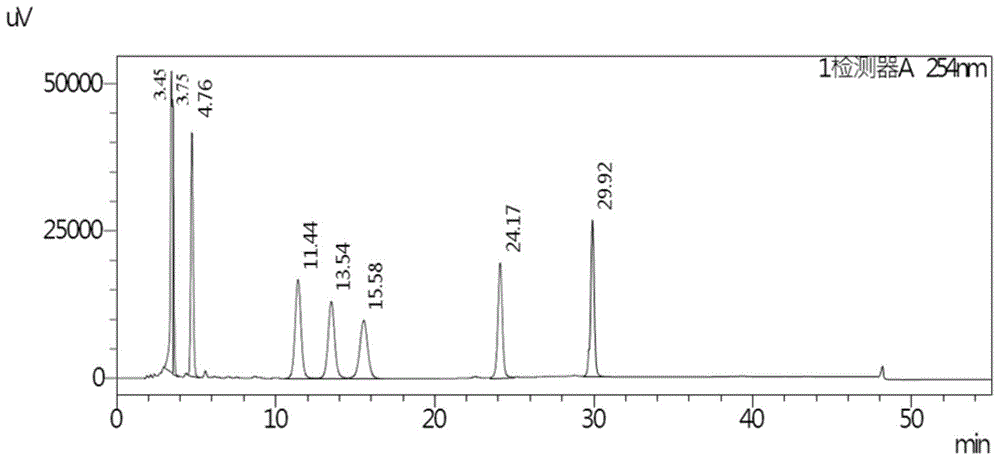
发明内容对实施方案进行非本质的改进和调整,仍属于本发明的保护范围。图1:实施例2色谱图;图2:实施例3色谱图;图3:实施例4色谱图;图4:实施例5色谱图;图5:实施例6空白试验色谱图;图6:实施例60小时进样供试品进样色谱图;图7:实施例6放置4小时供试品溶液进样色谱图;图8:实施例7色谱图;图9:实施例8定量限色谱图;图10:实施例8检测限色谱图。具体实施方式所举实施例是为了更好地对本发明进行说明,但并不是本发明的内容仅局限于所举实施例。所以熟悉本领域的技术人员根据上述
发明内容对实施方案进行非本质的改进和调整,仍属于本发明的保护范围。以下实施例是本发明方法的优选实施例的示例,在优选实施例中未完全注明条件方法,示例作为与本发明方法的结果对比。实施例1用品及方法3-氨基-4-亚氨基利福霉素s标准品以及3-氨基利福霉素s、利福霉素s标准品均从市售渠道获得。3-氨基-4-亚氨基利福霉素s的供试品和3-溴利福霉素s、杂质a、杂质b、杂质c、杂质d的标准品与供试品来源均为重庆华邦胜凯制药有限公司。使用的试验仪器均为岛津高效液相色谱仪(uv检测器)色谱柱为zorbaxeclipsexdb-c18,4.6×250mm,5-micron;柱温30℃;进样量为15μl;流速为1.0ml/min;样品浓度为0.4mg/ml。流动相a:乙腈和甲醇的体积比为900:100;流动相b:磷酸二氢铵缓冲液与乙腈的混溶液,体积比为800:200,磷酸二氢铵溶液的浓度为0.1mol/l,ph值为6~8.5。流动相梯度条件如下:稀释剂∶水∶乙腈=40∶60(用koh调ph至6.5);试剂及试药:乙腈(色谱级);甲醇(色谱级);蒸馏水;氢氧化钠(分析纯);氢氧化钾(分析纯);磷酸二氢钠(分析纯);磷酸二氢钾(分析纯);磷酸二氢铵(分析纯)。使用测试的样品为3-氨基-4-亚氨基利福霉素s(图例中标记为z3)、3-氨基利福霉素s(图例中标记为z2)、3-溴利福霉素s(图例中标记为z1)、利福霉素s(图例中标记为sm1)、杂质a、杂质b、杂质c、杂质d的混合样品,以及3-氨基-4-亚氨基利福霉素s的供试品。方法步骤:1)配制系统适用性溶液;取3-氨基-4-亚氨基利福霉素s和3-氨基利福霉素s、3-溴利福霉素s、利福霉素s、杂质a、杂质b、杂质c、杂质d适量经甲醇溶解后用溶剂稀释,得系统适应性溶液;2)配制供试品溶液和对照溶液:取3-氨基-4-亚氨基利福霉素s溶液加溶剂溶解后经滤膜滤过,得供试品溶液;将配置得到的供试品溶液取适量加溶剂稀释,得自身对照溶液;3)配制对照品溶液:取3-氨基-4-亚氨基利福霉素s对照品适量,加溶剂溶解并稀释,得3-氨基-4-亚氨基利福霉素s溶液;4)取系统适用性溶液进样,记录色谱图;取空白溶液(溶剂),3-氨基-4-亚氨基利福霉素s对照品溶液、自身对照溶液、供试品溶液分别注入高效液相色谱仪进行梯度洗脱,进入检测器进行检测,记录色谱图,按外标法计算杂质3-氨基-4-亚氨基利福霉素s的含量;按加校正因子的主成分自身稀释法计算供试品中其它单个杂质的含量。实施例2采用的缓冲盐为磷酸二氢钠水溶液,ph为6.0,梯度洗脱,结果见附图1。实施例3采用的缓冲盐为磷酸二氢钾水溶液,ph为6.0,梯度洗脱结果见附图2。实施例4:采用的缓冲盐为磷酸二氢铵水溶液,ph为6.0,梯度洗脱结果见附图3。实施例5采用的缓冲盐为磷酸二氢铵水溶液,ph为8.0,梯度洗脱结果见附图4。测试样品配制:配制0.4mg/ml的sm1、z1、z2、z3溶液,各取5ml于100ml容量瓶中用稀释剂定容至刻度、摇匀,过滤,即得。进样并记录色谱图。结论:通过不同缓冲溶液的液相色谱图比较,可知当缓冲盐为铵盐时各峰的分离效果明显。由色谱图可见当缓冲盐ph调整在7.0~8.0之间时,主峰与各杂质峰的分离效果能达到要求。实施例6采用本发明方法的稀释剂水∶乙腈=40∶60,ph为6.5的供试品稳定性。供试品溶液配制:称取3-氨基-4-亚氨基利福霉素s(图例中标记为z3)适量,用稀释剂溶解并配制成0.4mg/ml的溶液,摇匀,过滤,即得。进样并记录色谱图。空白试验:用本方法做空白试验结果见附图5。实验结果:0小时进样供试品进样的实验结果见附图6,放置4小时供试品溶液进样的试验结果见附图7,由色谱图可见该稀释剂配制的溶液稳定。实施例7采用杂质加入供试品溶液中试验法。测试溶液配制:精密称取各杂质标准品配制成0.4mg/ml,再移取适量于供试品溶液中,摇匀,过滤,即得。进样并记录色谱图。试验结果:由色谱图可见在供试品中各杂质的分离效果能达到要求,其结果见附图8。实施例8采用本发明方法检测杂质的定量限和检测限。各杂质定量限溶液配制,分别称取各杂质对照品,精密称量,加稀释剂稀释至合适浓度,摇匀,即得,进样并记录色谱图。3-氨基-4-亚氨基利福霉素s中各杂质的定量限(定量限取s/n≥10.0)结果见下表1、表2(见附图9):表1定量限检测结果表表2定量限检色谱图积分表峰号面积高度分离度s/n171057-12.902700531.92512.063827573.88812.9546444731.09310.655679522.79611.726680563.42012.667625568.81112.7086294411.34010.03总计54944243-氨基-4-亚氨基利福霉素s中各杂质的检测限(检测限取2.0≤s/n≤5.0)结果见下表3、表4(见附图10):表3检测限检测结果表表4检测限色谱图积分表峰号面积高度分离度s/n116717-3.212147152.2482.823176175.6203.2841351642.9142.945190173.2153.296161163.9123.0271261411.4982.6381891613.4422.96总计1292128通过实施例的结果表明,本发明方法以有机溶剂和铵盐的水溶液为流动相,采用梯度洗脱能有效的对3-氨基-4-亚氨基利福霉素s和其杂质进行有效分析。最后说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的宗旨和范围,其均应涵盖在本发明的权利要求范围当中。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1