一种人参皂苷CK软胶囊中人参皂苷CK的含量测定方法与流程
本发明属于软胶囊含量检测领域,具体涉及一种人参皂苷ck软胶囊中人参皂苷ck的含量测定方法。
背景技术:
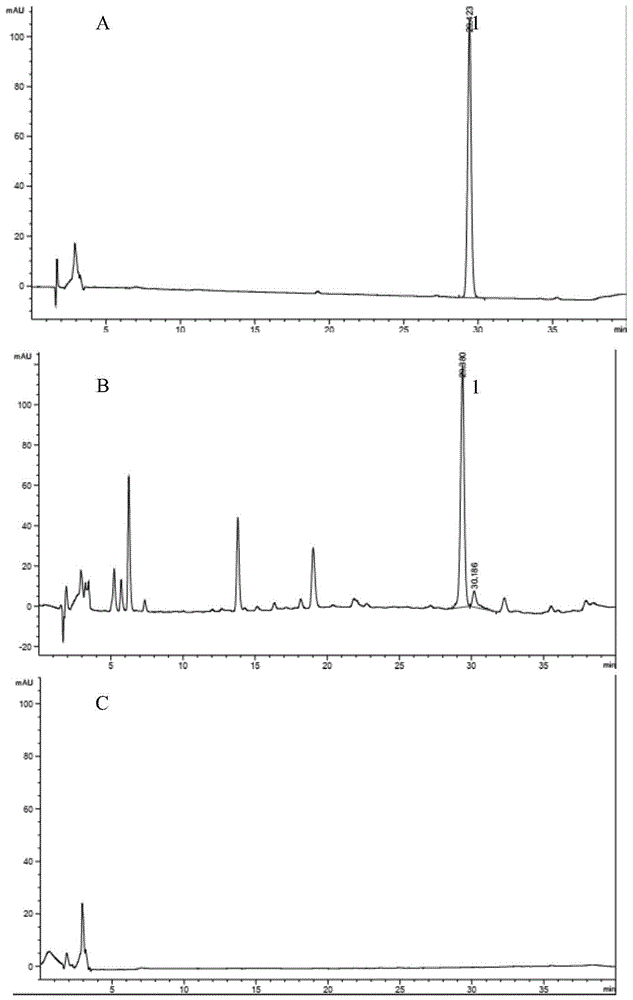
:人参皂苷ck为原人参二醇类人参皂苷,其结构属四环三萜达玛烷型人参皂苷。1972年yasioka等通过土壤中的细菌降解人参二醇型皂苷rb1、rb2和rc的混合物,从中首次发现了人参皂苷ck,并鉴定了ck的结构为20(s)原人参二醇-20-o-β-d-吡喃葡萄糖苷,但其药理活性并未得到重视。直到1991年日本学者karikura等在给予人参皂苷rb1、rb2的wistar大鼠肠道代谢物中再次发现并鉴定了人参皂苷ck,并通过比较酸水解物和肠道代谢物证明人参皂苷ck是肠道微生物的代谢物,而不是胃酸的水解产物。hasegawa等系统的研究了人参皂苷在体内的肠道细菌代谢产物和粪便菌群厌氧培养后的代谢产物,并提出了人参皂苷经过肠道细菌转化成人参皂苷ck的代谢过程,这为人参皂苷ck后续的研究奠定了坚实的基础。在之后的研究中发现人参皂苷ck具有抗肿瘤、抗皮肤衰老、抗炎、抗过敏、抗糖尿病、保护神经、保护心肌、保护肝脏等多种药理活性。它在人参属植物中含量极低,无法满足开发应用的需求,目前主要通过微生物转化和酶转化制备得到。软胶囊是将液体原料药物或由固体原料药物溶解或分散制成的溶液、混悬液、乳状液或半固体密封于软质囊材中的胶囊剂,具有有效成分含量高、生物利用度高、吸收迅速、稳定性好、能掩盖药物的不良气味、服用量小、外形美观等特点。当将人参皂苷ck制备成自微乳作为软胶囊的内容物时药物在基质中以分子、胶体或无定形态分散,对其溶出和吸收非常有利。因此,有必要对人参皂苷ck检测方法进行探索。技术实现要素:为了解决上述问题,本发明的目的是建立一种快速、全面、针对性强的人参皂苷ck软胶囊中人参皂苷ck的含量测定方法,本发明能够准确的定量测定人参皂苷ck软胶囊中人参皂苷ck的含量,具有很好应用价值。本发明的技术方案具体如下:一种人参皂苷ck软胶囊的含量测定方法,包括以下步骤:步骤(1)、对照品溶液的制备:制备对照品溶液,每1ml对照品溶液含人参皂苷ck10.13μg/ml~1.013mg/ml的溶液;步骤(2)、供试品溶液的制备:称取人参皂苷ck软胶囊内容物0.04~0.50g,精密称定,置于10ml容量瓶中,加入甲醇适量定容到10ml,超声10~30min,放冷,摇匀,取上清液过0.22μm的微孔滤膜,取续滤液即得;步骤(3)、样品检测:分别吸取对照品溶液与供试品溶液各5~20μl,注入液相色谱仪,测定,即得。进一步地,每1ml对照品溶液含人参皂苷ck0.2026mg/ml的溶液;进一步地,步骤(3)中,色谱条件如下:以十八烷基硅烷键合硅胶为填充剂;流速为0.5-1.5ml/min;柱温25-40℃;进样量5-20μl;检测波长为203nm;流动相:a-乙腈,b-超纯水;进行梯度洗脱。进一步地,步骤(3)中,梯度洗脱条件如下:时间乙腈(a)%超纯水(b)%总计030-60中任一数值余量100%3550-80中任一数值余量100%4030-60中任一数值余量100%进一步地,步骤(3)中,色谱条件如下:以十八烷基硅烷键合硅胶为填充剂;流速为1.0ml/min;柱温30℃;进样量10μl;检测波长为203nm;流动相:a-乙腈,b-超纯水;进行梯度洗脱。进一步地,步骤(3)中,梯度洗脱条件如下:通过以下实验研究对本发明进行进一步说明。(1)色谱柱的选择:人参皂苷ck极性较低,所以选择反相c18色谱柱。(2)检测波长的选择:人参皂苷ck为原人参二醇类人参皂苷,其结构属于四环三萜达玛烷型人参皂苷,因此决定选用203nm作为检测波长。(3)流动相系统的选择:以乙腈(a)-超纯水(b)溶液、甲醇(a)-超纯水(b)溶液的流动相系统为因素进行考察,结果发现,使用不同流动相系统,对人参皂苷ck的峰形及分离度影响不同,乙腈(a)-超纯水(b)溶液流动相系统下各成分分离度、拖尾因子、理论塔板数均较其它流动相条件要好,所以最终选用乙腈(a)-超纯水(b)溶液流动相系统。(4)供试品的处理方式选择:人参皂苷ck为脂溶性成分,因此选用100%甲醇作为供试品制备溶剂。(5)色谱条件与系统适用性试验:以十八烷基硅烷键合硅胶为填充剂;流速为0.5-1.5ml/min;进样量5-20μl;检测波长为203nm;柱温25-35℃;理论塔板数大于6000。流动相:a-乙腈,b-超纯水;按下表进行梯度洗脱。时间乙腈(a)%超纯水(b)%总计04060100%356535100%404060100%(6)专属性实验:在相同试验条件下,分别精密吸取人参皂苷ck对照品溶液,供试品溶液,阴性对照品溶液各10μl,注入高效液相色谱仪,参照步骤(5)所述方法进行测定。结果表明对照品溶液和供试品溶液在相同的保留时间均有出峰,阴性对照对人参皂苷ck的检测无干扰,说明该测定方法专属性强。结果如图1所示。(7)线性关系:依次配制浓度分别为1.013mg/ml、0.5065mg/ml、0.2026mg/ml、0.1013mg/ml、50.65μg/ml、10.13μg/ml的人参皂苷ck对照品溶液,各精密吸取10μl,注入高效液相色谱仪,参照步骤(5)所述方法进行测定。以峰面积(y)为纵坐标,人参皂苷ck对照品的质量浓度(x)为横坐标,得人参皂苷ck的线性回归方程为:y=4081.4x+3.2324,r2=1。结果表明用该检测方法检测人参皂苷ck在1.013mg/ml~10.13μg/ml范围内线性关系良好。结果如图2所示。(8)精密度考察:精密吸取浓度为0.2026mg/ml的人参皂苷ck对照品溶液,按上述色谱条件进样测定,连续测定6针,记录峰面积。计算得人参皂ck的峰面积rsd为:0.35%,表明仪器精密度良好。(9)重复性实验:平行制备供试品溶液6份,精密吸取各供试品溶液10μl,注入高效液相色谱仪,按上述色谱条件检测,记录峰面积,计算其含量的rsd为1.12%,表明本方法重复性良好。(10)稳定性实验:分别精密吸取对照品溶液和供试品溶液10μl,分别于0、2、4、6、8、10、12、24h注入高效液相色谱仪,按上述色谱条件检测,记录峰面积。对照品溶液峰面积的rsd为1.10%,供试品溶液峰面积的rsd为1.13%,表明对照品溶液和供试品溶液在24h内稳定性良好。(11)加样回收实验:精密称取人参皂苷ck软胶囊内容物适量,按浓度为80%、100%和120%精密加入人参皂苷ck对照品适量,每个浓度平行制备3份,按上述色谱条件检测,以外标法计算含量,并计算加样回收率,结果三个浓度的平均回收率分别为98.94%、97.07%、100.80%,rsd值分别为2.87%、0.91%、2.34%。结果如表1所示。表1加样回收实验结果表(12)耐用性实验:制备供试品溶液3份,精密吸取供试品溶液10μl,分别在不同变动因素:设备、柱温下分别进样,记录人参皂苷ck的峰面积,计算含量,考察色谱条件的耐用性。结果各条件下,人参皂苷ck含量的rsd%值均小于3%,表明该色谱条件耐用性良好。结果如表2所示。表2耐用性实验结果表(13)含量测定:精密称取0.1000g装量差异中挤出的人参皂苷ck软胶囊内容物,加甲醇稀释定容到10ml,超声10min过0.22μm的滤膜,取续滤液按上述色谱条件进行含量测定,人参皂苷ck软胶囊中人参皂苷ck的含量为12.30mg/粒。与现有技术相比,本发明的有益效果如下:(1)本发明的方法能够准确的定量测定人参皂苷ck软胶囊中人参皂苷ck的含量,可节约检测时间和成本,不仅准确且简单易行。实现了对人参皂苷ck软胶囊质量的全面评价和控制,从而为人参皂苷ck软胶囊临床用药的安全性和有效性提供了保障。(2)本发明的方法快速、全面、针对性强,操作简便,适用性好,能稳定的用于人参皂苷ck的含量测定。(3)本发明专属性强,稳定性好,重复性好,回收率高。附图说明图1为人参皂苷ck软胶囊含量测定hplc图;其中,a:人参皂苷ck对照品溶液;b:供试品溶液;c:人参皂苷ck阴性对照品溶液;图2为人参皂苷ck标准曲线图;具体实施方式为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过购买获得的常规产品。实施例1本实施例所述的人参皂苷ck软胶囊中人参皂苷ck的含量测定方法,具体包括如下步骤:步骤(1)、对照品溶液的制备:精密称取人参皂苷ck对照品10.13mg,加甲醇溶解并定容到10ml,制得浓度为1.013mg/ml的对照品储备液。精密吸取人参皂苷ck储备液2ml,加入甲醇定容到10ml,摇匀,过0.22μm的微孔滤膜,取续滤液,即得质量浓度为0.2026mg/ml的对照品溶液。步骤(2)、供试品溶液的制备:精密称取人参皂苷ck软胶囊内容物0.1000g,置于10ml容量瓶中,加入甲醇适量定容到10ml,超声10min,放冷,摇匀,取上清液过0.22μm的微孔滤膜,取续滤液即得。步骤(3)、样品检测:色谱条件:以十八烷基硅烷键合硅胶为填充剂;流速为1.0ml/min;进样量10μl;检测波长为203nm;柱温30℃;理论塔板数大于6000;流动相:a-乙腈,b-超纯水;按下表进行梯度洗脱。时间乙腈(a)%超纯水(b)%总计04060100%356535100%404060100%分别吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,即得。本实施例的人参皂苷ck软胶囊样品产地及含量测定结果如表3所示:表3人参皂苷ck软胶囊样品含量测定结果批号人参皂苷ck含量(mg/g)2020110145.772020110246.242020110346.74根据含量检测结果来看,该法可稳定用于人参皂苷ck软胶囊的含量检测。实施例2本实施例所述的人参皂苷ck软胶囊中人参皂苷ck的含量测定方法,具体包括如下步骤:步骤(1)、对照品溶液的制备:精密称取人参皂苷ck对照品10.13mg,加甲醇溶解并定容到10ml,制得浓度为1.013mg/ml的对照品储备液。精密吸取人参皂苷ck储备液1ml,加入甲醇定容到100ml,摇匀,过0.22μm的微孔滤膜,取续滤液,即得质量浓度为10.13ug/ml的对照品溶液。步骤(2)、供试品溶液的制备:精密称取人参皂苷ck软胶囊内容物0.0400g,置于10ml容量瓶中,加入甲醇适量定容到10ml,超声10min,放冷,摇匀,取上清液过0.22μm的微孔滤膜,取续滤液即得。步骤(3)、样品检测:色谱条件:以碳十八烷基键合硅胶为填充剂;流速为1.5ml/min;进样量5μl;检测波长为203nm;柱温25℃;理论塔板数大于6000;流动相:a-乙腈,b-超纯水;按下表进行梯度洗脱。时间乙腈(a)%超纯水(b)%总计03070100%355050100%403070100%分别吸取对照品溶液与供试品溶液各5μl,注入液相色谱仪,测定,即得。本实施例的人参皂苷ck软胶囊样品产地及含量测定结果如表4所示:表4人参皂苷ck软胶囊样品含量测定结果批号人参皂苷ck含量(mg/g)2020120141.122020120221.60根据含量检测结果来看,该法可稳定用于人参皂苷ck含量检测。实施例3本实施例所述的人参皂苷ck软胶囊中人参皂苷ck的含量测定方法,具体包括如下步骤:步骤(1)、对照品溶液的制备:精密称取人参皂苷ck对照品10.13mg,加甲醇溶解并定容到10ml,制得浓度为1.013mg/ml的对照品溶液。步骤(2)、供试品溶液的制备:精密称取人参皂苷ck软胶囊内容物0.5000g,置于10ml容量瓶中,加入甲醇适量定容到10ml,超声30min,放冷,摇匀,取上清液过0.22μm的微孔滤膜,取续滤液即得。步骤(3)、样品检测:色谱条件:以十八烷基硅烷键合硅胶为填充剂;流速为1.5ml/min;进样量20μl;检测波长为203nm;柱温35℃;理论塔板数大于6000;流动相:a-乙腈,b-超纯水;按下表进行梯度洗脱。分别吸取对照品溶液与供试品溶液各20μl,注入液相色谱仪,测定,即得。本实施例的人参皂苷ck软胶囊样品产地及含量测定结果如表5所示:表5人参皂苷ck软胶囊样品含量测定结果批号人参皂苷ck含量(mg/g)2021010219.972021010444.862021010544.63根据含量检测结果来看,该法可稳定用于人参皂苷ck含量检测。以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1