一种柔性葡萄糖传感器及其检测葡萄糖方法
1.本发明涉及材料领域,具体涉及一种柔性葡萄糖传感器及其检测葡萄糖方法。
背景技术:
2.临床上常用光电型和电极型血糖仪监测血糖,后者因其更科学的测试原理被广泛研究。因此,基于电化学的电极型血糖仪类型占商用手持式生物传感器市场的85%。因为血糖仪依赖于有创血液测试,所以这种类型的测试通常伴随着反复抽血带来的疼痛和不适。随着技术的发展,微型,便携式,稳定且无创的柔性测试设备可以更好地满足人们的需求。而对葡萄糖传感器的研究也从第一代的酶传感器到第四代的非酶葡萄糖传感器;一直不断的研究以期实现高灵敏、高选择性,低检测限,便捷及廉价的葡萄糖传感技术。尽管在非酶葡萄糖检测领域取得了许多研究成果,但是在生理条件下监测葡萄糖仍是巨大挑战,从而限制了它们的临床适用性。一方面,利用某些贵金属材料与葡萄糖相互作用时,其物理化学性质发生变化产生电极表面的电子传递过程,因此电极对葡萄糖产生电化学响应,以实现葡萄糖的检测。例如pt和pb材料在中性缓冲液中对葡萄糖分子显示出很高的催化性能,通过催化氧化葡萄糖形成葡萄糖酸内脂以产生电极与金属间的电子转移,从而引起电流的变化。然而在催化氧化葡萄糖的过程中其中性缓冲液中的cl
‑
和中间产物会吸附于电极表面,导致较差的灵敏度和稳定性,不利于传感界面的电化学反应。尽管也开发了廉价的铜基混合材料在中性条件下对葡萄糖有较高的传感性能,但因其检测限限制仍然无法实现汗液中的检测。此外,混合纳米材料的制备过程比单一金属的制备过程更为复杂且耗时。另一方面,1981年vassilyev提出,在中性和碱性条件下,金在葡萄糖上的葡萄糖电氧化反应速率都比铂和其他第viii族单金属更快,这使其更适合用于葡萄糖传感器。tominaga等人的另一项研究证明,在中性溶液中以0.1v和0.3v电压电解金颗粒以获得葡萄糖酸内酯(或葡萄糖酸)时,其脱氢步骤的速率低于在高ph条件下的脱氢速率。虽然在中性条件下检测葡萄糖的基于金材料的电化学传感器已经存在一些研究结果,但是大多数血糖监测都基于刚性基底的研究,这些传感器很难应用于可以附着在皮肤上的汗液传感器。而且需要较低的检测限来检测汗液中的微量葡萄糖,这又与金属材料的电催化活性有关。对金电极中葡萄糖氧化机理的研究表明,金的表面可以诱导羟基吸附(oh
ads
)层的产生,从而进行葡萄糖氧化反应机理中的脱氢步骤。同时,au活性表面附近的氧官能团也可以通过非共价相互作用诱导oh
ads
。因此,作为葡萄糖氧化机理的第一步也是最慢的一步,更多的oh
ads
可以刺激更快的脱氢反应,从而加快整个反应过程。使用上述原理,toi等人能够通过使用纳米金和带有含氧官能团的rgo
‑
pu支持基质来检测汗液中的葡萄糖。然而,其一周的催化寿命和纳米混杂纤维的复杂合成过程仍然需要改进。
3.综上所述,亟需一种新型柔性传感器,以改善葡萄糖的检测能力,克服上述诸多缺点。
技术实现要素:
4.本发明为了解决上述问题,提供了一种柔性葡萄糖传感器制备方法,在碳布(cc)柔性电极上电沉积金微米花(gmfs),碳布因为其三维结构和良好的孔隙率可促进gmfs和cc之间的介质渗透和协同效应,使其成为中性ph环境中检测葡萄糖浓度的合适基底;利用强酸处理cc,增加其含氧官能团数量,同时增加gmfs/cc的比表面积,使其能进行灵敏的电化学检测。
5.本发明目的之一在于提供一种柔性碳布,所述碳布表面电沉积有金微米花。
6.本发明目的之二在于提供一种增加上述柔性碳布表面含氧官能团的方法,具体技术方案如下:
7.一种增加表面电沉积有金微米花碳布的表面含氧官能团的方法,预先对碳布进行酸性处理。
8.具体的,所述酸性处理为碳布电沉积金前,预处理时浸入浓hno3和浓h2so4的混合溶液中煮沸。
9.具体的,所述浓hno3和浓h2so4的体积比为1:1。
10.本发明目的之三在于提供一种使柔性碳布表面形成大量auoh并促进脱氢反应的方法,具体技术方案如下:
11.一种使柔性碳布表面形成大量auoh并促进脱氢反应的方法,预先对碳布进行酸性处理,然后电沉积金得到所述柔性碳布。
12.具体的,步骤包括:
13.(1)对碳布进行预处理,所述预处理包括酸性处理;
14.(2)将预处理后的碳布浸泡于kcl和haucl4·
3h2o的混合溶液;
15.(3)将浸泡后的碳布进行电沉积金,得到所述柔性碳布。
16.具体的,所述酸性处理为将碳布浸入浓hno3和浓h2so4的混合溶液中煮沸。
17.具体的,浓hno3和浓h2so4的体积比为1:1。
18.具体的,所述kcl和haucl4·
3h2o的浓度分别为100mm和4mm。
19.具体的,所述预处理还包括超声处理和清洁处理。
20.具体的,所述超声处理为将碳布分别在丙酮,乙醇和去离子水中进行5分钟的超声处理。
21.具体的,步骤(3)在恒定
‑
0.3v的电势下电沉积金2800s。
22.本发明目的之四为利用上述技术方案中制备方法制备得到柔性碳布测定汗液或血清中葡萄糖含量的方法,具体技术方案如下:
23.利用上述技术方案中的方法制备得到的柔性碳布测定汗液或血清中葡萄糖含量的方法,将所述柔性碳布作为工作电极,铂丝电极作为对电极,ag/agcl电极作为参比电极,组成葡萄糖传感器;对所述汗液或血液进行安培i
‑
t检测;根据检测得到的电流值测定汗液或血清中葡萄糖含量。
24.具体的,所述方法能从尿素和/或乳酸和/或乙酸和/或抗坏血酸和/或木糖和/或麦芽糖和/或蔗糖和/或果糖中测定出葡萄糖含量。
25.具体的,所述葡萄糖传感器的检出限为0.70μm,检测限度为26664μm。
26.本发明的有益之处在于:本发明传感器克服了葡萄糖检测的碱性依赖过程,对葡
萄糖具有良好的电催化活性,宽的线性范围和出色的检出限;该传感器具有良好抗干扰传感性能、柔韧性和稳定性。该方法对葡萄糖的高精度和高准确的检测使其在开发小型化的人体柔性葡萄糖传感器方面具有巨大的潜力。
附图说明
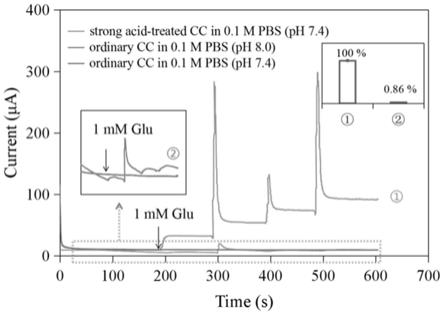
27.图1为强酸处理的碳布和普通碳布上电沉积的金微米花在0.1mpbs中对葡萄糖的电流响应实验结果图
28.图2为本发明的金微米花柔性碳布的sem图
29.图3为本发明的金微米花柔性碳布结合能强度图
30.图4为本发明的金微米花柔性碳布
具体实施方式
31.下面通过实施例对本发明进行进一步详细说明,应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明,本领域技术人员应该理解的是,在不偏离本发明的结构思路、使用范围下可以对本发明技术方案的细节和形式进行修改或替换,但这些修改和替换均落入本发明的保护范围内。
32.化学品和材料
33.碳布(cc)(ce tech co.,ltd)是从湖北rocktek仪器有限公司(中国,武汉)购买的。四水合金(iii)酸三水合物(haucl4·
3h2o)购自admas
‑
beta(中国上海)。尿素和葡萄糖购自acros organics(比利时)。氯化钠(nacl),氯化钾(kcl),磷酸氢二钠(na2hpo4),磷酸二氢钠(nah2po4),浓硫酸(h2so4)和浓硝酸(hno3)购自重庆川东化工集团有限公司(中国重庆)。木糖,麦芽糖,蔗糖,果糖,乙酸,乳酸和抗坏血酸均购自sigma
‑
aldrich(美国密苏里州圣路易斯)。所有实验均采用上海和泰公司的去离子水和超纯水(18.2mωcm)。
34.仪器
35.采用扫描电子显微镜(sem,su8010,日立,东京,日本)观察其微观结构。用x射线光电子能谱(xps,escalab250xi,thermo,usa)测定了所制备材料的元素状态和表面性质。在chi660e电化学工作站(中国上海辰华仪器有限公司)上,采用三电极系统进行了电化学实验。
36.样品
37.健康人血清样本来自中国重庆医科大学附属第一医院。真实的汗液样本来自健康志愿者
38.实施例1:柔性葡萄糖传感器的制备
39.1、电沉积之前,将一块cc(1cm
×
1cm)分别在丙酮,乙醇和去离子水中进行5分钟的超声处理。
40.2、洗涤后,将cc浸入体积比1:1浓hno3和浓h2so4的混合溶液中,加热并煮沸1小时。
41.冷却后,用大量超纯水冲洗cc,直至无酸。清洁后的cc在真空烘箱中于60℃干燥12小时。
42.3、通过将预定量的kcl和haucl4·
3h2o溶液混合(混合溶液中kcl和haucl4·
3h2o的浓度分别为100mm和4mm)来制备反应溶液。
43.4、将预处理的cc置于反应混合物中。为了增加cc与反应溶液的接触面积,将反应溶液置于真空干燥箱中以除去表面气泡。
44.5、浸入电解液中的cc使用传统的三电极系统,通过计时电流法(i
‑
t)在恒定电势(
‑
0.3v)下电沉积金2800s。
45.使用超纯水将所得cc(gmfs/cc)洗涤几次。然后在室温下在真空中干燥以进行后续测试。
46.利用本实施例柔性葡萄糖传感器检测葡萄糖的原理
47.葡萄糖在gmfs/cc上的电化学氧化机制通常通过三个步骤进行。首先,au表面吸附oh形成au(oh)
ads
,下标中的ads是指au表面化学吸附物质的类型。其次,au(oh)
ads
作为催化剂在葡萄糖氧化形成葡萄糖酸内酯中的作用是通过两个电化学过程发生的:葡萄糖分子的半缩醛基团中的c1碳原子形成的氢键首先被氧化,在金表面形成一个半缩醛基团,并将电子转移到电极表面(等式2)。接下来,形成的游离半缩醛基团进一步被氧化为葡萄糖酸内酯,并将另一个电子转移到电极表面(等式3)。最后,将葡萄糖酸内酯从gmfs/cc电极上解吸,并在pbs中水解形成葡萄糖酸钠(等式4)。因此,大量au(oh)
ads
的产生和脱氢步骤的速度对葡萄糖氧化有重要影响。用强酸处理的cc具有许多含氧基团。因此,cc上的含氧官能团可以与h2o具有非共价相互作用,从而增加au(oh)
ads
的形成(等式1)并促进脱氢反应(等式2和3)。而gmfs/cc的比表面积高,可为葡萄糖氧化提供更多的au(oh)
ads
结合位点,因此可以进行灵敏的电化学检测。
48.au+h2o
→
au(oh)
ads
ꢀꢀꢀ
(1)
[0049][0050]
随后通过计时电流法(i
‑
t)对比强酸处理的cc和普通cc上电沉积的gmfs在0.1m pbs中对葡萄糖的电流响应实验结果。如图1所示,普通cc上的gmfs不具有检测0.1m pbs(ph 7.4)中的葡萄糖(1mm)的作用。但是,强酸处理的cc上的gmfs随着连续注入葡萄糖而呈现出大的阶梯状电流增加。如插图显示,在0.1m pbs(ph 8.0)中添加1mm葡萄糖后,普通cc上的gmfs对葡萄糖的响应略有增加,这与溶液中氢氧根离子的变化有关。但是,与强酸处理的cc上的gmfs对葡萄糖的电流响应相比,普通cc上的gmfs的上升电流的比例(0.86%)甚至小于酸处理的cc上的gmfs的电极内相对标准误差(rsd 2.7%)。结合图1中的结果,说明影响葡萄糖检测性能的关键步骤是诱导大量oh
ads
在金表面上形成au(oh)
ads
并促进脱氢反应。结果表明ph值变化引起的氢氧根离子波动对此材料于检测葡萄糖过程而言影响不大,本方法构造的葡萄糖传感器克服了葡萄糖检测的碱性依赖过程。
[0051]
本实施例柔性葡萄糖传感器材料表征
[0052]
gmfs/cc的结构如图2中的a
‑
d所示,使用扫描电镜在不同放大倍数下观察。gmfs/cc由碳布(cc)和立体的金微球花(gmfs)组成,表明恒电位沉积法在cc上成功稳定地合成了gmfs。gmfs的大小分布相对均匀,平均直径约为4.5μm。其松散的结构、粗糙的表面和立体的金微米花结构(图2中的a
‑
d)赋予电极表面高比表面积和优异的传感导电性。gmfs均匀地覆盖了cc的表面,使构建的cc成为传感应用的理想选择。
[0053]
用xps表征了裸碳布材料的元素状态,揭示了c1s、o1s峰的存在。如图3所示c1s峰位于284.95ev,o1s位于531.71ev。这些峰识别了经过强酸处理后的碳布上具备氧元素,这些含氧基团(羟基和羧基)有助于在金表面上诱导大量氢氧根阴离子,从而提高葡萄糖感测中的脱氢速率。
[0054]
实施例2:葡萄糖的安倍分析
[0055]
1、以gmfs/cc作为柔性工作电极,铂丝电极作为对电极,ag/agcl电极作为参比电极。三个电极下端侵入至0.1m pbs液面同一高度下。打开chi 660e电化学工作站(上海辰华),分别连接三个电极,等待检测。
[0056]
2、gmfs/cc对葡萄糖的安培i
‑
t检测是在0.1m pbs缓冲液(ph 7.4)中连续注入葡萄糖(1μm至5mm)进行累加测试(表1)。电流响应随葡萄糖浓度的增加而增大,当葡萄糖浓度过高时,电流响应逐渐饱和。
[0057]
3、表1显示了相应的校准曲线。有两个线性区域:1μm到94μm(i=25.887x+0.0299,r2=0.9991);94μm到26664μm(i=18.981x+8.703,r2=0.9946)。检出限(lod)为0.70μm(s/n=3),相应校准曲线的具体数值如表1所示:
[0058]
表1.安培检测响应的拟合曲线数据
[0059]
浓度(μm)电流响应(μa)标准偏差浓度(μm)电流响应(μa)标准偏差10.0330.000577353649.040.03510460620.0680.00208166646411.6560.04118656730.10.00156414.2930.0587054850.1570.00115470176418.9620.05866003870.2160.0005773596423.5290.06900966190.2680.001732051116428.1290.007140.4070.025942244166439.230.003190.5210.02843120421645060.003240.6340.026274195266461.6960.005131601340.9230.025658007366483.670.009073772441.1860.0134288254664105.6220.393502647541.4610.0062449985664127.6560.12308669741.9750.0017664168.8560.2152974699424110.0152752529664208.6560.9979744491142.870.02409010911664247.921.4041874281644.0610.01436430816664336.5864.415731312145.250.02685764921664418.25212.336879442646.420.03251153626664486.91931.80767112
[0060]
其传感器线性范围的上限远远超出汗液(5.6μm
‑
2.77mm)和血液(3
‑
8mm)的生理水平,表明开发的电极可用于在生理和病理水平内测试葡萄糖。
[0061]
4、值得注意的是,本传感器的线性范围、低检测限和稳定性优于先前报告的在中性条件下检测的葡萄糖传感器,如表2所示:
[0062]
表2.中性条件下对葡萄糖的传感检测响应的性能比较
[0063][0064][0065]
这是因为cc上的含氧基团(羟基和羧基)诱导更多地au(oh)
ads
形成,促进葡萄糖氧化过程的脱氢速率,从而实现葡萄糖的灵敏检测。此外具有立体结构的金微米花不仅具有高比表面积,而且具有良好的导电性,促进了电极活性部位与葡萄糖之间的有效离子/电子转移。因此,gmfs/cc复合材料在葡萄糖分析领域具有广阔的应用前景。
[0066]
实施例3:葡萄糖检测的抗干扰、折叠和稳定性实验
[0067]
1、在人类的血液和汗液中,某些分子例如尿素(ua),乳酸(la),乙酸(aa)和抗坏血酸通常会干扰葡萄糖的测定。而在工业饮料中各种糖如木糖(xyl),麦芽糖(mal),蔗糖(suc)和果糖(fru)也会产生干扰。如图表3所示:
[0068]
表3.每种干扰物(0.2mm)分别与葡萄糖(1mm)混合检测的选择性实验
[0069]
样本名称浓度(mm)电流响应(μa)标准偏差glucose121.657333331.039487534glucose+urea0.221.936666670.790021097glucose+lactic acid0.220.553333330.453247541glucose+acetic acid0.219.566666671.230704405glucose+xylose0.220.163333331.36793031glucose+maltose0.227.303333331.632554236glucose+sucrose0.218.280.425088226glucose+fmctose0.217.153333331.092901337glucose+ascorbic acid0.224.623333331.256755081
[0070]
gmfs/cc对以上干扰化学品的反应很小。选择尿素(ua),乳酸(la),乙酸(aa),抗坏血酸,木糖(xyl),麦芽糖(mal),蔗糖(suc)和果糖(fru)评价gmfs/cc电极的抗干扰性能。将0.2mm干扰物种分别与1mm的葡萄糖混合以进行测试。如表3所示这些数据显示各种分子和各种糖都不影响葡萄糖的响应,结果证明了所提出的葡萄糖传感器具有良好的抗干扰能力。
[0071]
2、为了验证gmfs/cc的良好机械柔韧性,如图4所示将gmfs/cc弯曲,经过不同弯曲次数后在0.1m pbs溶液中检测葡萄糖。如表4所示经过200次弯曲后,电流响应保持在90.39%,如表4所示。表明弯曲对柔性gmfs/cc电极的催化性能影响很小。
[0072]
表4.不同弯曲次数(0、10、50、100、200)下的gmfs/cc对100μm葡萄糖的安倍响应
[0073]
折叠次数电流响应(μa)标准偏差02.6220.02548202102.60.025166115502.560.020816661002.490.0321455032002.370.064291005
[0074]
3、为了评估长期稳定性,每周测试gmfs/cc电极对0.1m pbs中100mm葡萄糖的电流响应(表5),电极之间在室温下保存。在暴露于空气中数天后,传感器的电流响应损失仅为12.6%(与原始电流相比)。所制备传感器的出色的长期稳定性可能归因于au的特性,该特性通过减轻中间物质的积累而有助于为活性位点提供稳定性。
[0075]
表5.gmfs/cc保持0
‑
35天后对100μm葡萄糖的电流响应
[0076]
稳定时间(天)电流响应(μa)标准偏差12.6113333330.00152752572.5516666670.042524503142.5243333330.02136196212.4956666670.076787586282.4303333330.098895568352.2833333330.030435725
[0077]
实施例4:人体汗液和血清真实样本检测
[0078]
在实际应用测试中,我们通过采用标准添加方法检测人汗液中的葡萄糖,进一步评估了gmfs/cc的可靠性。
[0079]
1、以gmfs/cc作为柔性工作电极,铂丝电极作为对电极,ag/agcl电极作为参比电极。三个电极下端侵入至0.1m pbs液面同一高度下。打开chi 660e电化学工作站(上海辰华),分别连接三个电极,等待检测。
[0080]
2、在汗液中加入已知浓度葡萄糖溶液,再加入pbs溶液进行检测,观察电流响应,使用此前得到的校正曲线计算出人汗液样品中的葡萄糖浓度。如数据摘要所示(表6),传感器测得的汗液葡萄糖水平与添加的葡萄糖浓度非常吻合,回收率在101.6
‑
108.7%之间。
[0081]
3、将构建的传感器可直接测定人血清样品中的葡萄糖含量。实验直接在pbs溶液中加入血液,观察电流响应,使用此前得到的校正曲线计算出人血清样品中的葡萄糖浓度,并通过市售血糖仪(三诺生物传感器有限公司)获得的值进行验证。结果总结在表6中,显示了90.0%至104.3%的良好回收率。这些观察结果表明,开发的葡萄糖生物传感器在分析人的汗液和人血清中的葡萄糖方面具有巨大的潜力。
[0082]
表6.对汗液和血液的实际应用检测
[0083]
样本名称浓度(μm)电流响应(μa)标准偏差汗液300.812917680.026汗液501.423571230.076汗液1002.67712490.053血液400078.87080.032血液450095.3580.037血液4700105.66250.037
[0084]
综上,本发明基于gmfs和cc的新型柔性葡萄糖传感器通过简单的恒电位沉积过程构建,并通过安培分析法用于分析人的汗液和血清中的葡萄糖浓度。其具有良好的电催化活性,宽的线性范围和出色的检出限。这归因于gmfs具有高比表面积和au(oh)
ads
的多活性位点。此外,该传感器具有良好抗干扰传感性能、柔韧性和稳定性。该方法对葡萄糖的高精度和高准确的检测使其在开发小型化的人体柔性葡萄糖传感器方面具有巨大的潜力。
[0085]
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1