紫地榆总鞣质对鼠急性胃溃疡保护作用的实验方法及应用
1.本发明属于紫地榆抗胃溃疡实验技术领域,具体是指紫地榆总鞣质对鼠急性胃溃疡保护作用的实验方法及应用。
背景技术:
2.紫地榆在大理白族等地区常用于治疗肠炎、痢疾等疾病,其具有的老鹳草素成分已有相关报道证明其抗氧化和抗炎能力,鞣料云实素、五没食子酰葡萄糖等,并且也有报道表明其抗胃溃疡的能力,但目前并没有明确的科学实验及技术检测对其证明。因此本发明拟选择昆明种小鼠为受试对象,探讨紫地榆鞣质类成分对阿司匹林和无水乙醇诱导的小鼠急性胃溃疡的保护作用。
技术实现要素:
3.针对上述情况,为克服现有技术的缺陷,本发明提供分别采用了阿司匹林和无水乙醇诱导小鼠急性胃溃疡模型,用来评价紫地榆总鞣质对胃溃疡的保护作用,这两个模型代表了人类胃溃疡的一些常见病因,同时通过实验结果,模型为药剂药量的使用及发展建立了参考的紫地榆总鞣质对鼠急性胃溃疡保护作用的实验方法及应用。
4.本发明采取的技术方案如下:本发明紫地榆总鞣质对鼠急性胃溃疡保护作用的实验方法,包括如下步骤:
5.步骤一、分组及造模
6.选取小鼠并随机分组,分别设置正常组、模型组、阳性对照组、紫地榆提取物低剂量组、紫地榆提取物中剂量组、紫地榆提取物高剂量组,适应性喂养一周后,正常组和模型组灌胃生理盐水(10ml/kg),阳性对照组灌胃2.0mg/ml的奥美拉唑悬浊液,紫地榆低剂量组灌胃总鞣质25mg/kg,中剂量组灌胃总鞣质50mg/kg,高剂量组灌胃总鞣质100mg/kg,每天给药1次,连续给药7天,在第7天给药完成1h后,按400mg/kg的剂量灌胃阿司匹林溶液,灌胃前禁食不禁水24h;
7.步骤二、取材
8.灌胃阿司匹林溶液后,各组小鼠继续禁食禁水饲养4h,4h后,摘掉小鼠眼球取血,所取的血液静置2h后,在4℃,4000r/min速度下离心10min,收集血清,
‑
20℃冰箱保存,再断颈处死小鼠,打开腹腔,取出胃,沿胃大弯剪开,用生理盐水洗净胃残留物,滤纸吸干,待测;
9.步骤三、溃疡指数评分
10.将各组小鼠洗净后的胃自然展开铺于白色洁净滤纸上,胃内面朝上,观察溃疡情况,拍照,用游标卡尺测量出血带长度和宽度,并按表3.1所示计算溃疡指数;
[0011][0012]
表3.1溃疡指数评分标准
[0013]
步骤四、胃组织样本前处理
[0014]
准确称取一半胃组织重量,按重量(g):体积(ml)=1:9的比例,加入9倍体积的生理盐水,匀浆,以3000转/分的速度,离心10min,取上清液,
‑
20℃冰箱保存,待测;
[0015]
步骤五、胃组织匀浆中总蛋白浓度定量
[0016]
精密量取步骤四中所得组织匀浆10μl于0.5ml离心管中,加入生理盐水190μl,用漩涡混匀器充分混匀,得到稀释20倍后的组织匀浆溶液,待测,采用bca微板法,根据蛋白定量试剂盒说明书操作步骤进行检测,记录吸光度值,按说明书上所列公式进行计算,蛋白定量(tp)生化试剂盒购自南京建成生物工程研究所;
[0017]
步骤六、胃组织中总超氧化物岐化酶(t
‑
sod)、丙二醛(mda)、一氧化氮(no)含量测定
[0018]
取胃组织匀浆,按试剂盒说明书操作步骤进行检测,记录吸光度值,按说明书上所列公式进行计算,超氧化物岐化酶(sod)、丙二醛(mda)、一氧化氮(no)生化试剂盒购自南京建成生物工程研究所;
[0019]
步骤七、胃组织中前列腺素e2(pge
‑
2)、血清中肿瘤坏死因子α(tnf
‑
α)含量测定
[0020]
采用elise法,按说明书所列流程测定组织中前列腺素e2(pge
‑
2)、血清中肿瘤坏死因子α(tnf
‑
α)含量;
[0021]
步骤八、统计
[0022]
采用spss 20.0统计软件进行分析,阿司匹林致小鼠急性胃溃疡和无水乙醇致小鼠急性胃溃疡阳性药组、紫地榆提取物低剂量组、紫地榆提取物中剂量组、紫地榆提取物高剂量组分别与正常组和模型组比较,采用单因素方差分析(one
‑
wayanova),用p<0.05代表具有显著统计学差异,p<0.01代表具有极显著统计学差异。
[0023]
本发明还提供了紫地榆总鞣质对鼠急性胃溃疡保护作用的实验方法的应用,应用于紫地榆总鞣质对胃溃疡保护作用实验。
[0024]
采用上述结构本发明取得的有益效果如下:本方案紫地榆总鞣质对鼠急性胃溃疡保护作用的实验方法及应用,分别采用了阿司匹林和无水乙醇诱导小鼠急性胃溃疡模型,用来评价紫地榆总鞣质对胃溃疡的保护作用,这两个模型代表了人类胃溃疡的一些常见病因,同时通过实验结果,模型为药剂药量的使用及发展建立了参考。
附图说明
[0025]
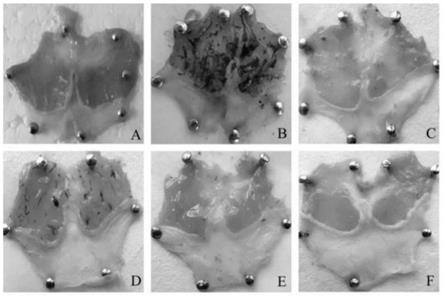
图1为本发明阿司匹林型小鼠急性胃溃疡的胃组织形态图;
[0026]
图2为本发明阿司匹林型小鼠急性胃溃疡的胃组织病理切片图;
[0027]
图3为本发明乙醇型小鼠急性胃溃疡的胃组织形态;
[0028]
图4为本发明乙醇型小鼠急性胃溃疡的胃组织病理切片图。
[0029]
其中,a、正常组,b、模型组,c、阳性对照组,d、紫地榆提取物低剂量组,e、紫地榆提取物中剂量组,f、紫地榆提取物高剂量组。
[0030]
附图用来提供对本发明的进一步理解,并且构成说明书的一部分,与本发明的实施例一起用于解释本发明,并不构成对本发明的限制。
具体实施方式
[0031]
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例;基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0032]
分组及造模
[0033]
将将48只小鼠随机分为6组,每组8只,分别为正常组、模型组、阳性对照组、紫地榆提取物低剂量组、紫地榆提取物中剂量组、紫地榆提取物高剂量组,适应性喂养一周。
[0034]
实施例1
[0035]
正常组灌胃生理盐水(10ml/kg),每天给药1次,连续给药7天。在第7天给药完成1h后,按400mg/kg的剂量灌胃阿司匹林溶液,灌胃前禁食不禁水24h。
[0036]
实施例2
[0037]
模型组灌胃生理盐水(10ml/kg),每天给药1次,连续给药7天。在第7天给药完成1h后,按400mg/kg的剂量灌胃阿司匹林溶液,灌胃前禁食不禁水24h。
[0038]
实施例3
[0039]
阳性对照组灌胃2.0mg/ml的奥美拉唑悬浊液,每天给药1次,连续给药7天,在第7天给药完成1h后,按400mg/kg的剂量灌胃阿司匹林溶液,灌胃前禁食不禁水24h。
[0040]
实施例4
[0041]
紫地榆提取物低剂量组灌胃总鞣质25mg/kg,每天给药1次,连续给药7天,在第7天给药完成1h后,按400mg/kg的剂量灌胃阿司匹林溶液,灌胃前禁食不禁水24h。
[0042]
实施例5
[0043]
紫地榆提取物中剂量组灌胃总鞣质50mg/kg,每天给药1次,连续给药7天,在第7天给药完成1h后,按400mg/kg的剂量灌胃阿司匹林溶液,灌胃前禁食不禁水24h。
[0044]
实施例6
[0045]
紫地榆提取物高剂量组灌胃总鞣质100mg/kg,每天给药1次,连续给药7天,在第7天给药完成1h后,按400mg/kg的剂量灌胃阿司匹林溶液,灌胃前禁食不禁水24h。
[0046]
实施例1
‑
6中小鼠灌胃阿司匹林溶液后,小鼠继续禁食禁水饲养4h,4h后,摘掉小鼠眼球取血,所取的血液静置2h后,在4℃,4000r/min速度下离心10min,收集血清,
‑
20℃冰箱保存,再断颈处死小鼠,打开腹腔,取出胃,沿胃大弯剪开,用生理盐水洗净胃残留物,滤纸吸干,待测,将各组小鼠洗净后的胃自然展开铺于白色洁净滤纸上,胃内面朝上,观察溃疡情况,拍照,用游标卡尺测量出血带长度和宽度,并按表3.1所示计算溃疡指数,准确称取一半胃组织重量,按重量(g):体积(ml)=1:9的比例,加入9倍体积的生理盐水,匀浆,以3000转/分的速度,离心10min,取上清液,
‑
20℃冰箱保存,待测,精密量取所得组织匀浆10μ
l于0.5ml离心管中,加入生理盐水190μl,用漩涡混匀器充分混匀,得到稀释20倍后的组织匀浆溶液,待测。采用bca微板法,根据蛋白定量试剂盒说明书操作步骤进行检测,记录吸光度值。按说明书上所列公式进行计算,取胃组织匀浆,按试剂盒说明书操作步骤进行检测,记录吸光度值。按说明书上所列公式进行计算。采用elise法,按说明书所列流程测定组织中前列腺素e2(pge
‑
2)、血清中肿瘤坏死因子α(tnf
‑
α)含量。采用spss 20.0统计软件进行分析,阿司匹林致小鼠急性胃溃疡和无水乙醇致小鼠急性胃溃疡阳性药组、紫地榆总鞣质低、中、高组分别与正常组和模型组比较,采用单因素方差分析(one
‑
way anova),用p<0.05代表具有显著统计学差异,p<0.01代表具有极显著统计学差异。
[0047]
结果
[0048]
1.造模给药后小鼠行为学考察
[0049]
阿司匹林致小鼠急性胃溃疡模型,给药阿司匹林后,各组小鼠与正常组相比无明显差异,均正常;无水乙醇致小鼠急性胃溃疡模型,给药无水乙醇后,与正常组相比,模型组、阳性药奥美拉唑组、紫地榆总鞣质低剂量组、紫地榆总鞣质中剂量组、紫地榆总鞣质高剂量组均出现不同程度的精神萎靡,步履不稳,嗜睡等现象,其中,模型组出现小鼠死亡现象,死亡两只。
[0050]
2.小鼠胃形态学观察
[0051]
2.1阿司匹林型小鼠急性胃溃疡的胃组织形态观察比较
[0052]
胃组织形态如图1,正常组如图1(a)所示,模型组如图1(b)所示,与正常组相比,模型组胃部呈现明显的坏死现象,未见出血,紫地榆总鞣质低剂量组溃疡坏死现象明显改善,但还是存在一定的溃疡坏死情况,如图1(c、e、f)所示,阳性药组和紫地榆总鞣质中、高剂量组基本无溃疡坏死现象。病理切片见图2,如图2(a)所示,正常组小鼠胃粘膜结构完整,上层细胞排列整齐。如图2(b)所示,模型组上皮细胞脱落,有出血现象,如图2(c、e、f)所示,阳性药组和总鞣质中、高剂量组上皮结构完整,细胞排列整齐,基本无出血现象和炎症细胞浸润,如图2(d)所示,总鞣质低剂量组上皮结构基本完整,粘膜层有一定出血现象。
[0053]
2.2乙醇型小鼠急性胃溃疡的胃组织形态观察比较
[0054]
胃组织形态见图3,正常组如图3(a)所示,模型组如图3(b)所示,与正常组相比,模型组胃部呈现明显的出血现象,有大面积的溃疡,甚至存在胃穿孔现象,如图3(c)所示,阳性药组水肿、溃疡、坏死状况明显改善,无大面积出血,有少量线状血丝,如图3(d)所示,总鞣质低剂量组溃疡、坏死现象较模型组减轻,但仍存在出血和水肿现象,点状出血点极多并有带状出血,面积较大,如图3(e、f)所示,总鞣质中、高剂量组溃疡、坏死现象明显改善,呈现轻微水肿,少量出血点。病理切片见图4,如图4(a)所示,正常组小鼠胃粘膜结构完整,上层细胞排列整齐,模型组如图4(b)所示,与正常组相比,胃粘膜损坏,不完整,腺体结构消失,炎症细胞浸润,如图4(c、e、f)所示,阳性药组和总鞣质中、高剂量组上皮结构完整,细胞排列整齐,基本无出血现象和炎症细胞浸润,如图4(d)所示,总鞣质低剂量组上皮结构基本完整,粘膜层有一定出血现象。
[0055]
3.紫地榆总鞣质对阿司匹林致小鼠急性胃溃疡保护作用溃疡指数
[0056]
与模型组相比,紫地榆总鞣质低剂量组溃疡指数下降,差异显著,阳性药组和紫地榆总鞣质中、高剂量组溃疡指数均下降,差异极显著,结果如表3.2所示。
[0057][0058]
表3.2紫地榆总鞣质对阿司匹林致小鼠急性胃溃疡溃疡指数注:与正常组相比,*p<0.05,**p<0.01;与模型组相比,
#
p<0.05,
##
p<0.01。
[0059]
4.紫地榆总鞣质对阿司匹林致小鼠急性胃溃疡保护作用血清中tnf
‑
α及组织中pge
‑
2水平测定结果
[0060]
与正常组相比,模型组tnf
‑
α含量显著上升(p<0.01),与模型组相比,阳性药组和紫地榆总鞣质低、中、高剂量组tnf
‑
α含量显著下降(p<0.05或p<0.01),与正常组相比,模型组pge
‑
2含量显著下降(p<0.01),与模型组相比,阳性药组和紫地榆总鞣质低、中、高剂量组pge
‑
2含量均显著上升(p<0.05或p<0.01),结果如表3.3所示。
[0061][0062][0063]
表3.3紫地榆总鞣质对阿司匹林致小鼠急性胃溃疡tnf
‑
α及pge
‑
2水平测定结果
[0064]
注:与正常组相比,*p<0.05,**p<0.01;与模型组相比,
#
p<0.05,
##
p<0.01。
[0065]
5.紫地榆总鞣质对阿司匹林致小鼠急性胃溃疡保护作用组织中sod、mda、no水平测定结果
[0066]
与正常组相比,模型组sod含量显著下降(p<0.01),与模型组相比,阳性药组和紫地榆总鞣质低、中、高剂量组sod含量显著上升(p<0.05或p<0.01),与正常组相比,模型组mda、no含量显著上升(p<0.01),与模型组相比,阳性药组和紫地榆总鞣质低、中、高剂量组mda、no含量均显著下降(p<0.05或p<0.01),结果如表3.4所示。
[0067][0068]
表3.4紫地榆总鞣质对阿司匹林致小鼠急性胃溃疡sod、mda及no水平测定结果
[0069]
注:与正常组相比,*p<0.05,**p<0.01;与模型组相比,
#
p<0.05,
##
p<0.01。
[0070]
6.紫地榆总鞣质对无水乙醇致小鼠急性胃溃疡保护作用溃疡指数
[0071]
与模型组相比,紫地榆总鞣质低剂量组溃疡指数下降,差异显著,阳性药组和紫地榆总鞣质中、高剂量组溃疡指数均下降,差异极显著,结果如表3.5所示。
[0072][0073]
表3.5紫地榆总鞣质对无水乙醇致小鼠急性胃溃疡溃疡指数
[0074]
注:与正常组相比,*p<0.05,**p<0.01;与模型组相比,
#
p<0.05,
##
p<0.01。
[0075]
7.紫地榆总鞣质对无水乙醇致小鼠急性胃溃疡保护作用血清中tnf
‑
α及组织中pge
‑
2水平测定结果
[0076]
与正常组相比,模型组tnf
‑
α含量显著上升(p<0.01),与模型组相比,阳性药组和紫地榆总鞣质低、中、高剂量组tnf
‑
α含量显著下降(p<0.05或p<0.01),与正常组相比,模型组pge
‑
2含量显著下降(p<0.01),与模型组相比,阳性药组和紫地榆总鞣质低、中、高剂量组pge
‑
2含量均显著上升(p<0.05或p<0.01),结果如表3.6所示。
[0077][0078][0079]
表3.6紫地榆总鞣质对无水乙醇致小鼠急性胃溃疡tnf
‑
α及pge
‑
2水平测定结果
[0080]
注:与正常组相比,*p<0.05,**p<0.01;与模型组相比,
#
p<0.05,
##
p<0.01。
[0081]
8.紫地榆总鞣质对无水乙醇致小鼠急性胃溃疡保护作用组织中sod、mda、no水平测定结果
[0082]
与正常组相比,模型组sod含量显著下降(p<0.01),与模型组相比,阳性药组和紫地榆总鞣质低、中、高剂量组sod含量显著上升(p<0.05或p<0.01),与正常组相比,模型组mda、no含量显著上升(p<0.01),与模型组相比,阳性药组和紫地榆总鞣质低、中、高剂量组mda、no含量均显著下降(p<0.05或p<0.01),结果如表3.7所示。
[0083][0084]
表3.7紫地榆总鞣质对无水乙醇致小鼠急性胃溃疡sod、mda及no水平测定结果
[0085]
注:与正常组相比,*p<0.05,**p<0.01;与模型组相比,
#
p<0.05,
##
p<0.01。
[0086]
结论
[0087]
本发明分别采用了阿司匹林和无水乙醇诱导小鼠急性胃溃疡模型,用来评价紫地榆总鞣质对胃溃疡的保护作用,这两个模型代表了人类胃溃疡的一些常见病因,实验结果表明紫地榆总鞣质对阿司匹林诱导的急性胃溃疡和无水乙醇诱导的急性胃溃疡具有显著的保护作用,紫地榆总鞣质低、中、高剂量组均体现出一定的抗胃溃疡活性,其中中、高剂量组效果明显优于低剂量组。
[0088]
在实验过程中,造模时考察了灌胃无水乙醇5ml/kg和10ml/kg,灌胃阿司匹林混悬
液200mg/kg和400mg/kg,无水乙醇给药剂量为5ml/kg时,小鼠胃组织无明显损伤,胃粘膜基本未见溃疡坏死,各生化指标无明显差别,同样,阿司匹林混悬液给药剂量为200mg/kg时,小鼠胃组织未见明显损伤,胃粘膜也基本无溃疡坏死,各生化指标无明显差别。因此,分别选择10ml/kg和400mg/kg的给药剂量。考察了小鼠分别灌胃无水乙醇和阿司匹林混悬液之前禁食时间,分别为12h和24h,结果发现,禁食12h时,小鼠胃排空较差,胃内容物较多,一定情况下减少了无水乙醇和阿司匹林混悬液与胃壁的接触,对造模的结果产生影响,在禁食24h后,胃排空明显改善,因此选择禁食24h。紫地榆总鞣质可以显著降低阿司匹林和无水乙醇诱导的胃溃疡的过氧化反应,通过下调mda水平和上升sod水平,达到保护胃粘膜的作用,还可以通过减少炎症因子no和tnf
‑
α的分泌,最终促进pge
‑
2的生成,且呈现剂量依赖关系,体现了良好的抗炎和抗氧化作用。
[0089]
需要说明的是,在本文中,诸如第一和第二等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。
[0090]
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
[0091]
以上对本发明及其实施方式进行了描述,这种描述没有限制性,附图中所示的也只是本发明的实施方式之一,实际的结构并不局限于此。总而言之如果本领域的普通技术人员受其启示,在不脱离本发明创造宗旨的情况下,不经创造性的设计出与该技术方案相似的结构方式及实施例,均应属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1