髓母细胞瘤/细胞标志物及其应用
1.本发明属于肿瘤诊断/预后的试剂制备技术领域,具体涉及一种髓母细胞瘤/细胞标志物及其应用。是基于gpr37蛋白、rab35蛋白、rps10蛋白、nudt3蛋白、usp6nl蛋白、rere 蛋白、cacybp蛋白、ckap5蛋白中的一种或多种的smo激活性突变性的髓母细胞瘤/细胞中的蛋白研究及应用。
背景技术:
2.hedgehog(hh)信号通路在维持胚胎发育和成体组织稳态平衡中起重要的作用,hh通路一旦发生异常调控,就会产生机体缺陷或者肿瘤等。在许多肿瘤中hh信号通路都异常活跃,其中smo是hh信号通路中关键的信号转导分子,靶向smo已经成为药物研究热点。目前已有smo抑制剂进入临床使用治疗各种肿瘤,如vismodegib(gdc
‑
0449)已经被批准用于治疗晚期和转移性基底细胞癌。虽然不少肿瘤患者接受gdc
‑
0449治疗后,临床治疗获得显著益处,但是也有些患者容易会产生耐药性。对这些耐药患者进行基因组分析,发现gdc
‑
0449 耐药性与hh通路再活化有关,主要是smo发生突变,导致smo持续表达,hh信号通路激活,导致药物作用失效。这些突变体主要有smo
‑
w535l和smo
‑
d473h等,其中smo
‑
w535l突变体不需要hh激活就可以自我持续激活,smo
‑
d473h破环了gdc
‑
0449药物与smo相互作用结合靶点。国内外大量的研究工作,主要还是集中于利用模式生物果蝇,研究果蝇smo的各种翻译后修饰作用;而对于smo如何直接传导生物信号,与哪些蛋白质直接发生相互作用研究的比较少。smo
‑
w535l和smo
‑
d473h等突变体与野生型smo之间直接传导信号通路的蛋白质存在怎么样的差异性都不清楚。
3.髓母细胞瘤/细胞是人颅内的一种恶性肿瘤,找到一种简单、方便、精准的诊断/预后试剂是势在必行。但是现在鲜有通过蛋白层面进行肿瘤/肿瘤细胞进行诊断/预后的试剂,如果不知道smo之间直接传导信号通路的蛋白质的情况,就无法准确的通过蛋白层面制备试剂去诊断/预后肿瘤/肿瘤细胞。
技术实现要素:
4.有鉴于此,本发明检测了smo激活性突变型髓母细胞瘤/细胞的特异性蛋白表达,通过这些蛋白的表达可以制备髓母细胞瘤/细胞诊断/预后的试剂。
5.本发明目的在于提供一种髓母细胞瘤/细胞检测试剂盒或检测试剂,包括:gpr37蛋白、 rab35蛋白、rps10蛋白、nudt3蛋白、usp6nl蛋白、rere蛋白、cacybp蛋白、ckap5蛋白中的一种或多种的特异性结合物。
6.优选地,所述髓母细胞瘤/细胞为smo突变型髓母细胞瘤/细胞。
7.优选地,所述smo突变型髓母细胞瘤/细胞为smo w535l突变型髓母细胞瘤/细胞。
8.具体地,所述髓母细胞瘤/细胞检测试剂盒或检测试剂可以直接以患者的体液作为检测样品。
9.在某些具体实施中,通过韦恩和gliovis分析患者生存曲线发现gpr37、rab35、
rps10、 nudt3、usp6nl、rere、cacybp、ckap5八个蛋白与髓母细胞瘤的生存期负相关。
10.具体地,所述特异性结合物可以是特异性结合蛋白,也可以是一些与这些蛋白结合产生物理或化学变化的化学试剂。
11.本发明目的之二在于提供一种gpr37蛋白、rab35蛋白、rps10蛋白、nudt3蛋白、usp6nl 蛋白、rere蛋白、cacybp蛋白、ckap5蛋白中的一种或多种的特异性结合物在制备诊断/预后髓母细胞瘤/细胞的产品中的应用,所述产品包括试剂盒、试剂、芯片。
12.具体地,所述试剂盒包括pcr荧光试剂盒、pcr试剂盒、elisa试剂盒等;所述试剂包括荧光探针、引物等;所述芯片包括基因芯片和蛋白表达芯片。
13.优选地,所述应用包括:使用所述产品检测所述gpr37蛋白、rab35蛋白、rps10蛋白、 nudt3蛋白、usp6nl蛋白、rere蛋白、cacybp蛋白、ckap5蛋白中的一种或多种的含量,所述含量与所述髓母细胞瘤/细胞的生存呈负相关。
14.具体地,所述特异性结合物可以是特异性结合蛋白,也可以是一些与这些蛋白结合产生物理或化学变化的化学试剂。
15.优选地,所述髓母细胞瘤/细胞为smo突变型髓母细胞瘤/细胞。
16.优选地,所述smo突变型髓母细胞瘤/细胞为smo w535l突变型髓母细胞瘤/细胞。
17.本发明目的在于还提供一种(a)gpr37蛋白、rab35蛋白、rps10蛋白、nudt3蛋白、 usp6nl蛋白、rere蛋白、cacybp蛋白、ckap5蛋白中的一种或多种的特异性结合物或(b) rab10蛋白、rheb蛋白、pfkp蛋白、prkaa1蛋白、pkm蛋白、tpi蛋白1、csnk2b蛋白、cdk1 蛋白、pfkp蛋白中的一种或多种的抑制剂在制备髓母细胞瘤/细胞抑制剂中的应用。
18.在某些具体实施例中,ons76
‑
w535l(lde225/sag)中smo的ip中独立的蛋白进行davidfunctional annotation bioinformatics microarray analysis分析,这些蛋白富集于ampk signaling pathway和glycolysis/gluconeogenesis信号通路。进一步,对其中的激酶分析,联合靶向rab10蛋白、rheb蛋白、pfkp蛋白、prkaa1蛋白、pkm蛋白、tpi1蛋白、csnk2b 蛋白、cdk1蛋白等,是靶向治疗耐药性髓母细胞瘤的靶点。
19.具体地,所述特异性结合物可以是特异性结合蛋白,也可以是一些与这些蛋白结合产生物理或化学变化的化学试剂。
20.优选地,所述髓母细胞瘤为som突变耐药性髓母细胞瘤/细胞。
21.优选地,所述som突变耐药性髓母细胞瘤为smo w535l突变耐药型髓母细胞瘤/细胞。
22.本发明中,所涉及的英文或中文专业技术的词汇,如“smo”“gpr37蛋白”“pfkp蛋白”“w535l突变型”等,均为本领域技术人员的常规用语,非特别含义用语。
23.本发明中,所述涉及到的生物信息分析工具均是本领域技术人员常用的分析工具,无本领域技术人员不知晓的分析工具。
24.本发明中,符号“/”代表或的意思,如髓母细胞瘤/细胞的意思为:可以是髓母细胞瘤,也可以是髓母细胞。
25.本发明有益效果在于
26.本发明提供的髓母细胞瘤/细胞检测试剂盒或检测试剂,能更加简单、方便、精准的诊断/预后髓母细胞瘤/细胞,特别是更加更加精确地筛选出耐药性髓母细胞瘤/细胞,更好对症下药。
27.本发明提供的rab10、rheb、pfkp、prkaa1、pkm、tpi1、csnk2b、cdk1、pfkp中的一种或多种的抑制剂更加精准的靶向smo耐药性髓母细胞瘤/细胞,减缓其耐药性进行用药。
附图说明
28.图1为ons76
‑
52 wb化学发光显影图。
29.图2为ons76
‑
53 wb化学发光显影图。
30.图3为ons76
‑
54 wb化学发光显影图。
31.图4为ons76
‑
w535l(lde225/sag)与ons76
‑
wt(lde225/sag)的韦恩(venn)图。
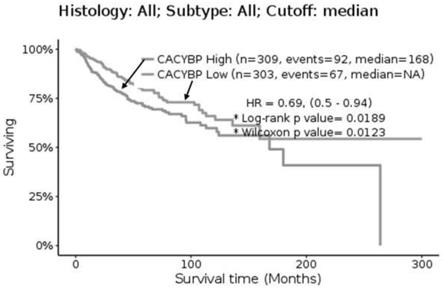
32.图5为gliovis分析cacybp蛋白与髓母细胞瘤的生存期相关性。
33.图6为gliovis分析ckap5蛋白与髓母细胞瘤的生存期相关性。
34.图7为gliovis分析gpr37蛋白与髓母细胞瘤的生存期相关性。
35.图8为gliovis分析nudt3蛋白与髓母细胞瘤的生存期相关性。
36.图9为gliovis分析rab35蛋白与髓母细胞瘤的生存期相关性。
37.图10为gliovis分析rere蛋白与髓母细胞瘤的生存期相关性。
38.图11为gliovis分析rps10蛋白与髓母细胞瘤的生存期相关性。
39.图12为gliovis分析usp6nl蛋白与髓母细胞瘤的生存期相关性。
具体实施方式
40.所举实施例是为了更好地对本发明进行说明,但并不是本发明的内容仅局限于所举实施例。所以熟悉本领域的技术人员根据上述发明内容对实施方案进行非本质的改进和调整,仍属于本发明的保护范围。
41.本发明实施例中,生物安全柜来自美国赛默飞(thermo scientific);细胞培养箱来自美国赛默飞(thermo scientific);高速离心机st 8r来自美国赛默飞(thermoscientific);mini
‑
protean tetra system来自美国bd公司;orbital shaker ts
‑
100摇床来自海门市其林贝尔仪器制造有限公司;chemidoc mp imaging system来自美国bio
‑
rad 公司;heal force超纯水系统来自香港力康生物医疗科技控股集团。
42.本发明实施例中,使用的材料包括:髓母细胞瘤ons76
‑
52,ons76
‑
53,ons76
‑
54细胞, lde225,sag(sag(hedgehog/smoothened激动剂)),ge protein g mag sepharose,flag m2 抗体(sigma monoclonal),mouse igg(satacruz lot#j2015),silver stain plus(catalognumber#161
‑
0449)等。
43.本发明实施例中,使用的ip裂解液配方(10ml 1%triton x
‑
100裂解液)如表1。
44.表1 ip裂解液配方
45.原料原液体积(μl)10%甘油100%200050mm tris
‑
cl(ph 7.5)1m1000150mm nacl5m6001%triton x
‑
100100%2001mm ddt1.25m16pmsf100*200
phosphostop inhibitor10*2000complete inhibitor25*800ddh2o100%13184
46.本发明实施例中,western blotting实验步骤为:
47.①‑
80℃冰箱取出的蛋白样品放置4℃冰上,融化后高速离心机4℃,20000g高速离心 5分钟;同时按照tgx stain
‑
free fastcast acrylamide kit,10%(cat.#161
‑
1083)使用说明书配置凝胶;配置1
×
running buffer电泳液(每l含25mm tris、192mm glycine和 0.1%sds),混匀;
48.②
用清水反复冲洗洗净跑胶需要使用的盒子和架子,使用配置好凝胶的玻板组装好设备,需要注意凝胶的玻板和架子之间的紧密结合,其是防止电泳过程中漏液的关键步骤;电泳槽中慢慢倒入混匀好的1
×
running buffer电泳液,最后富含气泡的电泳液体不要倒入中间玻板之间的槽内;
49.③
把加热好的蛋白样品依次加入凝胶玻板里面,完成加样后样品立刻放回冰箱继续保存;加样过程中,枪头一定要从加样孔的上方中间垂直插入,从靠近加样孔的底部位置缓慢开始加入样品,并且要随着样品的不断地加入加样孔过程,不断地将移液枪往上提,从而始终保持移液枪枪头口在刚加入的样品液面上方,这样以免最后排出样品时会产生一些气泡将加入的蛋白样品带出刚加入的加样孔(这是非常重要的加样步骤);
50.④
记录好加样的顺序,并用loading marker的量和顺序标记好凝胶的方位,插好电源,先80v恒压15分钟,再用120v恒压跑胶50分子左右,直到loading buffer中的溴芬蓝指示液到了底部凝胶边缘,停止跑胶;
51.⑤
用清水反复洗净所有将要使用的设备,包括:转膜使用的架子、盒子、绿色的取胶片、白色滤纸和黑色海绵等;白色的滤纸和黑色的海绵分别浸泡在不同的清水中待用;
52.⑥
配制电泳转膜缓冲液,1l需要加200ml甲醇和100ml 10
×
tris/glycine buffer,然后补充水至1l;裁好的pvdf膜放置于甲醇中泡5分钟左右,再转至刚配制好的转膜缓冲液里面浸泡;
53.⑦
将待转膜的架子放置于大量清水里面,打开摆放好,白色在下面黑色朝上面,再依次放置一张黑色的海绵、两张白色的滤纸和浸泡好的pvdf膜(平头镊子取);
54.⑧
用配制的撬胶器轻轻地取出凝胶,用绿色的取胶片裁去除掉多余部分,以便凝胶方便展平,先将凝胶放置于转膜缓冲液,再转移放置上步准备的pvdf膜上;再依次在pvdf膜上放一张张白色的滤纸、一张黑色的海绵,注意整个实验过程中一定不能产生气泡。注意,滤纸尽量使用新的,如果滤纸用的次数太多会产生一些碎屑,这些会影响转膜的效果,所以一定要将使用的滤纸先用清水洗净浸泡好。如果产生一些明显碎屑,需要丢掉更换新的滤纸。
55.⑨
使用清洗过的滚棒轻轻地滚动摆放好的转膜体系,赶出可能存在转膜体系中的气泡,再把加架子慢慢合起来扣好,从清水中拿出转膜体系,待流掉多余的清水后,转到转膜缓冲液中浸泡,等待下一张凝胶的安装。再一起将两张转膜架子放到放了转膜液的转膜盒子里,转膜架子的白色对转膜盒子白色,黑色对着黑色,倒入足量的转膜缓冲液充满整个转膜盒子,并加入存放在
‑
20℃预冰过的冰盒,然后插好电源,在整个盒子埋放在冰水混合物中,360man 的电流转膜2小时。
56.⑩
转膜结束后,转移至5%的脱脂奶粉中封闭1小时,先在pbs缓冲液中轻轻漂洗两次,再去除pbs缓冲液,加入第一抗体稀释液(根据产品说明稀释倍数),4℃冰箱里的摇床上轻轻地晃动,第二天回收第一抗体稀释液,再用pbs缓冲液中轻轻漂洗三次,每次15分钟,然后加同样属性的第二抗体稀释液,常温孵育1小时,再用pbs缓冲液中轻轻漂洗三次,每次15分钟。显影仪曝光显影及其对图片进行定量分析。
57.本发明实施例中,聚丙烯酰胺凝胶染色程序为:
58.①
聚丙烯酰胺凝胶固定步骤
59.凝胶电泳后,把聚丙烯酰胺凝胶放在加了固定增强剂溶液(见表2)的容器里面,放置于摇床上轻轻地摇,将凝胶固定20分钟;
60.表2固定增强剂溶液制备
61.甲醇100ml50%v/v乙酸20ml10%v/vfixative enhancer concentrate20ml10%v/vddh2o60ml30%v/v总共200ml100%v/v
62.②
冲洗步骤
63.把固定增强剂溶液从容器中倒掉。容器中加入200ml去离子双纯蒸馏水冲洗10分钟。10 分钟后,倒掉去离子双纯蒸馏水,更换新鲜的去离子双纯蒸馏水继续再冲洗10分钟。
64.③
银染
65.使用配置好的银染溶液(见表3)中立刻添加50ml development accelerator solution, 轻轻地混合好添加入凝胶的容器里,然后容器放置于摇床上缓慢地摇动。放置15分钟左右,根据经验终止银染;
66.表3银染溶液的制备
67.ddh2o35.0mlsilver complex solution5.0mlreduction moderator5.0mlimage development reagent5.0ml
68.④
终止银染
69.立刻倒掉银染试剂,5%的乙酸,维持15分钟,然后倒掉用100ml ddh2o双纯水清洗两次,每次10分钟。
70.本发明实施例中,ip实验过程为:
71.①
对收集的ons76
‑
52,53,54细胞(52为smo w535l突变型,53为smo d473h突变型, 54为smo wild type)(每种处理组细胞共收了2皿细胞),用新鲜配置的裂解液(用前补加 25
×
complete inhibitor、10
×
phosphostop inhibitor和100
×
pmsf)在冰上裂解细胞,每管细胞加800μl ip裂解液,添加过程中用移液枪上下反复吸裂解液充分打撒细胞,每隔 10分钟取出上下颠倒几次,冰上放置30分钟;4℃条件下高速离心机25000g离心15min,离心结束后转移上清液至新ep管中做预清除;
72.②
先取共约150μl*4磁珠,先用不含抑制剂的裂解液洗一遍,再用150μl*4裂解液重悬磁珠,再将装ons76
‑
w535l,d473h,wt蛋白的12个ep管中分别加入20μl磁珠预清除处理
(*使用200μl的黄色枪头前需要用剪刀剪掉一小节,以免破环磁珠),4℃旋转一个小时;同时再取90μl*4磁珠加12μl*4flag m2抗体形成磁珠
‑
抗体复合物4℃旋转一个小时;
73.③
取预清除后装蛋白的ep管放置于磁力架上,轻轻地吸取上清液至新的ep管中,磁珠裂解液冲洗后,再加100μl pbs(含0.5%的nan3)重悬4℃保存;
74.④
预清除后的ons76
‑
w535l,d473h,wt共12管上清蛋白液,每管取出80μl做input,剩余的720μl上清液,再各取出55μl混合在一起共660μl做igg对照;
75.⑤
剩余665μl的ons76
‑
w535l,d473h,wt 12管上清蛋白液中分别加入32μl上述处理好的磁珠
‑
抗体复合物,igg对照组中加入上述所有的磁珠
‑
igg复合物,4℃旋转2小时;
76.⑥
将上述ons76
‑
w535l,d473h,wt 12个ep管和igg对照组的ep管放置于磁力架上,轻轻吸取上清液做elution,再用1ml裂解液清洗磁珠,15min*3,4℃旋转,每次洗过的上清液都丢弃;pbs清洗磁珠2min*5,每次使用1ml pbs,4℃旋转,保留磁珠,最后一次用 1ml pbs重悬后,每管都取200μl分一管,800μl分一管,放置磁力架上吸干pbs后,分装200μl磁珠的ep管吸干液体后加50μl 1*loading,分装800μl磁珠的ep管吸干液体后放置
‑
80℃冰箱待送样检测;
77.⑦
input和elution分别加入26.7μl,192μl 4*loading;
78.⑧
进行western blotting。
79.本发明实施例中,磁珠
‑
抗体复合物及预前准备工作为:90μl(30μl*3)磁珠(geprotein g mag sepharose)+9μl(3μl*3)flag m2抗体(sigma monoclonal)*4;30μ l磁珠+10μl mouse igg(satacruz lot#j2015)*4;预清除:60μl磁珠(20μl*3) *4。
80.实施例1
81.(1)细胞处理及实验分组
82.生长状态良好的第3
‑
10代髓母细胞传代,第二天饥饿12小时后,更换新的无血清培养基,每种细胞各8皿,先分六个组实验如表4,24小时后再每个小组分成sag刺激组与非 sag刺激组如表5。
83.表4细胞处理分组
[0084][0085]
表5 ip实验分组
[0086]
[0087][0088]
(2)进行ip实验,在进行western blotting过程时,同时跑两块胶,上样量都是一样的,input和ip的上样量都是6μl每个样品,elution上样量20μl。一块胶做银染,另一块做wb化学发光显影(一抗flag
‑
m2),wb化学发光显影如图1
‑
图3所示。
[0089]
实施例2
[0090]
结合实施例1,对ons76
‑
w535l(lde225/sag)与ons76
‑
wt(lde225/sag)进行韦恩(venn) 分析,结果如图4所示:ons76
‑
w535l(lde225/sag)中smo蛋白质ip下拉的蛋白质中有65 个是ons76
‑
w535l特有的蛋白质,如:pfkp、pkm、prkaa1等;有117个蛋白质在ons76
‑
w535l 与ons76
‑
wt中都共同拥有,如激酶:cdc42bpa、csnk2b、cdk1、dapk3等;有65个 ons76
‑
w535l(lde225/sag)独立的蛋白。
[0091]
对有65个ons76
‑
w535l(lde225/sag)独立的蛋白进行david functional annotationbioinformatics microarray analysis分析,结果如表6,7,8所示,endocytosis,ampksignaling pathway,glycolysis/gluconeogenesis等通路在ons76
‑
w535l(lde225/sag)异常激活。特别是ampk signaling pathway和glycolysis/gluconeogenesis信号通路中的 rab10、rheb、pfkp、prkaa1、pkm、tpi1都是治疗靶向耐药性w535l型髓母细胞瘤的靶蛋白。
[0092]
表6 david functional annotation bioinformatics microarray analysis分析
[0093]
categorytermcount%p
‑
valuekegg_pathwayendocytosis6108.80e
‑
03kegg_pathwayampk signaling pathway46.72.80e
‑
02kegg_pathwayglycolysis/gluconeogenesis355.00e
‑
02kegg_pathwaybiosynthesis of amino acids355.70e
‑
02
[0094]
表7 ampk signaling pathway
[0095][0096]
表8 glycolysis/gluconeogenesis
[0097]
entrez_gene_idgene namespecies5214phosphofructokinase,platelet(pfkp)homo sapiens5315pyruvate kinase,muscle(pkm)homo sapiens7167triosephosphate isomerase 1(tpi1)homo sapiens
[0098]
对ons76
‑
w535l lde225/sag ip中独立的65个蛋白进行gliovis分析患者生存曲线发现gpr37、rab35、rps10、nudt3、usp6nl、rere、cacybp、ckap5八个蛋白的表达与髓母细胞瘤的生存期负相关(如图5
‑
图12所示)。
[0099]
实施例3
[0100]
对ons76
‑
w535l(dmso/sag)与ons76
‑
wt(dmso/sag)韦恩(venn)分析,ons76
‑
w535l(dmso/sag)中smo蛋白ip下拉的蛋白质有39个是其独特的蛋白质; ons76
‑
w535l(dmso/sag)与ons
‑
wt(dmso/sag)中smo共同拉下拉的蛋白45个。
[0101]
对39个ons76
‑
52 dmso/sag独立的蛋白进行david functional annotationbioinformatics microarray analysis分析,分析结果如表9所示,ons76
‑
52 dmso/sag细胞中carbon metabolism,biosynthesis of antibiotics和ras signaling pathway等通路激活。
[0102]
表9 david functional annotation bioinformatics microarray analysis分析
[0103][0104]
综上所述,本发明实施例中,对于ons76
‑
w535l(lde225/sag)与ons76
‑
wt(lde225/sag) 中smo的ip结果相比较,ons76
‑
w535l(lde225/sag)中smo的ip中独立的蛋白进行davidfunctional annotation bioinformatics microarray analysis分析,这些蛋白富集于ampksignaling pathway和glycolysis/gluconeogenesis信号通路。进一步,对其中的激酶分析,联合靶向rab10、rheb、pfkp、prkaa1、pkm、tpi1、csnk2b、cdk1等,可能是靶向治疗耐药性髓母细胞瘤的靶点;gpr37、rab35、rps10、nudt3、usp6nl、rere、cacybp、ckap5 八个蛋白的表达与髓母细胞瘤的生存期负相关。
[0105]
最后说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的宗旨和范围,其均应涵盖在本发明的权利要求范围当中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1