用于分析生物样品的方法与流程
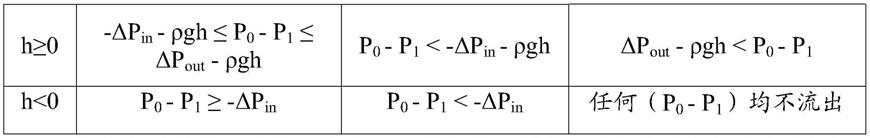
用于分析生物样品的方法
1.本技术是申请日为2016年06月08日、申请号为2016800338138、发明名称为用于多分析物分析的流体单元和流体卡式盒的专利申请的分案申请。
技术领域
2.本公开内容主要涉及可用于多分析物分析(multi
‑
analyte analyse)的方法,更具体是涉及用于分析生物样品的方法。
背景技术:
3.在体外诊断领域,通常要对诸如体液的生物样品(例如血液、尿液、唾液、脑脊髓液等等)、细胞悬浮液(例如在缓冲液中的组织细胞悬浮液),以及其他流体样品进行分析。对于某些情况,比如即时(point
‑
of
‑
care)检测,期望以卡式盒设备的形式进行上述分析。此外,还期望卡式盒在每次使用之后是一次性的,以避免交叉污染。微流体技术可用于构建这些卡式盒设备,并具有样品体积小以及卡式盒尺寸小的优点。然而,能用于测量多种生物标志物的卡式盒设备依然缺少。
技术实现要素:
4.在一方面,本公开内容是针对一种流体单元的设计,该流体单元用于构造测试生物样品的卡式盒。该流体单元包括:腔室、通气口和至少一个微流体通道,该微流体通道通入腔室并具有被动阀。该单元的操作依赖于重力或作为重力的替代力(比如离心力)的其它力,从而将流体保持在正确位置。此外,使用其它的力(比如气动压力)来输送流体。此种流体单元的设计具有固有的“自停”机制,其被配置成用于克服在气动致动的卡式盒中进行精确体积输送的难点。该流体单元有多种变型,以便实现各种流体功能,比如混合样品、去除气泡、输送固定体积的流体、分程传递流体流等等。借助于多个此类流体单元,可实现更加复杂的流体功能,比如连续稀释、替代微流体中的t形接头等等。流体单元可以由包括多个层的结构来实现。在一实施方式中,流体单元可被实现为双层结构。在另一实施方式中,流体单元可被实现为三层结构。
5.本公开内容还说明了如何设计具有所述流体单元的卡式盒,并用于检测各种生物样品。这些卡式盒可具有多个所述设计单元,并且可选地具有其它流体部件,比如流体通道、阀和泵等等。卡式盒设备可用于各类检测,比如全血细胞计数、流式细胞仪分析、血液化学、血气、免疫分析、核酸提纯以及分子诊断等等。对于将多个上述检测整合到一个卡式盒中来说,本公开内容是很理想的。
6.对依赖于重力的卡式盒的实施方式,维持垂直位置是适宜的。在这些卡式盒中,输送固定体积的流体的精度对于(从垂直位置发生的)倾斜而言是很敏感的。本公开内容引入了一些方法来减少或消除倾斜的影响。
7.卡式盒被插入读取装置中读出测量信号。本公开内容还包含了多个读取装置的设计,用于与包含所述流体单元的卡式盒一起使用。一种读取设备一次仅接收一个卡式盒。另
一种读取设备可同时接收多个卡式盒,其中这些卡式盒可以按串行方式、并行方式或流线型方式运行,以增加检测吞吐量。
8.在一个主要的示例性实施方式中,流体设备包括:流体腔室;至少一个微流体通道,其与流体腔室流体连通;通气口,其被配置成将气动力施加至流体腔室;至少一个被动阀,其位于至少一个微流体通道内并且被配置成基于压力差允许或阻止流体流动通过至少一个微流体通道;以及,控制器,其被配置成控制经由通气口施加至流体腔室的气动力。
9.在另一实施方式中,所述流体腔室位于一次性卡式盒内,该卡式盒被配置成通过流体设备的壳体保持在垂直位置。
10.在另一实施方式中,当所述流体腔室被保持在垂直位置时,通气口位于流体腔室的顶部部分。
11.在另一实施方式中,当所述流体腔室被保持在垂直位置时,至少一个微流体通道位于在通气口下方的高度。
12.在另一实施方式中,所述至少一个微流体通道包括第一微流体通道和第二微流体通道,当所述流体腔室保持在垂直位置时,第一微流体通道位于在第二微流体通道上方的高度。
13.在另一实施方式中,所述至少一个被动阀包括以下项中的至少一个:(i)疏水片区;(ii)亲水片区;(iii)疏水通道的直径骤增部分;以及,(iv)疏水通道的直径骤缩部分。
14.在另一实施方式中,所述控制器被配置成基于以下项控制经由通气口施加至流体腔室的气动力:(i)与通气口相关的压力(p0);以及,(ii)与至少一个微流体通道相关的压力(p1)。压力差(p0‑
p1)提供了气动力以驱动流体和空气。
15.在另一实施方式中,所述控制器被配置成通过根据以下方程式控制经由通气口施加至流体腔室的气动力,来将流体存储在流体腔室中:
‑
δp
in
‑
ρgh≤p0‑
p1≤δp
out
‑
ρgh,如果h≥0;以及,p1‑
p0≤δp
in
,如果h<0,其中(i)δp
in
是与流体进入流体腔室的第一方向相关的第一阈值压力;(ii)δp
out
是与流体离开流体腔室的第二方向相关的第二阈值压力;以及,(iii)ρgh是流体的液压,其因重力或者重力的替代力,比如离心力而产生。
16.在另一实施方式中,所述控制器被配置成通过根据以下方程式控制经由通气口施加至流体腔室的气动力,来将流体输送至流体腔室中:p1‑
p0>δp
in
+ρgh,如果h≥0;以及,p1‑
p0>δp
in
,如果h<0,其中(i)δp
in
是与流体进入流体腔室的方向相关的阈值压力,以及(ii)ρgh是流体的液压。
17.在另一实施方式中,所述控制器被配置成通过根据以下方程式控制经由通气口施加至流体腔室的气动力,来将流体从流体腔室向外输送:p0‑
p1>δp
out
‑
ρgh,其中(i)δp
out
是与流体离开流体腔室的方向相关的阈值压力;以及,(ii)ρgh是流体的液压。
18.在另一实施方式中,所述流体腔室包括滤膜,其具有的通孔孔径小于流体中已知的颗粒。
19.在另一实施方式中,所述设备包括多个流体腔室,并且其中控制器控制着相互独立地施加至多个流体腔室的相应通气口的气动压力。
20.在另一实施方式中,所述多个流体腔室包括第一流体腔室和第二流体腔室,第一流体腔室和第二流体腔室仅经由一个微通道流体连通。
21.在另一个主要的示例性实施方式中,流体检测系统包括:一个包括气动源和被配
置成控制该气动源的控制器的设备;以及,流体卡式盒,其被配置成要插入所述设备中,所述流体卡式盒包括:被配置成接收流体样品的入口;被配置成从入口接收流体样品的样品容纳腔室;被配置成存储或接收试剂的第一流体腔室,该第一流体腔室与样品容纳腔室流体连通;以及,与样品容纳腔室流体连通的第二流体结构。
22.在另一实施方式中,所述控制器被配置成通过致动气动源以使来自第一流体腔室的试剂将流体样品冲入第二流体结构,使流体样品与试剂在第二流体结构中混合。
23.在另一实施方式中,所述第二流体结构包括感测结构,并且其中控制器被配置成首先将流体样品推过感测结构,并且其次将试剂推过感测结构。
24.在另一实施方式中,所述第二流体腔室包括滤膜,该滤膜具有的通孔孔径小于流体样品中的目标细胞。
25.在另一实施方式中,所述样品容纳腔室被定位和布置成通过毛细力将流体样品吸取通过入口。
26.在另一个主要的示例性实施方式中,流体设备包括:流体腔室;至少一个微流体通道,其与流体腔室流体连通;倾斜传感器,其被配置成感测流体腔室的倾斜角;以及,控制器,其被配置成基于由倾斜传感器感测的倾斜角确定要经由至少一个微流体通道泵送至流体腔室中或者从流体腔室向外泵送的流体的体积。
27.在另一实施方式中,所述设备包括通气口,其被配置成将气动力施加至流体腔室,并且其中控制器被配置成控制经由通气口施加至流体腔室的气动力,以便将一定体积的流体从流体腔室排出。
28.在另一实施方式中,所述控制器被配置成基于流体腔室的形状和由倾斜传感器感测的倾斜角来确定流体的体积。
附图说明
29.现在将通过结合附图仅举例说明的方式以更多细节说明本公开内容的实施方式,其中:
30.图1显示了根据本公开内容的流体单元的示例性实施方式的设计;
31.图2a至2d显示了可与图1中的流体单元一起使用的被动阀的示例性实施方式;
32.图3显示了根据本公开内容的流体单元的示例性实施方式的设计;
33.图4a至4i显示了与根据本公开内容的流体单元的示例性实施方式相关的流体输送示例性实施方式;
34.图5a和5b显示了与根据本公开内容的流体单元的示例性实施方式相关的流体输送示例性实施方式;
35.图6a和6b显示了与根据本公开内容的流体单元的示例性实施方式相关的流体输送示例性实施方式;
36.图7a和7b显示了与根据本公开内容的流体单元的示例性实施方式相关的流体输送示例性实施方式;
37.图8a至8j显示了根据本公开内容的流体单元的示例性实施方式的设计;
38.图9a和9b显示了与根据本公开内容的流体单元的示例性实施方式相关的流体输送示例性实施方式;
39.图10a至10d显示了与根据本公开内容的流体单元的示例性实施方式相关的流体输送示例性实施方式;
40.图11a至11c显示了与根据本公开内容的流体单元的示例性实施方式相关的流体输送示例性实施方式;
41.图12a至12c显示了根据本公开内容的流体单元的示例性实施方式的设计;
42.图13a至13e显示了与根据本公开内容的流体单元的示例性实施方式相关的流体输送示例性实施方式;
43.图14a至14f显示了根据本公开内容的、带有试剂的流体单元的示例性实施方式;
44.图15a至15c显示了根据本公开内容的、带有滤膜的流体单元的示例性实施方式;
45.图16显示了根据本公开内容的流体流路的示例性实施方式;
46.图17a和17b显示了根据本公开内容的流体流路的示例性实施方式;
47.图18显示了根据本公开内容的流体流路的示例性实施方式;
48.图19a至19d显示了与根据本公开内容的流体流路的示例性实施方式相关的流体输送示例性实施方式;
49.图20a至20c显示了根据本公开内容的流体流路的示例性实施方式;
50.图21a至21c显示了根据本公开内容的、具有多个层的流体单元的示例性实施方式;
51.图22a至22c显示了根据本公开内容的、具有多个层的流体单元的示例性实施方式;
52.图23a显示了根据本公开内容的流体流路的示例性实施方式;
53.图23b显示了根据本公开内容的流体流路的示例性实施方式;
54.图24显示了根据本公开内容的流体流路的示例性实施方式;
55.图25显示了根据本公开内容的流体流路的示例性实施方式;
56.图26显示了根据本公开内容的流体流路的示例性实施方式;
57.图27显示了根据本公开内容的流体流路的示例性实施方式;
58.图28显示了根据本公开内容的流体流路的示例性实施方式;
59.图29显示了根据本公开内容的流体流路的示例性实施方式;
60.图30显示了根据本公开内容的流体流路的示例性实施方式;
61.图31显示了根据本公开内容的流体流路的示例性实施方式;
62.图32显示了根据本公开内容的流体流路的示例性实施方式;
63.图33显示了根据本公开内容的流体流路的示例性实施方式;
64.图34a至34g显示了本公开内容的实施方式是如何说明流体卡式盒倾斜的。
具体实施方式
65.图1显示了流体单元1001的设计,该流体单元1001包括:腔室1002;通气口1003;以及,微流体通道1004,其与腔室流体连通且通入该腔室并包括被动阀1005。流体单元可用于处理不同的流体,比如液体、含有气泡的液体或者含有颗粒的液体。流体可为体液(例如血液、尿液、唾液等等)、试剂溶液、包含悬浮珠粒的缓冲液等等。
66.流体腔室1002提供了包围在内的空间以接收和存储流体。流体腔室1002被设计成
可通过重力或其它力(比如气动力或离心力)使得流体可下沉或被下拉至腔室底部并且气泡可上浮至顶部。实现该特性的一种方法是使流体腔室1002的尺寸足够大,从而导致重力的作用比流体的表面张力更强。该特性也可通过其它方式来实现,例如,通过施加作用比表面张力更强的离心力。流体腔室1002的优选尺寸为:宽度0.1mm至50mm;深度0.1mm至50mm;以及,高度0.1mm至100mm。流体腔室1002可为任意形状,例如方形、圆柱形、球形或者本领域技术人员已知的其它容器形状,其尺寸在上述范围内。
67.通气口1003被配置成将气动压力施加至流体腔室1002。在设备使用时,应将通气口1003定位在流体上方。当设备处于存储或其它非使用状态时,通气口1003可在流体下方。其可有任意尺寸和任意表面特性。通气口1003优选为具有疏水表面的微尺寸通道,该通道内表面张力的作用比重力更强。被施加到通气口1003的气动压力可为:大气压、比大气压高的压力、或低于大气压的真空。当通气口1003连通大气压时,其可作为压力缓冲装置从而保持腔室内的压力恒等于大气压。
68.微流体通道1004与流体腔室1002包围在内的空间是流体连通的并通入该包围在内的空间。微流体通道1004优选为微尺寸通道,该通道处表面张力的作用比重力更强。在一实施方式中,微流体通道1004具有宽度0.1um至5mm且深度0.1um至5mm的截面。该截面的形状可为长方形、梯形、圆柱形或本领域技术人员已知的任何其它形状。此外,微流体通道1004包括被动阀1005,该被动阀在流体液面(fluid meniscus)的压力差低于指定阈值δp的情况下阻挡液体流动。优选将阀1005定位为接近腔室,从而使得在阀与腔室之间的流体体积与被操纵的流体体积相比可以忽略不计。在一示例性实施方式中,被动阀1005可为疏水片区(图2a)、亲水片区(图2b)、亲水通道的直径骤增部分(图2c)、疏水通道的直径骤缩部分(图2d)、或者本领域技术人员已知的其它设计。在微流体通道的尺寸范围中,流体的表面张力的作用比惯性力(比如重力)更强。
69.为了简化附图,如图3中所示的设计符号3001用于代表流体单元,其具有流体腔室3002、通气口3003、微流体通道3004以及被动阀3005。两个阈值压力与被动阀相关联,δp
in
在流体进入腔室的方向上,而δp
out
在流体离开腔室的方向上。阈值压力可为任意值,如下所讨论的:
70.δp
in
>0,δp
out
=0:用于阻挡流入腔室的单向阀
ꢀꢀꢀꢀꢀꢀꢀꢀ
1.71.δp
in
=0,δp
out
>0:用于阻挡流出腔室的单向阀
ꢀꢀꢀꢀꢀꢀꢀꢀ
2.72.δp
in
>0,δp
out
>0:双向阀
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
3.73.δp
in
=0,δp
out
=0:不提供压力屏障的阀
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
4.74.在工作中,应考虑流体单元的两个状态。状态1:通道4004在流体下方(h≥0),如图4a中所示。状态2:通道4004在流体上方(h<0),如图4b中所示。参数h代表从流体表面4006到微流体通道的高度差。
75.当在腔室4002中存储流体而无流动时,如图4a(h≥0)和图4b(h<0)中所示,在通气口4003(p0)与微流体通道(p1)之间的压力差应满足:
76.‑
δp
in
‑
ρgh≤p0‑
p1≤δp
out
‑
ρgh,如果h≥0
ꢀꢀꢀꢀꢀꢀꢀꢀ
5.77.p1‑
p0≤δp
in
,如果h<0
ꢀꢀꢀꢀꢀꢀꢀꢀ
6.78.其中ρgh是流体的液压。如图4c(h≥0)和图4d(h<0)中所示,为了将流体输送至腔室中,压力差应当满足:
79.p1‑
p0>δp
in
+ρgh,如果h≥0
ꢀꢀꢀꢀꢀꢀꢀꢀ
7.80.p1‑
p0>δp
in
,如果h<0
ꢀꢀꢀꢀꢀꢀꢀꢀ
8.81.如图4e(h≥0)中所示,为了将流体从腔室向外输送,压力差应满足:
82.p0‑
p1>δp
out
‑
ρgh,如果h≥0
ꢀꢀꢀꢀꢀꢀꢀꢀ
9.83.如图4f中所示,通过施加压力差(p0‑
p1),在状态1(h<0)将不会有流体从腔室向外输送。该特性可用作“自停”机制,如图5中所示。如图5a中所示,在腔室中的流体初始在微流体通道5004上方,并且通过施加压力差(p0‑
p1)将流体从腔室向外输送。当流体水平面降至通道5004的高度,如图5b中所示,流体输送自动停止,并不需要精确控制取消压力差(p0‑
p1)的时间。该“自停”机制有助于解决在气动致动的卡式盒中的精确体积控制的问题。尽管如此,腔室可被倾斜,直至通道5004位于流体下方(从h<0的状态2进入h>0的状态1),从而使得流体可根据需要被进一步输送出来。
84.表1总结了流体单元的操作。
85.表1:压力差(p0‑
p1),其用于致动流体输送。
[0086][0087][0088]
被施加到通气口的气动压力p0可进行独立调节,例如通过外部压力源(比如大气压力)或者内部压力源(比如压力控制器)调节。在微流体通道中的压力p1可取决于若干因素,所述因素包括:沿着通道中的流体和空气的液压传播;通道的流阻;表面张力(流体相对于通道壁临界面、流体相对于空气临界面、以及流体相对于具有不同表面张力的另一流体等等);以及,通过外部或内部压力源施加的气动压力等等。在某些实施方式中,保持通气口中没有流体。在某些实施方式中,微流体通道能够:完全填充流体;部分填充流体;或者,没有流体。
[0089]
在一实施方式中,包括具有上述流体单元的流体卡式盒的设备或者包括上述流体单元的设备可进一步包括控制器,该控制器被配置成控制被施加至上述流体单元的压力,例如通过控制经由通气口施加至流体腔室的气动力。在一实施方式中,控制器被配制成控制气动压力,从而使得根据上述方程发生流入、流出或无流动。例如,控制器可控制在通气口处施加的气动力,以导致p0发生改变从而满足上述方程,并且引起流入、流出或无流动状态。
[0090]
由于表面张力,在腔室中存储的流体可具有平的顶面(例如在图4g中示出),或者不平的顶面(例如在图4h和图4i中示出)。流体单元适用于这两种情况。通过测量表面轮廓可做出修正,从而补偿流体的体积精度。在其它实施方式中,化学品(比如表面活性剂)可被添加至流体,从而修正流体的表面张力,并因此也改变流体的表面轮廓。
[0091]
图6和图7显示了实现流体单元的两个示例。图6显示了去除气泡的应用。如所示,将含有气泡的流体输送至单元中,如图6a中所示。并且在进入腔室之后,如图6b中所示,由于通过重力或替代力(比如离心力)所导致的浮力,气泡上浮并破裂。为了加速气泡的去除,
可将比气泡内部的气压更低的气动真空施加至通气口。该流体单元可用在卡式盒中,从而去除在初始生物样品中的气泡,例如在指尖采取血样中不期望出现的气泡。流体单元还可用于去除在卡式盒中引发的气泡,例如来自于聚合酶链式反应(pcr)的热循环导致的气泡。
[0092]
图7显示了加速流体混合的应用。如所示,在单元中接收两种流体,如图7a中所示。为了加速混合,将气体(例如空气)泵送至流体中从而引发乱流,如图7b中所示。通过这种操作可快速实现正确的混合。一旦混合完成,气泡可离开流体,如图6的示例中所示。
[0093]
在一实施方式中,包括具有上述流体单元的流体卡式盒的设备或者包括上述流体单元的设备可包括控制器,该控制器被配置成控制上述流体混合。
[0094]
不同形态的流体单元的设计
[0095]
流体单元的设计可被修改为有多种形态。在一实施方式中,微流体通道可处在就腔室而言不同的位置上,如图8a
‑
c中所示。在另一实施方式中,微流体通道可垂直于或不垂直于腔室的侧壁,如图8d中所示。在又一实施方式中,替代直通道,微流体通道可有弯曲,如图8e中所示。在另一实施方式中,流体单元可具有两个或更多个微流体通道,如图8f中所示。在另一实施方式中,在一通入腔室的流体通道中可存在多于一个的被动阀。流体单元可具有多个上述不同形态和/或这些不同形态的组合。
[0096]
对具有多于一个的通入腔室的微流体通道的流体单元而言,每个通道的操作可被考虑是相对于通气口的,比如在表1中所描述的。同时,在每个通道中的压力并不完全彼此独立,而是通过在腔室和通道内的流体和空气的液压彼此耦连。例如,如图8g中所示,两个微流体通道8004和8006都通入腔室8002,并且在腔室中不存在流体。在这种情况下,p1和p2通过在腔室和通道内部的空气的液压来耦连。当p1和p2之间存在压力差时,在两个通道之间将产生气流,并且对抗腔室和通道的流阻来平衡压力差。
[0097]
在另一示例中,如图8h中所示,两个微流体通道p1和p2都通入腔室,并且在腔室中的流体在通道的高度下方。在这种情况下,p1和p2以相同的方式耦连,如图8g的示例中所示。
[0098]
在另一示例中,如在图8i中所示,两个微流体通道p1和p2都通入腔室,在该腔室中的流体在一个通道的高度下方并在另一个通道的高度上方。在这种情况下,p1和p2通过空气和流体(p1通过空气到达腔室,p2通过流体到达腔室)两者的液压耦连。当p1和p2之间存在压力差,在两个通道之间生成空气流和/或流体流,并且对抗流体和/或空气的流阻来平衡压力差。
[0099]
在另一示例中,如在图8j中所示,两个微流体通道p1和p2都通入腔室,在腔室中的流体在两个通道的高度上方。在这种情况下,p1和p2通过流体的液压耦连。当p1和p2之间存在压力差,在两个通道之间生成流体流,并且对抗流体的流阻来平衡压力差。
[0100]
因为有外力比如重力朝着单元的底部拉动流体,所以没有流体流被生成进入通气口内。因此,在施加到通气口处的气动压力相对于在腔室中的气动压力之间的压力差通过空气流阻来平衡,该空气流阻可被控制成相对最小。
[0101]
在具有两个或更多个微流体通道的流体单元中,在每个通道中的流体输送能够以依次进行、同时进行或者这两者组合的方式来完成。例如,图9显示了具有三个微流体通道9004、9006和9008的流体单元。在图9a中,这三个通道中的流体输送以依次进行的方式完成。更具体地,在步骤1:流体经由通道9004输送至单元中。在步骤2:流体经由通道9006输送
至单元中。在步骤3:单元中的流体经由通道9008输送出去。在图9b中,经由通道9004、9006和9008的流体输送是以依次进行和同时进行两种方式组合实现的。在步骤1:经由通道9004和9006的流体输送是以同时进行的方式完成的。在步骤2:经由通道9008的流体输送相对前一步骤而言是按依次进行的方式实现的。
[0102]
图10显示了用于混合流体的流体单元10001的示例。首先,将一种流体10010经由通道10004输送至单元中,如图10a中所示,并且另一种流体10011经由通道10006输送至单元中,如图10b中所示。这两种流体可通过扩散混合,如图10c中所示,或者借助于气泡加速混合,如图10d中所示。
[0103]
图11显示了使用流体单元借助上方讨论的“自停”机制输送固定体积流体的示例。如图11a中所示,可将体积v0的流体从通道11004向外输送。体积v0通过初始流体水平面以及通道11004关于流体腔室的高度来确定,并且不依赖于气动致动的时间。如图11b中所示,可随后将体积v1的流体从通道11006输送出来。体积v1通过两个通道11004和11006的高度差来确定。在一实施方式中,如图11c中所示,微流体通道11008可定位在腔室的底部处,以便输送体积v2(该体积依赖于通道11006的位置)的流体,以便完全排空该单元。在其它实施方式中,流体单元可具有多个微流体通道以便输送一系列固定体积的流体。
[0104]
图12显示了用于流体分程传递的示例。图12a显示了用于流体分程传递的单元,其具有两个入口通道12004和12006以及一个出口通道12008。流体流可从12004送至腔室中,并随后通过通道12008排出腔室之外。流体流还可从12006送至腔室中,并随后通过通道12008排出。以这种方式,两个流体流(一个流体流从12004到12008,并且一个流体流从12006到12008)能够分离地和按顺序地实现,但是两者都使用12008作为出口。类似地,图12b显示了一个用于流体分程传递的流体单元,其具有一个入口通道12014和两个出口通道12016和12018。从通道12014到通道12016的流体流相对从通道12014到通道12018的流体流而言,可分离地和按顺序地实现。图12c显示了用于从两个入口通道12024和12026到两个出口通道12028和12030进行流体分程传递的单元。从两个入口通道12024和12026中的任一个进入两个出口通道12028和12030中的任一个的流体流可分离地和按顺序地实现。流体分程传递的操作可在上述单元中重复超过一次。在其它实施方式中,可存在多于一个流体入口和多于一个流体出口的任意组合。
[0105]
图13显示了用于洗涤流体中的颗粒悬浮物的示意图。洗涤是在针对流体样品中的被提纯细胞、珠粒或其它颗粒的流式细胞仪、分子诊断或其它生物分析中经常用到的步骤。图13a
‑
d显示了洗涤具有比流体更高密度的颗粒的示例性实施方式。首先,带有颗粒悬浮物的流体13001被输送至腔室中,如图13a中所示,并且允许颗粒13002沉淀到腔室的底部,如图13b中所示。过量的流体随后经由在颗粒沉淀物上方的通道13016排出,如图13c中所示。随后,可将洗涤缓冲液13003输送至腔室中,以使得颗粒重新悬浮,如图13d中所示。这四个步骤可根据需要来重复,从而进一步提纯颗粒。如图13e中所示,对于具有比流体更低密度的颗粒13004,其可在单元中上浮。过量的流体经由通道13018排出,所述通道13018在漂浮的颗粒下方且在腔室的底部表面上。颗粒的沉淀或悬浮可通过离心、磁场、声波或本领域技术人员已知的其它方法来加速。
[0106]
流体单元还可具有其它变化。对于一示例,该单元可一开始在腔室中就提供有试剂,如图14中所示。试剂可以是如图14a中所示的流体,如图14b中所示的固体珠粒,和/或如
图14c中所示的珠粒的流体悬浮物。试剂还可为如图14d中所示的干燥的膜覆盖物,如图14e中所示的干燥的粉末,如图14f中所示的干燥的块体,或者任何其它形式的试剂。同样,被输送至流体单元中的流体可与试剂混合并且反应,从而帮助进一步分析。在一实施方式中,在将流体引入到腔室中之前将试剂存储在腔室中。
[0107]
在其它变化中,可将额外的特征添加至单元。图15a显示了被添加至单元腔室的滤膜15008的示例。滤膜15008有助于如图13中所描述的洗涤过程,并且还有助于其它过程,比如从流体分离颗粒。通过选择具有比目标颗粒15001更小的通孔孔径的过滤器,如图15b中所示,该过滤器可截留颗粒并且允许流体流过,这在生物检测中——例如从全血样品中分离血浆——是有用的。在其它实施方式中,滤膜15008可在不同方向上,比如在如图15c中所示的垂直方向上。在其它实施方式中,流体单元可具有多于一个的滤膜,以便捕获不同的目标颗粒(例如不同尺寸的目标颗粒)。
[0108]
在一实施方式中,包括具有上述流体单元的流体卡式盒的设备或者包括上述流体单元的设备可包括控制器,该控制器被配置成控制流体流动通过上述流体单元,例如通过控制经由通气口施加到流体腔室的气动力,或者通过控制与流体单元的微流体通道流体连通的泵和/或阀。
[0109]
具有多个单元的流体流路
[0110]
多个上述流体单元可以一起使用,以便形成不同功能的流体流路。流体单元可以按串行方式、并行方式或者这两者组合的方式来使用,并且可以与其它流体流路连接。在流体流路的一个优选实施方式中,该流路中的任意两个流体单元由不多于一个的流体通道相互连通。在流体流路的其它实施方式中,可存在多于一个的流体通道,该流体通道将流路中的两个流体单元相连接。在流路中使用多个单元时,独立地控制在每个单元中的腔室的通气口是有用的。例如,如果一个通气口受到控制与外界大气相连接,随后腔室中的压力就会恒等于大气压(或者有极小的压力差)。通过这种方式,沿着流体和/或空气的压力传播可从实现单元和单元之间的去耦合,从而简化了流体流路的操作。
[0111]
图16显示了具有按照串行配置的两个流体单元16011和16021的流体流路的示例。流体导管16001将单元16011的通道16018与单元16021的通道16026相连接。图17a显示了流体流路的一示例性实施方式,该流体流路具有按照并行配置的两个流体单元17011和17021,这两个流体单元按照串行配置连接到第三流体单元17031。图17b显示出流体流路的另一示例性实施方式,该流体流路具有与两个流体单元17051和17061串行连接的第一流体单元17041,所述两个流体单元17051和17061按照并行配置。在其它实施方式中,在流体流路中存在多个流体单元。图18显示了一个具有六个流体单元的流体流路的示例性实施方式。给定基本流体单元的设计及其工作角色,可由本领域技术人员实现多种复杂流路的设计。
[0112]
图19显示了用于连续稀释的流体流路的一示例性实施方式。连续稀释的功能常用于生物检测,比如全血计数和elisa分析。流体流路具有按照串行配置的两个单元19011和19021。图19a显示了将流体样品19001输送至单元19011中。在图19b中,第一稀释剂随后经由同一流体通道或另外的流体通道输送至单元19011中,并且与腔室19012中的初始样品进行混合,从而形成被稀释一次的样品19002。此后,将固定体积的被稀释一次的样品19002输送至流体单元19021的第二流体腔室19022,如图19c中所示。最后,将第二稀释剂输送至流
体单元19021中,以便与被稀释一次的样品19002进行混合并且形成被稀释两次的样品19003,如图19d中所示。在其它实施方式中,可将固定体积的被稀释两次的样品19003输送至随后的单元中进行进一步的稀释。
[0113]
t形接头,其作为流体通道的交叉部分,可与本文所公开的微流体设计一起使用。例如,图20a显示了t形接头20104,其由三个流体导管20101、20102和20103的交叉形成。然而,t形接头面临压力平衡复杂的问题,因此最好避免使用t形接头。本公开内容的流体单元可用来替代t形接头,应用在包括在本公开内容中所讨论的卡式盒中或者其它的微流体卡式盒中。图20a显示了一示例性的实施方式,其使用流体单元20031来替代图20a中的t形接头20104。流体单元20031用于流体的分程传递,如同图12的示例所述,以便在三个流体导管20101、20102和20103之间分离地输送流体。在其它实施方式中,如图20b中所示,由多于三个通道交叉形成的t形接头可通过流体单元来替代。在其它实施方式中,能够以级联形式形成多个t形接头,如图20c中所示。在一实施方式中,流体单元可用于替代图20c中每个交叉部分的t形接头。
[0114]
在一实施方式中,包括具有上述流体单元的流体卡式盒的设备或者包括上述流体单元的设备,可进一步包括控制器,该控制器被配置成控制流体流动通过上述流体单元,例如通过控制经由通气口施加至流体腔室的气动力或者通过控制与流体单元的微流体通道流体连通的泵和/或阀。
[0115]
流体单元的结构
[0116]
本公开内容的流体单元能够以多个层形成。例如,流体单元能够以双层结构形成,如图21中所示。图21a显示了基础流体单元的侧视图,同时图21b显示了所述双层结构的截面图。在该示例性实施方式中,第一层21011具有空腔结构,同时第二层21012是平坦的基底。将这两层结合到一起以形成单元的流体通道和腔室。该示例的被动阀21013以通道几何形状的骤增部分以及表面特性的局部疏水处理来形成。通气口21003可为:在第一层21011中的通孔;第一层21011侧壁中的开口;或者,第二层21012中的通孔。通气口可直接通入腔室,或者经由连接到腔室的流体通道间接通入腔室。
[0117]
在其它实施方式中,第一层21011可由下方材料形成,比如:热塑性材料(例如丙烯酸、聚碳酸酯、聚乙烯等等)、硅树脂、聚对二甲苯,或者其它材料,所述其它材料比如是聚合物、塑料、玻璃、硅或者流体技术领域中的技术人员已知的其它材料。第一层21011的空腔能够以如下制造工艺形成,所述制造工艺比如是注塑成形、压印、3d打印、cnc、蚀刻或者是本领域技术人员已知的其它工艺。在其它实施方式中,第二层21012可为刚性件或者柔性膜。所述刚性件可与第一层是相同材料的,或者是不同材料的。在一示例性实施方式中,膜可以是塑料膜。在另一示例性实施方式中,膜可以是层压有铝箔的塑料膜。对于使用膜作为第二层21012的实施方式,该膜可在卡式盒操作期间被刺穿。例如,通气口初始由膜密封,并且在操作期间将膜刺穿。
[0118]
在其它实施方式中,第二层21012也可具有空腔。如图21c中所示,流体通道和腔室可通过以下组合中的任一个形成:第一层21011中的空腔与第二层21012中的平坦部分;第二层21012中的空腔与第一层21011中的平坦部分;以及,第一层21011中的空腔与第二层21012中的空腔。术语“第一”和“第二”指代附图中的顶层和底层,并且是可互换使用的。在一些实施方式中,至少一个层可以是透明的,用于进行光学观察和测量。
[0119]
根据本公开内容的流体单元还能够以三层结构来实现,如图22中所示。在第一层22001和第二层22002之间可添加中间层22003。该中间层22003可覆盖第一和第二层之间的交界面的至少一部分。在一些实施方式中,中间层22003可为具有空腔的结构层,从而可形成多层流体通道和腔室,如图22a中所示。在另一实施方式中,如图22b中所示,中间层22003可为膜,所述膜在示例中可用于密封流体腔室中的试剂并且可在使用中被刺穿。在另一实施方式中,中间层22003可为金属电极,其表面可被处理以便用作一个或多个传感器。在其它实施方式中,如图22c中所示,中间层22003可为网格结构,以便形成在图15中所述的滤膜。
[0120]
用于生物检测的实施方式:全血细胞计数
[0121]
包括多个流体单元的流体流路可一起使用,从而形成用于一个或多个生物检测的卡式盒。流体流路还可包括其它流体组件以形成卡式盒。这些组件可包括但不限于流体通道、样品容纳腔室、泵、阀、流动传感器或者本领域技术人员已知的任何其它组件。流体卡式盒的某些实施方式可用于生物样品的细胞分析,比如全血细胞计数(cbc)。cbc分析包括四个部分,这四个部分包括白细胞(wbc)、红细胞(rbc)、血小板细胞(血小板)和血红蛋白的分析。
[0122]
图23a显示了用于cbc分析的流体卡式盒。流体流路具有四个流体单元23011、23021、23031和23041。流体单元23011和23031初始分别加载有试剂溶液23005和23006。为了操作流体流路,在步骤1:通过入口23001引入血液样品;通过毛细力将血液样品吸入样品容纳腔室23003;以及,在毛细中断部分23004处停止。血液样品的体积可基于容纳腔室的几何形状确定。在步骤2:关闭阀23002以封住入口23001。在步骤3:第一试剂23005从单元23011输送出来,并将容纳腔室23003中的血液样品冲入流体单元23021从而进行混合。试剂23005的体积可根据在单元中所存储的已知体积来确定,或者是根据其它方法(比如输送固定体积的功能,如图11中所示)来确定。血液样品与试剂23005的混合可通过泵送空气泡来加速,并且在流体单元23021中形成被稀释一次的样品。在步骤4:将固定体积的被稀释一次的样品输送至流体单元23041中。在步骤5:将第二试剂23006输送至流体单元23041中,在该处与被稀释一次的样品混合并形成被稀释两次的样品。在步骤6:固定体积的被稀释两次的样品可被输送至通道23044之外,用于下游分析。
[0123]
在一些实施方式中,生物样品可以是全血,并且第一试剂23005与第二试剂23006这两者是等渗稀释剂。在该实施方式中,为了分析cbc中的wbc、rbc和血小板,可使用被稀释两次的样品来实现血液样品的各种稀释率,比如稀释率1:10至1:10,000。连续两次稀释被用于实现较高的稀释率,而同时只使用较小体积的稀释剂。在其它实施方式中,可使用一个单元进行一次稀释。在其它实施方式中,可使用多于两个的单元进行连续稀释。在另一实施方式中,第一试剂23005可为非等渗稀释剂,并且第二试剂23006可为wbc标记试剂。在该实施方式中,被稀释一次的样品内的rbc被溶血后用于血红蛋白的分析。被稀释两次的样品可用于下游的wbc分析。
[0124]
图23b显示了上述卡式盒的示例,其具有无鞘流的微流体通道23007以执行wbc、rbc和血小板的细胞仪分析。无鞘流通道23007的内径应当大于用于分析的目标细胞,并且要足够小从而最小化重合误差,即多个细胞重叠在一起的可能性。在被稀释的样品流过通道23007时,通过比如流式细胞仪的光学感测、阻抗感测或者本领域技术人员已知的任何其
它方法来测量单个细胞。在分析之后,残余的样品可被输送至作为废液存储装置的流体单元23051。借助于此种卡式盒设备,可从血液样品测量出:wbc、rbc和血小板的总数;细胞指数,其包括但不限于平均血细胞体积(mcv)、平均红细胞血红蛋白(mch)、平均红细胞血红蛋白浓度(mchc);以及,wbc特性,其包括但不限于wbc分化(例如淋巴细胞、单核细胞、嗜中性粒细胞、嗜酸性粒细胞以及嗜碱性粒细胞)。
[0125]
图24显示了卡式盒的一种实施方式,该卡式盒覆盖了全套的cbc参数。该卡式盒包括两个重复的、图23a中的卡式盒,并添加了额外的特征以实现cbc参数的两部分:第一,wbc和血红蛋白分析;以及,第二,rbc和血小板分析。一个特征是共同的入口24011用于将血液样品同时吸入两个容纳腔室24014和24015,其被分别用于rbc/血小板分析和wbc/血红蛋白分析。另一个特征是流体单元24009,该流体单元作为流体分程传递以便将被两次稀释的样品分别地引入一个无鞘流通道24022,用于进行细胞仪分析。在其它实施方式中,还可通过修改存储在卡式盒中的试剂来测量额外的cbc参数,比如网织红细胞计数、有核红细胞计数、血小板聚集体等等。
[0126]
在一实施方式中,所述设备包含了具有上述流体单元的卡式盒、或者包含了上述流体单元,该设备可进一步包含控制器,该控制器被配置成控制上述流体单元中的流体流动,例如可以控制经由通气口施加到流体腔室的气动力或者控制与流体单元的微流体通道流体连通的泵和/或阀来实现所述控制。例如,控制器可被配置成控制:在流体单元23011的通气口处的压力p10;在流体单元23021的通气口处的压力p20;在流体单元23031的通气口处的压力p30;在流体单元23041的通气口处的压力p40;在流体单元24001的通气口处的压力p10;在流体单元24002的通气口处的压力p20;在流体单元24003的通气口处的压力p30;在流体单元24004的通气口处的压力p40;在流体单元24005的通气口处的压力p50;在流体单元24006的通气口处的压力p60;在流体单元24007的通气口处的压力p70;在流体单元24008的通气口处的压力p80;在流体单元24009的通气口处的压力p90;和/或,在流体单元24010的通气口处的压力p100。控制器还可被配置成控制在任意流体通道中的泵和/或阀,例如允许加压导致的、重力导致的或毛细作用导致的流动通过通道。所述加压导致的流动的所施压力可受到控制,例如根据上述等式来控制。
[0127]
用于生物检测的实施方式:流式细胞仪分析
[0128]
图25显示了用于流式细胞仪分析的卡式盒设备。该卡式盒具有:四个流体单元,其用于样品制备;以及,无鞘流通道25011,其用于细胞仪测量。在步骤1:通过毛细力将生物样品吸入容纳腔室25009并且在毛细中断部分25010处停止。在步骤2:关闭阀25008以封住入口25007。在步骤3:第一试剂25005被从流体单元25001中输送出去,并进一步将样品冲入单元25003内进行混合。在孵育一段时间周期之后,混合物形成了被稀释一次的样品。在步骤4:第二试剂25006也从流体单元25002输送至流体单元25003中用于进行混合和孵育。在孵育一段时间周期之后,混合物形成了被稀释两次的样品,其随后流过无鞘流通道25011用于进行感测,比如在流式细胞仪中的光学测量。测量废液被输送至用于存储的流体单元25004。在一实施方式中,生物样品为全血,第一试剂是标记淋巴细胞亚群的荧光团缀合的抗体,并且第二试剂是用于裂解样品中不期望出现的rbc的裂解溶液。该实施方式可被用于淋巴细胞亚群的细胞仪分析,其常用于免疫学和传染病诊断。在其它实施方式中,该卡式盒设备可用于使用不同样品和试剂的其它细胞仪分析。例如,其可用于基于珠粒分析的分析,
或者本领域技术人员已知的其它细胞仪分析。
[0129]
在一实施方式中,包括具有上述流体单元的流体卡式盒的设备或者包括上述流体单元的设备可进一步包括控制器,该控制器被配置成控制流体流动通过上述流体单元,例如通过控制经由通气口施加到流体腔室的气动力或者通过控制与流体单元的微流体通道流体连通的泵和/或阀。例如,控制器可被配置成控制:在流体单元25001的通气口处的压力p10;在流体单元25002的通气口处的压力p20;在流体单元25003的通气口处的压力p30;和/或,在流体单元25004的通气口处的压力p40。控制器还可被配置成控制在任意流体流道中的泵和/或阀,例如允许加压导致的、重力导致的或毛细作用导致的流动通过流道。所述加压导致的流动的压力可受到控制,例如根据上述等式来控制。
[0130]
图26显示了卡式盒设备的另一示例性实施方式,其用于流式细胞仪分析。前四个步骤类似于图25的卡式盒,收集生物样品以及在单元26003中形成被稀释两次的混合物。在步骤5:将混合物输送至流体单元26005。要注意的是,流体单元26005具有滤膜26011,该滤膜具有的孔径小于样品的目标细胞。在步骤6:将样品中过量的流体输送至废液存储单元26006,并且在滤膜26011上收集目标细胞。在步骤7:将第三试剂26010输送至流体单元26005中,以使得目标细胞在流体中重新悬浮。步骤6和7共同组成了在流式细胞仪分析中的洗涤步骤,并且可重复多次以便将样品中的目标细胞与其它不期望出现的成分分离提纯出来。在步骤8:目标细胞的流体悬浮液流过无鞘流通道26012,用于进行感测比如光学测量。在一实施方式中,生物样品是全血,第一试剂是标记wbc亚群的荧光团缀合的抗体,第二试剂是非等渗溶液以裂解rbc以及第三试剂是等渗稀释缓冲剂。滤膜26011可具有的孔径小于wbc但是大于rbc,从而将目标wbc在细胞仪感测之前从其它细胞成分(比如rbc溶解的碎片)中分离提纯出来,其中目标wbc使用了荧光团缀合的抗体来标记。在其它实施方式中,卡式盒设备可被用于使用不同样品和试剂的其它细胞仪分析。例如,卡式盒设备能被用于基于珠粒分析的分析,或者本领域技术人员已知的其它细胞仪分析。也可将其它卡式盒变化用于流式细胞仪分析。
[0131]
在一实施方式中,包括具有上述流体单元的流体卡式盒的设备或者包括上述流体单元的设备可进一步包括控制器,该控制器被配置成控制流体流动通过上述流体单元,例如通过控制经由通气口施加到流体腔室的气动力或者通过控制与流体单元的微流体通道流体连通的泵和/或阀。例如,控制器可被配置成控制:在流体单元26001的通气口处的压力p10;在流体单元26002的通气口处的压力p20;在流体单元26003的通气口处的压力p30;在流体单元26004的通气口处的压力p40;在流体单元26005的通气口处的压力p50;在流体单元26006的通气口处的压力p60;和/或,在流体单元26007的通气口处的压力p70。控制器还可被配置成控制在任意流体导管中的泵和/或阀,例如允许加压的、重力或毛细作用流通过导管。该压力可受到控制,例如根据上述等式来控制。
[0132]
用于生物检测的实施方式:临床化学
[0133]
图27显示了一种用于临床化学分析的卡式盒设备。在步骤1:经由入口27011将生物样品加载至样品容纳腔室27013中。在步骤2:关闭阀27012以封住入口。在步骤3:第一试剂27009从流体单元27001向外输送,并且将样品冲入流体单元27002用于进行混合。在步骤4:将被混合的样品输送至具有滤膜27010的流体单元27003。该过滤装置挡住大于孔径的颗粒并且允许其它流体成分通过。在步骤5:将通过过滤装置的、已知体积的流体输送至单元
27004中。在步骤6:将多个已知体积的流体分别输送至多个反应腔室,例如流体单元27005、27006、27007和27008。这些已知的体积可通过流体通道相对于流体单元27004的高度来确定。在反应腔室中,流体与初始存储在腔室中的试剂27015分别混合并反应,用于感测测量。在一实施方式中,生物样品可以是全血、血浆或血清。第一试剂可为等渗缓冲液。滤膜可具有的孔径足够小,以便从样品去除所有比如wbc、rbc和血小板之类的细胞成分。初始存储在反应腔室中的试剂可以是被干燥的试剂,其在与流体混合时溶解,其中样品中的血清或血浆成分可被稀释、过滤并且输送至反应腔室,以便与试剂珠粒反应。光学测量(比如分光计)或其它测量可在每个腔室中执行,从而确定目标临床化学分析物的浓度。根据已知体积的化学样品和已知体积的等渗缓冲液,可由测量数据计算出分析物的初始浓度。此外,根据全血样品中已知体积百分比的血浆或血清,也可获得关于血浆或血清的分析物的初始浓度。
[0134]
在一实施方式中,包括具有上述流体单元的流体卡式盒的设备或者包括上述流体单元的设备可进一步包括控制器,该控制器被配置成控制流体流动通过上述流体单元,例如通过控制经由通气口施加到流体腔室的气动力或者通过控制与流体单元的微流体通道流体连通的泵和/或阀。例如,控制器可被配置成控制:在流体单元27001的通气口处的压力p10;在流体单元27002的通气口处的压力p20;在流体单元27003的通气口处的压力p30;在流体单元27004的通气口处的压力p40;在流体单元27005的通气口处的压力p50;在流体单元27006的通气口处的压力p60;在流体单元27007的通气口处的压力p70;和/或,在流体单元27008的通气口处的压力p80。控制器还可被配置成控制在任意流体导管中的泵和/或阀,例如允许加压的、重力或毛细作用流通过导管。该压力可受到控制,例如根据上述等式来控制。
[0135]
图28显示了一种用于临床化学分析的卡式盒设备的另一实施方式。在该设备中,可使用二级过滤来改善过滤效率,并且最小化rbc溶血现象。在图27中的过滤步骤可使用两个流体单元28003和28004来替代,每个流体单元分别具有滤膜28015和28016。在一实施方式中,滤膜28015具有的孔径小于rbc但是大于血小板,然而滤膜28016具有的孔径小于血小板。在该设备中,相比于在图27的设计单元27003中,驱动流体通过膜28015所需的流压力较小,因此rbc可从样品去除且发生溶血现象的可能性降低。相比于在图27的设计单元27003中,驱动流体通过膜28016所需的流压力较小,因此分解血小板的可能性也降低。通过避免溶血现象,可改善临床化学分析的灵敏度和精确度。
[0136]
在一实施方式中,包括具有上述流体单元的流体卡式盒的设备或者包括上述流体单元的设备可进一步包括控制器,该控制器被配置成控制流体流动通过上述流体单元,例如通过控制经由通气口施加到流体腔室的气动力或者通过控制与流体单元的微流体通道流体连通的泵和/或阀。例如,控制器可被配置成控制:在流体单元28001的通气口处的压力p10;在流体单元28002的通气口处的压力p20;在流体单元28003的通气口处的压力p30;在流体单元28004的通气口处的压力p40;在流体单元28005的通气口处的压力p50;在流体单元28006的通气口处的压力p60;在流体单元28007的通气口处的压力p70;在流体单元28008的通气口处的压力p80;和/或,在流体单元28009的通气口处的压力p90。控制器还可被配置成控制在任意流体导管中的泵和/或阀,例如允许加压的、重力或毛细作用流通过导管。该压力可受到控制,例如根据上述等式来控制。
[0137]
也可将卡式盒设备的其它变化用于临床化学分析。在不同的实施方式中,也可测
量各种化学参数,比如基础代谢功能检查(basic metabolic panel)、完整代谢功能检查(complete metabolic panel)、血脂检查、葡萄糖浓度、c反应蛋白浓度、hba1c血红蛋白浓度、d二聚体、肌酸酐、白蛋白等等。也可测量各种样品,比如全血、血浆、血清、尿液等等。
[0138]
用于生物检测的实施方式:免疫分析
[0139]
图29显示了一种用于免疫分析检测(比如elisa分析)的卡式盒设备。在该卡式盒中,流体单元29001实现流体分段传输,用于将样品和试剂顺序地输送至感测区域。在步骤1:将生物样品29014经由样品入口29006加载至测定容积的腔室29008。在步骤2:关闭阀29007以封住入口。在步骤3:空气被从单元29001泵送出来,并且推动样品29014以便流过感测区域29010、29011、29012和29013。在步骤4:第一试剂29015、第二试剂29016和第三试剂29017先后地被输送至单元29001中并随后被从单元29001向外输送,以便顺序地流过感测区域。样品和试剂在流过感测区域之后进入废液存储单元29005。在一实施方式中,生物样品可为全血、血浆或血清。感测区域可初始包覆有一级抗原和阻断试剂。阻断试剂,例如中性蛋白(比如bsa),阻断在感测区域上未被一级抗原所占据的位点。当样品流过时,所包覆的抗原将目标抗体捕获到感测区域上。第一试剂可为洗涤缓冲液,以便去除残留的样品,并且第二试剂可为酶缀合的二级抗体,其进一步结合到被捕获的目标抗体。第三试剂可以是与酶反应用于比色测量的底物。感测区域可根据需要使用第一试剂多次洗涤。在其它实施方式中,第二试剂可为荧光团缀合的第二抗体,其允许进行荧光测量而无需与第三试剂的比色反应。在其它实施方式中,卡式盒设备可与用于不同的elisa分析的其它试剂组合一起使用,所述不同的elisa分析比如是直接的、间接的夹心分析等等,其对于本领域技术人员而言是已知的。
[0140]
在一实施方式中,包括具有上述流体单元的流体卡式盒的设备或者包括上述流体单元的设备可包括控制器,该控制器被配置成控制流体流动通过上述流体单元,例如通过控制经由通气口施加到流体腔室的气动力或者通过控制与流体单元的微流体通道流体连通的泵和/或阀。例如,控制器可被配置成控制:在流体单元29001的通气口处的压力p10;在流体单元29002的通气口处的压力p20;在流体单元29003的通气口处的压力p30;在流体单元29004的通气口处的压力p40;和/或,在流体单元29005的通气口处的压力p50。控制器还可被配置成控制在任意流体导管中的泵和/或阀,例如允许加压的、重力或毛细作用流通过导管。该压力可受到控制,例如根据上述等式来控制。控制器还可被配置成控制在区域29010、29011、29012和29013处发生的感测和分析。
[0141]
图30是用于免疫分析的卡式盒设备的另一实施方式,所述免疫分析比如是elisa分析。相比于图29,使用多个单元存储试剂。此外,在被进一步输送以流过感测区域之前,两个或更多个存储的试剂可被输送至流体单元30001中以进行混合和反应。在一实施方式中,试剂30007、30008、30009和/或30010可在单元30001中混合以进行化学反应或生物反应,从而形成新鲜制备的试剂,其可在预定的时间周期内流过感测区域。在一实施方式中,卡式盒设备可用来执行对血液中的人类igg的免疫分析,其使用银加强剂来进行信号放大。试剂30007、30009可为银盐的溶液,和试剂30008、30010可为氢醌的溶液。这两种试剂在混合时发生信号放大,并且在测试之前被存储到分离的单元中。除了图29和图30中的设备之外,还可设计卡式盒的其它变化以执行不同的免疫分析。
[0142]
在一实施方式中,包括具有上述流体单元的流体卡式盒的设备或者包括上述流体
单元的设备可包括控制器,该控制器被配置成控制流体流动通过上述流体单元,例如通过控制经由通气口施加到流体腔室的气动力或者通过控制与流体单元的微流体通道流体连通的泵和/或阀。例如,控制器可被配置成控制:在流体单元30001的通气口处的压力p10;在流体单元30002的通气口处的压力p20;在流体单元30003的通气口处的压力p30;在流体单元30004的通气口处的压力p40;在流体单元30005的通气口处的压力p50;和/或,在流体单元30006的通气口处的压力p60。控制器还可被配置成控制在任意流体导管中的泵和/或阀,例如允许加压的、重力或毛细作用流通过导管。该压力可受到控制,例如根据上述等式来控制。控制器还可被配置成控制在区域30017、30018、30019和30020处发生的感测和分析。
[0143]
用于生物检测的实施方式:分子诊断
[0144]
该流体单元的实施方式也可用于分子诊断。图31显示了卡式盒设备的一实施方式,其用于从生物样品提纯核酸。在步骤1:将具有用于核酸提纯的细胞的生物样品经由入口通道31010输送至流体单元31001。在步骤2:可将第一试剂31013、第二试剂31014、第三试剂31015和第四试剂31016连续输送至单元31001,用于进行混合和孵育。在一实施方式中,第一试剂31013可为蛋白酶k溶液,其分解细胞膜并将细胞团和核酸释放到流体中。第二试剂31014可为洗涤剂溶液,其溶解细胞并且使除核酸之外的细胞团溶液化;第三试剂31015可为结合溶液(binding solution),其提高核酸与二氧化硅表面结合的亲和力;以及,第四试剂31016可为珠粒的流体悬浮液,所述珠粒具有二氧化硅表面涂层。在孵育之后,在步骤2结束时,所述珠粒可捕获被释放到流体内的核酸。在步骤3:可将样品混合物输送至具有滤膜31012的流体单元31006。在一实施方式中,该滤膜31012的孔径可小于珠粒,并因此将珠粒截留在膜上方,并且允许过量的流体通过。在步骤4:可随后将过量的流体输送至废液存储单元31009中。在步骤5:可将来自流体单元31007的第五试剂31017输送至流体单元31006中。在一实施方式中,第五试剂31017可为洗涤缓冲液,以便纯化所捕获的珠粒。随后可将过量的流体输送至废液存储单元31009中,并且洗涤步骤可根据需要重复多次。在步骤6:可将来自流体单元31008的第六试剂31018输送至流体单元31006中。在一实施方式中,第六试剂31018可为洗脱缓冲液,其从珠粒结合物释放出核酸。最后,包括被释放的核酸的洗脱缓冲液可从通道31011向外输送,用于进一步的分析,然而珠粒被截留在滤膜上方。此类卡式盒的其它实施方式还涉及:不同的试剂;加速或稳定反应的热处理;以及,优化核酸提纯工艺的其它变化。
[0145]
在一实施方式中,包括具有上述流体单元的流体卡式盒的设备或者包括上述流体单元的设备可包括控制器,该控制器被配置成控制流体流动通过上述流体单元,例如通过控制经由通气口施加到流体腔室的气动力或者通过控制与流体单元的微流体通道流体连通的泵和/或阀。例如,控制器可被配置成控制:在流体单元31001的通气口处的压力p10;在流体单元31002的通气口处的压力p20;在流体单元31003的通气口处的压力p30;在流体单元31004的通气口处的压力p40;在流体单元31005的通气口处的压力p50;在流体单元31006的通气口处的压力p60;在流体单元31007的通气口处的压力p70;在流体单元31008的通气口处的压力p80;和/或,在流体单元31009的通气口处的压力p90。控制器还可被配置成控制在任意流体导管中的泵和/或阀,例如允许加压的、重力或毛细作用流通过导管。该压力可受到控制,例如根据上述等式来控制。
[0146]
卡式盒设备的其它变化还可包括:扩增被提纯的核酸的pcr步骤;和/或,确定核酸
量的测量步骤。图32显示了一种卡式盒设备,其用于基于珠粒的流式细胞仪分析以确定核酸量。在步骤1:将包含dna片段的样品吸入容纳腔室32015。在步骤2:关闭阀32014以封住入口32013。在步骤3:来自流体单元32001的第一试剂32008可从流体单元32001向外输送,并且将样品冲入流体单元32003用于进行混合和孵育。在一实施方式中,第一试剂32008可为珠粒的流体悬浮液,所述珠粒初始包覆有探针以捕获dna片段。这些珠粒可包覆有多种探针,用于分析多种dna片段。在步骤4:可将来自流体单元32002的第二试剂32009输送至流体单元32003中,用于与样品混合并孵育。在一实施方式中,第二试剂32009可为荧光团缀合的探针,以结合到所捕获的dna片段。在孵育之后,在珠粒上捕获的dna片段以荧光团标记。在步骤5:过量的流体可从流体单元32003向外输送,并进入废液存储单元32005,然而珠粒则被截留在滤膜32011上方。接着,第三试剂32010可从流体单元32004输送至流体单元32003中,以使得珠粒重新悬浮。在一实施方式中,第三试剂32010可为洗涤缓冲液,并且步骤5洗涤掉过量的荧光团以降低背景噪声。该洗涤步骤可根据需要重复多次。在步骤6:将制备的样品输送至无鞘通道32012用于细胞仪分析(比如荧光检测)从而确定dna片段的量。将测量废液输送至废液存储单元32006。
[0147]
在一实施方式中,包括具有上述流体单元的流体卡式盒的设备或者包括上述流体单元的设备可包括控制器,该控制器被配置成控制流体流动通过上述流体单元,例如通过控制经由通气口施加到流体腔室的气动力或者通过控制与流体单元的微流体通道流体连通的泵和/或阀。例如,控制器可被配置成控制:在流体单元32001的通气口处的压力p10;在流体单元32002的通气口处的压力p20;在流体单元32003的通气口处的压力p30;在流体单元32004的通气口处的压力p40;在流体单元32005的通气口处的压力p50;和/或,在流体单元32006的通气口处的压力p60。控制器还可被配置成控制在任意流体导管中的泵和/或阀,例如允许加压的、重力或毛细作用流通过导管。该压力可受到控制,例如根据上述等式来控制。控制器还可被配置成控制在无鞘通道32012处发生的感测和分析。
[0148]
用于生物检测的实施方式:血气
[0149]
图33显示了一种用于血气分析的卡式盒设备。在步骤1:生物样品33008(比如全血或血浆或血清)通过毛细力吸入容纳腔室33007并且在毛细中断部分33009处停止。在步骤2:关闭阀33006以封住入口33005;以及,在步骤3:将第一试剂33010从流体单元33002中继至流体单元33003并且进入感测区域33011、33012、33013和33014,用于进行测量。在一实施方式中,第一试剂33010是标准溶液。在步骤4:将空气或第二试剂从单元33001向外输送,并且将血液样品33008推至流体单元33003的腔室。随后,将血液样品或血液和第二试剂的混合物进一步输送至感测区域,用于进行测量。在存储单元33004中收集测量废液。在一实施方式中,感测区域是具有暴露的电极的流体腔室,这些电极可初始包覆有用于电化学感测血气成分的试剂。在其它实施方式中,电极可为金属层或者预先制备的传感件。
[0150]
在一实施方式中,包括具有上述流体单元的流体卡式盒的设备或者包括上述流体单元的设备可包括控制器,该控制器被配置成控制流体流动通过上述流体单元,例如通过控制经由通气口施加到流体腔室的气动力或者通过控制与流体单元的微流体通道流体连通的泵和/或阀。例如,控制器可被配置成控制:在流体单元33001的通气口处的压力p10;在流体单元33002的通气口处的压力p20;在流体单元33003的通气口处的压力p30;和/或,在流体单元33004的通气口处的压力p40。控制器还可被配置成控制在任意流体导管中的泵
和/或阀,例如允许加压的、重力或毛细作用流通过导管。该压力可受到控制,例如根据上述等式来控制。控制器还能被配置成控制在区域33011、33012、33013、33014处发生的感测和分析。
[0151]
除了上述实施方式,卡式盒可被用于在一个卡式盒中测量一个或多个上述生物检测,和/或执行其它生物检测。
[0152]
补偿倾斜的方法
[0153]
对于利用重力的流体单元和卡式盒的实施方式,期望的是维持垂直位置。例如,输送固定体积的流体的精度对于(从垂直位置发生的)倾斜而言是很敏感的,如图34a中所示。流体单元34001被设计成使用“自停”机制输送固定的体积v1,对于该体积v1而言在两个通道34002和34003之间的高度差为h。当该单元处于倾斜位置,如图34b中所示,在两个通道之间的高度差降低至h'=hcosθ。所输送的体积v1'与设计体积的差别为偏差δv=v1'
‑
v1,该偏差依赖于倾斜角度θ和腔室的几何形状。在本公开内容中教导了三种补偿该偏差的方法。
[0154]
第一种方法是设计一种具有期望几何形状的腔室以补偿该偏差。例如,单元34001的腔室可为圆柱体,如图34c中所示,其中在倾斜之后,在圆柱体中存储的流体的直径d变为d'=d/cosθ,如图34d中所示。因此,体积偏差可以根据下式计算:
[0155]
δv=v1'
‑
v1=v1
÷
cosθ
‑
v1=(1/cosθ
‑
1)v1
ꢀꢀ
[10]
[0156]
对于另一示例,单元34001的腔室是如图34e中所示的长方体。当倾斜仅在边l的方向上,如图34f中所示,则长方体的长度变为l'=l/cosθ并且宽度保持w'=w(在边w的方向上没有倾斜)。因此,体积偏差可根据下式计算:
[0157]
δv=v1'
‑
v1=hcosθ
×
l/cosθ
×
w
‑
hlw=0
ꢀꢀ
[11]
[0158]
在以特定角度倾斜时,对于体积偏差的补偿而言,长方体几何形状比圆柱体几何形状更加优选。在以任意角度倾斜时,可将腔室几何形状的其它变化,比如截头圆锥体,用于补偿体积偏差。
[0159]
第二种方法是使用倾斜传感器——比如倾斜仪或倾斜计——测量倾斜角θ,其中可计算体积偏差,如在方程[10]和方程[11]的示例中所示。所计算的体积偏差可被用作参数来补偿关于在卡式盒上测量的生物检测数据的倾斜。此外,卡式盒的倾斜可在生物检测之前、期间和之后被连续监控。因此,不仅倾斜,还可监控和补偿振动,所述振动可被解释为倾斜角的连续改变。各种倾斜仪或倾斜计可为该目的使用,无论是装在卡式盒上还是被分离地安装在容纳卡式盒的读取装置中。在一实施方式中,倾斜仪可为基于mems加速计的倾斜仪,其具有的优点在于:成本低、可靠性高、量程大以及0.1至1度的分辨率。
[0160]
第三种方法是在单元的出口处添加流传感器34005,如图34g的示例中所示。流传感器可测量要输送的精确体积v1',并且该体积v1'与倾斜无关。各种流传感器可用于该目的。
[0161]
与卡式盒一起使用的读取设备
[0162]
将本公开内容的卡式盒插入到用于信号读出的读取装置。该读取装置可被设计为每次容纳一个卡式盒,或者每次容纳多个卡式盒。通过按照串行的、并行的、或者流线型的配置来运行多个卡式盒,可实现高的检测吞吐量。流线型的配置意味着多个卡式盒可在样品制备阶段以并行方式运行,并且在信号感测阶段以串行方式运行。在该流线型的配置中,仅需要一组外部传感组件进行信号读出。在其它实施方式中,读取装置可设计为仅适应一
类卡式盒(比如用于测量全血计数的卡式盒),或是适应多类卡式盒(比如用于全血计数、血液化学、免疫分析等等的卡式盒)。在其它实施方式中,将读取装置设计成读取整合了多类生物测试的卡式盒。
[0163]
应当理解的是,对于本领域技术人员而言,很明显可以对此处描述的优选实施方式进行各种改变和修正。可做出此类改变和修正而不偏离本主体内容的精神和范围,并且不会削弱其预期的优势。因此,所附权利要求应当涵盖此类改变和修正。
[0164]
除非另有说明,在说明书和权利要求中所使用的所有代表成分量、特性(比如分子量)、反应条件等等的数字要理解为在所有情况下都用术语“大约”修饰。因此,除非有相反指示,在以下说明书和所附权利要求中所阐述的数字参数是近似值,其可能根据通过本公开内容所获得的期望特性来改变。至少无意于限制将等效原则应用到权利要求的范围,每个数字参数至少应当根据所报告的有效数位的数字并通过应用普通的四舍五入技术来进行解释。尽管阐述本公开内容的宽范围的数字范围和参数是近似值,在具体示例中所阐述的数字值被尽可能精确地报告。然而,任何数字值固有地包含必然会由其相应测试测量中发现的标准偏差导致的特定误差。
[0165]
除非文中另有指明或与上下文有明显矛盾,在本公开内容的上下文中(特别是在以下权利要求书的上下文中)使用的术语“一个(a和an)”、“所述(the)”以及类似指示对象要解释为涵盖单数和多数两种情况。本文中对数值范围的记载仅仅是要用作速记的方法,其单独指示落入该范围内的每个独立的数值。除非另有指明,每个单独的数值被并入说明书中,就好像其被单独列举在本文中一样。除非文中另有指明或与上下文有明显矛盾,在本文中所描述的所有方法能够以任意适当的顺序执行。本文提供的任何示例和所有示例,或者示例性的语言(例如“比如”)仅仅旨在更好地阐释本公开内容,并且不构成对本公开内容所要求保护的范围的限制。在说明书中没有任何语言应被解释为指示任何在实现本公开内容时必不可少的未要求保护权利的要素。
[0166]
除非明确指出仅指代替代物或者与替代物是相互矛盾的,即使本公开内容支持的定义涉及的是仅替代物以及“和/或”,但术语“或”的用法在权利要求中仍是被用来表示“和/或”。
[0167]
对本文公开的公开内容的可选元素或实施方式的分组并不被解释为是限制性的。每个分组成员可被单独引用和要求权利,或者可与所述分组中的其它成员或可在本文中找到的其它元素进行组合。可预见的是,出于简洁和/或可专利性方面的原因可将分组中的一个或多个成员包括在一分组中或从一分组中删除。当发生任何此类包括或删除时,说明书在这里被认为是包含了修改后的分组,由此满足在所附权利要求中所使用的所有马库什组的书面写法。
[0168]
本公开内容的优选实施方式在此处进行了描述,其中包括了本技术的发明人已知的执行本公开内容的最佳模式。当然,在阅读了以上说明书之后,基于这些优选实施方式的改变对于本领域中的普通技术人员而言是很明显的。本技术的发明人期望本领域中的普通技术人员可适当地采用这些变化,并且发明人预期本公开内容可采用与本文中具体描述的不同的方式来实践。因此,本公开内容包括所附权利要求中所记载的主题内容的(如适用法律所允许的)所有修正和等价形式。此外,除非文中另有指明或与上下文有明显矛盾,在其所有可能变化中的上述元素的任意组合由本公开内容所覆盖。
[0169]
此处所公开的具体实施方式可在权利要求中使用表述“由...组成”或者“基本由...组成”来进一步限定。当在权利要求中使用时,无论是如所提交的申请文件所记录的亦或是通过修改来添加的,过渡性的术语“由...组成”排除了未在权利要求中具体指明的任何元素、步骤、或成分。过渡性的术语“基本由...组成”将权利要求的范围限定在具体指明的材料或步骤以及那些不会对基础特征和新颖性特征造成实质影响的材料或步骤。如此要求保护权利的本公开内容的实施方式被本质地或清楚地描述并且在此能够实现。
[0170]
此外,要理解的是,本文公开的公开内容的实施方式是对本公开内容原理的说明。可在该公开内容的范围内进行其它的修正。因此通过举例说明而非限制性的方式,本公开内容的替代配置可以根据本文的教导来应用。因此,本公开内容并不限于如所示和所描述的一样。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1