胃癌诊断的蛋白标志物组合及其应用的制作方法
1.本发明属于医疗诊断技术领域,具体涉及胃癌诊断的蛋白标志物组合及其应用。
背景技术:
2.胃癌是全球第五大常见恶性癌症,死亡率居全身肿瘤第四位,严重威胁人类健康。根据世界卫生组织(who)最新的《2020年世界癌症报告》数据显示,2020年中国胃癌新发病例47.9万人(占全球胃癌发病率的44%)、死亡人数37.4万人(占全球胃癌死亡率的49%),发病率和死亡率均位居第三。由于特殊的饮食习惯,中国胃癌高危人群基数庞大,随着人口老龄化的趋势加重,我国胃癌的疾病负担还会持续增加。然而,由于早期胃癌症状不典型,中国胃癌的早期诊断率不足20%,70%-80%的患者确诊时已处于中晚期,预后较差(ⅳ期胃癌患者5年生存率不足2%)。
3.目前,胃癌筛查的方式主要为上消化道内镜检查。但是上消化道内镜检查要求具备先进的仪器设备和专门的操作人员,技术要求高、费用较贵,而且具有侵入性,需要提前禁食,受试者依从性差,不适用于反复检查和人群普查。此外,还有一些其他筛查方法,如幽门螺杆菌(helicobacter pylori,hp)抗体检测、血清胃蛋白酶原(pepsinogen,pgi/ii)检测、胃泌素(gastrin-17,g-17)检测等。pgi/ii、g-17本质上是表征萎缩的标志物,有助于识别萎缩性胃炎高危人群,但不适合用于胃癌的诊断。当pgi/ii或g-17水平发生异常时,必须通过胃镜和活检进一步诊断是否发生了癌变。幽门螺杆菌感染与胃癌的发生有着密切的关系,约有三分之二的胃癌发生与幽门螺杆菌感染有关,因此临床上将幽门螺旋杆菌的检测作为胃癌筛查的方法之一,但是该方法假阳性率高,阳性结果不足以作为胃癌诊断的依据,因此也不推荐用于广泛的人群筛查。血清常规肿瘤标志物,如癌胚抗原(cea)、碳水化合物抗原19-9(ca19-9),也被广泛应用于临床实践,但是他们的诊断灵敏度较低(早期肿瘤灵敏度《20%,晚期肿瘤灵敏度20-50%),也不适用于胃癌的早期诊断。
技术实现要素:
4.本技术的主要目的在于找到与胃癌诊断相关的新型生物标志物,并通过构建体外诊断联合检测计算模型,以提高临床胃癌诊断的灵敏度和特异性,为胃癌的早期筛查和辅助诊断提供新的手段。
5.为了实现上述目的,本发明提供如下技术方案:
6.一种检测胃癌的蛋白标志物组合,所述蛋白标志物组合选自col10a1、gkn1、gkn2、lipf中的至少一种,和选自pgi/ii、g-17中的至少一种。
7.胃癌检测没有一种标志物可以同时以非常高的灵敏度和特异性诊断胃癌,而且胃癌患者非肿瘤区域常伴随萎缩性胃炎,因此结合发现的新型蛋白标志物和表征胃窦萎缩的常规标志物(pgi/ii、g-17)进行联合检测,可有效提高胃癌检测精准度。
8.上述一种检测胃癌的蛋白标志物组合,作为一种优选的实施方案,所述检测方法为放射方法、免疫方法、荧光方法、流式荧光法、胶乳比浊法、生化法、酶法、杂交法、气质联
用法、液质联用法、层析法、化学发光方法、磁电法或光电转换方法。
9.上述一种检测胃癌的蛋白标志物组合,作为一种优选的实施方案,所述检测样本选自人体或动物体的组织、血液、尿液、唾液或粪便。
10.本发明的第二方面,提供一种检测胃癌的试剂盒,包括上述蛋白标志物组合特异性结合的试剂、用于制备活检样品所需的试剂、组织匀浆所需的试剂、制备肽段样品的试剂或对肽段进行脱盐所需的试剂。
11.优选地,用于制备活检样品所需的试剂为4%多聚甲醛、20%蔗糖(含0.05%nan3)等;组织匀浆所需的试剂为pbs(0.01m,ph 7.4)、sdt裂解缓冲液(4%sds,0.1m tris-hcl ph7.6,0.1m dtt)等;制备肽段样品的试剂(如对细胞裂解液的蛋白进行fasp酶解所需的酶解试剂trypsin/lys-c等);对肽段进行脱盐所需的试剂(0.1%tfa水溶液、75:25不含任何tfa的乙腈/水溶液、含0.2%甲酸和0.01%tfa的5:95乙腈/水溶液等)。
12.上述一种检测胃癌的试剂盒,作为一种优选的实施方案,与所述蛋白标志物组合特异性结合的试剂为肽、肽模拟物、核酸适配体、抗体或其抗原结合片段。
13.本发明的第三方面,提供一种基于蛋白标志物联合检测构建胃癌体外诊断计算模型的方法,所述方法包括从样本中检测至少两种权利要求1所述的蛋白标志物的浓度,并对测定的蛋白标志物浓度进行logistic回归,得到回归方程,建立计算模型;
14.logistic回归方程为:
15.其中logit(p)为胃癌蛋白标志物的logistic回归模型结果,c为回归得到的自然常数,α为回归分析得到的每个标志物的系数,标志物浓度i为每个蛋白标志物的浓度,n为大于等于2的整数。
16.上述一种基于蛋白标志物联合检测构建胃癌体外诊断计算模型的方法,所述样本选自人体或动物体的组织、血液、尿液、唾液或粪便;
17.所述检测方法为:放射方法、免疫方法、荧光方法、流式荧光法、胶乳比浊法、生化法、酶法、杂交法、气质联用法、液质联用法、层析法、化学发光方法、磁电法或光电转换方法。
18.本发明的有益效果为:本发明所述检测胃癌的蛋白标志物组合包括从样本中检测至少两种蛋白标志物的浓度,并对测定的蛋白标志物浓度进行logistic回归,得到回归方程,建立计算模型。将检测的每个蛋白标志物浓度代入回归方程,得到胃癌风险概率;进一步,通过约登指数最大的一点确定概率截断值(cut-off),最终确定每个样本是否患胃癌的情况及胃癌风险;有效地提高了胃癌检测的精准度。
19.本发明所述的蛋白标志物与胃癌具有很高的相关性,通过联合检测样本中新型蛋白标志物和表征胃萎缩的常规标志物的水平,可以极大提高胃癌诊断的精准度。与传统的消化道内镜检查或活检穿刺等侵入性诊断方法相比,本发明的无创检查普适性更好;与临床的血清常规肿瘤标志物(cea、ca19-9)检测相比,本发明采用多个蛋白标志物联合检测,并结合计算模型,对胃癌的诊断灵敏度和特异性更高,可用于胃癌的早期筛查和辅助诊断,有效促进胃癌精准诊疗。
附图说明
20.图1显示基于组织样本(80例胃癌、80例正常)的蛋白标志物联合检测(col10a1+gkn1+gkn2+lipf+pgi/ii+g-17)受试者工作特征曲线(roc);
21.图2显示基于临床血清样本(40例对照、60例胃癌)的蛋白标志物联合检测(col10a1+gkn1+gkn2+lipf+pgi/ii+g-17)受试者工作特征曲线(roc);
22.图3显示基于临床血清样本(60例胃癌、60例慢性胃炎)的蛋白标志物联合检测(col10a1+gkn1+gkn2+lipf+pgi/ii+g-17)受试者工作特征曲线(roc)。
具体实施方式
23.为了使本技术领域的人员更好地理解本技术方案,下面将结合案例对本技术实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本技术一部分的实施例,而不是全部的实施例。基于本技术中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都应当属于本技术保护的范围。
24.本发明公开了一种检测胃癌的蛋白标志物组合,所述蛋白标志物组合选自col10a1、gkn1、gkn2、lipf中的至少一种,和选自pgi/ii、g-17中的至少一种。
25.优选地,所述检测方法为放射方法、免疫方法、荧光方法、流式荧光法、胶乳比浊法、生化法、酶法、杂交法、气质联用法、液质联用法、层析法、化学发光方法、磁电法或光电转换方法。
26.优选地,所述检测样本选自人体或动物体的组织、血液、尿液、唾液或粪便。
27.本发明还提供了一种检测胃癌的试剂盒,包括与上述蛋白标志物组合特异性结合的试剂、用于制备活检样品所需的试剂、组织匀浆所需的试剂、制备肽段样品的试剂或对肽段进行脱盐所需的试剂。
28.优选地,与所述蛋白标志物组合特异性结合的试剂为肽、肽模拟物、核酸适配体、抗体或其抗原结合片段。
29.本发明还提供了一种基于蛋白标志物联合检测构建胃癌体外诊断计算模型的方法,其特征在于,所述方法包括从样本中检测至少两种权利要求1所述的蛋白标志物的浓度,并对测定的蛋白标志物浓度进行logistic回归,得到回归方程,建立计算模型;
30.logistic回归方程为:
31.其中logit(p)为胃癌蛋白标志物的logistic回归模型结果,c为回归得到的自然常数,α为回归分析得到的每个标志物的系数,标志物浓度i为每个蛋白标志物的浓度,n为大于等于2的整数。
32.优选地,所述样本选自人体或动物体的组织、血液、尿液、唾液或粪便;
33.所述检测方法为:放射方法、免疫方法、荧光方法、流式荧光法、胶乳比浊法、生化法、酶法、杂交法、气质联用法、液质联用法、层析法、化学发光方法、磁电法或光电转换方法。
34.实施例1
35.1、从cptac数据库下载胃癌(stomach)蛋白质组学数据及临床信息,样本量为胃癌组织:正常组织=80:80。
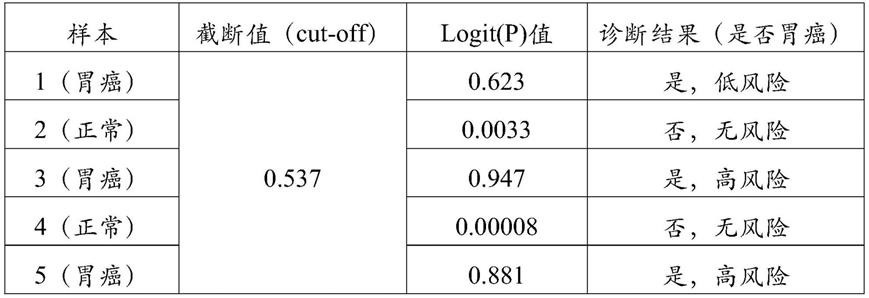
36.1.1抽取出本发明涉及的蛋白标志物col10a1、gkn1、gkn2、lipf、pgi、pgii、g-17在胃癌组织和癌旁组织中的浓度。进一步地,把上述相关蛋白标志物的浓度进行自然对数转换,经logistic回归分析,得到回归方程:logit(p)=c+α1*ln(col10a1)+α2*ln(gkn1)+α3*ln(gkn2)+α4*ln(lipf)+α5*ln(pgi/ii)+α6*ln(g17)。将检测的每个样本的蛋白标志物浓度代入回归方程,计算出每个样本患胃癌的概率,通过约登指数最大的一点确定概率截断值(cut-off),最终确定每个样本是否患胃癌的情况及胃癌风险(见表1)。
37.表1部分样本logistics回归分析结果判读
[0038][0039]
备注:当logit(p)值大于截断值时,存在胃癌风险;样本1-5是从80例胃癌组织、80例正常组织中随机抽取的5个样本。
[0040]
截断值是将检测的每个样本的蛋白标志物浓度代入logistic回归方程,计算出每个样本患胃癌的概率,通过约登指数最大的一点确定的。
[0041]
以表1数据为例,将80例胃癌和80例正常组织样本中蛋白标志物col10a1、gkn1、gkn2、lipf、pgi、pgii、g-17的浓度带入回归方程:logit(p)=c+α1*ln(col10a1)+α2*ln(gkn1)+α3*ln(gkn2)+α4*ln(lipf)+α5*ln(pgi/ii)+α6*ln(g17),可以计算得到每个样本的logit(p),即概率,然后通过软件计算出约登指数最大的一点的概率,即为截断值(cut-off)=0.537。
[0042]
表1的表格中:
[0043]
样本1、3、5为从80例胃癌组织中随机抽取的3个样本;
[0044]
样本2、4为从80例正常组织中随机抽取的2个样本。
[0045]
1.2蛋白标志物在胃癌组织中的诊断性能
[0046]
使用r包“proc”(版本1.15.0)绘制受试者工作曲线(roc),分析auc值、敏感性和特异性,判断标志物诊断性能。
[0047]
备注:auc为接受者操作曲线下面积,是表征诊断性能或精确性的一项指标,auc越接近1说明诊断性能越好。
[0048]
蛋白标志物在胃癌组织中的诊断性能见表2。col10a1、gkn1、gkn2、lipf、pgi/ii、g-17单个标志物独立使用在胃癌组织中均显示了较高的诊断性能,auc均在0.8以上。如图1所示:col10a1+gkn1+gkn2+lipf+pgi/ii+g-17的联合诊断性能auc可达0.99,灵敏度、特异性均在90%以上。
[0049]
表2蛋白标志物在胃癌组织中的诊断性能
[0050]
基因auc灵敏度特异性
col10a10.98391.1%99.4%gkn10.84284.3%69.0%gkn20.80181.4%68.4%lipf0.88497.6%70.7%pgi/ii0.81796.9%71.3%g170.71373.2%89.1%col10a1+pgi/ii0.98989.5%89.2%col10a1+gkn2+pgi/ii0.99094.1%99.6%col10a1+gkn1+g-170.98389.5%99.2%gkn1+gkn2+lipf+pgi/ii0.93795.9%85.3%col10a1+gkn1+gkn2+lipf+pgi/ii+g-170.99195.1%100%
[0051]
实施例2
[0052]
2、基于胃癌血样的诊断性能分析
[0053]
2.1用购买的酶联免疫检测试剂盒,分别测试临床血清样本(40例对照、60例胃癌、60例慢性胃炎)中蛋白标志物(col10a1、gkn1、gkn2、lipf、pgi、pgii、g-17)的浓度,同时登记病例的临床病理信息。
[0054]
进一步地,把上述3组病例的蛋白标志物的浓度分别进行自然对数转换,经logistic回归分析,剔除无贡献的标志物后,得到回归方程:logit(p)=c+α1*ln(col10a1)+α2*ln(gkn1)+α3*ln(gkn2)+α4*ln(lipf)+α5*ln(pgi/ii)+α6*ln(g17)。将检测的每个样本的蛋白标志物浓度代入回归方程,计算出每个样本患胃癌的概率,通过约登指数最大的一点确定概率截断值(cut-off),最终确定每个样本是否患胃癌的情况及胃癌风险,结果如表3和表4所示。
[0055]
表3 logistics回归分析结果判读(胃癌vs.健康)
[0056][0057]
备注:当logit(p)值大于截断值时,存在胃癌风险;样本1-5是从40例对照、60例胃癌血清样本中随机抽取的5个样本。
[0058]
表3中的样本1、3、5为从60例胃癌血清样本中随机抽取的3个样本;
[0059]
表3中的样本2、4为从40例对照组血清样本中随机抽取的2个样本。
[0060]
表4 logistics回归分析结果判读(胃癌vs.慢性胃炎)
[0061][0062]
备注:当logit(p)值大于截断值时,存在胃癌风险;样本1-5是从60例胃癌、60例慢性胃炎血清样本中随机抽取的5个样本。
[0063]
表4中的样本2、3为从60例胃癌血清样本中随机抽取的2个样本;
[0064]
表4中的样本1、4、5为从60例慢性胃炎血清样本中随机抽取的3个样本。
[0065]
2.2使用r包“proc”(版本1.15.0)分别绘制胃癌区分健康、胃癌区分慢性胃炎的受试者工作曲线(roc),分析auc值、敏感性和特异性,判断标志物诊断性能。
[0066]
备注:auc为接受者操作曲线下面积,是表征诊断性能或精确性的一项指标,auc越接近1说明诊断性能越好。
[0067]
蛋白标志物对胃癌和健康对照的诊断性能如表5所示,单个标志物独立使用时,col10a1的诊断性能最佳,auc=0.86。蛋白标志物联合诊断的性能优于单个标志物独立使用的性能,如图2所示:col10a1+gkn1+gkn2+lipf+pgi/ii+g-17的联合诊断性能auc可达0.92,灵敏度、特异性均在80%以上。
[0068]
表5蛋白标志物区分胃癌和健康的诊断性能
[0069]
基因auc灵敏度特异性col10a10.85789.3%68.7%gkn10.77296.4%56.2%gkn20.85089.3%75.0%lipf0.81989.3%66.7%pgi/ii0.56542.4%68.5%g170.53243.2%59.1%col10a1+pgi/ii0.86681.3%79.2%col10a1+gkn2+pgi/ii0.88682.1%87.5%col10a1+gkn1+g-170.88389.5%75.2%gkn1+gkn2+lipf+pgi/ii0.85789.5%85.3%col10a1+gkn1+gkn2+lipf+pgi/ii+g-170.91782.1%91.7%
[0070]
进一步的,本发明的蛋白标志物对胃癌和慢性胃炎也有一定的诊断性能(见表6)。
[0071]
单个标志物独立使用时,gkn2的诊断性能最佳,auc=0.80。蛋白标志物联合诊断的性能优于单个标志物独立使用的性能,如图3所示:col10a1+gkn1+gkn2+lipf+pgi/ii+g-17的联合诊断性能auc可达0.84,灵敏度、特异性均在75%以上。
[0072]
表6蛋白标志物区分胃癌和慢性胃炎的诊断性能
[0073]
基因auc灵敏度特异性col10a10.73181.7%60.0%gkn10.74166.7%76.7%gkn20.79568.3%76.7%lipf0.77963.3%83.3%pgi/ii0.68561.7%73.3%g170.50762.2%60.1%col10a1+pgi/ii0.73181.3%73.2%col10a1+gkn2+pgi/ii0.82976.7%83.3%col10a1+gkn1+g-170.78579.4%75.2%gkn1+gkn2+lipf+pgi/ii0.79774.5%68.3%col10a1+gkn1+gkn2+lipf+pgi/ii+g-170.84486.7%76.0%
[0074]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员,在不脱离本发明方法的前提下,还可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1