用于微粒分析的流体装置及相关方法与流程
用于微粒分析的流体装置及相关方法
1.本文中描述的发明公开了一种用于测量微粒(如微球、细胞、球状体和类器官)的质量密度、重量、尺寸和形状的装置及相关方法。特别地,该装置的架构适用于测量尺寸在一微米和五千微米之间的微粒。
2.对这类参数的详细信息的收集在如药理学、细胞生物学、农艺工业和食品与环境等领域的工业和/或研究应用中可具有重要影响。这种增长的需求可归因于单细胞和细胞团在广泛的生物医学应用中的大量使用。
3.特别地,细胞在质量密度上,而不是尺寸上,经常显示出更显著的变化,并且获得关于这类值的可靠数据是一个有待克服的挑战。因此,这类值的确定可以提供一种有效的分析手段,用于监测对外部刺激(如药物和环境变化)的细胞反应。此外,获得关于微粒体积和关于质量密度的同期信息允许与生物活动相关联,并且获得重要信息。这些包括细胞群在细胞团内的组织和活力的水平。
背景技术:
4.随着纳米机电系统(nanoelectromechanical system,nems)的问世,并且特别是随着纳米机械谐振器的发展,已经实施了用于确定细胞、微粒或分子的质量和密度的方法。
5.这些系统在经受取决于其质量、结构和刚性的特定频率时是谐振的。样品质量是通过谐振器在与其相互作用时的振荡频率的变化来测量的。对这种技术的生物应用的初始限制由于需要在真空条件下操作而产生的。悬浮微通道谐振器(suspended microchannel resonator,smr)已经克服了这个应用障碍,允许对溶液中的单细胞的密度进行测量并因此获得关于密度分布的统计。
6.然而,在使用微米级大小的流体通道时,上述系统允许分析尺寸小于几十微米的微粒。这对于关于可以达到毫米数量级直径的细胞团(如球状体和类器官)的应用或研究是一项重要的技术限制。
7.已知的方法使用沉淀速度来计算浮游植物和聚苯乙烯球的密度。而这种技术不允许达到球状体和类器官的平均尺寸。更重要地,数据是在单个步骤中收集的,而不能够重复测量以获得更准确的输出。
8.其他技术采用光学感应电动力学系统(optical induced electrokinetics system,oek)来提升先前引入微流体通道中的微粒。
9.这样一种解决方案造价昂贵,而且并不适用于测量尺寸大于20微米的微粒。
技术实现要素:
10.本发明的第一方面描述了一种用于测量微粒的质量密度和重量中的至少一者的流体装置。该流体装置包括沉淀室,其流体连接到配置成浸没在液体中的入口通道。该流体装置还包括连接到沉淀室的泵送系统。该泵送系统适用于控制沉淀室中的液体流。该流体装置的处理器配置成获得与沉淀室的至少一个区域中的微粒相关的微粒数据;并且基于所接收的数据计算微粒质量密度和重量中的至少一者。
11.该液体可以是培养液或溶液,例如盐溶液,其适用于储存并维持待引入沉淀室中的一个或多个微粒或微粒的团聚体。
12.由于存在直接连接到沉淀室的入口通道,可以对一群微粒执行单独的质量密度和重量测量。这个配置允许按顺序且以自动方式执行这类测量。测量值结合微粒数据(如微粒尺寸和形状)对于例如细胞动力学的研究或对于人类器官的生物模型的开发是重要的。
13.在第一方面的一个实施例中,流体装置还包括至少一个检测装置,其配置成采集微粒数据并将微粒数据提供给处理器。
14.在另一实施例中,流体装置配置成基于所接收的微粒数据的至少一部分来控制泵送系统。
15.在另一实施例中,微粒数据包括微粒速度、形状、位置、尺寸中的至少一者。
16.在另一实施例中,流体装置还包括温度控制装置,其配置成为处理器提供对沉淀室中液体的温度测量。处理器配置成基于所述温度测量来计算微粒质量密度和重量中的至少一者。
17.温度测量允许获得精确测量,即使是在装置并不处于受控温度环境的条件下。事实上,微粒在沉淀室中的运动还取决于它在其中移动的液体的黏度,而该黏度又取决于所使用的具体液体的性质及其温度。
18.在另一实施例中,温度控制装置还配置成基于由处理器提供的信息和预定温度值中的至少一者来调整沉淀室中液体的温度。
19.温度控制还允许将用于微粒维持的维持理想条件添加到测量准确度。例如,如果微粒由生物材料构成,那么理想条件是将其维持在37摄氏度,并且在一些使用方案中,可能需要改变温度用于观察具体的生物现象。
20.在另一实施例中,流体装置还包括可移动支撑件,其适用于容纳至少一个检测装置的至少一部分。处理器还配置成基于所接收的该微粒数据的至少一部分来引导可移动支撑件。
21.由于可移动支撑件,可以在微粒的移动期间跟随微粒,因此在质量密度和重量的测量中获得更高的精度,并且还可以在特别长的沉淀室中对以高速移动的微粒执行测量。此外,例如借助从不同角度或在不同焦平面上对样品进行观察,可以获得关于微粒的三维信息。所获得的关于物体的三维形状的数据允许更好地重构黏度系数,并且因此允许更好地解决质量和重量密度测量。
22.在另一实施例中,沉淀室还包括流动通道,其流体连接到入口通道并具有在流动通道的一部分中变窄的内部截面。
23.特别地,沉淀室包括具有至少两个部分的流动通道,其中第一部分的内部截面大于第二部分的内部截面。
24.第二部分定位成使得在沉淀室中的微粒适用于在微粒浸没的液体中没有流的情况下从第二截面移动到第一截面。
25.沉淀室的截面的变化允许获得汇聚的流线。在沉淀室中产生流的步骤期间,微粒跟随这类流线,并且因此朝向沉淀室的更中心的区域移动。由于这种现象,避免了取决于在微粒和沉淀室的侧表面之间的相互作用的测量伪像,并且可以产生更精确的测量。这还确保了微粒的定心,即使是对于长的测量时间而言,因此能够将样品维持在沉淀室中用于生
物实验。此外,定心对于抽取样品是有用的,因为它例如通过粘附到通道表面来降低在流体系统中样品损失的可能性。
26.在另一实施例中,沉淀室包括彼此并联连接并连接到入口通道的流动通道。每个流动通道还连接到流量调节器。在这种实施例中,处理器配置成接收与入口通道中的微粒相关的输入数据,并且基于输入数据来控制流量调节器。
27.几个沉淀室的存在允许微粒基于其尺寸而被导向进入适当的沉淀室。因此可以在单个仪器中实施对甚至尺寸显著不同(例如从一微米到5毫米)的微粒的测量。可替代地,多个沉淀室的存在允许在测量微粒群时有更大的流速。
28.在另一实施例中,流体装置还包括与沉淀室并联连接的再循环通道。再循环通道包括再循环装置,并且处理器配置成控制再循环装置,以使沉淀室中的液体再循环。
29.由于再循环系统,可以避免在流体系统内存在多于一个微粒,并且因此执行对单个微粒的重复的非破坏性分析以及对其回收。此外,将更少的分析液体用于随时间而延长的测量。
30.在另一实施例中,流体装置还包括流体连接到沉淀室的次级通道。处理器配置成选择性地控制次级通道中的流动,以通过次级通道将液体引入沉淀室中和/或将液体从沉淀室中排出。
31.次级通道可以直接地或通过入口通道或通过次级流体回路连接到沉淀室。
32.至少一个次级通道的存在允许在测量期间将新液体引入沉淀室中。因此可以例如执行生物实验方案。此外,还可以引入适用于对具体微粒的精确测量的新液体。例如,通过从一组测量液体中选择具有与微粒的质量密度最为接近的质量密度的液体,可以提高测量精度和准确度。此外,相同的次级通道可以用于移除样品并将其分类到具体容器中。例如,通过特殊的流体衍生,不同的微粒可以被收集在不同的容器中,即使基于所执行的测量的结果。
33.本发明的第二方面描述了一种用于测量微粒的质量密度和重量中的至少一者的方法。根据该方法,将待分析的微粒通过浸没在液体中的入口通道引入流体装置的沉淀室。获得与沉淀室的至少一个区域中的微粒相关的微粒数据。微粒在沉淀室中静止的液体中移动。基于所接收的数据来计算微粒质量密度和重量中的至少一者。
34.可以在微粒在静止的液体中移动时进行测量。静止的液体是指在沉淀通道中没有流动。在一种实施方式中,微粒随着受到力场的加速运动而移动。例如,沉淀室可以定位成使得微粒在受到重力加速的静止的液体中移动。
35.在第二方面的一个实施例中,获得微粒数据包括通过至少一个检测装置来采集微粒数据,并且向处理器提供所采集的微粒数据。
36.在另一实施例中,该方法还包括基于所接收的微粒数据的至少一部分来控制沉淀室中的流。
37.在另一实施例中,该方法还包括测量沉淀室中液体的温度;并且甚至基于所述温度测量来计算微粒质量密度和重量中的至少一者。
38.在另一实施例中,该方法还包括基于处理器所提供的信息和预定温度值中的至少一者来调整沉淀室中液体的温度。
39.在另一实施例中,该方法还包括基于所接收的微粒数据中的至少一部分来引导至
少一个检测装置的至少一部分。
40.在另一实施例中,该方法还包括将其中浸没有待分析的微粒的液体在与沉淀室流体并联连接的再循环通道中再循环。
41.在另一实施例中,该方法还包括在测量微粒质量密度和重量中的至少一者之前和/或之后,将其中浸没有待分析的微粒的液体替换成与该液体不同的第二液体。
42.在另一实施例中,该方法还包括基于质量密度、重量、尺寸和形状中的一者来选择微粒;并且基于质量密度、重量、尺寸和形状中的至少一者将所选择的微粒收集在预定容器中。
43.上述关于流体装置的优点也适用于关于第二方面及其实施例所描述的方法。
附图说明
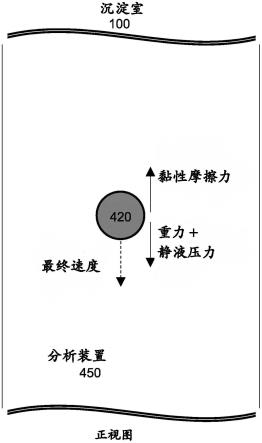
44.图1:包含分析介质和微粒的沉淀室的正视图。对涉及的力和最终速度的描绘。
45.图2:本发明的图示性描绘。
46.图3:对与温度控制装置相关的实施方式的图示性描绘。
47.图4:从作为时间的函数的微粒位置的垂直变化中获得的线性回归数据。
48.图5:对于经分析的每个批次(20、50和90μm)而测量的七个不同ps微球上所获得的平均密度的实验结果,以及对于每次测量在七次重复上所获得的相应的标准偏差。
49.图6:a)与由制造商宣称的值以及相应的标准偏差对比所示出的在三批ps微球上获得的平均密度的实验结果。b)对于被检验的微球的三个量,与理论速度相比的实验确定的最终速度。
50.图7:对定心装置(a)的图示性描述。对部分100c(a,b)的放大,用于对通过脉冲流(b)和通过调制流(c)进行的微粒定心的图示性描绘。
51.图8:对包括具有不同量的几个流动通道的沉淀室的图示性描述,其中几个流动通道连接到独立的流量调节器以满足微粒多样性。
52.图9:对与大微粒的移动的测量相关的技术解决方案的图示性描绘,其中测量是通过识别来自可调节且已知距离处的不同目标位置的微粒的通过来进行的。
53.图10:对用于双侧形态微粒表征的双摄像头系统的图示性描绘。
54.图11:对与关于微粒的三维信息的采集相关的实施方式的图示性描绘,其中基于从多个角度反射的图像的采集来采集关于微粒的三维信息。
55.图12:对与3d图像采集相关的实施方式的图示性描绘,其中基于相对于圆柱形沉淀室做轨道运行的检测装置来进行3d图像采集。
56.图13:对包含再循环通道和相关的次级泵送系统的实施方式的图示性描述。
57.图14:对包含用于引入和交换的另外分析介质的次级通道的实施方式的图示性描绘。
58.图15:对监测相对于时间的球状体直径和密度的图表性描绘,其中监测用于评估其在用药物治疗之前的成熟程度。
59.图16:对专用于微粒分类的实施方式的图示性描绘。
具体实施方式
60.对于单个医学或生物实验室而言,研究不同性质的微粒(如细胞、微球、球状体、类器官和/或其他形式的微粒聚集体)变得越来越普遍。
61.鉴于样品种类繁多以及对重量、密度、尺寸和形状测量的关注,以下描述的实施例和实施方式呈现了这样技术解决方案,即允许通过采用单一装置以及与之相关联的不同使用方法来测量这类参数。本发明的实施例描述了允许进行这类测量的第一解决方案。在一个示例中,对重量、密度、尺寸和形状的测量,可以在维度范围从一微米到五千微米的样品上伴随地、同时地或组合地执行。除了具有针对样品的大尺寸分布用单个仪器操作的优点之外,这也允许在单独的微粒上所获得的数据之间的固体相关性。
62.本发明中描述的流体装置和相关方法的实施例允许以经济、准确且非侵入的方式执行上述分析。这类流体方法和装置不仅可以用于执行对有机目标和生物目标的测量,而且还可以用于执行对无机样品的侧量。
63.以下段落描述了本发明的几个示例性实施例。通过示例的方式,并且为了便于理解,将参考对生物材料(如细胞或细胞团聚体)的分析来描述这些实施例,其中生物材料在下文中用通用术语微粒来指示。然而,理解的是,与本文中所示的本发明相关的方法和装置允许测量非生物微粒的质量密度、重量、尺寸以及形状。特别地,参考下文中描述的示例性实施例的实施方式还可以用于分析细胞或细胞团聚体之外的微粒。因此,在本发明的实施例的上下文中,用于指示细胞、细胞团聚体或生物材料的术语“微粒”总体上还可以用于指示微型微粒、工业生产过程的残留微粒、悬浮的大气粉尘、花粉、囊泡、水性悬浮液中的油滴、液体中的气泡。
64.同样地,术语“分析介质”或更通用的术语“液体”在本发明的说明性示例中用于表示与细胞培养物相容的介质。然而,术语“分析介质”和术语“液体”必须在其最一般的意义上进行解释,这对于本领域技术人员将是显而易见的。特别地,基于待分析的微粒的设计要求和性质,液体可以是另一性质的细胞培养介质或液体,如水基溶液或油,这对于本领域技术人员将是显而易见的。
65.对于涉及可能使用单一技术设备以及相关使用方法来伴随测量微粒质量密度、重量、尺寸和/或形状以及不同尺寸的现有技术,本发明具有桥接该现有技术内间隙的目的。事实上,现今存在的装置可以部分地在狭窄的尺寸分布中运行。此外,它们不允许获得对这类参数的同时或组合的测量。这导致获得难以相互关联的分段信息。
66.即使已经特别参考附图来描述该目的,但会在说明书和权利要求中使用附图标记来提高对本发明的理解,并且不对所要求保护的保护范围形成任何限制。
67.本发明公开了一种新装置以及相关的使用方法,其能够执行对生物和非生物微粒(如微球、细胞、球状体以及类器官)的质量密度、重量、尺寸和/或形状的伴随测量,这些微粒具有在1和5000微米之间的尺寸。
68.在详细描述适用于获得这样的测量的各种实施方式之后,将公开本发明的多种使用模式。后者包括对基本系统的适配,这种适配特别参考其在生物医学领域中的有用性。本发明适用于分析在静止的流动条件下由重力引导的运动中的微粒(420)(图1)。微粒的这类移动主要受到其质量密度、体积、形状、取向以及周围液体的质量密度和黏度的影响。
69.在图2中,示出了对本发明的实施例的图示性描绘。
70.参考图3至图16所描述的实施例描述了图1的流体装置随后的改进和发展。因此,下文参考单个附图描述的各个特征可以与参考其他附图描述的特征组合。
71.流体装置包括沉淀室100、泵送系统200、检测装置300和处理器500。微粒420的移动发生在具有透明壁的流体通道内,在本文中称为沉淀室100。泵送系统200包括流生成系统230,通过示例的方式,其可以是蠕动泵或压力控制系统。入口通道210和出口通道220可以连接到装载或卸载罐,可替代地,它们可以用作通风口。系统包括连接到处理器500的检测装置300,发挥监测微粒420的移动以及测量其形状和尺寸的双重作用。沉淀室100和检测装置300的尺寸都设定成允许对微粒420的移动、形状以及尺寸进行准确测量,如在下文中详细描述的。
72.虽然图2的装置包括检测装置300,但检测装置是可选的。在可替代实施方式中,流体装置可以制成为没有检测装置。
73.特别地,在本发明的实施例的上下文中,“测量微粒的形状和尺寸”是指对微粒的可以用于表示或近似微粒的三维几何形状的任何特征的测量。在球形微粒的情况下,这可以与半径的测量一致,或者在近乎球形和非球形微粒的情况下,这可以与其他几何特征一致。
74.为了装置的正确运行,包含在分析介质450内的微粒420被从罐400中取出,通过入口通道210引入沉淀室100中并在沉淀室100内部运输。微粒在泵送系统200内部的运输是通过流生成系统230的激活而发生的。在引入微粒420之后,将流阻断,并且微粒在由重力引导的分析介质450内移动。在没有其他流的情况下,并且在因加速步骤而引起的片刻时间之后,微粒将达到其恒定速度,这里定义为最终速度、漂移速度或沉淀速度。
75.一旦已经进行测量,入口通道210和出口通道220可以被无差别地用于回收微粒420。
76.该装置可以用于执行相对测量(其中不同微粒之间的差异被评估)或执行绝对测量。在后一种情况下,知道温度是有用的,以便限定分析介质450的质量密度和黏度。在本发明的实施例中,装置适用于在受控温度环境内部使用,例如在保温箱中。可替代地,可以在实验期间测量温度。在本发明的一个实施例中(图3),分析介质450的平均温度由温度控制装置600测量,温度控制装置600由至少一个传感器610组成并定位在沉淀室100附近。然后,处理器500适配所计算的黏度作为测量的温度的函数。
77.在另一实施例中,当运行条件要求具体的温度值(例如,对于活的生物样品是37℃)时,温度控制装置600配置成基于处理器500提供的信息(如当前的温度值、微粒的类型、液体黏度、当前的液体黏度值等)来调整沉淀室中液体的温度。在一个具体实施例中,温度控制装置600管理温度调整单元620,其允许在分析期间维持一个具体值。例如,温度控制装置600可以包括泵送系统200的几个加热器(620a和620b)和传感器(610a和610b),这些加热器和传感器位于流体装置的各个位置中,并且特别地位于沉淀室100附近。
78.从物理角度来看,并且为了使所获得的数据的准确度最大化,当达到微粒的最终速度时,而不是在过渡期间,可以考虑微粒的移动。微粒相对于分析介质的相对速度v(t)可以通过求解运动方程中的动态方程来获得:
79.f=m
p
a=(ρ
p-ρ
l
)v
p
g-kv
80.v(t)=vd+(v
0-vd)e-t/τ
81.其中τ是微粒动力学的过渡时期:
[0082][0083]
其中m
p
是微粒质量,ρ
p
是微粒质量密度,a是微粒加速度,ρ
l
是分析介质的质量密度,v
p
是微粒体积,vd是微粒漂移速度,v0是初始微粒速度,r是微粒半径,k是摩擦系数,η是分析介质的黏度,g是重力加速度。
[0084]
为了评估这种过渡时期的量级,下文中示出了在尺寸和类型不同的生物微粒的情况下,在水溶液中对其测量的计算。水基溶液具有约1mpa
·
s的黏度,并且生物微粒的质量密度平均为1020fg/μm3。在直径在1微米和2000微米之间的微粒的情况下,τ的量级从60ns(对于1μm的直径)到250ms(对于2000μm的直径)变化。在这种间隔中,微粒在很短的时间内达到最终速度。由于这个时间跨度可忽略不计,因此微粒的加速度对测量没有影响,并且微粒动力学因此可以被认为是均匀的线性运动。
[0085]
本发明的实施例的其他技术实施方式允许测量更大的微粒,特别是直径在2和5毫米之间。对于这样的实施方式,必须考虑过渡时间,这是因为在直径为5毫米的样品的情况下它可以达到1.5秒。
[0086]
例如,在本发明的一个实施例中,将微粒带到检测装置300的工作区域上方的预定距离处,以便将过渡时期排除在测量之外。
[0087]
在本发明的另一实施方式中,检测装置300的工作区域足够大,并且沉淀室100也足够长,以允许检测微粒的完全动态运动,包括加速度和最终速度。在微粒运动的过渡时期期间收集的数据可能不被考虑用于最终速度的计算。
[0088]
在本发明的一个实施例中,用于测量的理论是基于对斯托克斯定律(stokes’law)的详细阐述,其中:
[0089][0090]
和
[0091][0092]wp
=ρ
pvp
ꢀꢀꢀ
(等式3)
[0093]
其中,w
p
是微粒重量。
[0094]
为了证明这种发明的可靠性,使用了其具体实施方式(图2)来测量在20和90微米之间的聚苯乙烯微球的质量密度和尺寸。
[0095]
在这种实施方式中,检测系统300由具有4x放大率的光学显微镜系统组成。沉淀室100在共价地粘附到载玻片上的透明的聚二甲基硅氧烷(pdms)芯片内部获得。沉淀室100的架构具有6cm的长度,以及1x1mm的截面。微粒通过流生成系统230而定位在沉淀室100的上部中,流生成系统230在这个实施方式中由蠕动泵组成。在样品到达沉淀室100之前,它被运输通过泵送系统200,在这种情况下,泵送系统200由聚四氟乙烯(ptfe)管组成。处理器500由能够处理图像的计算机和相关软件组成,其中图像由显微镜单元收集。从这些图像中推断微粒形状的二维投影及其最终速度。后者是通过线性回归来计算的,而线性回归从作为时间的函数的微粒质心的位置的变化中获得(图4)。然后,处理器500通过采用先前示出的
数学模型来计算微粒的质量密度和直径。对每个微粒重复这个过程几次,以获得统计学上显著的结果。
[0096]
这个具体的实施方式被用来测量具有已知密度和直径的微粒以便验证本发明。特别地,选择了三个批次的聚苯乙烯(ps)中的微球(polysciences公司,美国),其直径为20、50和90微米。由销售者提供的产品薄片指示,对于ps球,平均质量密度值为1.050
±
10fg/um3。对于每批微球,分析七个不同的单位,并且对于每个单位重复测量七次,以增加统计显著性。图5示出了经分析的七个不同微球的平均密度值,以及从每个批次的七次重复外推出相应的标准偏差。与实验预期一致,在所有微球上进行的测量的标准偏差是可比的,证明了该实施方式的准确性和可靠性。
[0097]
此外,针对ps微球所获得的密度值发现比制造商宣称的平均值明显更加准确(图3a)。特别地,可以注意到,平均标准偏差具有比商业值(图6a)的量级更低的量级。通过比较理论最终速度(等式1)和实验最终速度(图6b),获得对结果的准确度的进一步确认。
[0098]
具体地,图2所示的相同配置用于对ps微球进行的验证分析,可以适用于分析大的生物样品,如球状体或类器官。
[0099]
这类应用的相关性涉及将本文中所示的方法例如用于监测球状体的生长阶段的可能性。事实上,允许掌握球状体群达到操作者需要或期望的成熟度的时刻,是继续生物学实验的重要方面。事实上,从分解的细胞的团聚开始并达到紧密的聚集阶段,球状体形成过程随着时间经历压实。这在生物医学领域中是特别重要的,其中通常用于分析的生物材料不是标准化的,从而导致结果较不可靠。对样品的堆积密度以及重量、形状和尺寸的同时测量,可以允许掌握标准球状体生长的最佳条件。此外,球状体可以从不同类型的细胞或其组合中生成,因此达到成熟所需的时间和成熟期的质量密度特征对于每种类型的球状体都是不同的。确定在球状体形成过程期间的质量密度值对于重要应用领域是重要的,该应用领域涉及工业药物筛选过程。在这个背景下,可以通过研究药物在球状体本身中的吸收来评估药理学治疗的功效。实际上,已知药物的渗透与聚集体的紧密性水平高度相关,其又可以与其质量密度相关。因此,在质量密度方面,对球状体的正确结构的评估可以大大提升这些结果的再现性。本发明的这个实施方式旨在改进研究的这个方面,这在目前代表了针对药物的发现和开发的3d生物模型的应用的主要限制之一。
[0100]
然而,球状体并不是在生物医学领域中使用的唯一微粒。微粒的各种性质也反映在它们所涵盖的广泛尺寸范围,这个范围从单个细胞到类器官。鉴于研究人员对整个微粒范围的关注,使用单一仪器对其质量密度、重量、尺寸以及形状进行同时测量的可能性,将会对科学界具有相当大的影响。
[0101]
对此,以下段落描述的方法和/或技术实施例被采用来扩展可以被分析的微粒的尺寸范围。
[0102]
例如,在本发明的适配例中,需要高放大率的光学器件来用于分析微米级微粒,并且能够具有足够的分辨率来检测其尺寸和形状。另一适配例涉及以下事实,即:通常,一毫米的微粒的下落速率往往比一微米的微粒更高。因此,沉淀室100必须足够长以允许测量其最终速度。因此,具体检测装置300和沉淀室100的正确选择可以与扩大本发明的操作领域有关。
[0103]
在上述实施方式的示例中,检测装置300由图像采集系统组成,该图像采集系统在
微粒420在沉淀室100内部移动期间采集其一系列帧。对这类图像进行处理以获得微粒质心相对于时间的尺寸、形状和位置。如图4所示,使用线性回归算法来计算最终速度。这个具体实施方式要求收集足够数量的运动微粒图像以便获得正确数量的点,然后这些点将由回归算法使用。例如,在球形微粒的条件下,可接受的点的数量可以是5,而在非球形微粒的条件下,可接受的点的数量可以更多,这是由于在识别微粒质心时会有额外的不确定度。具体地,在测量期间装置能够获得的点数取决于各种实验和技术因子。这些包括微粒的最终速度、由识别系统可观察到的沉淀室的部分的长度、帧速率以及光学分辨率。这类因子可以组合在公式中,该公式包括在具体的技术和实验条件下被检测的分析点的数量,在本文中示出为:
[0104][0105]
在本发明的实施例的特别实施方式中,可接受数量的分析点固定为具体值,例如10个。相反地,在本发明的另一实施例中,这样的可接受数量的分析点是可变的,并且由优化算法调节。例如,该算法可以基于作为时间的函数的微粒位置数据的适配质量来调整分析点的理想数量。
[0106]
此外,为了提高这些测量的准确度,装置允许在执行分析之前将微粒定位在沉淀室的中心。例如,在本发明的一个实施例中,装置通过沉淀室100的几何形状变化和/或变窄来使用微粒定心系统。该运行原理是基于沉淀室的一个具体几何形状的使用,该几何形状允许在其中获得具有非零水平分量的层流。在这类条件下,通过对泵送系统200的适当控制,微粒可以被运输到沉淀通道的区域中,而流在其中具有零水平分量。在下文中,并且更通常地,在本发明的上下文中,垂直是指平行于重力矢量的方向,而水平是指垂直于垂直方向的任何矢量。
[0107]
例如,如果沉淀室是垂直布置的,如果微粒处于沉淀室内部的一个位置,而流线在其中具有非零水平分量,那么微粒也受到因该流的水平分量所导致的横向推力的影响。在本发明的一个具体实施例中,沉淀室100是垂直定向并由具有不同尺寸的水平截面的两个部分组成,使得具有较宽截面的通道(100a)位于较窄截面的通道(100b)下方,如图7a所示。此外,在这个特别示例中,沉淀室(100)的两个部分(100a和100b)是由具有倾斜截面(100c)的通道部分同轴地连接的。对微粒进行定心所需的时间可以变化,取决于部分100c的壁的倾斜角的值、沉淀通道(100b)的较小部分相对于较大部分(100a)的截面的变窄百分比或者这两个截面的面积之间的关系(图7a)。在任何情况下,这些参数的具体值对定心系统的运行都不是必要的。在本发明的另一实施方式中,具有倾斜截面(100c)的通道部分由截面的不连续变化或者相对于垂直轴线的90
°
壁替换。
[0108]
在图7a中示出了定心系统的具体示例,以便描述定心系统的运行。在这个具体示例中,沉淀室100的最宽部分的几何形状具有边长为2mm的正方形截面(100a),而沉淀室100的最窄部分具有边长为1mm的正方形截面(100b)。这两个部分通过变窄部分(100c)连接,在这种情况下是渐变的,相对于沉淀室的纵向轴线具有45
°
的角度。在这个示例中给出的与沉淀室的正方形截面相关的这些测量是指示性的。因此,在沉淀室的两个部分的截面之间的关系以及变窄部分的倾斜度并不局限于来源于这类测量中的那些。在这个示例中给出的尺寸是指示性的,并且这些特别值是可选的。
[0109]
在定心装置的特别使用方法中,以脉冲方式调节流体系统。在一个示例中,在时间t1(420t1)时,微粒420处于图7b中所描述的位置。一旦泵送系统200已经激活,沿着由几何形状施加的流线运输微粒,直到它在时间t2(420t2)时如图7b所示定位。然后将流中断,允许微粒在重力和静液压力的平衡作用下开始下落。在此之后,在时间t3(420t3)时,微粒将相对于沉淀室100处于更中心的位置。泵送系统200的进一步激活允许重复该过程,直到实现微粒420的定心。
[0110]
在定心系统的另一使用方法中,微粒420通过沉淀室100内部的特殊调制流而保持在变窄部分100c中,以便平衡重力作用,如图7c所示。由此,因通道几何形状的变化生成的流线而引起的横向分量用作横向推力,从而将微粒从在时间ta(420ta)时的横向位置移动到在时间tb(420tb)时的更中心的位置。
[0111]
对于所示的两个解决方案,泵送系统200可以手动或自动操作。
[0112]
在本发明的一个实施例中,检测装置300由光学装置组成,该光学装置包括安装在可移动支撑件上的显微镜系统。光学装置的分辨率适用于采集所有关注微粒的图像,达到足以处理其尺寸和形状的细节水平。可移动支撑件由处理器500引导以跟随微粒在沉淀室100内的移动,使得观察到的下落长度可以长到足以测量足够的点,以获得对微粒420的最终速度的可靠处理。类似地,在另一实施例中,可移动支撑件适用于移动沉淀室100,使得微粒420保持在检测装置300的工作范围内。
[0113]
在另一实施方式中,检测装置300包括能够支持各种放大率的光学系统。例如,这是通过机械操作的光轴来实现的。处理器500为被检查的具体微粒选择正确的放大率,并且还能够在分辨率(用于测量微粒的几何特性)和视野的尺寸之间选择适当的平衡。后者必须大到足以允许处理微粒的最终速度。
[0114]
在另一实施例中,可以在没有移动部件帮助的情况下选择用于测量具体微粒的正确放大率。在这个实施例中,沉淀室包括多个流动通道,并且检测装置监测这些不同的流动通道,而每个流动通道均有不同的放大率。在测量之前,检测装置识别微粒,并且处理器管理将其引入合适的流动通道。此外,流动通道的架构可以以不同的配置实现,以便满足对微粒多样性的需求。事实上,尺寸、截面和几何形状可以是变化的,特别是注意通道的长度。由此,较大的微粒被插入较长的通道中,并且以较低的分辨率对其监测以用于较大的视场。相反地,较小的微粒被插入较短的通道中,并且以较高的分辨率对其监测以用于较小的视场。
[0115]
在这个具体实施例的变型例中,用于将微粒引入沉淀室100中的机构是一种流体多路复用器。在这个实施例的另一变型例中(图8),沉淀室包括几个流动通道(例如110a、110b和110c),这些流动通道连接到独立的流量调节器(例如开/关阀271a、271b、271c)上。所有的流动通道在流体装置内并联连接。在这种情况下,检测装置300在微粒到达分支之前在具体的光学可进入通道150中识别该微粒,并且选择流动通道,而微粒将通过对这些阀的控制而被引入该流动通道中。在这个实施例的另一变型例中,操作者通过操作定位在入口通道210上的选择阀来手动选择用于测量的流动通道。
[0116]
允许测量特别大的微粒的移动的一种不同的策略,在于其不同的定位方法,其中检测装置300能够识别微粒420通过沉淀室100中的不同目标位置的通过。可以调整这些目标位置之间的距离以及由这种定位系统覆盖的总距离,以精确地确定微粒的最终速度。然后,通过将行进的距离除以经过的时间来确定微粒的最终速度。
[0117]
在这个装置以及相关方法的一个技术实施方式中,检测装置300包括专用于沉淀室100的目标位置的几个图像识别系统。除了有助于测量最终速度之外,后者还收集关于微粒形状和尺寸的信息。在另一技术实施方式中,检测装置300包括位于沉淀室100的目标位置(例如,115a、115b和115c)处的一系列传感器(例如,图9中的315a、315b和315c),以及用于收集微粒420的形状和尺寸信息的独立图像识别系统320。
[0118]
允许测量特别大的微粒的移动的另一策略,在于作用于分析介质的质量密度和黏度。例如,在本发明的一个实施例中,该系统适用于承载分析介质450,分析介质450具有用于经分析的微粒420的类型的具体质量密度,并且特别地对应于微粒群的平均质量密度(例如,在sw620球状体的情况下为1035fg/um3)。因此,作用在微粒上的总力,即重力和静液压力之和,取决于微粒的质量密度而向下或向上导向。因此,在没有流的测量步骤期间,分析介质的密度较大的微粒往往会向下移动,而对于密度较小的微粒,反之亦然。
[0119]
在这个具体实施例中,处理器500和相关的处理算法适用于计算下降或上升的最终速度。此外,流生成系统230能够促进沉淀室100内部的流,以既用于重力矢量又对抗重力矢量。这允许样品相对于其最终速度在相对方向上被移动,因而允许重复测量。类似地,在本发明的另一实施例中,该系统适用于容纳高黏度分析介质450,其降低了微粒最终速度。
[0120]
在本发明的另一个实施例中,该装置适用于改变分析介质450,其中一个或多个分析介质450具有不同的质量密度。这个实施方式的装置的架构与图2中描述的架构相同,其中泵送系统200适用于选择待引入系统中的新分析介质。在这种情况下,检测装置300测量微粒最终速度,并且激活泵送系统300以修改分析介质,使得微粒最终速度下降。可以重复这个方案,直到微粒最终速度低到足以可容易检测和测量。
[0121]
在对本发明的实施例及其一些实施方式的上述描述中,已经描述了用于执行对一大组球形微粒的质量密度、重量、尺寸和/或形状的组合测量的方法和相关工具。然而,在生物医学领域中使用的许多生物样品(包括上述样品)可与球形度存在一些偏差。特别地,对于球状体和类器官,球形度主要取决于在聚集体自身的形成和成熟期间组成和/或细胞活性的局部可变性。由于例如细胞骨架的内部构造、细胞外基质的不均匀外部压力或刚性细胞结构的存在,单个细胞可以具有与球形形状相比的轻微变化。因此,在以下段落中,公开了本发明的变型例,这些变型例考虑了其中微粒的三维形状与球形度偏离的情况。
[0122]
对于球形微粒,许多检测方法和算法可用于计算与其半径相关的摩擦系数,与球形微粒的情况不同,非球形微粒的情况更为复杂,并且需要泛化先前讨论的理论。
[0123]
特别地,等式1和等式2泛化如下:
[0124][0125]
和
[0126][0127]
在这种形式中,摩擦系数k和体积v
p
都取决于微粒形状和取向。关于阐述物体的几何特征以近似摩擦系数k的理论,存在许多文献。这类几何特征可以是椭圆度,或者是在球(其具有与被检查的微粒相同的体积)的表面积和微粒本身的实际表面之间的比率。此外,如果微粒的完整3d形状是已知的,那么摩擦系数k理论上可以通过计算流体动力学模拟来
计算。
[0128]
因此,在本发明的实施例的上下文中(包括前述段落)使用的术语“半径”旨在作为在球形微粒的情况下的几何半径。然而,术语半径应理解为“有效半径”,并且还可以用于表示代表几乎球形或非球形的微粒的一维几何特征。例如,术语半径可以理解为表面点距质心的平均距离,或者甚至为二维面积与周界的比率的两倍,或者为费雷特半径(feret radius,周界除以两倍π)。
[0129]
因此,如先前所写的,在本发明的实施例的上下文中使用的术语“形状”和“尺寸”旨在作为对微粒的任何几何描述,这些几何描述可以用于表示或近似其二维或三维几何形状。例如,在球形微粒的情况下,可以理解为半径的量,或者在几乎球形和非球形微粒的情况下,可以理解为其他几何特征的量。
[0130]
此外,相应地,在本发明的实施例的上下文中使用的术语“质量密度”或简称的“密度”应理解为在球形微粒的情况下质量与体积的比率。然而,这些术语还可以用于表示“有效质量密度”,除了先前描述的密度定义之外,它还包括取决于形状因子(如在几乎球形和非球形微粒的情况下的椭圆度和表面粗糙度)的变化。
[0131]
同样地,在本发明的实施例的上下文中使用的术语“重量”在球形微粒的情况下应理解为重力质量。而在非球形或几乎球形的微粒的情况下,其旨在作为“有效重量”。类似于对术语“质量密度”给出的描述,术语“有效重量”包括取决于形状因子(如椭圆度和表面粗糙度)的变化。
[0132]
如先前在本发明的不同实施例中所述的,执行对相同微粒的不同测量允许提高结果的可靠性。在球形微粒的情况下,所获得的统计分布排他地与测量不确定度相关。相反地,对于几乎球形和非球形的微粒,最终速度测量的实验分布可以用于描述微粒的尺寸和形状。在这个实施例的变型例中,最终速度的标准偏差可用作用于确定微粒椭圆度的参数。这个信息例如对于均匀球状体的生成和选择是相关的,以用作药物开发的模型。在这个实施例的不同变型例中,从这些测量中获得的数据分布的不对称性可以与几何对称因子相关,峰度指数可以与形状的异质性相关,并且多模式可以与二维微粒投影的分布相关。
[0133]
在本发明的实施例的另一实施方式中,对微粒图像进行处理,以例如采用断层成像算法来获得其三维重构。这种重构然后可以由用于计算摩擦系数的计算工具来处理。这种方法改善了对几乎球形和非球形微粒的质量密度的绝对值的测量。
[0134]
特别地,可以采用不同的技术实施方式来获得对微粒的3d形状的重构或者改进其形态特征。
[0135]
在本发明的实施例的一个具体实施方式中,检测装置300包括双摄像头系统(图10)。这些摄像头相对于沉淀室100彼此垂直的取向确保了从两个不同的角度采集微粒图像。然后,这类图像由处理器500处理,以获得3d模型。
[0136]
相反地,如果使用单个图像采集系统,那么可以采用不同的光学、流体或机械策略。例如,在本发明的实施例的另一实施方式中,流体装置就包括其中两个光学反射镜113和114,它们靠近沉淀室100的后壁,并且相对于装置300具有预定的倾斜度(图11)。前置摄像头维持焦平面,以便包括分别从反射镜113和114获得的微粒430和440的反射图像。通过这种实施方式,可以同时从微粒的不同空间视角收集图像并将它们用于其3d重构。
[0137]
在本发明的实施例的另一实施方式中,该装置适用于采集微粒420的图像堆叠。在
这种实施方式中,检测装置300由至少一个摄像头组成,而焦平面在其中被调整成允许通过采集多个图像来扫描微粒。这种被收集的图像可以由处理器500通过图像滤波器的应用(如去卷积)来处理,以执行微粒的3d重构。还可以实施3d微粒重构等另外的实施例,如其他图像堆叠技术、全息显微术或光片显微术。
[0138]
在本发明的另一实施例中,检测装置300由围绕沉淀室100做轨道运行的图像采集系统组成,如图12中所示。在这个实施例的具体实施方式中,沉淀室100是圆柱形的。这允许从不同的微粒角度采集图像,然后通过断层摄影重构对这些图像进行处理,用于对其形态进行3d重构。在这个具体实施方式中,在沉淀室100附近使用参考标记,以减少在测量微粒420的位置中的不确定度,其中微粒420由检测装置300的旋转而引入。可以使用相同的策略来最小化在包括检测系统300的移动部件的任何其他实施方式中引入的不确定度。在这个实施例的变型例中,旋转的检测装置300适用于竖直移动并与样品的最终速度相关地跟随样品的移动。以上实施方式和方法采用了已知技术,其被重新布置,以获得微粒的3d重构。当然,其他现有的而在本文中未示出的解决方案也可以结合本发明的实施例。
[0139]
先前段落已经描述了本发明的方法、技术和主要使用模式。然而,在本文中将会示出本发明的不同使用模式,以便展示其进一步优点。
[0140]
例如,一些替代例会涉及:针对高通量分析(所产生的数据量上的增长)而导入的对微粒群的组合测量;与如药物测试等应用相关的随着时间对微粒的培养和延长分析;以及与医学应用或生物模型标准化相关的微粒分类。
[0141]
从对大量单微粒或群体所执行的研究中获得的高通量分析,在生物学领域中是极其重要的。例如,如受检查群体的异质性的信息允许了对存在于生物样品内的亚群的具体行为的掌握。事实上,这种行为经常往往与整个群体的平均值相比具有显著变化,并且变成重要的鉴别性分析因子。现今,用于测量群体中每个微粒的质量密度、重量、尺寸和形状的仪器在市场上是不可购得的。
[0142]
本发明针对现有技术中的这种缺点提出了解决方案,从而还允许总体上通过流体装置的实施方式来外推统计分析微粒群所需要的数据,其中处理器500从检测系统300接收的微粒数据与大量微粒相关,并且包括多于一个微粒的速度、形状、位置以及尺寸中的至少一者。具体实施例利用图2中描述的相同方案,其中检测系统300由连接到处理器500的显微镜系统组成。这个实施方式允许对群中每个微粒的质量密度、重量、尺寸以及形状的伴随测量。与上述主要的使用方法类似,容纳在分析介质450中的微粒420由罐400收集并通过泵送系统200的入口通道210引入。激活流生成系统230以引导微粒进入沉淀室100,然后将流停止,并且在微粒因重力下落期间执行分析。在这个具体的使用模式中,检测装置300适用于在测量期间同时监测存在于沉淀室100内部的每个微粒420。通过对沉淀室100内部监测的每个微粒420编入索引来计算该群的每个单独组分的最终速度和尺寸。由此,在几次重复测量之后,外推群的质量密度、重量、尺寸和形状的分布,同时仍维持关于每个微粒的信息。
[0143]
在另一实施方式中,通过沉淀室100的特别几何形状来获得了更大量的数据。虽然在图中所示出的装置中,沉淀室200或包括在其中的流动通道110是笔直的且没有曲线,但是沉淀室200也可以替代地具有一种曲线几何形状。在这个实施例中,沉淀室例如可以包括具有蛇形架构的单一通道,使得检测装置300可以对其中发生分析的几个垂直部分进行监测。应用于本发明的实施例的高通量允许外推重要的数据,如经分析的微粒群的统计分布。
例如,正常(或高斯)分布提供关于群的同质性的信息。这种分布的标准偏差的分析因此可以与定义样品的质量相关。例如,在细胞数据库的情况下,这是重要的,其中细胞数据库可以证明可用样品的质量。相反地,双峰或多峰分布可以识别不同亚群或类别的存在。例如,它可以提供关于存在于异质性群中的不同细胞系的信息,或者在同质性群的情况下,它可以区分处于细胞生命周期不同阶段的细胞。此外,还考虑了经受药理学治疗的同质性群的情况,从正态到双模态或多模态的统计分布的差异可以区分例如药物的渗透和/或其功效。
[0144]
本发明的另一方面旨在由能够保持微粒悬浮在沉淀室内部的装置通过闭环流体系统来避免浪费分析介质。这对于使用昂贵的分析介质的应用而言是特别重要的,如在药物的漫长的上市前特征化阶段期间。
[0145]
本发明另一实施方式涉及单个细胞或细胞团随时间的培养和同时分析。这样的方面在生物医学和临床领域中是非常令人关注的。例如,在药物治疗期间监测样品的物理性质的变化,这在用于如个人化医学、肿瘤学和医学辅助治疗的应用的药理学领域中是有用的。
[0146]
这个实施方式由用于在期望的时间段(长达几周)内测量微粒的质量密度、重量、尺寸和/或形状的装置和相应的方法组成。此外,该方法是非破坏性的,并且在分析之后可以适当地恢复被选择用于分析的具体微粒以用于进一步研究。
[0147]
虽然在图2和图3所示的流体装置中,泵送系统200是线性的,但是泵送系统200也可以包括一个或多个液体再循环系统,以及用于泵送系统200和沉淀室内部的液体循环的一个或多个流生成系统。在图13所示的具体实施方式中,泵送系统200包括另一再循环通道250和次级泵送系统,在本文中称为再循环装置240(图13)。用于将微粒引入流体装置中的方案与先前描述的类似。将包含在分析介质450中的微粒420从罐400中提取并通过入口通道210引入泵送系统200中。激活流生成系统230以将微粒引入沉淀室100中,沉淀室100由检测装置300监测。泵送系统200还包括再循环通道250和再循环装置240(图13),其中再循环通道250与沉淀室循环连接,而再循环装置240被处理器500激活以将微粒保持在沉淀室100内部,这是通过基于从检测系统300中获得的微粒数据来生成受控制的循环流所实现的。再循环通道250允许分析介质再循环,这有着使其消耗最小化的优点。
[0148]
本发明的实施例的一种实施方式允许在用一种或多种不同的分析介质451替换主分析介质450之前和之后,测量微粒质量密度、重量、尺寸以及形状。在这个实施方式中,泵送系统200还包括一个或多个与沉淀室100流体连接的次级通道,用于将液体和/或微粒引入一个或多个额外的罐中或从一个或多个额外的罐中移除。次级通道可以直接连接到沉淀室100,或者它们可以通过入口通道或通过次级流体回路连接。这个实施例的具体实施方式采用图2所示的流体装置的变型。通过泵送系统200将微粒420引入并保持悬浮在沉淀室100中的第一分析介质450内部。在这个实施方式中,泵送系统200包括用于缓冲液交换的次级通道260(图14),其连接到包含新分析介质451的第二罐401。该系统允许新分析介质451通过用于缓冲液更换的次级通道260引入沉淀室100中。在更换主分析介质450期间,将微粒保持在沉淀室100内部。经几次重复,这个过程会导致在沉淀室100和再循环通道250两者中分析介质之间实现完全交换。在这个实施例的一个具体变型例中,在用于缓冲液交换的次级通道260和入口通道210之间的接合处是选择阀270。在这个实施例的另一变型例中,该系统适用于由相同入口通道210从包含新分析介质451的罐401中进行抽取,通过或手动或自动
罐替换400将微粒通过入口通道210引入。在这个实施方式的另一变型中,泵送系统200包括用于缓冲液交换的次级通道260(图14)、再循环通道250和再循环系统240(图13)。这个实施方式允许在甚至几天或几周的时间段期间执行对微粒质量密度、重量、尺寸和/或形状的测量,在此期间可以执行保持和分析微粒所在的液体的变化。这些使用模式的组合实际上可以有利于不同的应用。例如,在执行分析介质的频繁变化的同时,可以在长时间段内处理微粒。这样,在每次替换期间,可以引入特征与先前不同的第二液体,例如药物浓度变化不大以用于分析其毒性。相反,对该处理的强度可以更大,从而引入特征与第一分析介质显著不同的第二分析介质,并且然后监测微粒对这种变化的反应。在本发明的一个实施例中,相同微粒在经受离子强度不同的一系列分析介质时,对它们进行分析。通过这个实施方式,可以测量离子强度对微粒420的影响。在一些使用方法中,对正确分析介质的使用对于这个实施例的技术实施方式是关键的一个方面:如果微粒具有半透膜(例如,如果它是单细胞或球状体),那么等渗分析介质(例如对于细胞而言pbs 0.9%w/v)允许测量天然微粒质量密度。在本发明的不同实施例中,测试介质并不与微粒等渗,并且可以测量离子强度对微粒的影响。
[0149]
在本发明的不同实施例中,用于处理微粒420的这一系列分析介质可以包含药物或其他生物活性化合物,可影响其尺寸、体积、质量密度和/或重量。在这种情况下,该系统测量化合物对细胞、球状体或类器官的影响。监测堆积密度和活样品尺寸的潜在结果示出在图15中所示的图表性描绘中。这里,微粒被视为具有球形几何形状,并且其尺寸被绘制为直径。所示示例旨在识别球状体的成熟阶段,以及其与药物相互作用所需的时间。在这个说明性的曲线图中,微粒在直径和质量密度两者上增长,直到达到时间t1。在此之后,观察到直径的稳定化,虽然密度还在继续增加。这表明直到时间t2的压实阶段,这时密度也达到平台期,其中球状体处于理想的成熟条件以改变分析介质。时间t3表示与药物引入有关的时刻,并且后续趋势示出了其影响。这个过程提供了观察和比较密度和直径随时间的变化以及收集关于微粒与药物的相互作用的有价值细节的可能性。
[0150]
这个实施例的一个变型例涉及培养物和长期微生物分析与用于改变分析介质的溶液的组合。事实上,科学研究的另一重要方面涉及在样品周围环境的变化(如ph、离子强度、介质中生长因子的变化)期间,或在使用药理学试剂和/或化学品的具体治疗期间,监测样品的可能性。
[0151]
本发明的实施例的另外的使用模式允许微粒的分类,即对微粒亚群的组织和分类。这个操作在生物医学领域中是重要的,因为它允许基于具体特性或几何特征来收集微粒亚群。细胞分类通常用于医学、药理学和科学研究。其应用包括例如再生医学和个人化医学领域,以及抗癌疗法或病毒学领域。当前的细胞分类方法基于如蛋白质标记物的存在或特异性生物化学相互作用的因子来选择样品。然而,目前没有能够基于质量密度、重量、尺寸和形状选择和分类大范围的样品的技术。因此,本发明的另一实施方式涉及用于基于这些特性的伴随测量对微粒进行选择性分类的一种方法以及相关装置。
[0152]
在这个实施方式的一个具体实施例中,沉淀室100包括分叉,该分叉将它连接到回收通道120上,进而流体连接到泵送系统200的具体部分上,本文中称为用于分类的次级通道280(图16)。用于分类的入口通道210和次级通道280都由流量调节器(例如阀270和290)控制。在这个实施方式中,当阀290关闭而阀270保持打开时,微粒420通过入口通道210被引入沉淀室100中。一旦如在先前的实施方式中所描述的完成了对微粒的测量,就会基于质量
密度、重量、尺寸以及形状值对结果进行评估以用于对样品分类。然后通过激活泵送系统200来收集所选择的微粒,同时阀270关闭而阀290保持打开,以允许微粒通过回收通道120和用于分类的次级通道280,最终到达罐700(图16)。
[0153]
在本实施例的一个变型例中,微粒是排他地基于其质量密度来选择和分类的。这与降低科学测试的非同质性相关,从而允许例如选择和收集压实度类似的球状体亚群。在本实施例的另一变型例中,可以组合几个测量参数以用于选择所收集的微粒。例如,如测量出的直径的标准偏差和最终速度等特征可以用于根据其球形度对微粒进行分类。这个具体应用可以与测试药物在不同同质性球状体批次上的扩散相关,并且可以提供关于药物到达细胞核所花费的时间的信息。这个相同应用还可以提供关于有效跨越多个细胞层所需的药物的浓度水平的信息,以及对其毒性执行研究。
[0154]
在本实施例的另外的变型例中,用于分类的参数和限值例如可以由用户定义,或者从数据库中提取;或者它们可以由无监督的算法自动定义,而该算法可以对群内类似的微粒族群进行分类。
[0155]
本发明的另一方面涉及从手动到自动化过程转变的重要性,特别是当从实验室用途移到大规模医疗和工业应用时。由于硬件组件数量少,所示本发明被构想为通过使用现有装置而容易自动化。利用现有技术,这样的部件也可以容易地小型化。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1