因突触功能不全引起的疾病或附带突触功能不全的疾病的判定方法与流程
1.本发明涉及一种能够早期且简便地判定因突触功能不全引起的疾病或附带突触功能不全的疾病的有无发病或重症度的判定方法、因突触功能不全引起的疾病或附带突触功能不全的疾病的预防剂和/或治疗剂的筛选方法、用于在该判定方法或该筛选方法中使用的抗体、用于进行该判定方法的试剂盒。
背景技术:
2.痴呆症的主要原因即阿尔茨海默病是不可逆的进行性脑疾病,其是由脑中的突触陷入功能不全而产生的。近年来,阿尔茨海默病患者的增加成为社会关注的重大问题,期望能确立其早期诊断方法或治疗药。在阿尔茨海默病患者的死后脑中观察到老年斑,已知其是“淀粉样蛋白β蛋白质”的聚集体(淀粉样蛋白斑)。据报道,淀粉样蛋白β蛋白质的沉积是在病理学上能确认到的最早期的病变,淀粉样蛋白β蛋白质聚集并直接表现出神经细胞毒性。而且,目前被广泛接受的是:根据家族性阿尔茨海默病患者的基因分析,淀粉样蛋白β蛋白质的产生和蓄积的异常与阿尔茨海默病的发病存在广泛的关联。这被称为淀粉样蛋白级联假说。由此,通过众多的研究已广泛接受淀粉样蛋白β蛋白质是阿尔茨海默病的主要原因(非专利文献1)。另外,可知淀粉样蛋白β蛋白质向脑中的蓄积是从距发病20年以上以前就开始的。
3.除了阿尔茨海默病以外,还已知因脑血流降低(抑郁症等)、脑出血、脑梗塞等也会产生突触功能不全。进而,还已知线粒体的基因疾病、糖尿病导致的痴呆症等。另外,有时也会因药物依赖等而引起突触功能不全。在这些因突触功能不全引起的疾病或附带突触功能不全的疾病中,认为因突触功能不全而使得认知功能降低,但其难以诊断。例如,阿尔茨海默病的诊断可以仅通过在死亡后进行病理解剖来确诊,生前的诊断通过提问式检查或图像检查进行,但都是出现自觉症状后的诊断,实际情况是不能开始早期的治疗。另外,还有报道能够通过脑脊髓液中的淀粉样蛋白β42蛋白质的浓度降低来进行阿尔茨海默病的诊断(非专利文献2),但存在由于是侵袭性高的检查而难以对高龄者应用的问题。另外,现状所使用的阿尔茨海默病的治疗药都是抑制症状的药,不存在有关根治的药物。另外,在其他的因突触功能不全引起的疾病或附带突触功能不全的疾病中,也依赖于提问式检查(抑郁症、痴呆症等)或图像检查(脑出血等),不存在用于简便且早期地诊断的方法。
4.本发明人们在世界上首次发现在生成过程的神经细胞中大量表达的作为肌动蛋白结合蛋白的脑发育调节蛋白(drebrin)(例如,参照非专利文献3及4),并且已经证明:该脑发育调节蛋白通过改变肌动蛋白纤维的性状来参与神经细胞的形态形成、尤其是突起形成(例如,参照非专利文献5~7);生成过程中移动的神经细胞存在于全部的细胞体和突起中,但成熟的神经细胞特异性地存在于棘结构(树突棘)中(例如,参照非专利文献8~10)。脑发育调节蛋白存在胚胎型(embryonic type)的脑发育调节蛋白e和成体型(adult type)的脑发育调节蛋白a这两种亚型(例如,参照非专利文献4),在成熟神经细胞的树突棘中特
异性地呈现的脑发育调节蛋白a具有仅在神经细胞中表达的特征(例如,参照非专利文献9和10)。本发明人们还报道在阿尔茨海默病等痴呆性疾病中树突棘的脑发育调节蛋白大范围消失(非专利文献11)。
5.现有技术文献
6.非专利文献
7.非专利文献1:齐藤贵志、西道隆臣“阿尔茨海默病的模型小鼠”,日药理志(folia pharmacol.jpn.)144,250-252,2014
8.非专利文献2:j.neurol.sci.148,41-45,1997
9.非专利文献3:j.neurochem.44,1210-1216,1985
10.非专利文献4:j.biochem.117,231-236,1995
11.非专利文献5:j.neurosci.res.38,149-159,1994
12.非专利文献6:exp.cell res.215,145-153,1994
13.非专利文献7:j.biol.chem.269,29928-29933,1994
14.非专利文献8:j.neurosci.15,7161-7170,1996
15.非专利文献9:dev.brain res.29,233-244,1986
16.非专利文献10:brain res.413,374-378,1987
17.非专利文献11:j neurosci.res.43(1),87-92,1996
技术实现要素:
18.发明要解决的课题
19.如上所述,现状是不能早期且简便地判定因突触功能不全引起的疾病或附带突触功能不全的疾病。而且,不能直接地治疗突触功能不全,例如在阿尔茨海默病的治疗中也达不到根治,现状是进行对症疗法。本发明的课题在于提供能够早期且简便地判定因突触功能不全引起的疾病或附带突触功能不全的疾病的有无发病或重症度的判定方法,并且提供因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗剂、预防剂的筛选方法。
20.用于解决课题的手段
21.本发明人们基于在阿尔茨海默病等痴呆性疾病中树突棘的脑发育调节蛋白a大范围消失的见解,认为在阿尔茨海默病患者中脑发育调节蛋白a从神经细胞漏出至血液中。因此,为了检测血液中的脑发育调节蛋白a,按照常规方法进行蛋白a/g磁珠(protein a/g beads)处理以除去血液中的抗体,之后,使用识别脑发育调节蛋白a及脑发育调节蛋白e的抗脑发育调节蛋白抗体,供于蛋白质印迹(western blotting)法,但是不能确认脑发育调节蛋白的条带。慎重起见,本发明人们针对血液试样的基于蛋白a/g磁珠的沉降级分使用抗脑发育调节蛋白抗体供于蛋白质印迹法,结果与预想相反,能够在约130kda的位置确认脑发育调节蛋白的条带。为了确认该脑发育调节蛋白的条带是否为脑发育调节蛋白a,针对血液试样的基于蛋白a/g磁珠的沉降级分采用抗脑发育调节蛋白a抗体进行蛋白质印迹,结果发现,约130kda的条带虽然不是脑发育调节蛋白a全长而是脑发育调节蛋白e,但是能够检测到多条比脑发育调节蛋白a全长小的分子量的条带(其能够通过抗脑发育调节蛋白a抗体来检测)。对于在此所检测到的条带,认为是具有对脑发育调节蛋白a基因具有特征性的ins2序列的翻译肽的脑发育调节蛋白a的片段、或者剪接变异体(splice variant)。本发明
人们进一步反复研究,发现这样的脑发育调节蛋白a关联蛋白质(darps:drebrin a related proteins)大多存在于来自罹患因突触功能不全引起的疾病、或附带突触功能不全的疾病的患者的生物体试样中。进而,本发明人们发现:darps经由自身抗体与蛋白a/g磁珠结合;识别脑发育调节蛋白的自身抗体能够损伤神经细胞;通过抑制由自身抗体带来的神经细胞的损伤,能够治疗或预防因突触功能不全引起的疾病或附带突触功能不全的疾病。本发明是根据这些见解而完成的。
22.即,本发明涉及以下内容。
23.〔1〕一种因突触功能不全引起的疾病或附带突触功能不全的疾病的发病风险、或者有无发病的判定方法,其特征在于,包括以下的步骤(a-1)~(c-1):
24.步骤(a-1),对从受试者提取的生物体试样中的脑发育调节蛋白a关联蛋白质(darps)的浓度进行测定;
25.步骤(b-1),将步骤(a-1)中测定得到的darps的浓度与对照者中的darps的浓度进行比较,所述对照者未发生因突触功能不全引起的疾病或附带突触功能不全的疾病;
26.步骤(c-1),当步骤(a-1)中测定得到的darps的浓度比上述对照者中的darps的浓度高时,评价为上述受试者发生因突触功能不全引起的疾病或附带突触功能不全的疾病发病的风险高、或者已发生因突触功能不全引起的疾病或附带突触功能不全的疾病的可能性高。
27.〔2〕一种因突触功能不全引起的疾病或附带突触功能不全的疾病的重症度的判定方法,其特征在于,包括以下的步骤(a-2)~(c-2):
28.步骤(a-2),对从受试者提取的生物体试样中的脑发育调节蛋白a关联蛋白质(darps)的浓度进行测定,所述受试者已发生因突触功能不全引起的疾病或附带突触功能不全的疾病;
29.步骤(b-2),将步骤(a-2)中测定得到的darps的浓度与对照者中的darps的浓度进行比较,所述对照者已发生因突触功能不全引起的疾病或附带突触功能不全的疾病;
30.步骤(c-2),当步骤(a-2)中测定得到的darps和/或darps自身抗体的浓度比上述对照者中的darps和/或darps自身抗体的浓度高时,评价为上述受试者与上述对照者相比因突触功能不全引起的疾病或附带突触功能不全的疾病重症化的可能性高。
31.〔3〕一种因突触功能不全引起的疾病或附带突触功能不全的疾病的预防剂、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗剂的筛选方法,其特征在于,包括以下的步骤(a-3)~(c-3):
32.步骤(a-3),对从施用了被检物质的突触功能不全模型非人动物提取的试样中的脑发育调节蛋白a关联蛋白质(darps)的浓度进行测定;
33.步骤(b-3),将步骤(a-3)中测定得到的脑发育调节蛋白a关联蛋白质(darps)的浓度与未施用上述被检物质的突触功能不全模型非人动物中的脑发育调节蛋白a关联蛋白质(darps)的浓度进行比较;
34.步骤(c-3),当步骤(a-3)中测定得到的脑发育调节蛋白a关联蛋白质(darps)的浓度比不施用上述被检物质的突触功能不全模型非人动物中的脑发育调节蛋白a关联蛋白质(darps)的浓度低时,评价为上述被检物质针对因突触功能不全引起的疾病或附带突触功能不全的疾病的预防、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗
有效。
35.〔4〕一种因突触功能不全引起的疾病或附带突触功能不全的疾病的预防剂、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗剂的筛选方法,其特征在于,包括以下的步骤(a-4)~(d-4):
36.步骤(a-4),对突触功能不全模型培养细胞施用被检物质并进行培养;
37.步骤(b-4),对上述突触功能不全模型培养细胞的培养液中的脑发育调节蛋白a关联蛋白质(darps)的浓度进行测定;
38.步骤(c-4),将步骤(b-4)中测定得到的darps的浓度与不施用上述被检物质的突触功能不全模型培养细胞的培养液中的darps的浓度进行比较;
39.步骤(d-4),当步骤(b-4)中测定得到的darps的浓度比不施用上述被检物质的突触功能不全模型培养细胞的培养液中的darps的浓度低时,评价为上述被检物质针对因突触功能不全引起的疾病或附带突触功能不全的疾病的预防、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗有效。
40.〔5〕根据上述〔1〕~〔3〕中任一项所述的方法,其特征在于,生物体试样为脑脊髓液试样或血液试样。
41.〔6〕根据上述〔1〕~〔5〕中任一项所述的方法,其特征在于,darps为选自darp40、darp60、darp70、darp90及darp100中的1或2种以上。
42.〔7〕根据上述〔1〕~〔6〕中任一项所述的方法,其特征在于,因突触功能不全引起的疾病或附带突触功能不全的疾病为神经变性疾病。
43.〔8〕根据上述〔7〕所述的方法,其特征在于,神经变性疾病选自阿尔茨海默病、大脑皮质基底核综合征、帕金森病、脊髓小脑变性症及肌萎缩性侧索硬化症。
44.〔9〕根据上述〔1〕~〔8〕中任一项所述的方法,其特征在于,darps的浓度使用识别脑发育调节蛋白a特异性表位的抗体来测定。
45.〔10〕一种用于在上述〔9〕所述的方法中使用的抗体,其特征在于,所述抗体识别脑发育调节蛋白a特异性表位。
46.〔11〕一种因突触功能不全引起的疾病或附带突触功能不全的疾病的发病风险、有无发病或重症度的判定用试剂盒,其特征在于,所述试剂盒包含上述〔10〕所述的抗体。
47.〔12〕一种因突触功能不全引起的疾病或附带突触功能不全的疾病的预防剂、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗剂的筛选方法,其特征在于,探索针对脑发育调节蛋白a关联蛋白质(darps)自身抗体的显性负肽。
48.另外,作为本发明的其他实施方式,可列举:
49.一种因突触功能不全引起的疾病或附带突触功能不全的疾病的发病风险、或者有无发病的判定方法,其中,所述判定方法包括步骤(a-1),所述步骤(a-1)对从受试者提取的生物体试样中的脑发育调节蛋白a关联蛋白质(darps)的浓度进行测定;
50.一种因突触功能不全引起的疾病或附带突触功能不全的疾病的重症度的判定方法,其中,所述判定方法包括步骤(a-2),所述步骤(a-2)对从受试者提取的生物体试样中的脑发育调节蛋白a关联蛋白质(darps)的浓度进行测定,所述受试者已发生因突触功能不全引起的疾病或附带突触功能不全的疾病;
51.一种因突触功能不全引起的疾病或附带突触功能不全的疾病的发病风险或有无
发病的判定用生物标记物、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的重症度的判定用生物标记物,其中,所述判定用生物标记物包含1种或2种以上的脑发育调节蛋白a关联蛋白质(darps);
52.一种因突触功能不全引起的疾病或附带突触功能不全的疾病的预防剂、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗剂的筛选方法,其中,所述筛选方法包括步骤(a-3),所述步骤(a-3)对从施用了被检物质的突触功能不全模型非人动物中提取的试样中的脑发育调节蛋白a关联蛋白质(darps)的浓度进行测定;
53.一种因突触功能不全引起的疾病或附带突触功能不全的疾病的预防剂、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗剂的筛选方法,其中,所述筛选方法包括上述步骤(a-4)及(b-4);
54.一种对用于诊断因突触功能不全引起的疾病或附带突触功能不全的疾病的发病风险或有无发病的数据进行收集的方法,其中,所述方法包括上述步骤(a-1)~(c-1);
55.一种对用于诊断因突触功能不全引起的疾病或附带突触功能不全的疾病的重症度的数据进行收集的方法,其中,所述方法包括上述步骤(a-2)~(c-2);
56.一种对因突触功能不全引起的疾病或附带突触功能不全的疾病的预防剂、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗剂的有效性进行判定的方法,其中,所述方法包括上述步骤(a-3)~(c-3);
57.一种对因突触功能不全引起的疾病或附带突触功能不全的疾病的预防剂、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗剂的有效性进行判定的方法,其中,所述方法包括上述步骤(a-4)~(d-4);
58.一种因突触功能不全引起的疾病或附带突触功能不全的疾病的预防剂、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗剂,其中,所述预防剂或治疗剂包含针对脑发育调节蛋白a关联蛋白质(darps)自身抗体的显性负肽。
59.发明效果
60.根据本发明的判定方法,能够早期且简便地判定迄今为止依赖于提问式检查(抑郁症、痴呆症等)或图像检查(脑出血等)的因突触功能不全引起的疾病或附带突触功能不全的疾病的有无发病或重症度,因此能够预防或早期治疗这些疾病的发病。进而,darps或抗darps自身抗体也会成为预防剂、治疗剂的筛选指标,能够有助于药物开发研究。
附图说明
61.图1中,上部分是表示通过蛋白质印迹对实施例1的磁珠吸附级分(beads absorbed)、血浆(plasma)及预澄清血浆(preclear plasma)进行解析的结果的图。下部分是表示通过蛋白质印迹对实施例1的各ip级分进行解析的结果的图。
62.图2是表示使用各种抗脑发育调节蛋白抗体(m2f6、28d8、3d9、22g5、17c3、33a4:自家制)及抗脑发育调节蛋白a抗体(4c2:自家制;das2:免疫生物学研究所)对实施例1的磁珠吸附级分进行蛋白质印迹的结果的图。
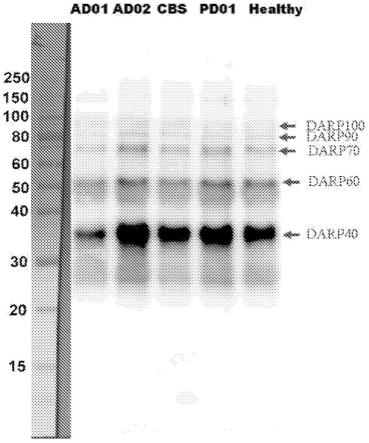
63.图3是表示实施例2的、从阿尔茨海默病患者2名(ad01、ad02)、大脑皮质基底核综合征患者1名(cbs)、帕金森病患者1名(pd01)、健康65岁男性(healthy)取得血液试样、使用抗脑发育调节蛋白a抗体das2(免疫生物学研究所)对蛋白a/g磁珠的吸附级分进行蛋白质
印迹的结果的图。
64.图4是表示实施例2的、使用ad02和控制血浆(ctrl)、通过蛋白质印迹进行darps检测的结果的图。darp40、darp60、darp70、darp90、darp100的所有darp在ad02中浓度均上升。
65.图5是表示实施例2的、从阿尔茨海默病患者2名(ad01、ad02)、大脑皮质基底核综合征患者1名(cbs)、帕金森病患者1名(pd01)、健康65岁男性(healthy)取得血液试样、使用抗脑发育调节蛋白抗体3d9(自家制)对蛋白a/g磁珠的吸附级分进行蛋白质印迹的结果的图。与图3不同,未观察到在样品间的差异。
66.图6是表示实施例3的、从阿尔茨海默病患者3名(ghad01~03、均为轻度的痴呆症)、肌萎缩性侧索硬化症患者1名(als01)、脊髓小脑变性症患者1名(scd01)及抑郁症患者1名(dep01)取得脑脊髓液试样、使用抗脑发育调节蛋白a抗体das2(免疫生物学研究所)对蛋白a/g磁珠的吸附级分进行蛋白质印迹的结果的图。
67.图7是表示通过蛋白质印迹对实施例4的表1中记载的6名阿尔茨海默病患者检测脑脊髓液试样中的darps得到的结果的图。
68.图8是表示实施例5的、将附加了gfp标签的人脑发育调节蛋白a(gfp-hda)供于sds-page、以抗脑发育调节蛋白抗体(3d9:自家制)(左)及来自阿尔茨海默病患者的血浆(ad plasma)(右)作为一次抗体、通过蛋白质印迹进行检测得到的结果的图。
69.图9是表示实施例5的、确认抗脑发育调节蛋白抗体(22g5:自家制)对大鼠海马培养细胞是否具有毒性的结果的图。(a)表示进行了22g5处理的大鼠海马培养细胞,(b)表示进行了正常小鼠igg处理的大鼠海马培养细胞。
70.图10是表示实施例6的、确认到培养大鼠大脑皮质细胞中存在darps的蛋白质印迹的结果的图。
具体实施方式
71.本发明只要为以下判定方法,就没有特别限制。
72.一种因突触功能不全引起的疾病或附带突触功能不全的疾病的发病风险、或者有无发病的判定方法(以下,有时称作“本件判定方法1”),包括以下的步骤,即,步骤(a-1),对从受试者提取的生物体试样中的脑发育调节蛋白a关联蛋白质(darps)的浓度进行测定;步骤(b-1),将步骤(a-1)中测定得到的darps的浓度与对照者中的darps的浓度进行比较,该对照者未发生因突触功能不全引起的疾病或附带突触功能不全的疾病;以及步骤(c-1),当步骤(a-1)中测定得到的darps的浓度比上述对照者中的darps的浓度高时,评价为上述受试者发生因突触功能不全引起的疾病或附带突触功能不全的疾病的风险高、或者已发生因突触功能不全引起的疾病或附带突触功能不全的疾病的可能性高;
73.一种因突触功能不全引起的疾病或附带突触功能不全的疾病的重症度的判定方法(以下,有时称作“本件判定方法2”。另外,以下,有时将本件判定方法1和本件判定方法2统称为“本件判定方法”),包括以下的步骤,即,步骤(a-2),对从受试者提取的生物体试样中的脑发育调节蛋白a关联蛋白质(darps)的浓度进行测定,该受试者已发生因突触功能不全引起的疾病或附带突触功能不全的疾病;步骤(b-2),将步骤(a-2)中测定得到的darps的浓度与对照者中的darps的浓度进行比较,该对照者已发生因突触功能不全引起的疾病或附带突触功能不全的疾病;以及步骤(c-2),当步骤(a-2)中测定得到的darps和/或darps自
身抗体的浓度比上述对照者中的darps和/或darps自身抗体的浓度高时,评价为上述受试者与上述对照者相比因突触功能不全引起的疾病或附带突触功能不全的疾病重症化的可能性高。在此,“重症度”包括突触障碍的发展速度快的急性加重期。在一个方式中,本件判定方法是辅助医生对因突触功能不全引起的疾病或附带突触功能不全的疾病的发病风险的诊断、或者对有无发病或重症度的诊断的方法,有时也不包括医生的诊断行为。
74.另外,本发明只要为以下筛选方法,就没有特别限制。
75.一种因突触功能不全引起的疾病或附带突触功能不全的疾病的预防剂、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗剂的筛选方法(以下,有时称作“本件筛选方法1”),包括以下的步骤,即,步骤(a-3),对从施用了被检物质的突触功能不全模型非人动物中提取的试样中的脑发育调节蛋白a关联蛋白质(darps)的浓度进行测定;步骤(b-3),将步骤(a-3)中测定得到的脑发育调节蛋白a关联蛋白质(darps)的浓度与不施用上述被检物质的突触功能不全模型非人动物中的脑发育调节蛋白a关联蛋白质(darps)的浓度进行比较;以及步骤(c-3),当在步骤(a-3)中测定得到的脑发育调节蛋白a关联蛋白质(darps)的浓度比不施用上述被检物质的突触功能不全模型非人动物中的脑发育调节蛋白a关联蛋白质(darps)的浓度低时,评价为上述被检物质针对因突触功能不全引起的疾病或附带突触功能不全的疾病的预防、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗有效;
76.一种因突触功能不全引起的疾病或附带突触功能不全的疾病的预防剂、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗剂的筛选方法(以下,有时称作“本件筛选方法2”。另外,以下,有时将本件筛选方法1和本件筛选方法2统称为“本件筛选方法”),包括以下的步骤,即,步骤(a-4),对突触功能不全模型培养细胞施用被检物质并进行培养;步骤(b-4),对上述突触功能不全模型培养细胞的培养液中的脑发育调节蛋白a关联蛋白质(darps)的浓度进行测定;步骤(c-4),将步骤(b-4)中测定得到的darps的浓度与不施用上述被检物质的突触功能不全模型培养细胞的培养液中的darps的浓度进行比较;以及步骤(d-4),当步骤(b-4)中测定得到的darps的浓度比不施用上述被检物质的突触功能不全模型培养细胞的培养液中的darps的浓度低时,评价为上述被检物质针对因突触功能不全引起的疾病或附带突触功能不全的疾病的预防、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗有效。
77.本发明是基于如下的首次发现而完成的,即,定位于脑的人脑发育调节蛋白a(序列号1)的片段或作为剪接变异体的脑发育调节蛋白a关联蛋白质(darps:drebrin a related proteins)大量存在于来自罹患因突触功能不全引起的疾病或附带突触功能不全的疾病的患者的生物体试样中。在本发明中,darps只要是具有对脑发育调节蛋白a特异性的ins2翻译序列rpycpfikasdsgpssssssssspprtpfpyitchrtpnlssslpc(序列号2)的至少一部分的脑发育调节蛋白a的片段或剪接变异体即可,可优选例示分子量约100kda的darp100、分子量约90kda的darp90、分子量约70kda的darp70、分子量约60kda的darp60及分子量约40kda的darp40。darps可单独用于本件判定方法或本件筛选方法,也可以1种或2种以上的darps的组合用于本件判定方法或本件筛选方法。另外,还可测定darps的总浓度来用于本件判定方法或本件筛选方法。
78.在本发明中,darps浓度可以利用公知的任意方法来测定。在优选的方式中,darps
浓度通过使用了识别darps的抗体(以下,有时称作“抗darps抗体”)的蛋白质印迹法、elisa(enzyme-linked immuno sorbent assay)法、免疫沉降等来测定。作为抗darps抗体,只要是以darps的一部分作为表位的抗体即可,可以为单克隆抗体、多克隆抗体中的任意者,可以单独使用1种,也可以组合使用2种以上。另外,为了与存在于全身的脑发育调节蛋白e相区别,优选使用识别脑发育调节蛋白a特异性表位的抗体来测定。在一个方式中,本发明涉及用于在本件判定方法和/或本件筛选方法中使用的、识别脑发育调节蛋白a特异性表位的抗体(以下,有时称作“本件抗体”)。在此,“脑发育调节蛋白a特异性表位”是指不存在于脑发育调节蛋白e而存在于脑发育调节蛋白a的表位,优选为包含ins2翻译序列rpycpfikasdsgpssssssssspprtpfpyitchrtpnlssslpc(序列号2)的至少一部分的区域、和/或为了使脑发育调节蛋白a包含ins2翻译序列而制作的特异性立体结构。
79.在进行蛋白质印迹法或elisa法的情况下,可优选使用如下方法:使用抗darps抗体作为一次抗体,通过识别一次抗体的标记化二次抗体进行检测。例如,在一次抗体为兔抗体的情况下,可以使用标记化抗兔igg抗体作为二次抗体,在一次抗体为小鼠抗体的情况下,可以使用标记化抗小鼠igg抗体作为二次抗体。
80.作为上述标记化二次抗体中的标记物质,可列举酶、放射线同位元素、荧光物质、发光物质、金胶体等。其中,从灵敏度及操作的简便性的观点出发,优选酶,更优选辣根过氧化物酶(horseradish peroxidase)(hrp)、碱性磷酸酶(ap)、葡糖氧化酶(god)等。在使用hrp作为标记物质的情况下,可以使用tmb(3,3’,5,5
’‑
四甲基联苯胺)等作为基质,在使用ap作为标记物质的情况下,可以使用amppd(3-(2'-螺旋金刚烷)-4-甲氧基-4-(3
”‑
磷酰氧基)苯基-1,2-二氧杂环丁烷
·
二钠盐)、9-(4-氯苯硫基磷酰氧基亚甲基)-10-甲基二氢吖啶二钠盐等作为基质。另外,作为标记物质,除此以外还可以使用fitc(fluorescein isothiocyanate)、罗丹明等荧光色素等。
81.darps的检测
·
定量方法根据标记方法不同而不同,可以利用本领域技术人员公知惯用的方法来进行。例如,在使用hrp、ap、god等作为标记物质的情况下,可以添加发色基质或发光基质、测定吸光度或发光强度来对测定对象物质进行定量。另外,在使用荧光物质作为标记物质的情况下,可以通过测定其荧光强度来对测定对象物质进行定量。另外,在使用放射性同位元素作为标记物质的情况下,可以通过测定放射能来对测定对象物质进行定量。另外,在使用金胶体作为标记物质的情况下,可以通过测定吸光度来对测定对象物质进行定量。在定量时,例如可以预先利用已知darps浓度的试样制作校准曲线(标准曲线),将测定值与校准曲线核对,算出试样中的darps浓度,用于本件判定方法或本件筛选方法中的比较,但是,也可以不算出darps浓度而将吸光度、放射能、发光强度直接用于本件判定方法或本件筛选方法中的比较。在此,在本件判定方法中,为了对受试者中的darps浓度(上述算出的darps浓度、吸光度、放射能、发光强度)是否高于或低于对照者中的darps浓度(上述算出的darps浓度、吸光度、放射能、发光强度)进行评价(判定),阈值(截止值)可以设定任意的值,作为该阈值,可列举例如对照者中的darps浓度的平均值、平均值+标准偏差(sd)、平均值+2sd、平均值+3sd、平均值-sd、平均值-2sd、平均值-3sd、中央值、中央值+sd、中央值+2sd、中央值+3sd、中央值-sd、中央值-2sd、中央值-3sd等。另外,在本件筛选方法中,为了对施用了被检物质的突触功能不全模型非人动物或突触功能不全模型培养细胞中的darps浓度(上述算出的darps浓度、吸光度、放射能、发光强度)是否高于或低于未施用上述被检物
质的突触功能不全模型非人动物或突触功能不全模型培养细胞中的darps浓度(上述算出的darps浓度、吸光度、放射能、发光强度)进行评价(判定),阈值(截止值)可以设定任意的值,作为该阈值,可列举例如未施用被检物质的突触功能不全模型非人动物或突触功能不全模型培养细胞中的darps浓度的平均值、平均值+标准偏差(sd)、平均值+2sd、平均值+3sd、平均值-sd、平均值-2sd、平均值-3sd、中央值、中央值+sd、中央值+2sd、中央值+3sd、中央值-sd、中央值-2sd、中央值-3sd等。
82.在本发明中,生物体试样是指从受试者或对照者中提取的体液。在此,体液可列举血液、淋巴液、组织液、体腔液、脑脊髓液等,其中,优选脑脊髓液或血液。血液包括血清、血浆等。生物体试样可以直接供于darps浓度的测定,但优选在测定前实施用于提高darps的检测灵敏度的前处理。作为前处理的方法,只要是提高生物体试样中的测定对象蛋白质的检测灵敏度的方法即可,可列举例如使用了抗darps抗体的免疫沉降。另外,本发明人们通过用蛋白a/g磁珠在生物体试样中进行处理、将吸附于磁珠的级分供于本件判定方法或本件筛选方法,从而成功地提高darps的检测灵敏度。蛋白a/g磁珠处理是在免疫沉降之前以降低由自身抗体产生的背景为目的而进行的处理,目标蛋白质本来能够由蛋白a/g磁珠处理后的流通级分来检测出。本发明人们的darps吸附于蛋白a/g磁珠的这一发现是预料之外的发现,而且还启示了在生物体试样中存在抗darps自身抗体。本发明人们通过进一步的研究确认在生物体试样中存在抗darps自身抗体,进而发现了抗darps自身抗体能损伤脑神经细胞。这些发现表明:针对抗darps自身抗体的显性负肽能够抑制由抗darps自身抗体所致的脑神经细胞的损伤、能够治疗和/或预防因突触功能不全引起的疾病或附带突触功能不全的疾病。因此,在一个方式中,本发明涉及一种因突触功能不全引起的疾病或附带突触功能不全的疾病的预防剂、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗剂的筛选方法,其特征在于,所述筛选方法探索针对抗darps自身抗体的显性负肽。
83.在本发明中,因突触功能不全引起的疾病或附带突触功能不全的疾病是指因突触功能不全、即突触中的信息传递产生障碍而发病的疾病(阿尔茨海默病、脑血管性痴呆症、路易小体型痴呆症、帕金森病、大脑皮质基底核变性症、肌萎缩性侧索硬化症、脊髓小脑变性症等)、在疾病的发病后产生突触功能不全的疾病(脑出血、脑梗塞、脑肿瘤等)。已知因脑的血流降低而产生的抑郁症、药物依赖、线粒体的基因疾病、糖尿病等也伴随突触功能不全,认知功能降低,包含在因突触功能不全引起的疾病或附带突触功能不全的疾病中。再者,在产生脑外伤时的后遗症的评价中也可以使用本件判定方法。因突触功能不全引起的疾病或附带突触功能不全的疾病优选是指神经变性疾病,其中,优选为选自阿尔茨海默病、大脑皮质基底核综合征、帕金森病、脊髓小脑变性症及肌萎缩性侧索硬化症中的神经变性疾病。
84.作为本件判定方法1中的受试者,在判定因突触功能不全引起的疾病或附带突触功能不全的疾病的发病风险的情况下,通常可列举未发生因突触功能不全引起的疾病或附带突触功能不全的疾病、且不清楚将来是否发生因突触功能不全引起的疾病或附带突触功能不全的疾病的受试者,另外,在判定因突触功能不全引起的疾病或附带突触功能不全的疾病有无发病的情况下,通常可列举不清楚是否已发生因突触功能不全引起的疾病或附带突触功能不全的疾病的受试者,优选为通过本发明的发病风险的判定方法评价(判定)为发生因突触功能不全引起的疾病或附带突触功能不全的疾病的风险高的人。本件判定方法1
中的对照者是指发生因突触功能不全引起的疾病或附带突触功能不全的疾病的风险低或者几乎无风险的、未发生因突触功能不全引起的疾病或附带突触功能不全的疾病的健康者。另外,在上述阈值的设定时,可以将以下的任1种以上作为对照者,即,(i)已测定出darps浓度的所有健康者或随意抽取的健康者;(ii)与受试者相同的年龄或年龄范围的健康者(脑内脑发育调节蛋白量随着年龄减少);以及(iii)疾病发病前的受试者。可以使用基于这些对照者的darps浓度设定的阈值来辨别突触功能不全的急性加重期。
85.作为本件判定方法2中的受试者,可列举例如虽然已发生因突触功能不全引起的疾病或附带突触功能不全的疾病、但是因突触功能不全引起的疾病或附带突触功能不全的疾病的重症度不清楚的受试者。本件判定方法2中的对照者是指例如已发生因突触功能不全引起的疾病或附带突触功能不全的疾病、且判定为重症度的患者。在此,“判定为重症度的患者”可以是基于公知的诊疗手册判定为重症度的患者。作为公知的诊疗手册,期望使用对象疾病的诊疗手册,可列举例如痴呆症的诊疗手册、脑出血
·
脑梗塞的诊疗手册等。例如,在阿尔茨海默病的痴呆症中,通过问诊等将痴呆症分成初期、中期、后期等,但是认为血浆中的darps在发病初期至中期为最大。实际上,在后期广泛引起神经细胞死亡后(重症的痴呆症患者),表现为darps反而变少(实施例2的ad01的患者)。另外认为:在脑出血中,出血发生后不久darps变高,经过一段时间而变为慢性期时,darps变低而成为一定的值。这样,根据对象疾病的不同,对照者的darps的变化与重症度的关系不同,因此优选通过适当的诊疗手册进行重症度判定。
86.作为本件筛选方法1中的突触功能不全非人动物,可以是自然地发生突触功能不全的非人动物,也可以是诱导了突触功能不全发生的非人动物。具体而言,诱导了突触功能不全的非人动物可以是上述因突触功能不全引起的疾病或附带突触功能不全的疾病的模型非人动物。作为上述非人动物,除小鼠以外,可例示大鼠、仓鼠、豚鼠、猴、牛、猪、马、兔、绵羊、山羊、猫、狗等非人哺乳动物。
87.作为本件筛选方法2中的突触功能不全模型培养细胞,可以是自然地发生突触功能不全的培养细胞,也可以是诱导了突触功能不全的培养细胞。具体而言,诱导了突触功能不全发病的培养细胞可以是上述因突触功能不全引起的疾病或附带突触功能不全的疾病的模型培养细胞。作为上述培养细胞,可优选例示培养神经细胞,除来自人的培养细胞以外,还可例示来自小鼠、大鼠、仓鼠、豚鼠、猴、牛、猪、马、兔、绵羊、山羊、猫、狗等非人哺乳动物的培养细胞。
88.在一个方式中,本发明涉及包含本件抗体的、因突触功能不全引起的疾病或附带突触功能不全的疾病的发病风险、有无发病或重症度的判定用试剂盒(以下,有时称作“本件试剂盒”)。在优选的方式中,本件试剂盒为用于在本件判定方法中使用的试剂盒。除本件抗体以外,本件试剂盒还可以包含用于从受试者中取得生物体试样的手段、识别本件抗体的标记化二次抗体、记载了工艺或诊断基准的添附文件。
89.以下,通过实施例对本发明进行更具体地说明,但是本发明的技术范围并不受这些例示限定。
90.实施例1
91.1.来自血液试样的darps的检测
92.本发明人们认为在阿尔茨海默病患者的血浆中存在脑发育调节蛋白,虽然使用抗
脑发育调节蛋白抗体对血浆进行了蛋白质印迹,但是不能检出脑发育调节蛋白。因此,为了除去血浆中夹杂的抗体成分,进行蛋白a/g磁珠处理,供于蛋白质印迹。
93.实验工艺如以下所示。
94.(1)将血浆1.8ml和蛋白a/g磁珠(protein a/g plus-agarose:santa cruz公司制)200μl进行悬浊,在4℃下利用旋转器(rotator)使其反应(预澄清)1小时。
95.(2)进行离心而制备上清(preclear plasma:预澄清血浆)和沉淀(beads absorbed:磁珠吸附级分)。
96.(3)向磁珠吸附级分中添加sds样品缓冲液30μl进行热变性而使其溶出。
97.(4)经离心的上清(preclear plasma:预澄清血浆)的一部分保存于input用,将其余的预澄清血浆和四种抗体(抗脑发育调节蛋白抗血清dep:自家制;识别脑发育调节蛋白a及e的抗脑发育调节蛋白单克隆抗体28d8和3d9:自家制;控制igg:富士胶片和光纯药株式会社制)分别混合,以o/n进行反应(ip:免疫沉降)。
98.(5)在以o/n反应后的上述(4)的ip管中进一步悬浊蛋白a/g磁珠30μl,在4℃下利用旋转器使其反应1小时,之后,清洗磁珠,向磁珠级分中添加sds样品缓冲液30μl,进行热变性,使其溶出(ip、免疫沉降级分)。
99.(6)通过蛋白质印迹对各样品(上部分:beads absorbed、plasma、preclear plasma;下部分:各ip级分)进行解析(检测用抗体使用单克隆抗体28d8和3d9的混合物)
100.将结果示于图1中。在进行了免疫沉降的下部分的蛋白质印迹中未能检测出脑发育调节蛋白,与此相对,从用于预澄清的蛋白a/g磁珠的吸附级分(beads absorbed)中与预想相反地确认到脑发育调节蛋白的条带(上部分、箭头)。因此,为了确认该条带是存在于全身的脑发育调节蛋白e还是定位于脑突触的脑发育调节蛋白a,使用识别脑发育调节蛋白a及e两者的各种抗脑发育调节蛋白抗体(m2f6、28d8、3d9、22g5、17c3、33a4:自家制)及识别在脑发育调节蛋白a中包含ins2的至少一部分的区域的抗脑发育调节蛋白a抗体(4c2、自家制;das2:免疫生物学研究所),对蛋白a/g磁珠的吸附级分进行蛋白质印迹,结果发现约130kda的脑发育调节蛋白全长的条带未被作为脑发育调节蛋白a特异性抗体的4c2、das2染色,为脑发育调节蛋白e的条带(图2)。认为该脑发育调节蛋白e来自肾肿瘤。另一方面,在比脑发育调节蛋白e的条带更低分子量侧观察到多个条带,其被认为是被作为抗脑发育调节蛋白a抗体的4c2或das2染色的脑发育调节蛋白a的片段或剪接变异体。将它们命名为脑发育调节蛋白a关联蛋白质(drebrin a related proteins、darps)。需要说明的是,在图2中,用箭头表示脑发育调节蛋白e和darps中分子量约40kda的darp40。darp40未被控制igg或脑发育调节蛋白的通用抗体m2f6明确地染色,这是本发明人们首次发现的。脑发育调节蛋白a定位于脑的树突棘,由此暗示着darps在阿尔茨海默病患者中从损伤的树突棘漏出、通过血脑屏障而转移至血液中。
101.实施例2
102.2.血液试样中darps的作为诊断生物标记物的使用
103.由实施例1认为darps在阿尔茨海默病患者中从损伤的树突棘漏出。在其他因突触功能不全引起的疾病或附带突触功能不全的疾病中,也存在darps从损伤的树突棘漏出、转移至血液中的可能性。因此,为了确认血液试样中darps是否能够作为因突触功能不全引起的疾病或附带突触功能不全的疾病的诊断生物标记物来使用,进行了以下的实验。
104.从阿尔茨海默病患者2名(ad01(发病后经过5年,有肾肿瘤)、ad02(发病后3年、mmse21点))、大脑皮质基底核综合征患者1名(cbs)、帕金森病患者1名(pd01)、健康65岁男性(healthy)取得血液试样,与实施例1同样地将蛋白a/g磁珠的吸附级分供于蛋白质印迹。使用抗脑发育调节蛋白a抗体das2(免疫生物学研究所)进行检测。
105.将结果示于图3中。从所有血液试样都能观察到多条darps的条带。将能够确认到的darps根据分子量命名为darp40、darp60、darp70、darp90、darp100。在来自除ad01以外的疾病患者的血液试样中,darps浓度比健康65岁男性(healthy)增加。进而,如图4所示,使用ad02和控制血浆(ctrl:kohjin-bio(kjb)公司制、正常人血浆
·
pool edta-2na、批号:hmn389081),通过同样的工艺进行了darps的检测,结果:对于darp40、darp60、darp70、darp90、darp100的任意darp,在ad02中浓度均上升。因此表明这些darps能够作为因突触功能不全引起的疾病或附带突触功能不全的疾病的诊断生物标记物来使用。另一方面,在ad01中,darps浓度比healthy低(图3)。这被认为是:在引起神经细胞死亡而进入痴呆的最终阶段(tau蛋白高,mmse的分数差)的慢性期ad患者中,不会引起如急性加重期那样的darps的急速漏出,darps浓度变低。
106.进而,利用识别脑发育调节蛋白a及e两者的抗脑发育调节蛋白抗体3d9(自家制)对与图3同样的样品进行了染色,结果在疾病患者和健康65岁男性(healthy)中未观察到条带的浓度差异(图5)。由此处的结果表明:来自脑发育调节蛋白e的脑发育调节蛋白关联蛋白质不能作为诊断生物标记物来使用,并且识别在脑发育调节蛋白a中包含ins2的至少一部分的区域的抗体(das2等)能够用于疾病的诊断。
107.实施例3
108.3.脑脊髓液试样中darps的作为诊断生物标记物的使用
109.由实施例2可确认到血液试样中的darps能够作为因突触功能不全引起的疾病或附带突触功能不全的疾病的诊断生物标记物来使用。darps与定位于脑的脑发育调节蛋白a相关联,因此认为在因突触功能不全引起的疾病或附带突触功能不全的疾病的患者中也会在脑脊髓液中存在大量darps。因此,为了确认脑脊髓液试样中darps能够作为因突触功能不全引起的疾病或附带突触功能不全的疾病的诊断生物标记物来使用,进行了以下的实验。
110.从阿尔茨海默病患者3名(ghad01~03、均为轻度的痴呆症)、肌萎缩性侧索硬化症患者1名(als01)、脊髓小脑变性症患者1名(scd01)及抑郁症患者1名(dep01)取得脑脊髓液试样,代替血液试样而使用脑脊髓液试样,除此以外,与实施例2同样地将蛋白a/g磁珠的吸附级分供于蛋白质印迹。使用抗脑发育调节蛋白a抗体das2(免疫生物学研究所)进行检测。
111.将结果示于图6中。从所有脑脊髓液试样中均观察到多条darps的条带,能够与血液试样同样地确认到darp40、darp60、darp70、darp90、darp100。在神经变性疾病的阿尔茨海默病患者2名(ghad01及03)、肌萎缩性侧索硬化症患者1名(als01)、脊髓小脑变性症患者1名(scd01)中,与抑郁症患者1名(dep01)相比,darps浓度更高。另外,即使是罹患相同阿尔茨海默病的患者,如ghad01及03的比较所示那样,darps浓度存在差异,因此暗示着darps浓度能够反映疾病的重症度(树突棘的损伤程度)。另一方面,ghad02是与抑郁症患者1名(dep01)相同程度的darps浓度。认为在ghad02中,ad发展转移至慢性期,不会引起如急性加重期那样的darps的急速漏出,darps浓度变低。另外,与其他神经变性疾病相比,抑郁症患
者中的darps浓度低,但是鉴于有时从抑郁症转移至认知功能障碍,认为在抑郁症患者中也能通过darps浓度的上升来评价向认知功能障碍的转移。
112.实施例4
113.4.阿尔茨海默病患者的其他指标与darps量的关系
114.由实施例3表明脑脊髓液试样中darps能够作为阿尔茨海默病的诊断生物标记物来使用。另一方面,认为:在阿尔茨海默病发展而转移至慢性期的患者中,不引起如急性加重期那样的darps的急速漏出,darps浓度变低。因此,针对以下的表1中记载的6名阿尔茨海默病患者,与实施例3同样地通过蛋白质印迹对脑脊髓液试样中的darps进行了检测。需要说明的是,表中“tau
↑”
是指tau蛋白的浓度高而达到tau蛋白蓄积,“aβ
↑”
是指淀粉样蛋白β的浓度高而达到淀粉样蛋白β蓄积。
115.[表1]
[0116][0117]
将结果示于图7中。由来自所有患者的脑脊髓液试样能够确认到darp100、darp70及darp40。在未达到tau蛋白蓄积的加重期的患者(病例编号1107~1110)中,darps浓度高,但是在tau蛋白最高的病例登记编号1111的患者中,darps浓度低。由此处的结果也表明:在阿尔茨海默病发展而转移至慢性期的患者中,darps浓度变低。
[0118]
实施例5
[0119]
5.darps自身抗体的存在确认及神经细胞毒性的验证
[0120]
由实施例1表明darps吸附于具有对抗体(igg、iga)的结合能力的蛋白a/g磁珠。为了确认该吸附是darps直接吸附于蛋白a/g磁珠还是介由血液试样中的darps自身抗体进行的吸附,将附加了gfp标签的人脑发育调节蛋白a(gfp-hda:在hek293中表达、并且用sds缓冲液进行均质的样品)供于sds-page,以抗脑发育调节蛋白抗体(3d9:自家制)及来自阿尔茨海默病患者的血浆(ad plasma)作为一次抗体进行了检测。
[0121]
将结果示于图8中。在图8左侧的用3d9进行检测的情况和图8右侧的用来自阿尔茨海默病患者的血浆(ad plasma)进行检测的情况下,能够在相同位置(图中箭头)确认条带。
由该结果表明在来自阿尔茨海默病患者的血浆中存在能够识别脑发育调节蛋白a的自身抗体。认为darps经由该自身抗体而吸附于蛋白a/g磁珠。
[0122]
脑脊髓液的darps也吸附于蛋白a/g磁珠,因此认为抗darps自身抗体也存在于脑脊髓液中。为此,为了确认抗darps自身抗体是否对脑的神经细胞具有毒性,对div23(在体外的培养天数)的大鼠海马培养细胞(自家制)施用抗脑发育调节蛋白抗体(22g5:自家制)或市售的正常小鼠igg(富士胶片和光纯药株式会社制),培养1小时后,用pbs进行清洗并固定后,与抗map2抗体(abcam公司制)反应,用抗小鼠igg-alexa568(thermo fisher scientific公司制)使22g5及正常小鼠igg可视化,用抗兔igg-alexa488(thermo fisher scientific公司制)使map2可视化,由此验证抗脑发育调节蛋白抗体对神经细胞的影响。
[0123]
将结果示于图9中。对于施用1小时市售的正常小鼠igg(富士胶片和光纯药株式会社制)并清洗、固定得到的大鼠海马培养细胞,小鼠igg(红色。未被检测出)未被导入细胞内,确认到与正常细胞同样的map2的染色(绿色)(图9b)。另一方面,对于施用1小时抗脑发育调节蛋白抗体(22g5)并清洗、固定得到的培养神经细胞,确认到22g5进入细胞体或一部分树突的像(红色)。进而,在导入了22g5的区域中,微小管发生异常,正常的map2的染色(绿色)消失(图9a)。由此处的结果暗示:darps自身抗体由于发生因突触功能不全引起的疾病或附带突触功能不全的疾病而在体内大量地生产时,损伤脑的神经细胞,使病状进一步发展。因此认为:抑制由darps自身抗体引起的脑神经细胞损伤作用的显性负肽成为能够抑制脑的神经细胞损伤的上述疾病的治疗剂和/或预防剂的候补化合物。
[0124]
实施例6
[0125]
6.大鼠神经细胞中的darps的存在确认
[0126]
为了确认疾病模型动物或来自疾病模型动物的培养神经细胞是否能够用于疾病的治疗剂、预防剂的筛选,通过以下的工艺验证了在大鼠神经细胞中是否存在darps。
[0127]
(1)将2dish量(60mm dish)的div8(在体外的培养天数)的培养大鼠大脑皮质细胞用pbs回收,进行超声处理,对细胞进行了破碎。
[0128]
(2)在15000rpm下离心20min后,将上清回收(图10左栏、input)。
[0129]
(3)对于免疫沉降,向上清中添加抗脑发育调节蛋白抗体(28d8:自家制)和蛋白a/g磁珠30μl,使其旋转(1小时),之后,磁珠用pbs清洗3次(添加pbs进行混合,在1500g下离心10秒,除去上清),用sds缓冲液50μl溶出结合物(图10中央栏、28d8 ip)。
[0130]
(4)作为负控制,向上清中添加蛋白a/g磁珠30μl,使其旋转(1小时),之后,磁珠用pbs清洗3次(添加pbs进行混合,在1500g下离心10秒,除去上清),用sds缓冲液50μl溶出结合物(图10右栏、a/g beads)。
[0131]
(5)将所得的各级分供于蛋白质印迹。检测使用抗脑发育调节蛋白a抗体das2(免疫生物学研究所)来进行。
[0132]
将结果示于图10中。通过抗脑发育调节蛋白抗体,能够在免疫沉降的级分中确认darps的条带,表明在除人以外的具有脑发育调节蛋白的动物和其培养细胞中也存在darps。由此处的结果表明:因突触功能不全而漏出至细胞外(培养液中)的darps的浓度变化能够作为因突触功能不全引起的疾病或附带突触功能不全的疾病的预防剂、或者因突触功能不全引起的疾病或附带突触功能不全的疾病的治疗剂的筛选指标来使用。
[0133]
实施例7
[0134]
7.阿尔茨海默病模型小鼠中的darps的存在确认
[0135]
本发明人们报道了通过使5xfad小鼠(具有5个家族性阿尔茨海默病基因的小鼠)和脑发育调节蛋白敲除小鼠(纯合体)交配而杂合具有5xfad基因和脑发育调节蛋白基因(+/-)的小鼠(5xfad/dxko
+/-)(日本特愿2019-185245)。从该小鼠取得血液试样,与实施例1同样地将蛋白a/g磁珠的吸附级分供于蛋白质印迹。使用抗脑发育调节蛋白a抗体das2(免疫生物学研究所)进行检测,结果能够确认到5xfad/dxko
+/-的darp100浓度比野生型小鼠高。
[0136]
产业上的可利用性
[0137]
根据本发明的判定方法,能够早期且简便地判定迄今为止依赖于提问式检查(抑郁症、痴呆症等)或图像检查(脑出血等)的因突触功能不全引起的疾病或附带突触功能不全的疾病的有无发病或重症度,因此能够预防这些疾病的发病或进行早期治疗。进而,darps或抗darps自身抗体也成为预防剂、治疗剂的筛选指标,能够有助于药物开发研究。
[0138]
因此,本发明在医疗
·
制药领域中的产业上的可利用性极高。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1