一种涎液化糖链抗原KL-6测定试剂盒及其制备方法与流程
一种涎液化糖链抗原kl-6测定试剂盒及其制备方法
技术领域
1.本发明涉及检测试剂盒技术领域,具体涉及一种涎液化糖链抗原kl-6测定试剂盒及其制备方法。
背景技术:
2.涎液化糖链抗原kl-6是一种跨膜高分子量黏蛋白,属于黏蛋白muc1家族,含有涎液化糖链结构。该糖链结构具有被特异性抗体识别的空间结构表位。kl-6主要表达于ⅱ型肺泡细胞和支气管上皮细胞。当肺部发生炎症时,ii型肺泡的大量再生和肺间质上皮细胞屏障的破损会导致kl-6大量释放到血液中。有研究表明,通过检测血样中的kl-6含量可以用来诊断肺部的炎症尤其是间质性肺炎的发生。
3.间质性肺炎(ip)是以肺间质为主要病变部位的疾病。正常肺泡壁出现炎症或损伤后,肺间质逐渐变厚、变硬,随着病情恶化肺部会出现纤维化,从而引起肺部通气功能障碍,导致供氧不足,表现出呼吸困难等症状。间质性肺炎已知的病因包括自身免疫疾病引起、长期吸入粉尘颗粒物、以及使用药物等。患者表现为活动后气嘴、日常干咳,药物副作用加重等症状。
4.kl-6可以对肺间质状态进行检测,帮助选择治疗药物,也可用于判断停药时间。当发生间质性肺炎等情况时,肺泡上皮细胞受到损伤后会向血液中释放kl-6,使血液中kl-6蛋白的浓度升高。活动期的间质性肺炎患者血液中存在高浓度的kl-6,有效的治疗可以降低测定值。
5.kl-6的常见检测方法有酶联免疫法、荧光层析法、胶乳增强免疫比浊法。这些方法中以胶乳增强免疫比浊法最先进,灵敏度更高,线性范围更广,操作也相对简便。胶乳增强免疫比浊法利用吸附在直径几十到几百纳米的胶乳微粒上的kl-6抗体捕捉测试样品中的kl-6,从而形成微粒之间的交联,改变了溶液的散射度或者透射吸光度(即浊度)。通过测量溶液的散射度或者透射吸光度的变化,可以根据定标曲线定量地计算出测试样品中kl-6的浓度。该测试方法既可以在通用的大型自动生化分析仪上运用,也可以在特定蛋白分析仪等小型的即时检测设备上采用,有很强的适用性,可以很好地满足我国从大型三甲医院到社区基层医院的使用需求。
6.如中国专利申请202011000129.4中公开了一种涎液化糖链抗原测定试剂盒及其检测方法。所述的涎液化糖链抗原检测试剂盒,包括试剂r1、试剂r2;试剂r1包括:稳定剂5-50g/l、防腐剂0.05-2g/l,并利用缓冲液调节ph为2-9;试剂r2包括:表面活性剂5-30g/l、稳定剂5-30g/l、抗人涎液化糖链抗原抗体乳胶颗粒结合物0.1-2g/l、防腐剂0.05-2g/l,并利用缓冲液调节ph为2-9。该申请具有灵敏度高,线性范围广的特点,可实现对涎液化糖链抗原的准确检测,但是试剂盒并没有关注试剂r2中胶乳颗粒的稳定性,以后该试剂盒长期放置后检测的灵敏性。
7.因此,需要提供一种灵敏度高、精密度好,线性范围广,且长期放置稳定性高的涎液化糖链抗原kl-6测定试剂盒及其制备方法。
技术实现要素:
8.因此,针对现有技术的不足,本发明的目的在于提供一种涎液化糖链抗原测定试剂盒及其制备方法,可以实现对涎液化糖链抗原的准确检测,并且该试剂盒具有灵敏度高、精密度好,线性范围广,且长期放置稳定性高的特点。
9.为实现上述目的,本发明采取的技术方案为:一种涎液化糖链抗原测定试剂盒,所述的试剂盒包括试剂r1和试剂r2;
10.所述的试剂r1包括:缓冲液80-120g/l;渗透液80-120g/l;表面活性剂a10-30g/l;防腐剂1-2g/l;
11.所述的试剂r2包括:缓冲液80-120g/l;表面活性剂b 20-30g/l;稳定剂5-20g/l;涎液化糖链抗原kl-6抗体胶乳颗粒20-40mg/l;防腐剂1-2g/l。
12.优选地,所述的试剂盒包括试剂r1和试剂r2;
13.所述的试剂r1包括:缓冲液90-110g/l;渗透液90-110g/l;表面活性剂a15-25g/l;防腐剂1.2-1.8g/l;
14.所述的试剂r2包括:缓冲液90-110g/l;表面活性剂b 25-30g/l;稳定剂10-15g/l;涎液化糖链抗原kl-6抗体胶乳颗粒25-30mg/l;防腐剂1.2-1.8g/l。
15.再优选地,所述的试剂盒包括试剂r1和试剂r2;
16.所述的试剂r1包括:缓冲液100g/l;渗透液100g/l;表面活性剂a 24g/l;防腐剂1.5g/l;
17.所述的试剂r2包括:缓冲液100g/l;表面活性剂b 30g/l;稳定剂12g/l;涎液化糖链抗原kl-6抗体胶乳颗粒30mg/l;防腐剂1.5g/l。
18.其中,所述的缓冲液选自三羟甲基氨基甲烷缓冲液、甘氨酸缓冲液、磷酸盐缓冲液、hepes缓冲液、tris-hcl缓冲液和good's缓冲液中的一种或几种;
19.优选地,所述的缓冲液为三羟甲基氨基甲烷缓冲液、甘氨酸缓冲液、磷酸盐缓冲液和tris-hcl缓冲液中的一种或几种;
20.再优选地,所述的缓冲液为三羟甲基氨基甲烷缓冲液。
21.所述的渗透液为氯化钠;
22.所述的表面活性剂a选自椰油酰胺丙基甜菜碱、椰油酰谷氨酸钠、椰油酰甘氨酸钾和月桂酰谷氨酸钠中的一种或几种;
23.优选地,所述的表面活性剂a选自椰油酰胺丙基甜菜碱、椰油酰谷氨酸钠和月桂酰谷氨酸钠中的一种或几种;
24.再优选地,所述的表面活性剂a为椰油酰胺丙基甜菜碱和椰油酰谷氨酸钠的混合物;所述的椰油酰胺丙基甜菜碱和椰油酰谷氨酸钠的质量比为1:3。
25.所述的表面活性剂b选自吐温60、吐温80、聚乙二醇4000、聚乙二醇8000和聚乙二醇10000中的一种或几种;
26.优选地,所述的表面活性剂b选自吐温60、吐温80、聚乙二醇4000、聚乙二醇8000和聚乙二醇10000中的一种或几种;
27.再优选地,所述的表面活性剂b为吐温80和聚乙二醇8000的混合物,所述的吐温80和聚乙二醇8000的质量比为3:1。
28.所述的稳定剂选自蔗糖、海藻糖、牛血清白蛋白、螺旋藻多糖和藻蓝蛋白中的一种
或几种;
29.优选地,所述的稳定剂选自蔗糖、牛血清白蛋白、螺旋藻多糖和藻蓝蛋白中的一种或几种;
30.再优选地,所述的稳定剂为蔗糖、螺旋藻多糖和藻蓝蛋白的混合物;所述的蔗糖、螺旋藻多糖和藻蓝蛋白的质量比为10:1:1。
31.由于抗体或者抗原包被的微球的胶乳溶液是热力学不稳定体系,胶乳会自发地凝集。因此在在制备试剂r2时需要在试剂中加入表面活性剂或者稳定剂等组分保证胶乳溶液的稳定性,从而防止胶乳在储存时发生自发凝集,从而使试剂盒的灵敏性和准确性降低,本发明在实施过程中意外地发现控制试剂r2中的表面活性剂为吐温80和聚乙二醇8000的混合物,并控制两者的质量比为3:1;并控制稳定剂为蔗糖、螺旋藻多糖和藻蓝蛋白的混合物,三者的质量比为10:1:1,能够更好的保证胶乳的稳定性,长时间放置不会出现自发凝集的现象,从而提高了检测的稳定性和准确性。
32.而本发明是基于胶乳增强免疫比浊法,其原理是采用化学偶联法将特异性抗体结合于一定粒径的胶乳颗粒表面,当交联有抗体的微球与抗原结合后,短时间内迅速聚集在一起,从而改变反应液的吸光度。根据吸光度增加量,即可在特定波长处测定免疫复合物浊度,定量检测血清中的涎液化糖链抗原含量。因此当胶乳溶液用于测试时,需要抗原抗体的特异性结合导致的胶乳凝集,因此试剂r1需要在一定程度上促进胶乳凝集的形成,而本发明在实施过程中意外地发现试剂r1中采用椰油酰胺丙基甜菜碱和椰油酰谷氨酸钠的混合物作为表面活性剂,并控制椰油酰胺丙基甜菜碱和椰油酰谷氨酸钠的质量比为1:3,可以有效促进检测过程中抗原抗体的特异性结合,从而提高检测效率,提高检测的灵敏度。
33.所述的防腐剂选自叠氮化钠、硫柳汞、proclin 300、异噻唑啉酮中的任意一种或多种;优选地,所述的防腐剂为proclin 300。
34.其中所述的涎液化糖链抗原kl-6抗体胶乳颗粒,通过本领域常方法制备得到。
35.在一些优选实施方案中,所述的涎液化糖链抗原测定试剂盒,所述的试剂盒包括试剂r1和试剂r2;
36.所述的试剂r1包括:三羟甲基氨基甲烷80-120g/l;氯化钠80-120g/l;表面活性剂a 10-30g/l;proclin 300 1-2g/l;
37.所述的试剂r2包括:三羟甲基氨基甲烷80-120g/l;吐温80 10-20g/ll;表面活性剂b 20-30g/l;稳定剂5-20g/l;涎液化糖链抗原kl-6抗体胶乳颗粒20-40mg/l;proclin 300 1-2g/l。
38.在另一个更有选的实施方案中,所述的涎液化糖链抗原测定试剂盒,所述的试剂盒包括试剂r1和试剂r2;
39.所述的试剂r1包括:三羟甲基氨基甲烷100g/l;氯化钠100g/l;椰油酰胺丙基甜菜碱6g/l;椰油酰谷氨酸钠18g/l;proclin 300 1g/l;
40.所述的试剂r2包括:三羟甲基氨基甲烷100g/l;吐温80 22.5g/l;聚乙二醇8000 7.5g/l;蔗糖10g/l;螺旋藻多糖1g/l;藻蓝蛋白1g/l;涎液化糖链抗原kl-6抗体胶乳颗粒30mg/l;proclin 300 1g/l。
41.所述的试剂盒还包括校准品和质控品。
42.本发明还提供了所述的涎液化糖链抗原测定试剂盒测定试剂盒在定量检测涎液
化糖链抗原含量时的应用。
43.本发明还提供了涎液化糖链抗原测定试剂盒的使用方法。
44.本试剂盒适用于日立7170/7600/7180、迈瑞bs2000、迪瑞cs600、雅培c16000、东芝tba120fr/tba-fx8、贝克曼au5800/au680/au2700/dxc800、西门子advia2400、罗氏c701/c702/p800、杜邦ar等全自动生化分析仪。
45.该测定试剂盒的测定方法为终点法,反应方向为升反应:
46.(1)将180μl试剂r1和3μl待测样本混合均匀,37℃孵育5min后得到反应液1,测定吸光度a1,测定主波长为570nm;
47.(2)加入60μl试剂r2混合均匀,反应5min,得到反应液2,测定吸光度a2,测定主波长为570nm;
48.(3)按照步骤(1)-(2),对不同浓度的涎液化糖链抗原标准品的吸光度进行测定,得到吸光度a空白和a标准;
49.(4)以标准品的吸光度变化值δa(a标准-a空白)为纵坐标,以相应的标准品浓度c为横坐标,绘制标准曲线,得到标准曲线方程;
50.(5)计算样本的吸光度变化值δa(a2-a1),根据标准曲线方程,得到样本中涎液化糖链抗原浓度。
51.与现有技术相比本发明的有益效果在于:
52.(1)本发明提供的涎液化糖链抗原测定试剂盒实施过程中控制试剂r2中的表面活性剂为吐温80和聚乙二醇8000的混合物,并控制两者的质量比为3:1;并控制稳定剂为蔗糖、螺旋藻多糖和藻蓝蛋白的混合物,三者的质量比为10:1:1,能够更好的保证胶乳的稳定性,长时间放置不会出现自发凝集的现象,从而提高了检测的稳定性和准确性;
53.(2)本发明提供的涎液化糖链抗原测定试剂盒实施过程中控制试剂r1中采用椰油酰胺丙基甜菜碱和椰油酰谷氨酸钠的混合物作为表面活性剂,并控制椰油酰胺丙基甜菜碱和椰油酰谷氨酸钠的质量比为1:3,可以有效促进检测过程中抗原抗体的特异性结合,从而提高检测效率,提高检测的灵敏度。
54.(3)本发明提供的脂联素测定试剂盒,通过控制试剂r1和试剂r2中各组分的具体组分以及浓度比,能够明显提高试剂盒的抗干扰能力,样本中血红蛋白≤5.0g/l,胆红素≤500mg/l,抗坏血酸≤10.0g/l,甘油三酯≤10.0g/l对测试结果无明显干扰。
具体实施方式
55.为了使本发明实现的技术手段、创作特征、达成目的与功效易于明白了解,下面结合具体实施例,进一步阐明本发明,但下述实施例仅仅为本发明的优选实施例,并非全部。基于实施方式中的实施例,本领域技术人员在没有做出创造性劳动的前提下所获得其它实施例,都属于本发明的保护范围。下述实施例中的实验方法,如无特殊说明,均为常规方法,下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
56.测试条件与方法:
57.仪器:日立7170全自动生化分析仪
58.参数:
59.主波长570nm样品3μl
次波长800nm试剂1180μl反应温度37℃试剂260μl反应方向升反应反应类型终点法
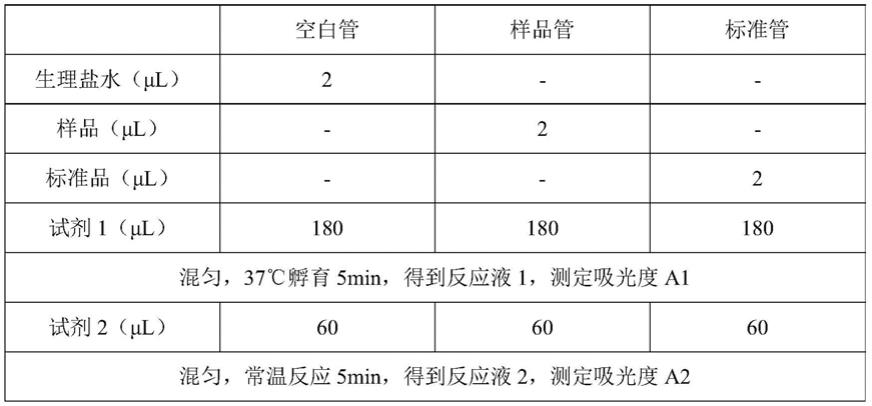
60.操作步骤:
[0061][0062]
实施例1一种涎液化糖链抗原测定试剂盒
[0063]
所述的试剂盒包括试剂r1和试剂r2;
[0064]
所述的试剂r1包括:三羟甲基氨基甲烷缓冲液80g/l;氯化钠80g/l;椰油酰胺丙基甜菜碱10g/l;proclin 300 1g/l;
[0065]
所述的试剂r2包括:三羟甲基氨基甲烷缓冲液80g/l;吐温-80 20g/l;蔗糖5g/l;涎液化糖链抗原kl-6抗体胶乳颗粒20mg/l;proclin 300 1g/l。
[0066]
实施例2一种涎液化糖链抗原测定试剂盒
[0067]
所述的试剂盒包括试剂r1和试剂r2;
[0068]
所述的试剂r1包括:三羟甲基氨基甲烷缓冲液120g/l;氯化钠120g/l;椰油酰谷氨酸钠30g/l;proclin 300 1g/l;
[0069]
所述的试剂r2包括:三羟甲基氨基甲烷缓冲液80g/l;聚乙二醇4000 30g/l;蔗糖20g/l;涎液化糖链抗原kl-6抗体胶乳颗粒20mg/l;proclin 300 1g/l。
[0070]
实施例3一种涎液化糖链抗原测定试剂盒
[0071]
所述的试剂盒包括试剂r1和试剂r2;
[0072]
所述的试剂r1包括:三羟甲基氨基甲烷缓冲液90g/l;氯化钠110g/l;月桂酰谷氨酸钠15g/l;叠氮化钠1.2g/l;
[0073]
所述的试剂r2包括:三羟甲基氨基甲烷缓冲液90-110g/l;聚乙二醇10000 30g/l;牛血清白蛋白10g/l;涎液化糖链抗原kl-6抗体胶乳颗粒25mg/l;叠氮化钠1.2g/l。
[0074]
实施例4一种涎液化糖链抗原测定试剂盒
[0075]
所述的试剂盒包括试剂r1和试剂r2;
[0076]
所述的试剂r1包括:三羟甲基氨基甲烷80g/l;氯化钠80g/l;椰油酰胺丙基甜菜碱2.5g/l;椰油酰谷氨酸钠7.5g/l;proclin 300 1g/l;
[0077]
所述的试剂r2包括:三羟甲基氨基甲烷80g/l;吐温80 5g/l;聚乙二醇8000 15g/l;蔗糖5g/l;螺旋藻多糖0.5g/l;藻蓝蛋白0.5g/l;涎液化糖链抗原kl-6抗体胶乳颗粒
20mg/l;proclin 300 1g/l。
[0078]
实施例5一种涎液化糖链抗原测定试剂盒
[0079]
所述的试剂盒包括试剂r1和试剂r2;
[0080]
所述的试剂r1包括:三羟甲基氨基甲烷120g/l;氯化钠120g/l;椰油酰胺丙基甜菜碱7.5g/l;椰油酰谷氨酸钠22.5g/l;proclin 300 2g/l;
[0081]
所述的试剂r2包括:三羟甲基氨基甲烷120g/l;吐温80 18g/l;聚乙二醇8000 6g/l;蔗糖16g/l;螺旋藻多糖1.6g/l;藻蓝蛋白1.6g/l;涎液化糖链抗原kl-6抗体胶乳颗粒40mg/l;proclin 300 2g/l
[0082]
实施例6一种涎液化糖链抗原测定试剂盒
[0083]
所述的试剂盒包括试剂r1和试剂r2;
[0084]
所述的试剂r1包括:三羟甲基氨基甲烷100g/l;氯化钠100g/l;椰油酰胺丙基甜菜碱6g/l;椰油酰谷氨酸钠18g/l;proclin 300 1g/l;
[0085]
所述的试剂r2包括:三羟甲基氨基甲烷100g/l;吐温80 22.5g/l;聚乙二醇8000 7.5g/l;蔗糖10g/l;螺旋藻多糖1g/l;藻蓝蛋白1g/l;涎液化糖链抗原kl-6抗体胶乳颗粒30mg/l;proclin 300 1g/l
[0086]
对比例1
[0087]
与实施例6的区别在于:试剂r1中不添加表面活性剂,即试剂r1包括:三羟甲基氨基甲烷100g/l;氯化钠100g/l;proclin 300 1g/l;其他组分与操作与实施例6相同。
[0088]
对比例2
[0089]
与实施例6的区别在于:试剂r1中椰油酰胺丙基甜菜碱和椰油酰谷氨酸钠的质量比为5:1,即椰油酰胺丙基甜菜碱20g/l;椰油酰谷氨酸钠4g/l;其他组分与操作与实施例6相同。
[0090]
对比例3
[0091]
与实施例6的区别在于:试剂r1中添加的表面活性剂为十二烷基磺酸钠,即试剂r1包括:三羟甲基氨基甲烷100g/l;氯化钠100g/l;十二烷基磺酸钠24g/l;proclin 300 1g/l;其他组分与操作与实施例6相同。
[0092]
对比例4
[0093]
与实施例6的区别在于:试剂r2中的稳定剂为螺旋藻多糖和藻蓝蛋白,即试剂r2包括:三羟甲基氨基甲烷100g/l;吐温80 22.5g/l;聚乙二醇8000 7.5g/l;螺旋藻多糖6g/l;藻蓝蛋白6g/l;涎液化糖链抗原kl-6抗体胶乳颗粒30mg/l;proclin 300 1g/l;其他组分与操作与实施例6相同。
[0094]
对比例5
[0095]
与实施例6的区别在于:试剂r2中的表面活性剂为曲拉通x-100,即试剂r2包括:三羟甲基氨基甲烷100g/l;曲拉通x-100 30g/l;蔗糖10g/l;螺旋藻多糖1g/l;藻蓝蛋白1g/l;涎液化糖链抗原kl-6抗体胶乳颗粒30mg/l;proclin 300 1g/l;其他组分与操作与实施例6相同。
[0096]
效果实验
[0097]
1、线性
[0098]
实验要求:在40-5000u/ml的线性范围内,相关系数r应≥0.990。
[0099]
实验方法
[0100]
将接近线性范围上限的高值样本(5000u/ml)与零浓度样本混合成6个稀释浓度,理论浓度分别为5000u/ml、2500u/ml、1000u/ml、500u/ml、200u/ml、40u/ml。对每一浓度的样本各重复测试3次得到浓度值,记录各样品的测量结果,并计算各样品3次测量值的平均值(yi)。以稀释浓度(xi)为自变量,以测定结果均值(yi)为因变量求出线性回归方程。按公式(1)计算线性回归的相关系数(r),应符合实验的要求,检测数据见下表1。
[0101][0102]
式中:
[0103]
r-相关系数;
[0104]
x
i-稀释比例;
[0105]yi-各个样本测定结果均值;
[0106]-稀释比例的均值;
[0107]-样本测定结果总均值。
[0108]
表1
[0109][0110][0111]
根据上表1的检测结果可以看出,本发明实施例1-3制备的试剂盒的线性相关系数(r)实验结果不低于0.9880,线性关系较好;而实施例4-6中制备的试剂和的线性相关系数(r)实验结果不低于0.9900,线性关系良好。因此可以定义实施例4-6制备的试剂盒的线性范围为40-5000u/ml;而使用对比例1-5制备的试剂盒进行检测,线性相关系数(r)实验结果低于0.9900,线性关系虽然比较好,但是不符合要求。
[0112]
2、重复性
[0113]
实验要求:对高浓度样本和低浓度样本各测试10次,cv≤10%。
[0114]
实验方法
[0115]
同批号试剂盒重复测试高浓度样本(4500-5000u/ml)、低浓度样本(40-45u/ml)各10次,计算10次测试结果的平均值和标准差sd。按公式(2)计算变异系数(cv),结果应符合实验要求,检测结果见下表2。
[0116][0117]
式中:
[0118]
sd-样本测试值的标准差;
[0119]-样本测试值的平均值。
[0120]
表2重复性检测结果
[0121]
8℃、无腐蚀性气体的避光环境中贮存,分别在储存1个月、3个月、6个月、12个月、24个月时检测涎液化糖链抗原样本试剂,每月1号检测准确度,检测数据如表3所示。
[0126]
实验方法
[0127]
将浓度约为500u/ml(允许偏差
±
10%)的涎液化糖链抗原液(a)加入到0浓度样本b中,所加入涎液化糖链抗原与样本b之间的体积比例为1:9,根据公式(3)计算回收率r,回收率应在85%-115%范围内,具体检测结果见下表3。
[0128][0129]
式中:
[0130]
r—回收率;
[0131]
v-样本a液的体积;
[0132]v0-样本b液的体积;
[0133]
c-样本b液加入a液后的3次测量平均值;
[0134]c0-样本b液的3次测量平均值;
[0135]cs-样本a液的浓度。
[0136]
表3
[0137] 1个月3个月6个月12个月24个月实施例188.56%92.63%85.65%93.6%118.2%实施例2110.32%95.51%92.94%114.86%119.42%实施例390.25%91.53%88.56%95.58%112.34%实施例492.56%94.63%95.46%98.25%102.55%实施例596.75%94.54%98.36%100.23%95.64%实施例698.62%95.56%97.63%92.69%100.52%对比例1112.32%98.56%99.69%73.98%125.63%对比例299.69%96.36%105.63%114.58%80.69%对比例3102.59%95.63%112.23%85.28%118.45%对比例4105.69%89.56%86.95%118.47%75.96%对比例585.63%89.69%92.69%75.69%122.69%
[0138]
根据上表3的检测结果可以看出,本发明实施例3-5制备的检测试剂盒,将将已知浓度的涎液化糖链抗原加入到低值样本中,其回收率在85%-115%范围内,符合要求,并且将试剂盒放置24个月后依然能够满足条件,说明试剂盒的稳定性比较高,而实施例1-3制备的试剂盒放置12个月后,其回收率在85%-115%范围内,符合要求,放置24个月后,试剂和的检测准确定明显降低;对比例1-5制备的试剂盒放置24个月后,试剂盒的检测准确性均出现不同程度的降低,回收率明显不满足要求,说明改变试剂盒中试剂的种类或质量比会明显影响试剂盒的稳定性,放置24个月后回收率低于85%或高于115%,不符合要求。
[0139]
根据以上检测结果可见,本发明实施例1-6,尤其是实施例4-6制备的试剂盒的线性、重复性、稳定性(准确性)等指标的研究符合要求,在全自动化学发光免疫分析仪上验证合格,测定结果满足企业标准要求。
[0140]
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保
护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1