用于检测自身抗体的方法和工具与流程
1.本发明涉及用于检测样品中的与具有序列seq id no1、seq id no11或seq id no24的多肽结合的自身抗体的方法,包含所述多肽的承载体,结合所述多肽的自身抗体,所述自身抗体用于疾病诊断的用途,用于分离与所述多肽结合的自身抗体的方法,包含所述多肽的药盒,所述多肽、所述承载体或所述自身抗体用于制造药盒或医疗装置的用途,所述方法包括将包含所述多肽的医疗或诊断装置与包含与所述多肽特异性结合的抗体的缓冲溶液接触的步骤,包含所述自身抗体作为阳性对照的样品和包含所述自身抗体的稀释的样品的用途。
2.自身免疫性疾病被理解为指其中免疫系统针对对于身体是内源性的完好结构的疾病。在许多自身免疫性疾病中,身体产生可检测的自身抗体,所述自身抗体可与对于身体是内源的蛋白质结合,从而导致病症。在其它情况下,自身抗体的存在似乎不是负责疾病爆发的原因。
3.ana(抗核自身抗体)是一组靶向哺乳动物细胞核组分的自身抗体。它们主要与系统性自身免疫性风湿性疾病(sard)相关,并且一些ana是某些sard的生物标志物。例如,抗双链dna(dsdna)、抗sm和抗核糖体p与系统性红斑狼疮(sle)密切相关,而抗scl70、抗着丝粒和抗rna聚合酶iii是系统性硬化症(ssc)的生物标志物。同时,越来越多的证据表明,癌症患者中升高的ana水平在对抗肿瘤细胞中具有重要意义。例如,多项研究表明,抗dsdna自身抗体可以诱导癌细胞凋亡,并抑制肿瘤生长。发现针对sard得以确认的ana与不同的癌症相关联,例如抗dsdna、抗ro/ss-a和抗scl70分别与胃肠癌、血液恶性肿瘤和肺癌相关。另外,可以在大约5.9-30.8%的健康个体中检测到ana,在女性中比男性中更常见。年长的人显示出较高的阳性率。这增加了在诊断中应用ana的复杂性,从而推动了对个体ana的鉴定和对其临床价值的评估。
4.炎性风湿性疾病中抗核抗体的频率(流行率)介于20%与100%之间。因此,鉴别ana诊断对于诊断个体风湿性疾病以及将它们与其它自身免疫性疾病相的鉴别是必不可少的。
背景技术:
5.用于检测ana的免疫测定法可追溯到1948年,hargraves等人发现并应用了红斑狼疮(le)细胞,以帮助诊断sle患者,尽管后来发现le细胞测试既不敏感也不够特异(r.b.conn,"practice parameter-the lupus erythematosus cell test:an obsolete test now superseded by definitive immunologic tests,"american journal of clinical pathology,pp.65-66,1january 1994)。在20世纪50年代后期,建立了基于动物组织基质(诸如大鼠肾脏)的间接免疫荧光测定法(ifa)。该测试的原理是通过荧光标记的抗人抗体来检测与涂覆在载物片上的抗原结合的特异性ana,所述荧光标记的抗人抗体可以在荧光显微镜下观察到。为了更好地评估结果,将观察到的阳性荧光信号描述为不同的图样,如同质的和颗粒状的,这在阳性结果的亚分类中是有用的(kavanaugh等人,"
guidelines for clinical use of the antinuclear antibody test and tests for specific autoantibodies to nuclear antigens,"archives of pathology&laboratory medicine,第124卷,第1期,第71-81页,2000年8月)。结果评估中的另一个重要参数是最高血清稀释度,在该稀释度下图样仍然可见;这被定义为滴度。二十年后,hela来源的人上皮2型(hep-2)细胞显示出更好的灵敏度和特异度,被应用于ifa。当与动物组织的冷冻切片相比时,hep-2细胞具有细胞核大、其它细胞器可见性更好、分裂率高以及含有100多种自身抗原的表达谱等有利方面,这有助于更容易地观察和解释结果。根据ana测试指南,阴性ifa结果表明非sard疾患,而阳性结果应进一步使用可用的单特异性测试进行辨别。
6.自20世纪60年代以来,随着相应的核自身抗原的鉴定,开发了单特异性ana测试(tan等,"characteristics of a soluble nuclear antigen precipitating with sera of patients with systemic lupus erythematosus,"j immunol,96(3):第464-471页,1966年3月1日)。关于间接免疫荧光中hep-2细胞图样的标准化命名的第一个国际一致性声明(www.anapatterns.org icap)定义了与各种自身免疫性疾病的诊断相关的15种细胞核图样和9种细胞质图样。目前,不同种类的基于固相的测定法,包括酶联免疫吸附测定法(elisa)、线印迹法(lineblot)、蛋白质印迹法和化学发光免疫测定法(clia),可用于天然或重组抗原。这些测试具有与ifa类似的原理,其中用能够产生变色反应或发光反应的酶或化合物标记第二抗人抗体(ludwig等人,"mechanisms of autoantibody-induced pathology,"frontiers in immunology,第8页:603,2017年5月31日)。
7.高滴度的ana可能在临床综合征出现之前数年出现。arbuckle及其同事报道,在疾病发作前平均3.3年,可在88%的sle患者中检测到ana(arbuckle等人,,"development of autoantibodies before the clinical onset of systemic lupus erythematosus,"n engl j med,349:第1526-33页,2003)。这证明了ana在疾病的早期诊断和可能的特异性治疗中的重要性。然而,ana诊断剂的效用因人而异。一些ana表现出高度的疾病特异性,并被包括在诊断标准中,和/或反映疾病活动,而另一些ana表现出与sard的弱关联,或甚至是负相关。
8.因此,ana是重要的诊断和预后标志物。然而,尽管有超过半个世纪的研究和经验,但在ana诊断中仍然存在一些差距,这迫切需要解决。如今,更多的医生,而不仅仅是风湿病学家,正在为预防医学和精确健康订购ana测试,这导致越来越多的ana测试阳性结果,特别是关于hep-2细胞的阳性ifa,其临床价值尚不清楚。然而,重要的不仅是报告hep-2细胞上的ana图样和滴度,而且还要进一步区分ana以进行正确诊断。一些ana,如抗scl70抗体,具有高度特异性,但在sard患者中的流行率有限;另一方面,某些ana如抗dfs70与sard呈负相关。因此,需要额外的努力来鉴定未知的ana并研究相应的临床关联性。
9.系统性硬皮病或系统性硬化症是自身免疫性风湿性疾病,其特征在于皮肤和内脏器官中胶原蛋白的过度产生和积聚(称为纤维化)和对小动脉的损伤。基于皮肤受累的程度,系统性硬化症有两个主要的亚组:局限性和弥漫性亚组。受限形式影响肘部和膝盖以下的区域,但不影响肘部和膝盖以上区域,具有或不具有面部受累。弥漫性形式也影响肘部和膝盖以上的皮肤,也可以蔓延到躯干。包括肾脏、心脏、肺和胃肠道在内的内脏器官也会受到纤维化过程的影响。预后取决于疾病的形式和内脏受累的程度。局限性系统性硬化症患者比弥漫型患者预后更好。死亡最常见由肺、心脏和肾脏受累引起。患癌症的风险也略有增
加。
10.约60-95%的系统性硬皮病/系统性硬化症患者具有阳性ana。在可能患有这种疾病的人中,ana亚组测试可以有助于区分所述疾病的两种形式,即局限性形式对比弥漫性形式。
11.核含缬酪肽的蛋白样(同义词:核vcp样,nvlp,核vcp样蛋白,nvl)与含缬酪肽的蛋白显示高水平的氨基酸相似性,并且仅位于细胞核中。nvl属于与各种细胞活动相关的atp酶蛋白家族(aaa蛋白家族)。nvl的主要同种型包含两个串联的aaa结构域、核定位信号和核仁定位信号(fujiwara等人,"structure and function of the n-terminal nucleolin binding domain of nuclear valosin-containing protein-like 2(nvl2)harboring a nucleolar localization signal,"journal of biological chemistry,第21732-21741页,2011年6月17日)。其无所不在地被表达并主要位于核仁中,并参与60s核糖体亚单位的生物发生。据报道,nvl中的突变可能在精神疾病如重度抑郁障碍和精神分裂症中起作用(wang等人,"the nvl gene confers risk for both major depressive disorder and schizophrenia in the han chinese population,"progress in neuro-psychopharmacology and biological psychiatry,第7-13页,2015年10月1日和ripke等人,"a mega-analysis of genome-wide association studies for major depressive disorder,"molecular psychiatry,第497-511页,2013年4月。
12.cd2抗原胞质尾结合蛋白2(cd2bp2)在细胞中无所不在地被表达。根据细胞类型,其在细胞核和细胞质中具有重要功能。在表达cd2受体的细胞如t细胞、胸腺细胞和天然杀伤细胞中,cd2bp2中的gyf结构域可以通过cd2的胞质尾部中富含脯氨酸的基序与cd2相互作用,这发出产生白细胞介素-2的信号(nielsen等人,"structural basis for the bifunctionality of the u5 snrnp 52k protein(cd2bp2)",journal of molecular biology,369(4):第902-908页,2007年4月4日和heinze等人,"investigating the functional role of cd2bp2 in tcells",international immunology,第19卷,第11期,第1313-1318页,2007年11月)。除了在免疫反应中的功能之外,cd2bp2还在pre-mrna加工中发挥作用。cd2bp2也称为u5 snrnp 52k蛋白(u5-52k),因为其是u5小核核糖核蛋白(snrnp)的组分,其与其它snrnp一起形成剪接体(nielsen等人,"structural basis for the bifunctionality of the u5 snrnp 52k protein(cd2bp2)",journal of molecular biology,369(4):第902-908页,2007年4月4日)。还报道了cd2bp2对于胚胎发生是至关重要的(albert et al.,"the gyf domain protein cd2bp2 is critical for embryogenesis and podocyte function,"journal of molecular cell biology,7(5),第402-414页,2015年6月16日)。现有技术中尚未报道cd2bp2/u5-52k与自身免疫性疾病相关。
13.闭锁小带(zonula occludens)-1(zo-1),也称为紧密连接蛋白-1(tjp1),是220-kd的外周膜蛋白,其由人中的tjp1基因编码。其属于闭锁小带蛋白家族(zo-1、zo-2和zo-3),是紧密连接相关蛋白,其中zo-1是第一个被克隆的。其由stevenson和goodenough在1986年使用在啮齿动物肝脏中产生的单克隆抗体首次分离,所述单克隆抗体识别全肝匀浆和富集有紧密连接的膜级分中的225-kd多肽。tjp1特别富集在上皮细胞和内皮细胞的紧密连接处。其属于膜相关鸟苷酸激酶(maguk)蛋白家族,在细胞核与紧密连接之间穿梭(hou,"paracellular channel formation,"in the paracellular channel,academic press,
2019,第9-27页)。
技术实现要素:
14.本发明的根本问题是提供未知ana的方法、相关测定和相关试剂和/或提供或定义用于诊断的新的ana和相应的诊断方法、测定和相关试剂,其可用于诊断,尤其是用于系统性自身免疫性风湿性疾病的诊断。
15.本发明的另一个根本问题是提高诊断系统性自身免疫性风湿性疾病,优选区分系统性自身免疫性风湿性疾病的自身免疫性类型的诊断灵敏度。
16.在第一方面,本发明的根本问题是通过这样的方法解决的,所述方法用于检测优选来自患者的样品中的与具有序列seq id no1、seq id no11或seq id no24的多肽或其变体结合的自身抗体。
17.在优选实施方案中,所述多肽由根据seq id no1的序列或其变体组成或包含所述序列。在又一优选实施方案中,所述多肽由以下序列中的至少一个组成或包含所述序列:根据seq id no1,seq id no35,seq id no38,seq id no41,seq id no44,seq id no45,seq id no46,seq id no47,seq id no48,seq id no49,seq id no50,seq id no51,seq id no52,seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。在更优选的实施方案中,多肽由根据seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列中的至少一个序列组成或包含所述序列。在另一优选实施方案中,所述多肽由根据seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列中的两个、三个、四个、五个、六个、七个或所有序列组成或包含所述序列。
18.在优选实施方案中,所述自身抗体是igg类抗体。
19.在优选实施方案中,所述样品是包含抗体的体液,其优选选自由以下各项组成的组:全血、血浆、血清、脑脊液和唾液。优选地,所述样品来自哺乳动物,更优选来自人患者。
20.在优选实施方案中,所述患者具有一种或多种,优选两种或更多种选自由以下各项组成的组的症状:肌肉疼痛、疲劳、关节僵硬、关节肿胀和发红、轻度发热、注意力不集中、皮疹(包括脸颊上的“蝴蝶”皮疹)、脱发、手脚麻木和刺痛、皮下出现结节、不适、日光敏感性。
21.在优选实施方案中,患者患有或被认为患有系统性自身免疫性风湿性疾病,优选ssc。
22.在优选实施方案中,使用来自包括以下各项的组的方法检测抗体、优选自身抗体:免疫扩散、免疫电泳、光散射免疫测定、凝集反应、标记免疫测定(诸如来自包括以下各项的组的那些:放射性标记免疫测定、诸如比色测定等酶免疫测定、化学发光免疫测定和免疫荧光,优选为免疫荧光,更优选为间接免疫荧光)。在优选实施方案中,使用利用生物芯片的重组间接免疫荧光技术检测抗体,优选自身抗体。
23.在第二方面,本发明的根本问题是通过具有序列seq id no1、seq id no11或seq id no24的多肽或其变体解决的,其中优选地将所述多肽固定,更优选固定在固体承载体上,和/或其中所述多肽是重组蛋白,优选纯化的重组蛋白。
24.在优选实施方案中,根据本发明的多肽由根据seq id no1的序列或其变体组成或包含所述序列或其变体。在又一优选实施方案中,多肽由以下序列中的至少一个组成或包含所述序列:根据seq id no1,seq id no35,seq id no38,seq id no41,seq id no44,seq id no45,seq id no46,seq id no47,seq id no48,seq id no49,seq id no50,seq id no51,seq id no52,seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。在更优选的实施方案中,多肽由以下序列中的至少一个组成或包含所述序列:根据seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。在又一优选的实施方案中,所述多肽由以下序列中的至少两个、三个、四个、五个、六个、七个或所有序列组成或包含所述序列:根据seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。
25.在优选实施方案中,被分离、纯化和/或固定根据本发明的多肽。
26.在优选实施方案中,根据本发明的多肽是重组蛋白,优选为纯化的重组蛋白。
27.在优选实施方案中,根据本发明的多肽用于治疗疾病,其中所述疾病优选为sard,更优选为ssc。
28.在优选实施方案中,根据本发明的多肽用于治疗疾病,其中所述疾病优选为sard,更优选为ssc。
29.在第三方面,本发明的根本问题通过承载体(优选固体承载体)来解决,所述承载体包含具有序列seq id no1、seq id no11或seq id no24的多肽或其变体,其中优选将所述多肽固定在承载体上,和/或其中所述多肽优选为重组蛋白,更优选为纯化的重组蛋白。
30.在优选实施方案中,所述承载体包含由下列序列中的至少一个组成或包含所述序列的多肽:根据seq id no1,seq id no35,seq id no38,seq id no41,seq id no44,seq id no45,seq id no46,seq id no47,seq id no48,seq id no49,seq id no50,seq id no51,seq id no52,seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。在更优选实施方案中,所述承载体包含多肽,所述多肽由以下序列中的至少一个组成或包含所述多肽:根据seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。在又一优选实施方案中,所述承载体包含由以下序列中的两个、三个、四个、五个、六个、七个或所有序列组成或包含所述序列:根据seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。
31.在优选的实施方案中,根据本发明的承载体是诊断上有用的承载体。
32.在优选实施方案中,根据本发明的承载体是固体承载体,其中将所述多肽固定在承载体上,并且其中所述多肽优选是重组蛋白,更优选是纯化的重组蛋白。
33.在优选实施方案中,根据本发明的承载体选自包括以下各项的组:珠粒(优选为顺磁珠粒)、测试条、微量滴定板、膜(优选选自包括以下各项的组:蛋白质印迹、线印迹和点印迹)、侧流装置、玻璃表面、显微镜载玻片、微阵列和生物芯片,优选为显微镜载玻片。在又一优选实施方案中,所述承载体是线印迹或生物芯片。
34.在优选实施方案中,任何固定的多肽是由固定在根据本发明的承载体上的细胞(优选固定的细胞)表达的,或者是固定在根据本发明的承载体上的重组或分离的多肽。
35.在优选实施方案中,任何固定的多肽都是由固定在根据本发明的承载体上的细胞表达的,并且所述承载体还包含模拟转染的细胞。
36.在优选实施方案中,与具有序列seq id no1、seq id no11或seq id no24的多肽或其变体特异性结合的自身抗体与具有序列seq id no1、seq id no11或seq id no24的多肽或其变体和任选的包含标记物的二抗结合。
37.在优选实施方案中,与具有序列seq id no1的多肽或其变体特异性结合的自身抗体与由以下序列中的至少一个组成或包含所述序列的多肽以及任选的包含标记物的二抗结合:根据seq id no1,seq id no35,seq id no38,seq id no41,seq id no44,seq id no45,seq id no46,seq id no47,seq id no48,seq id no49,seq id no50,seq id no51,seq id no52,seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。
38.在优选实施方案中,根据本发明的承载体是包含空间上分离的试剂的测试条,所述试剂包括具有序列seq id no1、seq id no11或seq id no24的多肽或其变体,以及选自包含以下各项的组的一种或多种:一种或多种校准品和指示二抗(优选识别igg类抗体的二抗)存在的试剂。
39.在第四个方面,本发明的根本问题是通过与具有序列seq id no1、seq id no11或seq id no24的多肽或其变体结合的自身抗体(优选分离的自身抗体)解决的,其中所述自身抗体,优选分离的自身抗体,优选与具有序列seq id no1、seq id no11或seq id no24的多肽或其变体复合。
40.在优选实施方案中,自身抗体是分离的。
41.在优选实施方案中,将自身抗体(优选分离的自身抗体)在缓冲溶液中稀释或包含在稀释的样品(优选患者样品)中,和/或所述自身抗体(优选分离的自身抗体)存在于含有选自包括以下各项的组的一种或多种,优选所有试剂的溶液中:稳定剂(优选一组稳定剂)、洗涤缓冲液、抗降解剂。
42.在优选实施方案中,使用选自包括以下各项的组的方法检测自身抗体或复合物:免疫扩散技术、免疫电泳技术、光散射免疫测定、凝集技术、标记免疫测定,诸如选自包括以下各项的组的那些:放射性标记免疫测定、酶免疫测定,更优选elisa、化学发光免疫测定,优选电化学发光免疫测定和免疫荧光,优选间接免疫荧光。
43.在第五方面,本发明的根本问题是通过根据本发明的自身抗体用于诊断疾病(优选系统性自身免疫性风湿性疾病,更优选系统性硬化症)的用途解决的。
44.在优选实施方案中,所述疾病是系统性自身免疫性风湿性疾病或结缔组织疾病,更优选选自包括以下各项的组:系统性硬化症、抗合成酶综合征(ass)、类风湿性关节炎(ra)、系统性红斑狼疮、原发性干燥综合征(pss)、包涵体肌炎(ibm)、肌炎、混合性结缔组织疾病(mctd)或未分化结缔组织疾病(uctd)。
45.在优选实施方案中,所述疾病与一种或多种(优选两种或更多种)选自包括以下各项的组的症状相关联:皮肤增厚和紧绷、手指肿胀、指端硬化、指尖损伤、皮肤色素沉着过度或不足、肿胀、全身疼痛、胸痛、钙质沉着、雷诺现象、毛细血管扩张、异常甲襞毛细血管、呼吸急促、肺动脉高压、肺纤维化、肌肉疼痛、疲劳、关节僵硬、关节肿胀和发红、轻度发热、注意力不集中、皮疹(包括脸颊上的“蝴蝶”皮疹)、脱发、手脚麻木刺痛、皮下出现结节、不适,
对日光敏感。
46.在优选实施方案中,所述用途包括检测样品中的与具有序列seq id no1、seq id no11或seq id no24的多肽或其变体结合的自身抗体的步骤。在又一优选实施方案中,所述用途包括检测样品中的与多肽结合的自身抗体的步骤,所述多肽由以下序列中的至少一个组成或包含所述序列:根据seq id no1,seq id no35,seq id no38,seq id no41,seq id no44,seq id no45,seq id no46,seq id no47,seq id no48,seq id no49,seq id no50,seq id no51,seq id no52,seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。
47.在第六方面,本发明的根本问题是通过用于分离与具有序列seq id no1、seq id no11或seq id no24的多肽或其变体结合的自身抗体的方法解决的,该方法包括以下步骤:
48.a)在与复合物的形成相容的条件下,使包含自身抗体的样品与具有序列seq id no1、seq id no11或seq id no24的多肽或其变体接触,其中所述自身抗体与所述多肽结合,
49.b)分离步骤a)中形成的所述复合物,
50.c)解离步骤b)中分离的所述复合物,以及
51.d)从所述多肽中分离出所述自身抗体。
52.在第七方面,本发明的根本问题是通过包含具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的药盒解决的。
53.在优选实施方案中,根据本发明的药盒包含由以下序列中的至少一个组成或包含所述序列的多肽:根据seq id no1,seq id no35,seq id no38,seq id no41,seq id no44,seq id no45,seq id no46,seq id no47,seq id no48,seq id no49,seq id no50,seq id no51,seq id no52,seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。
54.在优选实施方案中,该药盒还包括用于检测复合物的工具,所述复合物包含具有序列seq id no1、seq id no11或seq id no24的多肽或其变体,以及与所述多肽结合的抗体。
55.在第八方面,本发明的根本问题是通过药盒解决的,该药盒包括:
56.a)根据本发明的承载体和用于检测与所述承载体结合的自身抗体的工具,所述工具优选为二抗,或具有序列seq id no1、seq id no11或seq id no24的多肽或其变体,优选为由以下序列中的至少一个组成或包含所述序列的多肽:根据seq id no1,seq id no35,seq id no38,seq id no41,seq id no44,seq id no45,seq id no46,seq id no47,seq id no48,seq id no49,seq id no50,seq id no51,seq id no52,seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列,或者
57.b)诊断上有用的承载体,其包含用于在液体溶液中捕获根据本发明的自身抗体的工具,优选为未标记的二抗,和用于检测结合到载体上的自身抗体的工具,优选为具有序列seq id no1、seq id no11或seq id no24的多肽或其变体,更优选为由以下序列中的至少一个组成或包含所述序列的多肽:根据seq id no1,seq id no35,seq id no38,seq id no41,seq id no44,seq id no45,seq id no46,seq id no47,seq id no48,seq id no49,
seq id no50,seq id no51,seq id no52,seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列,甚至更优选具有可检测的标记物,
58.其中除了a)或b)之外,该药盒优选还包括一种或多种、优选所有选自包括以下各项的组的试剂:校准品(优选一组校准品)、洗涤缓冲液、阳性对照和阴性对照。
59.在优选实施方案中,根据本发明的药盒是用于诊断疾病(优选sard,更优选ssc)的药盒,所述药盒包含根据本发明的多肽,其中所述药盒优选还包含用于检测包含根据本发明的多肽和与根据本发明的所述多肽结合的抗体的复合物的工具。
60.在优选实施方案中,根据本发明的药盒还包含用于检测针对另一种sard相关自身抗原的自身抗体的工具,所述另一种sard相关自身抗原优选地选自包括以下各项的组:dsdna、核小体、组蛋白、ss-a、ro-52、ssb、rnp/sm、sm、mi-2α、mi-2β、ku、cenp a、cenp b、sp100、pml、scl-70、pm100、pm75、rp11、rp155、gp210、pcna、核仁纤维蛋白、nor90、th/to、pdgfr和dsf70。优选地,该药盒可包含用于分别检测针对一种、两种或更多种另外的sard相关自身抗原的自身抗体的一种、两种或更多种另外的工具,其中所述一种、两种或更多种另外的sard相关自身抗原优选选自包括以下各项的组:dsdna、核小体、组蛋白、ss-a、ro-52、ssb、rnp/sm、sm、mi-2α、mi-2β、ku、cenp a、cenp b、sp100、pml、scl-70、pm100、pm75、rp11、rp155、gp210、pcna、核仁纤维蛋白、nor90、th/to、pdgfr和dsf70。
61.在第九方面,本发明的根本问题是通过根据本发明的多肽、承载体或自身抗体或针对具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的抗体用于制造药盒、医疗装置(优选为诊断装置,优选用于疾病诊断,更优选用于sard的诊断,甚至更优选用于ssc的诊断)的用途解决的。
62.在第十方面,本发明的根本问题是通过药物组合物或医疗装置(优选为诊断装置)解决的,所述药物组合物或医疗装置包含具有序列seq id no1、seq id no11或seq id no24的多肽或其变体。
63.在优选实施方案中,药物组合物或医疗装置包含由根据seq id no1的序列或其变体组成或包含所述序列或其变体。在另一个优选实施方案中,该多肽由以下序列中的至少一个组成或包含所述序列:根据seq id no1,seq id no35,seq id no38,seq id no41,seq id no44,seq id no45,seq id no46,seq id no47,seq id no48,seq id no49,seq id no50,seq id no51,seq id no52,seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。在更优选的实施方案中,该多肽由以下序列中的至少一个组成或包含所述序列:根据seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。在又一优选实施方案中,该多肽由以下序列中的两个、三个、四个、五个、六个、七个或全部序列组成或包含所述序列:根据seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。
64.在优选实施方案中,药物组合物或医疗装置还包含一种或多种佐剂。
65.在优选实施方案中,医疗装置选自包括以下各项的组:载玻片(优选用于显微镜检查)、生物芯片、微量滴定板、侧流装置、测试条、膜(优选为线印迹)、色谱柱和珠粒(优选为磁性或荧光珠粒)。
66.在第十一方面,本发明的根本问题是通过方法解决的,所述方法包括使包含具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的医疗或诊断装置与缓冲溶液接触的步骤,所述缓冲溶液包含与具有序列seq id no1、seq id no11或seq id no24的所述多肽或其变体特异性结合的抗体,所述溶液不是来自需要诊断的患者的包含未知浓度的所述抗体的样品,其中优选地
67.a)溶液中抗体的浓度是已知的,和/或
68.b)抗体是重组抗体,和/或
69.c)使医疗或诊断装置与两种或更多种包含抗体的溶液接触,其中所述两种或更多种溶液具有不同的抗体浓度,和/或
70.d)抗体被与igg类抗体特异性结合的二抗识别,
71.随后检测指示抗体是否与多肽结合的信号,任选地与一种或多种溶液中的抗体浓度相关的信号。
72.在第十二方面,本发明的根本问题是通过使用包含根据本发明的自身抗体作为阳性对照的样品(优选为患者样品,其优选被稀释)解决的。
73.在第十三方面,本发明的根本问题是通过包含本发明自身抗体的稀释样品解决的,其中优选将样品在缓冲水溶液中稀释,和/或其中稀释样品还包含选自包括以下各项的组的一种或多种、优选所有试剂:校准品(优选一组校准品)、稳定剂、洗涤缓冲液、阳性对照和阴性对照。
74.在第十四方面,本发明的根本问题是通过包含根据本发明的自身抗体的水溶液解决的。
75.在优选实施方案中,水溶液包含来自人类患者的样品。
76.在优选实施方案中,溶液包含浓度高于生理水平的非生理缓冲液或生理缓冲液,更优选具有为5至9,优选为6至8的ph。
77.在第十五方面,本发明的根本问题是通过用于从患者的血液(优选为血清)中去除根据本发明的自身抗体的装置解决的,其中所述装置包含根据本发明的承载体。
78.在第十六方面,本发明的问题是通过用于从患者的血液(优选为血清)中去除根据本发明的自身抗体的离体方法解决的。
79.根据本发明,一种或多种被抗nvl自身抗体识别的表位是根据seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的一种、两种、三种、四种、五种、六种、七种或全部c末端片段,或者位于一种、两种、三种、四种、五种、六种、七种或全部所述c末端片段上。
80.本发明基于本发明人的惊人发现,即样针对nvl、cd2bp2和tjp1的自身抗体存在于样品中并且可被检测。它们可以用免疫测定法检测,并可用于设置用于诊断疾病(尤其是sard,特别是ssc)的血清学免疫测定法。包含nvl、cd2bp2或tjp1或其变体的固定多肽的承载体可用于检测此类自身抗体。
81.根据本发明,如本文中所用,术语“具有序列seq id no1、seq id no11或seq id no24的多肽或其变体”是指具有序列seq id no1的多肽或其变体、具有序列seq id no11的多肽或其变体、具有序列seq id no24的多肽或其变体。
82.根据本发明,如本文中所用,术语“具有序列的多肽”是指由所述序列组成或包含
所述序列的多肽。
83.根据本发明,如本文中所用,术语“具有seq id no1序列的多肽或其变体”是指由以下序列中的至少一个组成或包含所述序列的多肽:根据seq id no1,seq id no35,seq id no38,seq id no41,seq id no44,seq id no45,seq id no46,seq id no47,seq id no48,seq id no49,seq id no50,seq id no51,seq id no52,seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的多肽。
84.根据本发明,例如通过用具有序列seq id no1、seq id no11或seq id no24的多肽或其变体涂覆根据本发明的诊断上有用的承载体,或者通过使用具有序列seq id no1、seq id no11或seq id no24的可溶性多肽或其变体(如果所述多肽或其变体与自身抗体结合,则其可被检测到),将具有序列seq id no1、seq id no11或seq id no24的多肽或其变体用于检测针对seq id no1、seq id no11或seq id no24或其变体的自身抗体。在优选实施方案中,所提及的任何序列被理解为作为多肽的一部分或类似形式存在,其可用于检测目标自身抗体。
85.优选地,具有序列seq id no1、seq id no11或seq id no24的多肽或其变体被固定在承载体的固相上。当与样品接触时,其可被直接固定在固相上,但是也可以使用直接或间接的竞争性测定、捕获桥测定、免疫计量测定、固相上的类别特异性二抗、类别捕获测定。这些形式中的每一种的原理在由david wild编辑的the immunoassay handbook,第3版,elsevier,2005中有详细描述。更优选地,固相是测试条或用于elisa的微量滴定板的孔,优选为用于elisa的微量滴定板的孔。
86.本发明的教导不仅可以使用多肽来实施,特别是包含称为诸如人nvl-同种型1(seq id no1)、人cd2bp2(seq id no11)或人tjp1-同种型2(seq id no24)的多肽的天然序列的多肽,或具有本技术中明确提及(例如通过功能、名称、序列或登录号)或隐含提及的确切序列的多肽来实施,而且还可使用此类多肽的变体来实施。
87.在优选实施方案中,本发明的教导使用具有序列seq id no1或其变体、具有序列seq id no11或其变体或具有序列seq id no24或其变体的多肽来实施。
88.在优选实施方案中,本发明的教导使用具有序列seq id no10的多肽,即称为诸如与六组氨酸标签(h6)融合的nvl[人]-if1或其变体来实施。
[0089]
在优选实施方案中,本发明的教导使用具有称为诸如h8-nvl[人](aa1-117)(seq id no49)、h8-nvl[人](aa106-292)(seq id no50)、h8-nvl[人](aa281-560)(seq id no51)、h8-nvl[人](aa549-856)(seq id no52)的多肽的序列的多肽或其变体来实施。
[0090]
在优选实施方案中,本发明的教导使用由以下序列中的一个组成或包含所述序列的多肽来实施:根据seq id no1,seq id no35,seq id no38,seq id no41,seq id no44,seq id no45,seq id no46,seq id no47,seq id no48,seq id no49,seq id no50,seq id no51,seq id no52,seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。
[0091]
在优选实施方案中,本发明的教导使用由以下序列中的一个组成或包含所述序列的多肽来实施:根据seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。
[0092]
在优选实施方案中,本发明的教导使用具有称为诸如与n末端八组氨酸-标签(h8)融合的cd2bp2[人]的多肽的序列(seq id no23)的多肽或其变体来实施。
[0093]
在优选实施方案中,本发明的教导使用具有称为诸如h8-cd2bp2[人](aa117-260)(seq id no66)、h8-cd2bp2[人](aa249-341)(seq id no67)的多肽的序列的多肽或其变体来实施。
[0094]
在优选实施方案中,本发明的教导使用具有称为诸如与n末端八组氨酸-标签(h8)融合的pet24d-n-tjp1[human](aa1-575)的多肽的序列(seq id no82)的多肽或其变体来实施。
[0095]
在优选实施方案中,本发明的教导使用称为诸如与c末端八组氨酸-标签(h8)融合的tjp1[人]-同种型2(seq id no32)、h8-tjp1[人](aa1-156)(seq id no83)、h8-tjp1[人](aa144-306)(seq id no84)、h8-tjp1[人](aa294-575)(seq id no85)的多肽的序列的多肽或其变体来实施。
[0096]
在优选实施方案中,如本文中所用,术语“变体”可以指所提及的全长序列的至少一个片段,更具体地说是相对于全长序列在一端或两端被截短一个或多个氨基酸的一个或多个氨基酸或核酸序列。这种片段包含或编码具有原始序列的至少6个、7个、8个、10个、12个、15个、20个、25个、50个、75个、100个、150,200个、300个、400个、500个、600个、700个、800个、900个、1000个、1100个、1200个、1300个、1400个、1500个、1600个或1650个连续氨基酸的肽或其变体。变体的总长度可以是至少6个、7个、8个、9个、10个、11个、12个、20个、25个、30个、40个、50个、60个、70个、80个、90个、100个、200个、300个、400个、500个、600个、700个、800个、900个、1000个、1100个、1200个、1300个、1400个、1500个、1600个、1650个或1668个或更多个氨基酸。
[0097]
在优选实施方案中,如本文中所用,术语“变体”可以指全长序列或与另外的标签一起提及的全长序列的至少一个片段,所述标签选自包括以下的标签的组:his、18a、acp、aldehyd、avi、bccp、钙调蛋白、壳多糖结合蛋白、e-标签、elk16、flag、flash、聚谷氨酸、聚天冬氨酸、gst、gfp、ha、isope、麦芽糖结合蛋白、myc、nus、ne、prota、protc、tho1d4、s-标签、snooptag、spytag、softag、链抗生物素蛋白、strep-标签ii、t7表位标签、tap、tc、硫氧还蛋白、ty、v5、vsv和xpress标签。
[0098]
术语“变体”不仅涉及至少一个片段,而且还涉及包含与提及的参考氨基酸序列或其片段具有至少40%、50%、60%、70%、75%、80%、85%、90%、92%、94%、95%、96%、97%、98%、99%、99.3%、99.4%、99.5%、99.6%、99.7%、99.8%或99.9%,优选至少99.3%同一性的氨基酸序列的多肽或其片段,其中除生物活性(例如,抗原结合(自身)抗体的能力,或者多肽的折叠或结构)所必需的那些氨基酸外的氨基酸被删除或取代,和/或一个或多个此类必需氨基酸被以保守方式替换,和/或添加氨基酸,使得多肽的生物活性被保留。现有技术包括可用于比对两个给定核酸或氨基酸序列并计算同一性程度的各种方法,参见例如arthur lesk(2008),introduction to bioinformatics,oxford university press,2008,第3版。在优选实施方案中,使用默认设置,使用clustalw软件(larkin,m.a.,blackshields,g.,brown,n.p.,chenna,r.,mcgettigan,p.a.,mcwilliam,h.,valentin,f.,wallace,i.m.,wilm,a.,lopez,r.,thompson,j.d.,gibson,t.j.,higgins,d.g.(2007).clustal w and clustal x version 2.0.bioinformatics,23,2947-2948)。
[0099]
在优选实施方案中,多肽及其变体还可以包含化学修饰,例如同位素标记物或共价修饰,诸如糖基化、磷酸化、乙酰化、脱羧、瓜氨酸化、甲基化、羟基化等。本领域技术人员熟悉修饰多肽的方法。任何修饰都被设计成使得不会消除变体的生物活性。
[0100]
此外,变体还可以通过多肽、其片段或变体与其它已知多肽或其变体的n-末端或/和c-末端融合产生,并且包含活性部分或结构域,其在与参考序列的活性部分比对时,优选具有至少70%、75%、80%、85%、90%、92%、94%、95%、96%、97%、98或99%的序列同一性,其中如本文中所用,术语“活性部分”分别地指小于全长氨基酸序列的氨基酸序列,或者在核酸序列的情况下,编码小于全长的氨基酸序列,和/或其是天然序列的变体,但保留至少一定的生物活性。优选地,活性部分是具有序列seq id no10或其变体、具有seq id no23或其变体或具有seq id no82或其变体的活性部分。优选地,活性部分是具有序列seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92或seq id no93的活性部分或其变体。
[0101]
在本发明的优选实施方案中,seq id no1的变体是指根据seq id no35,seq id no38,seq id no41,seq id no44,seq id no45,seq id no46,seq id no47,seq id no48,seq id no49,seq id no50,seq id no51,seq id no52,seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的序列。
[0102]
多肽的变体具有生物活性。在优选实施方案中,这种生物活性是与自身抗体特异性结合的能力,所述自身抗体特异性结合目标自身抗原,优选如优选在患有与这种抗体相关的自身免疫性疾病(优选为sard,更优选为ssc)的患者中发现的具有seq id no1,seq id no11,seq id no24,seq id no10,seq id no23或seq id no82的序列的自身抗原或其变体。例如,多肽的变体是否具有这种生物活性可以通过确定其是否与来自sard的样品,优选ssc患者的样品(其包含与野生型自身抗原特异性结合的自身抗体)的自身抗体特异性结合(优选如通过间接免疫荧光所测定的)来检查。
[0103]
根据本发明,具有序列seq id no1、seq id no11或seq id no24的多肽或其变体可以是组合蛋白。在优选实施方案中,如本文中所用,术语“重组的”是指在生产过程的任何阶段使用遗传工程方法(例如通过将编码多肽的核酸与强启动子融合以便在细胞或组织中过表达,或者通过工程改造多肽本身的序列)产生的多肽。本领域技术人员熟悉用于工程改造核酸和编码的多肽的方法(例如,sambrook,j.,fritsch,e.f.和maniatis,t.(1989),molecular cloning,csh or in brown t.a.(1986),gene cloning
–
an introduction,chapman&hall中所描述的)以及用于生产和纯化天然或重组多肽的方法(例如,由ge healthcare life sciences出版的handbooks“strategies for protein purification”,“antibody purification”和burgess,r.r.,deutscher,m.p.(2009):guide to protein purification中的)。在另一个优选实施方案中,根据本发明提供或使用的多肽,诸如具有序列seq id no1、seq id no11或seq id no24的多肽或其变体或根据本发明的自身抗体是分离的多肽,其中术语“分离的”意指所述多肽与其使用生物技术或合成方法生产时的状态相比已被富集,并且优选是纯的,即相应液体中至少60%、70%、80%、90%、95%或99%的多肽由所述多肽组成,如通过sds聚丙烯酰胺凝胶电泳,接着考马斯亮蓝染色和目视检查所判断的。优选地,用作捕获抗体的工具的承载体上的任何多肽是纯的。
[0104]
根据本发明,医疗或诊断装置诸如诊断上有用的承载体可以通过以下方法制备:
在诸如真核或原核细胞等细胞中表达具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的重组变体,所述多肽或其变体包含亲和标签,任选地具有可包含蛋白酶切割位点的人工接头,将表达的变体接触与亲和标签特异性结合的配体(所述配体被固定在固相上),洗涤固相以使得从细胞中除去非特异性结合的物质,并优选通过加入过量的非固定配体从固相上洗脱表达的变体。然后可将变体固定在装置上。任选地,在固定之前,可以通过将变体与蛋白酶(优选为识别蛋白酶切割位点的蛋白酶)接触来去除亲和标签。所述亲和标签可以选自包括以下的标签的组:his、18a、acp、aldehyd、avi、bccp、钙调蛋白、壳多糖结合蛋白、e-标签、elk16、flag、flash、聚谷氨酸、聚天冬氨酸、gst、gfp、ha、isope、麦芽糖结合蛋白、myc、nus、ne、prota、protc、tho1d4、s-标签、snooptag、spytag、softag、链抗生物素蛋白、strep-标签ii、t7表位标签、tap、tc、硫氧还蛋白、ty、v5、vsv和xpress标签。有用的蛋白酶包括但不限于tev、凝血酶、因子xa或肠肽酶。合适的接头是载体例如pet载体系列(novagen)的一部分。
[0105]
根据本发明,提供了优选与另外过表达另一种sard相关自身抗原的序列或其变体的另一种细胞组合的过表达具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的细胞。本文中的另一种sard相关自身抗原优选选自包括以下各项的组:dsdna、核小体、组蛋白、ss-a、ro-52、ssb、rnp/sm、sm、mi-2α、mi-2β、ku、cenp a、cenp b、sp100、pml、scl-70、pm100、pm75、rp11、rp155、gp210、pcna、核仁纤维蛋白、nor90、th/to、pdgfr和dsf70。在优选实施方案中,如本文中所用,术语“过表达”是指细胞已经被核酸瞬时或稳定(在所述核酸已经整合到细胞的基因组中的意义上)转染,所述核酸包含在启动子控制下的核酸序列,所述核酸序列编码具有序列seq id no1、seq id no11或seq id no24的多肽或其变体或另一种sard相关自身抗原或其变体。过量表达具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的细胞可以另外地过表达针对另一种sard相关自身抗原或其变体的多肽。因此,转染的细胞表达的被待检测的自身抗体识别的多肽比相同类型的细胞在正常情况下表达的多可能至少10%、20%、30%、50%、100%、200%或500%,如通过定量蛋白质印迹所判断的。启动子可以是诱导型启动子,其允许通过添加诱导物来诱导表达。本领域技术人员熟悉用于在真核细胞中瞬时过表达多肽的方案和载体,例如novagen的ptriex系统,以及熟悉用于稳定转染真核细胞的方案和载体,例如invitrogen的pcdnatm4/to载体系统。
[0106]
在优选实施方案中,可以使用固定的哺乳动物细胞。在优选实施方案中,如本文中所用,术语“固定的”细胞是指已经用反应性化合物处理过的细胞,其效果是该细胞不再具有代谢活性,但仍呈现其表位,用于抗体的免疫染色及其随后的检测(例如通过荧光)。更优选地,反应性化合物选自包括以下各项的组:丙酮、福尔马林、甲醇和乙醇或其混合物,优选为所有这些化合物。本领域技术人员熟悉可用于制备固定的细胞的方案。基本上,通过使用洗涤缓冲液洗涤附着于固体支持物的细胞,然后使其与反应性化合物接触,例如浸渍。可以使用纯丙酮或福尔马林或活性化合物的含水稀释液。
[0107]
根据本发明,细胞在用于显微免疫荧光分析的承载体上。这种承载体可以是载玻片。载玻片上的细胞可以用封固缓冲液覆盖。封固介质是这样的液体,其有助于维持接近生理的ph值,以维持任何诊断相关分子及其表位的分子结构,其与荧光信号的发射相容,并防止由于荧光团的漂白而导致的荧光过早损失。同时,其光学性质与所用的其它缓冲液相匹
配,特别是其折光率,这允许进行高有效的显微荧光分析。封固介质包含基础组分,其优选选自包括以下各项的组:水、甘油、天然油或塑料或其混合物,优选为水和甘油。其还可以包含可以减少漂白的抗衰减成分,优选选自包括以下各项的组:npg(没食子酸正丙酯)、dabco(1,4-二氮杂双环[2.2.2]辛烷)、4pobn((4-吡啶基-1-氧化物)-n-叔丁基硝酮)和ppd(对苯二胺)。在现有技术中,例如在以下文献中描述了各种组合物和方法:由wright cell imaging facility,toronto western research institute university health network出版的“mountants and antifades”(https://de.scribd.com/document/47879592/mountants-antifades),krenek等人(1989)comparison of antifading agents used in immunofluorescence,j.immunol.meth 117,91-97和nairn等人(1969)microphotometry in immunofluorescence,clin.exp.immunol.4,697-705。
[0108]
可以将盖玻片放置在包含样品和封固介质的组合物的顶部。带盖玻片(fb 112d-1005-1或zz 3000-0112)的载玻片可从欧蒙医学实验诊断股份公司,l
ü
beck,germany获得。然而,可以使用与荧光图样的显微分析相容的任何承载体。所述承载体可以包含模拟转染的细胞,所述模拟转染的细胞与过表达具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的细胞一样,已用相同但无编码后者的核酸的载体转染。这种模拟转染的细胞可以作为阴性对照。所述承载体被配置用于使用免疫荧光显微镜进行分析。
[0109]
在优选实施方案中,承载体可以包含含有根据本发明的细胞的区域。另外,承载体可以包含附加区域。所述区域优选被疏水表面包围。这些区域中的每一个都可以包含过表达另一种sard相关自身抗原或其变体的细胞。区域可以包括哺乳动物(优选为灵长类动物)肾或肝组织的切片。
[0110]
优选地,具有序列seq id no1、seq id no11或seq id no24的多肽或其变体被固定在承载体的固相上。当与样品接触时,其可以被直接固定在固相上,但也可以使用直接或间接的竞争性测定、捕获桥测定、免疫计量测定、固相上的类别特异性二抗、类别捕获测定。这些形式中的每一种的原理在由david wild编辑的the immunoassay handbook,第3版,elsevier,2005中有详细描述。更优选地,固相是测试条或用于elisa的微量滴定板的孔,优选为用于elisa的微量滴定板的孔。
[0111]
在优选实施方案中,二抗是与来自抗体类别,优选哺乳动物抗体类别,更优选人抗体类别的所有抗体诸如igg特异性结合的抗体。二抗通常识别所述类别的恒定结构域,但也可识别由来自目标类别的抗体共享的其它表位,例如跨越3d结构的构象表位。它们中的很大一部分是商购可得的,例如来自thermo fisher。其可以是单克隆或多克隆抗体。在优选实施方案中,如本文中所用,术语“识别的”意指二抗与待检测的一种或多种抗体特异性结合。二抗可以与来自抗体类别的所有同种型特异性结合。例如,针对igg类抗体的二抗可以与igg1、igg2、igg3和igg4同种型结合。这可以通过使用包含与每种igg同种型特异性结合的抗体的混合物或与所有目标同种型反应的单一抗体作为针对所述类别,优选针对igg类抗体的二抗来实现。二抗的使用在kruger,n.j.,detection of polypeptides on blots using secondary antibodies,in the protein protocols handbook(ed.j.m.walker),第967页,第1996卷,springer中进行了解释。简言之,此类二抗可以通过用待识别的抗体或待识别抗体混合物免疫实验动物来产生。
[0112]
待检测的自身抗体或所用的二抗优选分别与待检测的自身抗原或抗体特异性结
合。在优选实施方案中,如本文中所用,术语“特异性结合”优选意指结合反应强于特征在于为1x10-5
m,更优选1x10-7
m,更优选1x10-8
m,更优选1x10-9
m,更优选1x10-10
m,更优选1x10-11
m,更优选1x10-12
m的解离常数(如使用biacore设备在25℃下于ph 7的pbs缓冲液中通过表面等离子体共振测定的)的结合反应。
[0113]
在优选实施方案中,细胞结合至与针对具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的自身抗体,并且二抗结合至所述自身抗体。在更优选实施方案中,二抗识别igg类抗体。对于免疫荧光分析,二抗可以包含可检测的荧光标记物,更优选为fitc(异硫氰酸荧光素)。
[0114]
在优选实施方案中,根据本发明的方法包括提供根据本发明的承载体的步骤。然后,在允许任何自身抗体与细胞和由细胞表达的具有序列seq id no1、seq id no11或seq id no24的多肽或其变体结合的条件下,将承载体与怀疑包含自身抗体的样品接触。然后可以取出样品,并且可以清洗带有细胞的承载体以除去任何剩余的样品。然后,可在允许任何结合的自身抗体与二抗之间形成复合物的条件下,将第二自身抗体或类似试剂或与自身抗体结合并携带可检测标记物诸如荧光染料的工具与承载体接触。可以洗涤承载体,然后除去未结合的二抗。最后,通过检查是否可以优选通过免疫荧光(更优选通过荧光素或其衍生物,最优选fitc发射的)检测到二抗来检测自身抗体的存在。
[0115]
在优选实施方案中,如本文中所用,术语“诊断”以其最广泛的含义使用,可以指任何类型的旨在获得信息的方法,所述信息有助于评估患者(来自队列的已知或匿名受试者)是否在过去、在诊断时或在将来患有或者可能患有或者比平均或对比受试者(后者优选具有相似的症状)更可能患有某种疾病或病症,以发现疾病如何进展或在将来可能如何进展,或者评估一个或多个患者对某种治疗(例如免疫抑制药物的施用)的一般反应性,或者发现样品是否来自这样的患者。这种信息可以用于临床诊断,但也可以由实验和/或研究实验室出于一般研究的目的(例如确定患者队列或群体中患有该疾病的受试者的比例)而获得。换句话说,术语“诊断”不仅包括诊断,而且还包括预测和/或监测疾病或病症的过程,包括监测一个或多个患者对药物或候选药物的施用的反应,例如以确定其功效。虽然可以将结果分配给特定患者用于临床诊断应用,并且可以将结果传达给治疗所述患者的医生或机构,但是对于其它应用(例如在用于研究目的的诊断中),这不一定是这种情况,在其它应用中,将结果分配给来自匿名患者的样品可能就足够了。在另一个优选实施方案中,由于自身抗体的存在,针对具有seq id no1、seq id no11或seq id no24序列的多肽或其变体的自身抗体的检测被认为暗示了对sard(优选ssc)的明确诊断。
[0116]
在优选实施方案中,根据本发明的方法和产品可用于相互作用研究,包括确定候选药物或其它化合物是否会干扰自身抗体与具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的结合,或者是否可能影响任何下游过程或其与其靶标结合的强度。在优选实施方案中,它们可用于监测免疫反应,更优选地监测在向例如哺乳动物施用包含具有序列seq id no1、seq id no11或seq id no24的多肽或其变体或其免疫原性变体的免疫原性组合物后,针对具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的抗体的出现和/或滴度,所述哺乳动物可以是除人以外的哺乳动物,诸如实验动物。
[0117]
在另一个优选实施方案中,根据本发明的方法和产品可以用于测定针对具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的抗体的浓度。在更优选实施方
案中,所述抗体是来自sard患者,优选来自ssc患者的自身抗体。在另一个优选实施方案中,所述抗体是重组抗体,其与具有序列seq id no1、seq id no11或seq id no24的多肽或其变体结合,但被与人igg类抗体(优选igg1、igg2、igg3和igg4同种型)特异性结合的二抗识别。在更优选实施方案中,为了研究的目的,为了制备或为了监测试剂、动物模型或装置的质量,需要测定这样的浓度,所述试剂、动物模型或装置可以用于或可以不用于sard(优选ssc)的诊断。
[0118]
在许多情况下,仅仅检测自身抗体,换句话说,确定样品中是否存在可检测水平的抗体,就足以进行诊断。如果可以检测到自身抗体,这将是有助于临床医生诊断的信息,并表明患者患有疾病的可能性增加。
[0119]
本领域技术人员将理解,临床医生通常不仅仅基于单一诊断参数来推断患者是否患有或可能患有疾病、疾患或病症,而是需要考虑其它方面,例如其它自身抗体、标志物的存在、血液参数、患者症状的临床评估或医学成像或其它非侵入性方法诸如多导睡眠图的结果,以得出结论性诊断。参见baenkler h.w.(2012),general aspects of autoimmune diagnostics,in renz,h.,autoimmune diagnostics,2012,de gruyter,第3页。诊断剂或方法的价值也可以是排除一种疾病的可能性,从而允许间接诊断另一种疾病。在优选实施方案中,在本技术通篇提及的任何症状或疾病的含义与本领域技术人员截至本技术的提交日或者优选地与教科书和科学出版物所证明的本技术的最早优先权日所理解的含义一致。应该提及的是,单独使用本发明的方法或用途或产品,不能用于得出明确的最终诊断。
[0120]
在优选实施方案中,术语“诊断”也可以指用于为患者选择最有前景的治疗方案的方法或剂。换句话说,所述方法或剂可以涉及为受试者选择治疗方案。例如,自身抗体的检测可以表明要选择免疫抑制疗法,这可包括向患者施用一种或多种免疫抑制药物。
[0121]
在优选实施方案中,可以将证明自身抗体存在或不存在的任何信息或数据传达给患者或治疗患者的医生,优选通过电话、传真、书面形式或通过互联网(例如作为电子邮件或文本消息)。
[0122]
在优选实施方案中,如本文中所用,术语“自身抗体”是指与产生所述自身抗体的动物(优选哺乳动物,更优选人)的内源性分子特异性结合的抗体,其中与平均健康受试者相比,这种抗体的水平更优选被升高。自身抗体可具有来自动物(优选人)的抗体恒定区的序列,使其(但为可变区)能够与动物的内源性分子特异性结合,更具体地与具有序列seq id no1、seq id no11或seq id no24的多肽或其变体或sard相关(优选ssc相关)自身抗原结合。在优选实施方案中,从样品中分离和/或纯化自身抗体,所述样品优选为来自动物(优选为人)的组织、血清、血浆、血液或csf。自身抗体是来自动物的多克隆天然抗体,而不是合成或重组抗体。
[0123]
根据本发明的方法优选是体外方法。
[0124]
根据本发明,提供了一种药盒,其包含细胞和承载体,并且还包含来自包括以下各项的组的一种或多种、优选所有试剂:二抗(优选用可检测标记物标记的)、洗涤液、阳性对照、阴性对照、去垢剂、盖玻片、封固介质和生理盐溶液(优选为pbs)或制备其所需的盐。在优选实施方案中,阳性对照是来自患有sard(优选为ssc)的患者的稀释样品(优选血清或csf),或针对具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的单克隆抗体。阴性对照可以是来自健康受试者(例如献血者)的稀释样品。该药盒可包括如何进行
测定的说明书。优选地,二抗是针对igg类抗体(优选人igg类抗体)的二抗。
[0125]
在优选实施方案中,本发明提供了细胞、多肽、承载体用于制备用于疾病诊断的药盒和组合物的用途。
[0126]
在优选实施方案中,根据本发明的任何方法或用途可旨在用于非诊断用途,即确定与具有序列seq id no1、seq id no11或seq id no24的多肽或其变体结合的自身抗体的存在,用于除诊断患者外的用途。例如,该方法或用途可用于体外测试设计用于从患者血液中去除自身抗体的医疗装置的效率,其中该测试是在除患者血液外的液体中进行的。在对患者使用该医疗装置后,可通过使包含针对具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的抗体的溶液通过该装置,接着使用根据本发明的方法来确认已通过该装置的溶液中有较少抗体或无抗体(即显示该装置仍具有从溶液中去除抗体的能力)来检查其去除自身抗体的能力。
[0127]
在另一个优选实施方案中,该方法可用于确认诊断测定的可靠性,并且可包括检测溶液中针对具有seq id no1、seq id no11或seq id no24序列的多肽或其变体的抗体,所述溶液不是来自需要诊断的患者的样品,但是已知包含针对具有seq id no1、seq id no11或seq id no24序列的多肽或其变体的抗体(优选以已知的浓度存在)。例如,其可以是重组抗体或来自其身份无法追溯的匿名患者的稀释缓冲液(诸如pbs)中稀释的样品。或者,所述溶液可以是不含抗体的阴性对照,以检查背景。这种方法可以与诊断方法并行、在诊断方法之后或之前运行。在优选实施方案中,根据本发明的任何方法或用途可旨在用于产生自身抗体谱,优选用于检测哺乳动物,优选人的疾病。
[0128]
在优选实施方案中,根据本发明的任何方法或用途可用于鉴定有患或发展疾病,优选sard,更优选ssc和/或肿瘤的风险的受试者。
[0129]
在优选实施方案中,该方法可用于检测抗体,优选溶液中的自身抗体,所述溶液不是来自待诊断哺乳动物的样品,或者用于提供诊断,尤其不是sard的诊断。
[0130]
在优选实施方案中,本发明提供了用于分析来自患者的样品以检测针对具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的自身抗体,表明疾病或发展疾病的可能性增加的装置,所述装置包括:
[0131]
a.承载体,其包含当样品与承载体接触时从样品中捕获自身抗体的工具,其中所述工具是细胞,并且所述承载体是根据本发明的承载体,
[0132]
b.可检测工具,当该可检测工具与承载体接触时,其能够与被载体捕获的抗体结合,其中该可检测工具优选是能够与承载体上捕获的自身抗体结合的标记的二抗,
[0133]
c.任选地的用于从承载体和可检测工具中(优选通过洗涤)去除任何样品的工具;
[0134]
d.检测装置,其用于检测可检测工具的存在并将结果转化为电信号,例如与软件连接的荧光读取器或荧光显微镜,该软件能够在荧光读取器或照相机拍摄的细胞图像中识别过表达具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的染色细胞的图样特征,以及
[0135]
任选的工具,其用于接收来自检测装置的电信号,并通过与野生型或未染色细胞(优选通过与模拟转染的细胞或在同一承载体上未被与具有序列seq id no1、seq id no11或seq id no24的多肽或其变体异性结合的自身抗体阳性染色的细胞)的特征图样、或用来自健康受试者的样品获得的输入参考值,或通过将用一个样品获得的信号水平与用在稍后
时间点(优选至少一个月后)获得的第二样品获得的信号水平进行比较而获得的输入参考值、进行比较来确定信号水平是否指示患有或发展疾病的可能性增加。
[0136]
根据本发明,提供用于从sard患者(优选ssc患者)的血液(优选血清)中去除针对具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的自身抗体的装置(其中所述装置包含用具有序列seq id no1、seq id no11或seq id no24的多肽或其变体涂覆的承载体)作为离体方法,该方法用于从sard患者(优选ssc患者)的血液(优选血清)中除去针对具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的自身抗体。可以使用涂覆有具有序列seq id no1、seq id no11或seq id no24的多肽或其变体的装置,或者涂覆有捕获所有igg类抗体的二抗或蛋白质的装置,其中igg类自身抗体针对具有序列seq id no1、seq id no11或seq id no24的多肽或其变体。合适的方法描述于eisei noiri和noria hanafusa,the concise manual of apharesis therapy,springer tokyo,2014.hamilton,p.,kanigicherla,d.,hanumapura,p.,walz,l.,kramer,d.,fischer,m.,brenchley,p.和mitra,s.(2018)j.clin.aph.33(3),283-290中。在ep3477300中公开了另一种方法。
附图说明
[0137]
图1显示了使用hep-2细胞或猴肝脏和1:100稀释的患者血清(ps)的ifa。抗人igg-alexa 488(1:500)用作二抗。ps1对这两种底物都显示出核仁状图样。ps2和ps3显示出假致密细斑点状图样(放大倍数为200倍)。
[0138]
图2显示了患者(ps1-3)或对照血清(cs)与hep2提取物的免疫沉淀。将免疫沉淀物通过sds-page分离,然后进行考马斯染色。通过maldi-tof-ms将选择的蛋白质条带鉴定为nvl(条带1)、cd2bp2(条带2)或tjp1(条带3)
[0139]
图3显示了使用抗his标签(1:2000)、患者血清(1:200)和健康对照血清(1:200)以及重组抗原进行的免疫印迹:a)在大肠杆菌(e.coli)和ps1中表达的纯化的nvl-his,b)在大肠杆菌和ps2中表达的纯化的his-cd2bp2,c)在大肠杆菌和ps3中表达的纯化的his-tjp1 aa1-575,d)全长tjp1-his(hek293细胞裂解物)或his-tjp1 aa1-575(大肠杆菌裂解物)。在二次孵育中使用抗小鼠-igg-ap(1:2000)或抗人-igg-b/e-ap(1:10)。
[0140]
图4显示了分别使用nvl-his、tjp1-his或对照转染的hek293细胞和ps1(1:100)或ps3(1:10)的ifa。抗人igg-alexa488(1:500)用作二抗。箭头表示特定的荧光信号(放大倍数为200倍)。
[0141]
图5显示了用患者血清和hep-2细胞进行的ifa中和测定。将患者血清与稀释的纯化的重组抗原或对照缓冲液一起孵育,然后应用于使用hep-2细胞的ifa中应用之前。标明了单独的血清稀释度。抗人igg-alexa488(1:500)用作二抗(放大倍数为200倍)。
[0142]
图6显示了在hep-2、hek-tjp1和hek对照细胞中使用抗tjp1抗体(小鼠,单克隆的)和ps3进行的共定位分析。在ifa中施用了ps3(1:10)和抗tjp1(1:50)的混合物。抗人igg-alexa488(1:500)和抗小鼠igg-cy3(1:200)用作二抗。a)hep-2细胞。b)过表达tjp1-his的转染的hek293细胞。c,d)用空载体转染的对照hek293细胞(a-c放大倍数为200倍,d放大倍数为3200倍)。
[0143]
图7a、图7b和图7c显示了用大肠杆菌裂解物和相应的患者血清(ps1-3,1:200)、对
照血清(cs1-3,1:200)或抗his标签抗体(1:2000)进行的免疫印迹,所述裂解物包含图7a)nvl片段(aa1-117、aa106-292、aa281-560、aa549-856)、图7b)cd2bp2片段(aa117-260、aa249-341)或图7c)tjp1片段(aa1-156、aa145-306、aa295-575)。在二次孵育中使用抗小鼠-igg-ap(1:2000)或抗人-igg-b/e-ap(1:10)。具有主要反应的片段用粗体字母标示。
[0144]
图8显示了使用纯化的nvl-his(a)、his-cd2bp2(b)或his-tjp1 aa1-575(c)和来自系统性风湿性疾病(sard)队列的抗nvl、抗cd2bp2或抗tjp1线印迹阳性血清(1:200)进行的免疫印迹。作为阳性和阴性对照,并行孵育抗his-标签-ap(1:8000)、ps1-3(1:200)和对照血清(1:200)。抗人igg b/e-ap(1:10)用于二次孵育。
[0145]
序列:
[0146]
本发明包括一系列多肽。如果未在下文中公开,则确切的序列提供于序列表中:
[0147]
seq id no1[nvl-同种型1,uniprot o15381-1]
[0148]
mkprpagfvdnklkqrviqyltsnkcgkyvdigvlasdlqrvysidygrrkrnafriqvekvfsiissekelknlteledehlakrarqgeedneytesysdddssmedypdpqsanhmnssllslyrkgnpdsvsntpemeqrettsstprissktgsiplktpakdseggwfidktpsvkkdsffldlsceksnpkkpiteiqdskdssllesdmkrkgklknkgskrkkedlqevdgeieavlqkkakarglefqisnvkfedvggndmtlkevckmlihmrhpevyhhlgvvpprgvllhgppgcgktllahaiageldlpilkvaapeivsgvsgeseqklrelfeqavsnapciifideidaitpkrevaskdmerrivaqlltcmddlnnvaatarvlvigatnrpdsldpalrragrfdreiclgipdeasrerilqtlcrklrlpqafdfchlahltpgfvgadlmalcreaamcavnrvlmklqeqqkknpemedlpskgvqeerlgteptsetqdelqrllgllrdqdplseeqmqglcielndfivalssvqpsakregfvtvpnvtwadigaledireeltmailapvrnpdqfkalglvtpagvllagppgcgktllakavanesglnfisvkgpellnmyvgeseravrqvfqraknsapcviffdevdalcprrsdretgasvrvvnqlltemdglearqqvfimaatnrpdiidpailrpgrldktlfvglpppadrlailktitkngtkppldadvnleaiagdlrcdcytgadlsalvreasicalrqemarqksgnekgelkvshkhfeeafkkvrssiskkdqimyerlqeslsr
[0149]
seq id no2[nvl-同种型3]
[0150]
seq id no3[nvl基因合成]
[0151]
seq id no4[有义nvl-if1]
[0152]
seq id no5[反义nvl-if1]
[0153]
seq id no6[nvl-pcr-片段]
[0154]
seq id no7[ptriex-1-nvl[人]-if1-h8]
[0155]
seq id no8[nvl[人]-if1-h8]
[0156]
seq id no9[pet24d-nvl[人]-if1-h6]
[0157]
seq id no10[nvl[人]-if1-h6]
[0158]
mkprpagfvdnklkqrviqyltsnkcgkyvdigvlasdlqrvysidygrrkrnafriqvekvfsiissekelknlteledehlakrarqgeedneytesysdddssmedypdpqsanhmnssllslyrkgnpdsvsntpemeqrettsstprissktgsiplktpakdseggwfidktpsvkkdsffldlsceksnpkkpiteiqdskdssllesdmkrkgklknkgskrkkedlqevdgeieavlqkkakarglefqisnvkfedvggndmtlkevckmlihmrhpevyhhlgvvpprgvllhgppgcgktllahaiageldlpilkvaapeivsgvsgeseqklrelfeqavsnapciifideidaitpkrevaskdmerrivaqlltcmddlnnvaatarvlvigatnrpdsldpalrragrfdreiclgipdeasrerilqtlcrklrlpqafdfchlahltpgfvgadlmalcreaamcavnrvlmklqeqqkknpemedlpskgvqeerlgteptsetqdelqrl
lgllrdqdplseeqmqglcielndfivalssvqpsakregfvtvpnvtwadigaledireeltmailapvrnpdqfkalglvtpagvllagppgcgktllakavanesglnfisvkgpellnmyvgeseravrqvfqraknsapcviffdevdalcprrsdretgasvrvvnqlltemdglearqqvfimaatnrpdiidpailrpgrldktlfvglpppadrlailktitkngtkppldadvnleaiagdlrcdcytgadlsalvreasicalrqemarqksgnekgelkvshkhfeeafkkvrssiskkdqimyerlqeslsrvehhhhhh
[0159]
seq id no11[cd2bp2,uniprot o95400]
[0160]
mpkrkvtfqgvgdeededeiivpkkklvdpvagsggpgsrfkgkhsldsdeeeddddggsskydilasedvegqeaatlpseggvritpfnlqeemeeghfdadgnyflnrdaqirdswldnidwvkirerppgqrqasdseeedslgqtsmsaqallegllelllpretvagalrrlgargggkgrkgpgqpsspqrldrlsgladqmvargnlgvyqetrerlamrlkglgcqtlgphnptpppsldmfaeelaeeeletptptqrgeaesrgdglvdvmweykwentgdaelygpftsaqmqtwvsegyfpdgvycrkldppggqfynskridfdlyt
[0161]
seq id no12[cd2bp2,登录号bc001947]
[0162]
seq id no13[cd2bp2,基因合成片段1,aa1-173]
[0163]
seq id no14[cd2bp2,基因合成片段2,aa174-341]
[0164]
seq id no15[cd2bp2,基因合成片段1,bbsi]
[0165]
seq id no16[cd2bp2,基因合成片段2,bbsi]
[0166]
seq id no17[有义cd2bp2-片段-2]
[0167]
seq id no18[反义cd2bp2-片段-2]
[0168]
seq id no19[cd2bp2-pcr-片段]
[0169]
seq id no20[ptriex-1-cd2bp2[人]]
[0170]
seq id no21[cd2bp2[人]-h8]
[0171]
seq id no22[pet24d-n-cd2bp2[人]]
[0172]
seq id no23[h8-cd2bp2[人]]
[0173]
mshhhhhhhhsmpkrkvtfqgvgdeededeiivpkkklvdpvagsggpgsrfkgkhsldsdeeeddddggsskydilasedvegqeaatlpseggvritpfnlqeemeeghfdadgnyflnrdaqirdswldnidwvkirerppgqrqasdseeedslgqtsmsaqallegllelllpretvagalrrlgargggkgrkgpgqpsspqrldrlsgladqmvargnlgvyqetrerlamrlkglgcqtlgphnptpppsldmfaeelaeeeletptptqrgeaesrgdglvdvmweykwentgdaelygpftsaqmqtwvsegyfpdgvycrkldppggqfynskridfdlyt
[0174]
seq id no24[tjp1-同种型2,uniprot q07157-2]
[0175]
msaraaaakstameetaiweqhtvtlhrapgfgfgiaisggrdnphfqsgetsivisdvlkggpaegqlqendrvamvngvsmdnvehafavqqlrksgknakitirrkkkvqipvsrpdpepvsdneedsydeeihdprsgrsgvvnrrsekiwprdrsasrerslsprsdrrsvassqpakptkvtlvksrkneeyglrlashifvkeisqdslaardgniqegdvvlkingtvtenmsltdaktlierskgklkmvvqrderatllnvpdlsdsihsanaserddiseiqslasdhsgrshdrpprrsrsrspdqrsepsdhsrhspqqpsngslrsrdeeriskpgavstpvkhaddhtpktveevtvernekqtpslpepkpvyaqvgqpdvdlpvspsdgvlpnsthedgilrpsmklvkfrkgdsvglrlaggndvgifvagvledspaakegleegdqilrvnnvdftniireeavlflldlpkgeevtilaqkkkdvyrrivesdvgdsfyirthfeyekespyglsfnkgevfrvvdtlyngklgswlairigknhkevergiipnknraeqlasvqytlpktaggdradfwrfrglrsskrnlrksredlsaqpvqtkfpayervvlreagflrpvtifgpiadvareklareepdiyqiakseprdagtdqrssgiirlhtikqiidqdkhalldvtpnavdrlnyaqwypivvflnpdskqgvktmrmrlcpesrksarklyershklr
knnhhlftttinlnsmndgwygalkeaiqqqqnqlvwvsegkadgatsddldlhddrlsylsapgseysmystdsrhtsdyedtdteggaytdqeldetlndevgtppesaitrssepvredssgmhhenqtyppyspqaqpqpihridspgfkpasqqvyrkdpypeemmrqnhvlkqpavshpghrpdkepnltyepqlpyvekqasrdleqptyryesssytdqfsrnyehrlryedrvpmyeeqwsyyddkqpypsrppfdnqhsqdldsrqhpeessergyfprfeepaplsydsrpryeqaprasalrheeqpapgydthgrlrpeaqphpsagpkpaeskqyfeqysrsyeqvppqgftsraghfeplhgaaavpplipssqhkpealpsntkplpppptqteeeedpamkpqsvltrvkmfenkrsasletkkdvndtgsfkppevaskpsgapiigpkptsqnqfsehdktlyripepqkpqlkppedivrsnhydpeedeeyyrkqlsyfdrrsfenkppahiaashlsepakpahsqnqsnfssysskgkppeadgvdrsfgekryepiqatppppplpsqyaqpsqpvtsaslhihskgahgegnsvsldfqnslvskpdpppsqnkpatfrppnredtaqaafypqksfpdkapvngteqtqktvtpaynrftpkpytssarpferkfespkfnhnllpsetahkpdlssktptspktlvkshslaqppefdsgvetfsihaekpkyqinnistvpkaipvspsaveedededghtvvatargifnsnggvlssietgvsiiipqgaipegveqeiyfkvcrdnsilppldkekgetllsplvmcgphglkflkpvelrlphcdpktwqnkclpgdpnylvgancvsvlidhf
[0176]
seq id no25[有义tjp1-if2-zf1]
[0177]
seq id no26[反义tjp1-if2-zf1]
[0178]
seq id no27[有义tjp1-if2-zf2]
[0179]
seq id no28[反义tjp1-if2-zf2]
[0180]
seq id no29[tjp1-pcr-片段-1]
[0181]
seq id no30[tjp1-pcr-片段-2]
[0182]
seq id no31[ptriex-1-tjp1[人]-if2]
[0183]
seq id no32[tjp1[人]-if2-h8]
[0184]
seq id no33[有义nvl-f1]
[0185]
seq id no34[反义nvl-f1]
[0186]
seq id no35[nvl-pcr-片段1-117]
[0187]
seq id no36[有义nvl-f2]
[0188]
seq id no37[反义nvl-f2]
[0189]
seq id no38[nvl-pcr-片段106-292]
[0190]
seq id no39[有义nvl-f3]
[0191]
seq id no40[反义nvl-f3]
[0192]
seq id no41[nvl-pcr-片段281-560]
[0193]
seq id no42[有义nvl-f4]
[0194]
seq id no43[反义nvl-f4]
[0195]
seq id no44[nvl-pcr-片段549-856]
[0196]
seq id no45[pet24d-n-nvl[人](aa1-117)]
[0197]
seq id no46[pet24d-n-nvl[人](aa106-296)]
[0198]
seq id no47[pet24d-n-nvl[人](aa281-560)]
[0199]
seq id no48[pet24d-n-nvl[人](aa549-856)]
[0200]
seq id no49[h8-nvl[人](aa1-117)]
[0201]
seq id no50[h8-nvl[人](aa106-292)]
[0202]
seq id no51[h8-nvl[人](aa281-560)]
[0203]
seq id no52[h8-nvl[人](aa549-856)]
[0204]
seq id no53[有义cd2bp2-f1]
[0205]
seq id no54[反义cd2bp2-f1]
[0206]
seq id no55[cd2bp2-pcr-片段1-128]
[0207]
seq id no56[有义cd2bp2-f2]
[0208]
seq id no57[反义cd2bp2-f2]
[0209]
seq id no58[cd2bp2-pcr-片段117-260]
[0210]
seq id no59[有义cd2bp2-f3]
[0211]
seq id no60[反义cd2bp2-f3]
[0212]
seq id no61[cd2bp2-pcr-片段249-341]
[0213]
seq id no62[pet24d-n-cd2bp2[人](aa1-128)]
[0214]
seq id no63[pet24d-n-cd2bp2[人](aa117-260)]
[0215]
seq id no64[pet24d-n-cd2bp2[人](aa249-341)]
[0216]
seq id no65[h8-cd2bp2[人](aa1-128)]
[0217]
seq id no66[h8-cd2bp2[人](aa117-260)]
[0218]
seq id no67[h8-cd2bp2[人](aa249-341)]
[0219]
seq id no68[有义tjp1-f1/2]
[0220]
seq id no69[反义tjp1-f1/4]
[0221]
seq id no70[tjp1-pcr-片段1-575]
[0222]
seq id no71[反义tjp1-f2]
[0223]
seq id no72[tjp1-pcr-片段1-156]
[0224]
seq id no73[有义tjp1-f3]
[0225]
seq id no74[反义tjp1-f3]
[0226]
seq id no75[tjp1-pcr-片段144-306]
[0227]
seq id no76[有义tjp1-f4]
[0228]
seq id no77[tjp1-pcr-片段294-575]
[0229]
seq id no78[pet24d-n-tjp1[人](aa1-575)]
[0230]
seq id no79[pet24d-n-tjp1[人](aa1-156)]
[0231]
seq id no80[pet24d-n-tjp1[人](aa144-306)]
[0232]
seq id no81[pet24d-n-tjp1[人](aa294-575)]
[0233]
seq id no82[h8-tjp1[人](aa1-575)]
[0234]
mshhhhhhhhsmsaraaaakstameetaiweqhtvtlhrapgfgfgiaisggrdnphfqsgetsivisdvlkggpaegqlqendrvamvngvsmdnvehafavqqlrksgknakitirrkkkvqipvsrpdpepvsdneedsydeeihdprsgrsgvvnrrsekiwprdrsasrerslsprsdrrsvassqpakptkvtlvksrkneeyglrlashifvkeisqdslaardgniqegdvvlkingtvtenmsltdaktlierskgklkmvvqrderatllnvpdlsdsihsanaserddiseiqslasdhsgrshdrpprrsrsrspdqrsepsdhsrhspqqpsngslrsrdeeriskpgavstpvkhaddhtpktveevtvernekqtpslpepkpvyaqvgqpdvdlpvspsdgvlpnsthedgilrpsmklvkfrkgdsvglrlaggndvgifvagvledspaakegleegdqilrvnnvdftniireeavlflldlpkgeevtilaqkkkdvyrrivesdvgdsfyirthfeyekespyglsfnkgevfrvvdtlyngklgswlairigknhkevergiip
[0235]
seq id no83[h8-tjp1[人](aa1-156)]
[0236]
seq id no84[h8-tjp1[人](aa144-306)]
[0237]
seq id no85[h8-tjp1[人](aa294-575)]
[0238]
seq id no86[nvl-片段(aa591-603)]
[0239]
eeltmailapvrn
[0240]
seq id no87[nvl-片段(aa607-617)]
[0241]
fkalglvtpag
[0242]
seq id no88[nvl-片段(aa685-695)]
[0243]
alcprrsdret
[0244]
seq id no89[nvl-片段(aa742-753)]
[0245]
ktlfvglpppad
[0246]
seq id no90[nvl-片段(aa761-772)]
[0247]
itkngtkpplda
[0248]
seq id no91[nvl-片段(aa778-789)]
[0249]
aiagdlrcdcyt
[0250]
seq id no92[nvl-片段(aa809-826)]
[0251]
marqksgnekgelkvshk
[0252]
seq id no93[nvl-片段(aa844-856)]
[0253]
qimyerlqeslsr
[0254]
通过以下非限制性实施例进一步说明本发明,从这些实施例中可以获得本发明的进一步特征、具体实施方案、方面和优势。
具体实施方式
[0255]
实施例1:
[0256]
概述
[0257]
方法:选择了具有针对未知核自身抗原(una)的预定ana的三种患者血清(ps1-3),如通过在hep2细胞上进行的间接免疫荧光测定(ifa)和使用23种已知核抗原进行的线印迹所测定的。用hep-2细胞裂解物和质谱法在免疫沉淀试验中分析血清。在大肠杆菌和/或hek293细胞中重组表达经鉴定的候选自身抗原,并将其用于免疫印迹、线印迹、重组ifa和中和测定。另外,研究了系统性自身免疫性风湿性疾病患者队列(sard队列,n=488)中针对这些抗原的ana的流行率。
[0258]
结果:核vcp样蛋白(nvl)、cd2抗原胞质尾结合蛋白2(cd2bp2)和紧密连接蛋白zo-1(tjp1)被鉴定为ps1、ps2和ps3的相应靶抗原。在使用相应纯化的重组抗原nvl、cd2bp2和tjp1aa1-575 ps1-3的免疫印迹中,显示出与个体抗原的阳性反应,而健康对照(n=15)无反应。ps1与相应的nvl抗原以及ps2与相应的cd2bp2抗原的预孵育在hep2细胞ifa中消除了患者血清的ana反应。另外,ps1和ps3在重组hek293细胞ifa中与个体抗原反应。在基于相应纯化的重组抗原nvl、cd2bp2和tjp1 aa1-575的线印迹中筛选sard队列,鉴定了4名抗nvl(4x ssc)患者、10名抗cd2bp2患者(8x ssc、1x mctd、1x肌炎)和16名抗tjp1自身抗体患者(15x ssc、1x uctd),而所有对照血清(n=50)均为阴性。
[0259]
针对nvl、cd2bp2和tjp1的ana为sard,尤其是ssc或其它风湿性疾病提供了新型标志物。
[0260]
试剂
[0261]
如果没有另外说明,试剂获自德国达姆城的merck或德国海德堡的sigma-aldrich。
[0262]
方法
[0263]
患者
[0264]
对照集合包括50份健康供者血清。为了评估临床相关性,使用了患有系统性自身免疫性风湿性疾病(sard)的患者队列,其由来自488名患者的529份血清样品组成,其中378名患者患有系统性硬化症(ssc),110名患者患有其它疾病(抗合成酶综合征(ass)n=10;包涵体肌炎(ibm)n=4;混合型结缔组织病(mctd)n=6;肌炎n=15;原发性干燥综合征(pss)n=11;类风湿性关节炎(ra)n=24;系统性红斑狼疮(sle)n=30;未分化结缔组织病(uctd)n=10。在不同的时间点从相同的患者获得重复的血清。
[0265]
间接免疫荧光测定(ifa)
[0266]
使用具有丙酮固定的hep-2细胞的生物芯片阵列与肝组织冷冻切片的组合的载玻片进行ifa。将每个生物芯片镶嵌物与35μl 1:100的pbs稀释的样品在室温下孵育30分钟,用pbs-tween洗涤并浸入pbs-tween中5分钟。在第二步骤中,应用抗人igg-alexa488(1:500)(jackson immunoresearch,suffolk,uk)并在23℃的室温下孵育30分钟。将载玻片再次用pbs-tween冲洗,然后浸入pbs-tween中5分钟。将载玻片包埋在含甘油的pbs缓冲的dabco(每个区域约10μl)中,并通过荧光显微镜检术检查。
[0267]
对于共定位分析,在第一孵育步骤中使用抗tjp1抗体(1:50,33-9100,thermo fisher scientific,dreieich,德国)与患者血清(1:10)的混合物,在第二孵育步骤中使用抗人igg-alexa488(1:500)和抗小鼠igg-cy3(1:200)(jackson immunoresearch)。
[0268]
在竞争性抑制实验中,在hep2细胞上在ifa之前1小时,将重组抗原与个体患者血清混合。包括阳性和阴性对照。与对照转染的细胞和对照样品直接比较,基于转染的细胞的荧光强度将样品分类为阳性或阴性。终点滴度是指显示可见荧光的最后一次的稀释度。
[0269]
结果由两位独立的观察者使用eurostar ii显微镜(欧蒙医学实验诊断股份公司,l
ü
beck,德国)进行评估。
[0270]
免疫沉淀
[0271]
用500μl细胞hep-2细胞(10x106个细胞/ml)和5μl患者或对照血清进行免疫沉淀。将hep-2细胞在4℃下以16000x g离心10分钟。将沉淀物与患者或对照血清一起重悬于500μl ripa裂解缓冲液(pbs ph 7.4,0.1%(v/v)nonidet
tm p 40,1%(w/v)脱氧胆酸盐,0.1%(w/v)sds,1mm蛋白酶抑制剂混合物[sigma])中,并在4℃下旋转1小时。将悬浮液在4℃下以16000x g离心沉降20分钟。然后将上清液与蛋白g的dynabeads(thermofisher scientific,schwerte,德国)在4℃下一起孵育3小时以捕获免疫复合物。用pbs洗涤珠粒三次,并用含有25mmol/l二硫苏糖醇的nupage lds样品缓冲液(thermofisher scientific)在70℃洗脱10分钟。在sds-page(nupage,thermofisher scientific)之前用59mm碘乙酰胺(bio-rad,hamburg,德国)进行脲甲基化(carbamidomethylation)。用考马斯亮蓝(g-250)显现分离的蛋白质,并通过质谱分析进行鉴定。
[0272]
质谱法
[0273]
从考马斯亮蓝g-250染色的凝胶上切下可见的蛋白质条带。脱色和胰蛋白酶消化后,提取肽并用α-氰基-4-羟基肉桂酸点样到mtp anchorchip
tm 384tf靶标上。
[0274]
使用flexcontrol 3.4软件,使用autoflex iii smartbeam tof/tof200系统进行maldi-tof/tof测量。肽质量指纹图样(pmf)的ms谱以正离子反射器模式记录,拍摄次数为4,000-10,000次,质量范围为600da至4,000da。光谱用商购可得的肽校准标准品ii在外部校准,用flexanalysis 3.4处理,峰列表用biotools 3.2分析。
[0275]
通过使用mascot搜索引擎mascot server 2.3(matrix science,伦敦,英国)仅限于哺乳动物搜索ncbi或swissprot数据库用于蛋白质鉴定。搜索参数如下:质量耐受性设置为80ppm,接受一个缺失的切割位点,半胱氨酸残基的脲甲基化以及甲硫氨酸残基的氧化分别设置为固定和可变修饰。为了评估蛋白质命中,选择p《0.05的显著性阈值。
[0276]
为了进一步确认pmf命中,使用biotools的warp反馈机制,选择每种已鉴定蛋白质的2-5种肽进行ms/ms测量。母体和碎片质量分别用400和1000次拍摄记录。如上所述处理和分析光谱,碎片质量允差为0.7da。
[0277]
全长nvl、cd2bp2和tjp1在hek293或大肠杆菌中的重组表达
[0278]
nvl同种型1(核含缬酪肽的蛋白样)
[0279]
从source bioscience uk limited获得编码人nvl同种型1(seq id no 1)的部分序列(氨基酸206-856)的cdna克隆iraup969f0866d。该cdna克隆编码nvl同种型3(登录号bc012105,seq id no 2)。从eurofins genomics germany gmbh(ebersberg)订购编码nvl同种型1的缺失的氨基酸1-205的合成dna片段。用bsai(r3733,new england biolabs,frankfurt am main,德国)消化基因合成产物(seq id no 3),通过凝胶纯化分离614bp片段。
[0280]
使用cdna克隆iraup969f0866d和dna寡核苷酸引物有义nvl-if1(seq id no 4)和反义nvl-if1(seq id no 5)通过pcr扩增nvl-同种型1的氨基酸206-856的编码序列,产生seq id no6。
[0281]
将所述扩增产物用bsai消化,并与基因合成片段一起用ncoi和xhoi线性化的ptriex-1载体(merck,darmstadt,德国)连接,产生seq id no 7,编码与八组氨酸标签(h8)(seq id no 8)或pet24d载体(merck)融合的nvl[人]-if1,产生seq id no 9,编码与六组氨酸标签(h6)融合的nvl[人]-if1(seq id no 10)。
[0282]
cd2bp2(cd2抗原胞质尾结合蛋白2)
[0283]
编码全长人cd2bp2(seq id no 11)的cdna克隆是不可获得的。因此,编码人cd2bp2(登录号bc001947,seq id no 12)的两个合成基因片段获自eurofins genomics germany gmbh(ebersberg)。
[0284]
第一片段编码人cd2bp2的氨基酸1-173,且另一个片段编码包括终止密码子的人cd2bp2的氨基酸174-341。用bbsi(r3539,new england biolabs)消化两种基因合成产物(seq id no 13和seq id no 14),产生517bp的片段-1和510bp的片段-2(seq id no 15和seq id no 16),对所述两种片段进行凝胶纯化。使用基因合成产物(seq id no 14)作为模板以及使用dna寡核苷酸引物有义cd2bp2-片段-2(seq id no 17)和反义cd2bp2-片段-2(seq id no 18),通过pcr扩增cd2bp2的第三片段,产生无终止密码子的seq id no 19。扩
增产物用bbsi(r3539,new england biolabs)消化。
[0285]
将片段seq id no 15和seq id no 16与ncoi和xhoi线性化的ptriex-1载体(merck)连接,产生seq id no 20,编码与c-末端八组氨酸标签(h8)融合的cd2bp2[人](seq id no 21)。将片段seq id no 15和bbsi消化的片段seq id no 19与ncoi和xhoi线性化的pet24d载体(merck)连接,产生seq id no 22,编码与n-末端八组氨酸标签(h8)融合的cd2bp2[人](seq id no 23)。
[0286]
tjp1-同种型2(紧密连接蛋白zo-1)
[0287]
编码人tjp1-同种型1(登录号bc111712)的cdna克隆ircmp5012c0531d获自source bioscience uk limited。为了表达人tjp1-同种型2(seq id no 24),使用dna寡核苷酸引物有义tjp1-if2-zf1(seq id no 25)和反义tjp1-if2-zf1(seq id no 26)以及有义tjp1-if2-zf2(seq id no 27)和反义tjp1-if2-zf2(seq id no 28)通过pcr扩增两个片段。一个片段(seq id no 29)用bsai(r3733,new england biolabs)消化,另一个片段(seq id no30)用esp3i(r0734,new england biolabs)消化。将这两个片段都与ncoi和xhoi线性化的ptriex-1载体(merck)连接,产生seq id no 31,编码与c末端八组氨酸标签(h8)融合的人tj p1-同种型2(seq id no 32)。
[0288]
根据生产商的说明(biomol gmbh,hamburg,德国),在exgen500介导的转染(thermofisher scientific,dreieich,德国)后,分别在人细胞系hek293中表达nvl-his和tjp1-his。为了产生免疫荧光底物,将细胞在盖玻片上生长,转染两天后用丙酮固定。出于其它目的,在转染后5天收获细胞,并用nupage lds样品缓冲液(thermofisher scientific,schwerte,德国)裂解。
[0289]
nvl、cd2bp2和tjp1片段在大肠杆菌中的重组表达
[0290]
nvl
[0291]
用于表位作图,使用seq id no 7作为模板以及使用dna寡核苷酸引物有义nvl-f1(seq id no 33)和反义nvl-f1(seq id no34)(针对nvl-片段1-117(seq id no 35))、有义nvl-f2(seq id no 36)和反义nvl-f2(seq id no 37)(针对nvl-片段106-292(seq id no 38))、有义nvl-f3(seq id no 39)和反义nvl-f3(seq id no 40)(针对nvl-片段281-560(seq id no 41))以及有义nvl-f4(seq id no 42)和反义nvl-f4(seq id no 43)(针对nvl-片段549-856(seq id no 44)),通过pcr扩增跨越氨基酸残基1至117、106至292、281至560和549至856的人nvl片段。将扩增产物用bsai(r3733,new england biolabs)消化,并与ncoi和xhoi线性化的pet24d载体(merck)连接,产生编码4种与n末端八组氨酸-标签(h8)融合的蛋白质(seq id no 49至seq id no 52)的pet24d-n-nvl[人](aa1-117)(seq id no 45)、pet24d-n-nvl[人](aa106-296)(seq id no 46)、pet24d-n-nvl[人](aa281-560)(seq id no 47)和pet24d-n-nvl[人](aa549-856)(seq id no 48)。
[0292]
cd2bp2
[0293]
用于表位作图,使用seq id no 22作为模板以及使用dna寡核苷酸引物有义cd2bp2-f1(seq id no 53)和反义cd2bp2-f1(seq id no 54)(针对cd2bp2-片段1-128(seq id no 55))、有义cd2bp2-f2(seq id no 56)和反义cd2bp2-f2(seq id no 57)(针对cd2bp2-片段117-260(seq id no 58))以及有义cd2bp2-f3(seq id no 59)和反义cd2bp2-f3(seq id no 60)(针对cd2bp2-片段249-341(seq id no 61)),通过pcr扩增跨越氨基酸
残基1至128、117至260和249至341的人cd2bp2的片段。将扩增产物用esp3i(r0734,new england biolabs)消化,并与ncoi和xhoi线性化的pet24d载体(merck)连接,产生编码3种与n末端八组氨酸标签(h8)融合的蛋白质(seq id no 65至seq id no 67)的pet24d-n-cd2bp2[人](aa1-128)(seq id no 62),pet24d-n-cd2bp2[人](aa117-260)(seq id no 63)和pet24d-n-cd2bp2[人](aa249-341)(seq id no 64)。
[0294]
tjp1
[0295]
用于表位作图,使用seq id no 31作为模板以及使用dna寡核苷酸引物有义tjp1-f1/2(seq id no 68)和反义tjp1-f1/4(seq id no 69)(针对tjp1-片段1-575(seq id no 70))、有义tjp1-f1/2(seq id no 68)和反义tjp1-f2(seq id no 71)(针对tjp1-片段1-156(seq id no 72))、有义tjp1-f3(seq id no 73)和反义tjp1-f3(seq id no 74)(针对tjp1-片段144-306(seq id no 75))以及有义tjp1-f4(seq id no 76)和反义tjp1-f1/4(seq id no 69)(针对tjp1-片段294-575(seq id no 77)),通过pcr扩增跨越氨基酸残基1至575、1至156、144至306和294至575的人tjp1片段。将扩增产物用bsai(r3733,new england biolabs)消化,并与ncoi和xhoi线性化的pet24d载体(merck)连接,产生编码4种与n末端八组氨酸(h8)融合的蛋白(seq id no 82至seq id no 85)的pet24d-n-tjp1[人](aa1-575)(seq id no 78)、pet24d-n-tjp1[人](aa1-156)(seq id no 79)、pet24d-n-tjp1[人](aa144-306)(seq id no 80)和pet24d-n-tjp1[人](aa294-575)(seq id no 81)。
[0296]
基本上如pet系统手册(merck)中所述,使用大肠杆菌菌株rosettablue(de3)placi(merck)进行细菌表达。通过加入2mm异丙基β-d-硫代半乳糖苷(iptg)在37℃诱导蛋白质表达3小时。
[0297]
蛋白质纯化
[0298]
裂解细菌细胞,将蛋白质溶解在1x pbs ph 7.4、1m nacl、8m尿素缓冲液(nvl和tjp1)或20mm tris-hcl ph 8.5、600mm nacl缓冲液(cd2bp2)中,并按照如c.probst,w.schlumberger,w.stocker等人“development of elisa for the specific determination of autoantibodies against envoplakin and periplakin in paraneoplastic pemphigus,”clinica chimica acta,第410卷,第1-2期,第13
–
18页,2009中的方案通过ni
2+-亲和色谱和离子交换色谱进行纯化。将蛋白质以等分试样于-80℃下储存,直至进一步使用。
[0299]
免疫印迹
[0300]
将相应的缓冲液中的纯化的重组抗原(seq id no 10,23,82)或表达重组抗原片段(seq id no 49,50,51,52,66,67,83,84,85)的大肠杆菌或含重组抗原(seq id no 32)的hek细胞裂解物与含有25mmol/l二硫苏糖醇的nupage lds样品缓冲液(thermofisher scientific,schwerte,德国)在70℃孵育10分钟,然后进行sds-page(nupage,thermofisher scientific)。按照制造商的说明,使用转移缓冲液(thermofisher scientific)通过槽式印迹将分离的蛋白质电转移到硝酸纤维素膜上。用universal blot buffer plus(欧蒙医学实验诊断股份公司,l
ü
beck,德国)封闭膜15分钟,并在universal blot buffer plus中与患者或对照血清(稀释度为1:200)或抗-his(1:2000,70796-3,merck)一起孵育3小时,随后用universal blot buffer(欧蒙医学实验诊断股份公司,l
ü
beck,德国)进行三次洗涤步骤,与抗人-igg-ap(1:10,欧蒙医学实验诊断股份公司,l
ü
beck,德国)或抗小鼠-igg-ap(1:2000,jackson immunoresearch,suffolk,uk)一起进行第二次孵育30分钟,进行3次洗涤步骤,并用nbt/bcip底物(欧蒙医学实验诊断股份公司,l
ü
beck,德国)进行染色。或者,将在小鼠中产生的单克隆抗his-ap抗体(1:8000,a5588,sigma-aldrich)用于一步孵育。
[0301]
线印迹
[0302]
使用euroline ana profile(igg)23(dl 1590-5001-23g,欧蒙医学实验诊断股份公司,l
ü
beck,德国)测定了23种最常见的ana(dsdna、核小体、组蛋白、ss-a、ro-52、ssb、rnp/sm、sm、mi-2α、mi-2β、ku、cenp a、cenp b、sp100、pml、scl-70、pm100、pm75、rp11、rp155、gp210、pcna、dsf70)。简言之,将条带与1ml酪蛋白样品缓冲液(欧蒙医学实验诊断股份公司,l
ü
beck,德国)一起孵育5分钟,然后在1:101稀释的血清样品中孵育30分钟。之后,用1.5ml洗涤缓冲液洗涤每个条带三次,每次5分钟,然后用1ml抗人igg-ap(1:10,欧蒙医学实验诊断股份公司,l
ü
beck,德国)孵育30分钟。如上所述再次洗涤条带,并将其与nbt/bcip底物溶液(欧蒙医学实验诊断股份公司,l
ü
beck,德国)一起孵育10分钟。通过用1ml蒸馏水洗涤三次来停止反应。使用软件eurolinescan(欧蒙医学实验诊断股份公司,l
ü
beck,德国)分析条带。
[0303]
另外,在大肠杆菌中表达重组抗原(seq id no 10,23,82),并如上所述进行纯化,将所述重组抗原在相应的缓冲液中稀释并点样到预切割(3mm x 5mm)的空biodyne
tm b膜(biodyne
tm b尼龙膜,0.45μm,thermo fisher scientific,schwerte,德国)上。将膜在rt下干燥20分钟,然后如上所述进行患者血清孵育。
[0304]
结果
[0305]
患者自身抗体的表征
[0306]
患者血清在使用hep2细胞和肝组织切片的ifa中显示核仁状(ps1)或假致密细斑点状图样(ps2,ps3)(图1)。在用涂覆有23种ana自身抗原(dsdna,核小体,组蛋白,ss-a,ro-52,ssb,rnp/sm,sm,mi-2α,mi-2β,ku,cenp a,cenp b,sp100,pml,scl-70,pm100,pm75,rp11,rp155,gp210,pcna,dsf70)的线印迹进行的进一步单特异性分析中,排除了已知ana的存在。
[0307]
nvl、cd2bp2和tjp1作为靶自身抗原的鉴定
[0308]
为了鉴定靶抗原,用hep-2细胞匀浆对患者血清进行免疫沉淀(ip)。将免疫沉淀的蛋白质通过sds-page分离并用蓝银考马斯染色进行染色。在患者血清的ip洗脱液中,检测到约100kda处(ps1,条带1)、50kda处(ps2,条带2)和220kda处(ps3,条带3)的条带(图2),所述条带在对照血清ip洗脱液中不存在。通过质谱分析标记的条带,并将其鉴定为核含缬酪肽的蛋白样(nvl,条带1)、cd2抗原胞质尾结合蛋白2(cd2bp2,条带2)或紧密连接蛋白zo-1(tjp1,条带3)。
[0309]
nvl、cd2bp2和tjp1作为靶自身抗原的验证
[0310]
在大肠杆菌中重组表达人nvl、cd2bp2和tjp1 aa1-575。将纯化的抗原用于免疫印迹,并用抗his-标签抗体、个体患者血清和健康对照血清进行测试(n=15)。如图3a至图3c所示,抗his-标签抗体和患者血清显示出与重组抗原的阳性反应,而15份健康对照血清没有显示出可比的反应性。还可以检测到ps3但非对照血清与全长tjp1的结合(图3d)。另外,
使用表达重组nvl或tjp1的hek293细胞进行的ifa,证实了在相应患者血清中存在针对这些蛋白质的自身抗体(图4)。将纯化的抗原进一步用于中和测试,以检测它们消除患者血清中ifa的ana图样的能力。在hep-2细胞上进行标准ifa之前,将ps1-3与单独的抗原或对照缓冲液一起孵育。图4显示ps1与nvl和ps2与cd2bp2的预孵育导致hep-2细胞上ana图样的完全或部分减少。这些结果证实了ps1和ps2的相应ana图样确实是由靶向nvl或cd2bp2的自身抗体引起的。然而,在ps3与纯化的tjp1 aa1-575一起孵育后,与对照孵育相比,观察到相同的荧光信号。这表明ps3中存在的抗tjp1自身抗体不会导致观察到的ana图样。
[0311]
为了进一步证实这一点,将ps3和商业抗tjp1抗体与hep-2细胞、重组hek-tjp1细胞和hek对照细胞一起孵育。如图6a所示,商业抗tjp1抗体在hep-2细胞中显示出扩散的细胞质染色,这也在使用ps3进行的ifa中观察到。因此,在使用ps3进行的ifa中观察到的ana图样可能不是由抗tjp1自身抗体引起的。然而,商业抗tjp1抗体显示出与ps3一样的针对表达tjp1的转染hek293细胞的特异性免疫反应(图6b)和在hek对照细胞之间的接合处的特异性反应(图6c)。所选区域的放大图(图6d)显示也定位在细胞间接触区域的来自ps3的自身抗体,表明ps3除了识别未知的核抗原外,还识别细胞接合处的内源性tjp1。
[0312]
抗nvl、抗cd2bp2和抗tjp1自身抗体识别的表位特征
[0313]
在用含有nvl片段(aa1-117,aa106-292,aa281-560,aa549-856,图7a)、cd2bp2片段(aa117-260,aa249-341,图7b)或tjp1片段(aa1-156,aa145-306,aa295-575,图7c)的大肠杆菌裂解物进行的蛋白质印迹中,ps1或ps2显示出与相应的nvl或cd2bp2的c末端片段的最强反应性,表明患者的自身抗体识别位于nvl的最后308aa或cd2bp2的最后93aa中的表位。ps3主要与tjp1的n-末端片段反应,表明该表位位于tjp1的前156个aa中。
[0314]
进一步的结果(数据未显示)表明,一种或多种被抗nvl识别的表位是一种、两种、三种、四种、五种、六种、七种或全部根据seq id no86,seq id no87,seq id no88,seq id no89,seq id no90,seq id no91,seq id no92和seq id no93的c末端片段,或者位于所述c末端片段中。
[0315]
抗nvl、抗cd2bp2和抗tjp1自身抗体的临床相关性的验证
[0316]
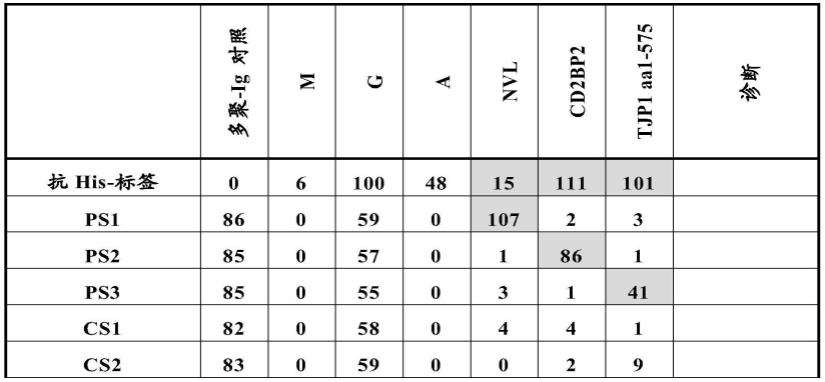
为了评估抗nvl、抗cd2bp2和抗tjp1自身抗体的临床相关性,开发了用纯化的重组nvl、cd2bp2和tjp1 aa1-575涂覆的线印迹,并用抗his-标签-ap、ps1-3和健康对照血清进行了验证(n=50)(表1),然后对临床表征的患者集合进行分析。ps1-3显示出针对相应抗原的阳性反应,而50份健康对照血清未显示出该反应。之后,分析了来自488名系统性风湿性疾病患者(sard队列)的529份血清。来自4名sard患者的6份血清为抗nvl,10名患者为抗cd2bp2,16名患者为抗tjp1阳性(表1)。用纯化的nvl、cd2bp2或tjp1aa1-575进行的蛋白质印迹分析证实了所有阳性反应(图8)。所有抗nvl阳性患者,以及8名抗cd2bp2阳性和15名抗tjp1阳性患者被诊断为ssc。一名抗cd2bp2阳性患者患有mctd,一名患有肌炎。另外,一名抗tjp1阳性患者患有uctd。
[0317]
在表1中显示总结的数据。已将使用纯化的nvl、cd2bp2和tjp1 aa1-575进行的线印迹与抗his-标签-ap、ps1-3、健康对照血清(n=50)和来自系统性风湿性疾病患者的血清(sard队列,n=529)一起孵育。显示了所有阳性反应和三个代表性阴性对照反应(cs1-3)的条带强度,以及抗nvl、抗cd2bp2和抗tjp1阳性患者血清的诊断。
[0318]
表1
[0319][0320]
[0321]
实施例2:
[0322]
补充:抗nvl自身抗体与更大队列的临床相关性的评估
[0323]
进一步研究了抗nvl自身抗体与附加的对照集合的临床相关性,所述附加的对照集合包括健康供体血清(n=100)和来自205名患病对照患者(自身免疫性肝炎(aih)n=40,类风湿性关节炎(ra)n=30;系统性红斑狼疮(sle)n=135)的血清。
[0324]
对于补充研究,如实施例1所述,用涂覆有纯化的重组nvl的线印迹分析附加的血清。来自附加的对照集合的血清均未显示阳性反应。
[0325]
综合实施例1和实施例2的数据,只有来自ps1的血清和4名ssc患者的6份血清显示出抗重组nvl的阳性反应,这一点通过使用纯化的重组nvl进行蛋白质印迹分析得到证实。对于150份健康对照血清和315份患病对照血清,未检测到反应。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1