伊沙匹隆有关物质的分析检测方法与流程
1.本发明属于药物分析技术领域,具体涉及伊沙匹隆有关物质的分析检测方法。
背景技术:
2.伊沙匹隆其化学名称为(1s,3s,7s,10r,11s,12s,16r)-7,11-二羟基-8,8,10,12,16-五甲基-3-[(1e)1-甲基-2-(2-甲基噻唑-4-基)乙烯基]-4-氮杂-17-氮杂二环[14.1.0]十七烷-5,9-二酮,分子量为506.70,具体结构式如下所示:
[0003][0004]
伊沙匹隆(ixabepilone,1)是一种半合成的埃博霉素内酰胺类似物,与紫杉醇药物作用机制类似,通过干预癌症细胞的分裂使肿瘤细胞凋亡。伊沙匹隆是由百时美施贵宝研制的全球第一个埃博霉素类抗肿瘤药物,于2007年10月美国fda批准上市,用于单药或联合卡培他滨治疗蒽环类、紫杉烷衍生物和卡培他滨治疗无效的转移性或局部进展的晚期乳腺癌患者。
[0005]
现有文献关于伊沙匹隆的制备和临床研究内容有较多的报道,但是关于其质量控制与研究的报道相对较少。李苏,翏海等人的文章中公开了一种液相色谱-串联质谱法测定人血浆中伊沙匹隆浓度的方法;francis y.f.lee等人的文章中同样公开了使用液相色谱-串联质谱法测定伊沙匹隆的药代动力学参数。但是测定伊沙匹隆原料药中的含量及杂质的分析方法未见报道。
[0006]
虽然美国药典usp43中,收载有伊沙匹隆原料及其制剂标准,提供了一种使用高效液相伊沙匹隆有关物质进行检测分析的方法。美国药典usp43标准中检测到的已知杂质有杂质4、杂质5、杂质6和杂质7,这些杂质来自于工艺杂质、中间产品及降解产物。但是,通过研究发现,在伊沙匹隆的原料中,还含有usp43检测方法中未检测到的其它杂质,使用usp43提供的检测条件无法有效的分离检测出所有杂质,且该检测条件下杂质3会发生降解,无法有效检测。
[0007]
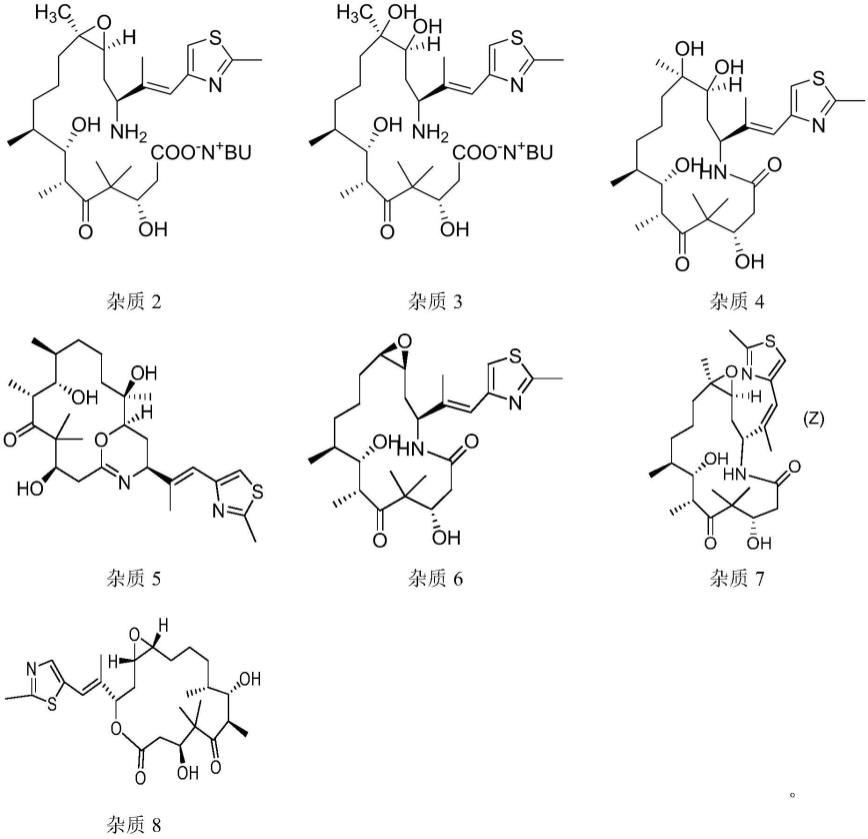
因此,为了严格控制伊沙匹隆药品质量,完整分析和检测杂质的组成及含量,对其杂质进行准确监测与控制,目前,对伊沙匹隆样品中有关物质的检测手段仍有待改进提高,各杂质结构如下所示:
[0008]
技术实现要素:
[0009]
针对目前尚无成熟可靠的分析检测伊沙匹隆有关物质的检测方法,本发明提供了一种伊沙匹隆有关物质的高效液相色谱检测方法,该方法具有操作简便、专属性强、分离度好、准确度高、分析结果重现性好等优点。
[0010]
本发明所采用的技术方案具体如下:
[0011]
一种伊沙匹隆有关物质的分析检测方法,具体使用高效液相色谱法,色谱条件为:色谱柱为c
18
色谱柱,以十八烷基硅烷键合硅胶填充柱,以缓冲盐溶液为流动相a,以乙腈或甲醇为流动相b,梯度洗脱。
[0012]
优选地,所述的c
18
色谱柱选自welch xb-c
18
、ultimate sx-c
18
或agilent zorbax sb-c
18
。
[0013]
优选地,所述的色谱柱规格为4.6
×
250mm,3μm。
[0014]
优选地,所述的流动相a与流动相b的体积比为20~90:80~10;优选流动相a与流动相b的体积比为35~75:65~25。
[0015]
优选地,所述的梯度洗脱的洗脱条件为:
[0016][0017]
进一步优选地,所述的洗脱条件为:
[0018][0019]
优选地,高效液相使用紫外线检测器检测,检测波长190~260nm。
[0020]
优选地,检测波长为245~255nm;优选为249nm。
[0021]
优选地,所述的缓冲盐为磷酸氢铵、磷酸氢二钠、磷酸氢二钾或磷酸氢二铵;优选为磷酸氢铵。
[0022]
优选地,所述的缓冲盐水溶液的浓度为0.002mol/l~0.2mol/l;优选为0.04~0.1mol/l。
[0023]
优选地,流动相的流速为0.8~1.2ml/min;优选为1.0ml/min。
[0024]
优选地,色谱柱温度为20~40℃;优选为25~30℃。
[0025]
优选地,进样量为10~30μl;优选为10μl。
[0026]
在一个优选的试验方案中,该检测方法包括如下步骤:
[0027]
(1)对照品溶液配制:
[0028]
有关物质对照品储备溶液:精密称取有关物质2~8对照品各2mg,分别置于10ml量瓶中,加乙腈超声溶解并用水稀释至刻度,摇匀,即得。
[0029]
对照品储备液:称取伊沙匹隆对照品10mg,置于10ml量瓶中,加溶剂超声溶解并用水稀释至刻度,摇匀,即得。
[0030]
(2)供试品溶液的配制:精密称取伊沙匹隆原料药10mg,置于10ml量瓶中,加溶剂超声溶解并用水稀释至刻度,摇匀,即得。
[0031]
(3)自身对照溶液:精密移取供试品溶液50μl,置于50ml量瓶中,加溶剂超声溶解并用水稀释至刻度,摇匀,即得。
[0032]
(4)系统适用性溶液:精密称取伊沙匹隆原料药置于10ml量瓶中,再分别精密移取有关物质对照品储备液各200μl至同一量瓶中,再加溶剂超声溶解并用水稀释至刻度,摇
匀,即得。
[0033]
(5)采用高效液相色谱仪分析制得的待测样品,其色谱条件为:色谱柱welch xb-c
18
,4.6mm
×
250mm,3μm,以十八烷基硅烷键合硅胶填充柱;进样量为10μl~30μl;检测波长,245~255nm;柱温,20~40℃;流速,0.8~1.2ml/min;以磷酸氢胺溶液为流动相a,以乙腈或甲醇为流动相b;依照如下洗脱条件进行梯度洗脱:
[0034][0035]
进一步优选地,依照如下条件进行梯度洗脱:
[0036][0037]
记录色谱图,由对照品溶液中各杂质的保留时间定性,以面积归一化法计算各杂质的含量。
[0038]
优选地,所述方法中,配制溶液使用的溶剂为:乙腈-水或甲醇-水;优选地,乙腈或甲醇与水的体积比为20:80。
[0039]
与现有技术相比,本发明取得的技术效果为:
[0040]
本发明的检测方法,能够快速有效检测伊沙匹隆有关物质,且各杂质间分离度较佳,系统适用性良好,线性关系良好,精密度高,准确度良好,重复性好。使用本发明提供的检测条件,可以有效解决杂质3的降解及检测基线上移的问题。有效的将主峰与各杂质峰分离,提供了高效、可行的伊沙匹隆中有关物质的分析检测方法。
附图说明
[0041]
图1:空白溶剂图谱;
[0042]
图2:杂质2定位图谱;
[0043]
图3:杂质3定位图谱;
[0044]
图4:杂质4定位图谱;
[0045]
图5:杂质5定位图谱;
[0046]
图6:杂质6定位图谱;
[0047]
图7:杂质7定位图谱;
[0048]
图8:杂质8定位图谱;
[0049]
图9:实施例1系统适用性图谱;
[0050]
图10:实施例1供试品图谱;
[0051]
图11:实施例2供试品图谱;
[0052]
图12:实施例3供试品图谱;
[0053]
图13:实施例4系统适用性图谱;
[0054]
图14:对比例1系统适用性图谱。
具体实施方式
[0055]
为了使本发明的目的、技术方案更加清楚明白,以下结合实施例,对本发明做进一步的说明,但是本发明的保护范围并不限于这些实施例,实施例仅用于解释本发明。
[0056]
本发明具体实施例使用的伊沙匹隆杂质2至杂质8来源于:山东新时代药业有限公司;伊沙匹隆原料药来源于:山东新时代药业有限公司,批号650180502。凡是不背离本发明构思的改变或等同替代均包括在本发明的保护范围之内。
[0057]
实施例1
[0058]
(1)溶液的配制
[0059]
①
有关物质对照品储备溶液:精密称取1(原料药)的有关物质2~8对照品各2mg,分别置于10ml容量瓶中,加乙腈超声溶解并稀释至刻度,摇匀,即得。
[0060]
②
1对照品储备液:称取1对照品10mg,置于10ml量瓶中,加溶剂超声溶解并稀释至刻度,摇匀,即得。
[0061]
③
供试品溶液:精密称取1原料药10mg,置于10ml量瓶中,加溶剂超声溶解并稀释至刻度,摇匀,即得。
[0062]
④
自身对照溶液:精密移取供试品溶液50μl,置于50ml量瓶中,加溶剂超声溶解并稀释至刻度,摇匀,即得。
[0063]
⑤
系统适用性溶液:精密称取1原料药置于10ml量瓶中,再分别精密移取有关物质对照品储备液各200ul至同一量瓶中,再加溶剂超声溶解并稀释至刻度,摇匀,即得。
[0064]
(2)色谱系统检测
[0065]
将上述供试品溶液、自身对照溶液、系统适用性溶液分别注入色谱仪检测,按加校正因子的自身对照法计算供试品的纯度。检测条件如下:
[0066]
色谱柱:welch xb-c
18
,4.6
×
250mm,3μm;
[0067]
色谱柱温度:25℃;
[0068]
流动相流速:1.0ml/min;
[0069]
检测波长:249nm;
[0070]
进样量:10μl。
[0071]
流动相:以0.04mol/l磷酸氢铵溶液为流动相a,以甲醇为流动相b,采用如下梯度洗脱:
[0072][0073]
系统适用性试验:混合对照溶液图谱中伊沙匹隆峰形好;理论板数不低于5000。如图9所示,混合杂质溶液出峰顺序依次为杂质2、3、4、5、6、主峰、7、8,各峰的峰形较好,与图2至图8所示的定位相一致,各峰的分离度不小于1.5。同样检测条件在供试品溶液中可准确检测各杂质,如图10所示。
[0074]
实施例2
[0075]
(1)溶液的配制
[0076]
溶液的配制同实施例1。
[0077]
(2)色谱系统检测
[0078]
将上述供试品溶液、自身对照溶液、系统适用性溶液分别注入色谱仪检测,按加校正因子的自身对照法计算供试品的纯度。检测条件如下:
[0079]
色谱柱:welch xb-c
18
,4.6
×
250mm,3μm;
[0080]
色谱柱温度:25℃;
[0081]
流动相流速:1.0ml/min;
[0082]
检测波长:249nm;
[0083]
进样量:10μl。
[0084]
流动相:以0.06mol/l磷酸氢铵溶液为流动相a,以甲醇为流动相b,采用如下梯度洗脱:
[0085][0086]
系统适用性试验:混合对照溶液图谱中伊沙匹隆峰形好;各已知杂质峰分离度不小于1.5。同样检测条件在供试品溶液中可准确检测各杂质,如图11所示。
[0087]
实施例3
[0088]
(1)溶液的配制
[0089]
溶液的配制同实施例1。
[0090]
(2)色谱系统检测
[0091]
将上述供试品溶液、自身对照溶液、系统适用性溶液分别注入色谱仪检测,按加校正因子的自身对照法计算供试品的纯度。检测条件如下:
[0092]
色谱柱:welch xb-c
18
,4.6
×
250mm,3μm;
[0093]
色谱柱温度:25℃;
[0094]
流动相流速:1.0ml/min;
[0095]
检测波长:249nm;
[0096]
进样量:10μl。
[0097]
流动相:以0.10mol/l磷酸氢二铵溶液为流动相a,以甲醇为流动相b,采用如下梯度洗脱:
[0098][0099]
系统适用性试验:混合对照溶液图谱中伊沙匹隆峰形好;各已知杂质峰分离度不小于1.5。同样检测条件在供试验品溶液中可准确检测各杂质,如图12所示。
[0100]
实施例4
[0101]
(1)溶液的配制
[0102]
溶液的配制同实施例1。
[0103]
(2)色谱系统检测
[0104]
将上述供试品溶液、自身对照溶液、系统适用性溶液分别注入色谱仪检测,按加校正因子的自身对照法计算供试品的纯度。检测条件如下:
[0105]
色谱柱:welch xb-c
18
,4.6
×
250mm,3μm;
[0106]
色谱柱温度:25℃;
[0107]
流动相流速:1.0ml/min;
[0108]
检测波长:249nm;
[0109]
进样量:10μl。
[0110]
流动相:以0.04mol/l磷酸氢铵溶液为流动相a,以甲醇为流动相b,采用如下梯度洗脱:
[0111]
[0112][0113]
系统适用性试验:混合对照溶液图谱中伊沙匹隆峰形好;各已知杂质峰峰型较好,但是杂质3和杂质4特征峰分离不理想,具体如附图13所示。
[0114]
实施例5
[0115]
(1)溶液的配制
[0116]
溶液的配制同实施例1。
[0117]
(2)色谱系统检测
[0118]
将上述供试品溶液、自身对照溶液、系统适用性溶液分别注入色谱仪检测,按加校正因子的自身对照法计算供试品的纯度。检测条件如下:
[0119]
色谱柱:welch xb-c
18
,4.6
×
250mm,3μm;
[0120]
色谱柱温度:25℃;
[0121]
流动相流速:1.0ml/min;
[0122]
检测波长:249nm;
[0123]
进样量:10μl。
[0124]
流动相:以0.04mol/l磷酸氢铵溶液为流动相a,以甲醇为流动相b,采用如下梯度洗脱:
[0125][0126]
系统适用性试验:混合对照溶液图谱中伊沙匹隆峰形好,但出峰较慢,出峰时间较晚。
[0127]
实施例6
[0128]
(1)溶液的配制
[0129]
溶液的配制同实施例1。
[0130]
(2)色谱系统检测
[0131]
将上述供试品溶液、自身对照溶液、系统适用性溶液分别注入色谱仪检测,按加校正因子的自身对照法计算供试品的纯度。检测条件如下:
[0132]
色谱柱:welch xb-c
18
,4.6
×
250mm,3μm;
[0133]
色谱柱温度:30℃;
[0134]
流动相流速:0.8ml/min;
[0135]
检测波长:249nm;
[0136]
进样量:10μl。
[0137]
流动相:以0.10mol/l磷酸氢二钠溶液为流动相a,以乙腈为流动相b,采用如下梯度洗脱:
[0138][0139]
系统适用性试验:混合对照溶液图谱中伊沙匹隆与各已知杂质峰分离度稍差,不能完好分离。
[0140]
实施例7
[0141]
(1)溶液的配制
[0142]
溶液的配制同实施例1。
[0143]
(2)色谱系统检测
[0144]
将上述供试品溶液、自身对照溶液、系统适用性溶液分别注入色谱仪检测,按加校正因子的自身对照法计算供试品的纯度。检测条件如下:
[0145]
色谱柱:welch xb-c
18
,4.6
×
250mm,3μm;
[0146]
色谱柱温度:20℃;
[0147]
流动相流速:1.2ml/min;
[0148]
检测波长:249nm;
[0149]
进样量:30μl。
[0150]
流动相:以0.10mol/l磷酸氢二钾溶液为流动相a,以甲醇为流动相b,采用如下梯度洗脱:
[0151]
[0152]
系统适用性试验:混合对照溶液图谱中伊沙匹隆与各已知杂质峰分离度稍差,不能完好分离。
[0153]
实施例8
[0154]
(1)溶液的配制
[0155]
溶液的配制同实施例1。
[0156]
(2)色谱系统检测
[0157]
将上述供试品溶液、自身对照溶液、系统适用性溶液分别注入色谱仪检测,按加校正因子的自身对照法计算供试品的纯度。检测条件如下:
[0158]
色谱柱:welch xb-c
18
,4.6
×
250mm,3μm;
[0159]
色谱柱温度:25℃;
[0160]
流动相流速:1.0ml/min;
[0161]
检测波长:249nm;
[0162]
进样量:10μl。
[0163]
流动相:以0.04mol/l磷酸氢铵溶液为流动相a,以甲醇为流动相b,采用如下梯度洗脱:
[0164][0165]
系统适用性试验:混合对照溶液图谱中伊沙匹隆与各已知杂质峰分离度稍差,不能完好分离。
[0166]
实施例9
[0167]
(1)溶液的配制
[0168]
溶液的配制同实施例1。
[0169]
(2)色谱系统检测
[0170]
将上述供试品溶液、自身对照溶液、系统适用性溶液分别注入色谱仪检测,按加校正因子的自身对照法计算供试品的纯度。检测条件如下:
[0171]
色谱柱:welch xb-c
18
,4.6
×
250mm,3μm;
[0172]
色谱柱温度:25℃;
[0173]
流动相流速:1.0ml/min;
[0174]
检测波长:249nm;
[0175]
进样量:10μl。
[0176]
流动相:以0.04mol/l磷酸氢铵溶液为流动相a,以甲醇为流动相b,采用如下梯度洗脱:
[0177][0178]
系统适用性试验:混合对照溶液图谱中伊沙匹隆与各已知杂质峰分离度稍差,不能完好分离。
[0179]
实施例10洗脱液
[0180]
(1)溶液的配制
[0181]
溶液的配制同实施例1。
[0182]
(2)色谱系统检测
[0183]
将上述供试品溶液、自身对照溶液、系统适用性溶液分别注入色谱仪检测,按加校正因子的自身对照法计算供试品的纯度。检测条件如下:
[0184]
色谱柱:welch xb-c
18
,4.6
×
250mm,3μm;
[0185]
色谱柱温度:25℃;
[0186]
流动相流速:1.0ml/min;
[0187]
检测波长:249nm;
[0188]
进样量:10μl。
[0189]
流动相:流动相a为0.04mol/l乙酸铵水溶液;流动相b为乙腈,采用如下梯度洗脱:
[0190][0191]
系统适用性试验:混合对照溶液图谱中伊沙匹隆与各已知杂质峰分离度较差,不能有效分离,部分杂质不能有效检出。
[0192]
对比实施例1
[0193]
(1)溶液的配制
[0194]
溶液的配制同实施例1。
[0195]
(2)色谱系统检测
[0196]
将上述供试品溶液、自身对照溶液、系统适用性溶液分别注入色谱仪检测,按加校正因子的自身对照法计算供试品的纯度。检测条件按照伊沙匹隆usp标准方法,具体如下:
[0197]
色谱柱:welch xb-c
18
,4.6
×
250mm,3μm;
[0198]
色谱柱温度:25℃;
[0199]
流动相流速:1.0ml/min;
[0200]
检测波长:249nm;
[0201]
进样量:10μl。
[0202]
流动相:流动相a为乙腈/缓冲盐=10:90;流动相b为乙腈/缓冲盐=90:10;缓冲盐为的三羟甲基氨基甲烷(5mm);采用如下梯度洗脱:
[0203][0204]
系统适用性试验:混合对照溶液图谱中伊沙匹隆与各已知杂质峰分离度较差,不能完好分离,不能有效检测出所有杂质;比如杂质3在检测过程中发生了降解,无法检测,且峰型较差,具体如附图14所示。
[0205]
验证实施例
[0206]
系统适用性试验
[0207]
取供试品溶液作为系统适用性溶液,连续测定6次,按照实施例1的色谱条件进行测定,记录色谱图,分别计算6次进样伊沙匹隆主峰保留时间和峰面积的平均值、相对标准偏差。测定结果见表1。
[0208]
表1.系统适用性试验结果
[0209][0210]
由表1可知,伊沙匹隆主峰保留时间平均值为15.070min,rsd为0.19%,峰面积平均值为218.309,rsd为0.18%,符合要求,仪器系统适用性良好。
[0211]
检测限与定量限
[0212]
精密量取杂质2~8储备溶液及伊沙匹隆对照品储备液,加溶剂采用逐步稀释法,得不同浓度的混合溶液;以信噪比s/n≈10时的浓度作为定量限浓度,以信噪比s/n≈3时的浓度作为检测限浓度。
[0213]
定量限重复性试验:1份定量限溶液,按照实施例1的色谱条件进行测定,连续进样6次,记录色谱图,计算各杂质及伊沙匹隆保留时间及峰面积的相对标准偏差。
[0214]
检测限重复性试验:1份检测限溶液,按照实施例1的色谱条件进行测定,连续进样3次,记录色谱图。
[0215]
通过计算可知,定量限重复性项下各杂质及伊沙匹隆的定量限与检测限均符合测定要求,具体如下表2:
[0216]
表2各组分保留时间和峰面积rsd
[0217] 保留时间峰面积rsd%杂质25.6512.8杂质36.0183.2杂质46.2681.8杂质57.6544.3杂质612.7893.9伊沙匹隆15.3892.7杂质716.1053.9杂质822.8561.7
[0218]
线性与检测范围测定
[0219]
按照“定量限与检测限”试验项下定量限溶液配制方法,分别精密量取“定量限与检测限”试验项下杂质2~8储备溶液及伊沙匹隆对照品储备溶液,逐级稀释,作为线性溶液1。
[0220]
分别精密量取“定量限与检测限”试验项下杂质2~8储备溶液及伊沙匹隆对照品储备溶液各约1ml,置同一50ml量瓶中,加溶剂稀释至刻度,摇匀,作为线性混合储备液。精密量取线性混合储备液0.5ml,置于10ml量瓶中,加水稀释至刻度,摇匀,作为100%线性溶液。同法分别配制10%、20%、40%、80%、100%、200%浓度的溶液,作为线性溶液2~7,取线性溶液1~线性溶液7,按照实施例1的色谱条件进行测定,记录色谱图,以浓度(x,μg/ml)为横坐标,峰面积(y,mau)为纵坐标,绘制标准曲线,并计算校正因子。
[0221]
杂质2线性方程为:y=0.518x+0.0138(r2=0.996);
[0222]
杂质3线性方程为:y=0.153x+0.0278(r2=0.997);
[0223]
杂质4线性方程为:y=0.134x+0.0188(r2=0.998);
[0224]
杂质5线性方程为:y=0.165x+0.0192(r2=0.998);
[0225]
杂质6线性方程为:y=0.110x+0.0132(r2=0.996);
[0226]
杂质7线性方程为:y=0.054x+0.0035(r2=0.994);
[0227]
杂质8线性方程为:y=0.156x+0.0138(r2=0.994);
[0228]
伊沙匹隆线性方程为:y=0.168x+0.0165(r2=0.998)。
[0229]
通过试验结果可知:
[0230]
杂质2在0.08~2.26μg/ml浓度范围内呈线性关系,相关系数r=0.998,线性关系
良好;
[0231]
杂质3在0.05~2.18μg/ml浓度范围内呈线性关系,相关系数r=0.998,线性关系良好;
[0232]
杂质4在0.10~2.09μg/ml浓度范围内呈线性关系,相关系数r=0.999,线性关系良好;
[0233]
杂质5在0.13~1.98μg/ml浓度范围内呈线性关系,相关系数r=0.999,线性关系良好;
[0234]
杂质6在0.11~1.96μg/ml浓度范围内呈线性关系,相关系数r=0.998,线性关系良好;
[0235]
杂质7在0.11~2.08μg/ml浓度范围内呈线性关系,相关系数r=0.997,线性关系良好;
[0236]
杂质8在0.31~2.11μg/ml浓度范围内呈线性关系,相关系数r=0.997,线性关系良好;
[0237]
伊沙匹隆在0.08~2.28μg/ml浓度范围内呈线性关系,相关系数r=0.999,线性关系良好。
[0238]
杂质的校正因子如下表3。
[0239]
表3各杂质校正因子
[0240]
名称校正因子杂质20.32杂质31.10杂质41.25杂质51.02杂质61.53伊沙匹隆—杂质73.11杂质81.08
[0241]
准确度试验
[0242]
(1)对照溶液1:精密量取“定量限与检测限”试验项下杂质2至杂质8储备溶液各50μl,置同一50ml量瓶中,加溶剂稀释至刻度,摇匀,即得。
[0243]
(2)对照溶液2:精密量取“定量限与检测限”试验项下杂质2至杂质8储备溶液各50μl,置同一50ml量瓶中,加溶剂稀释至刻度,摇匀,即得。
[0244]
(3)供试品溶液:精密称取原料药10.18mg,置20ml量瓶中,加溶剂溶解并稀释至刻度,摇匀,即得。
[0245]
(4)准确度溶液:精密称取原料药20.28mg,置于20ml量瓶中,精密量取各杂质储备液10μl,加溶剂稀释至刻度,摇匀,作为50%加标回收率溶液。同法分别配制100%、150%浓度的溶液,每个浓度平行配制3份。
[0246]
分别精密量取上述各对照溶液、供试品溶液及各准确度溶液10μl,按照实施例1的色谱条件进行测定,记录色谱图,按外标法计算各准确度溶液中各杂质的回收率及相对标准偏差。
[0247]
由结果知,各杂质回收率均在90%~110%之间,且9个回收率数据的rsd均小于2%,本法准确度较高。
[0248]
重复性试验
[0249]
取“准确度”试验项下对照溶液1,2作为重复性-对照溶液1,2。
[0250]
取原料药20mg,精密称定,置20ml量瓶中,加适量溶剂溶解,分别加入10μl各杂质储备溶液,溶剂稀释至刻度,摇匀,作为重复性溶液,平行配制6份,按照实施例1的色谱条件进行测定,记录色谱图。外标法计算各杂质含量、平均值及相对标准偏差,结果见表4。
[0251]
表4重复性试验结果
[0252][0253]
由结果知,6份重复性溶液各杂质含量的rsd均小于10%,本法重复性较好。
[0254]
本发明通过c
18
色谱柱,利用高效液相色谱仪能够快速准确检测伊沙匹隆中的有关物质,准确度高,重复性和耐用性好,分离度高,适用性强,填补了利用液相色谱仪检测伊沙匹隆有关物质的空白。
[0255]
本发明所述的一种利用高效液相色谱法检测伊沙匹隆原料中有关物质的检测方法,可以有效地检测伊沙匹隆中有关物质的含量,而且该方法分离度高,重复性及耐用性好,检测限低,专属性强,操作简单,结果稳定可靠,从而可用于伊沙匹隆原料的质量控制,为最终成品的质量提供有效保障。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1