一种用于检测滑液囊支原体的间接ELISA试剂盒及其检测方法与流程
一种用于检测滑液囊支原体的间接elisa试剂盒及其检测方法
技术领域
1.本发明申请型涉及生物工程技术领域,具体涉及一种用于检测滑液囊支原体的间接elisa试剂盒及其检测方法。
背景技术:
2.滑液囊支原体(mycoplasma synoviae,ms)一直被认为是家禽养殖中重要的禽支原体。滑液囊支原体在自然条件下仅感染鸡与火鸡,但是如果通过人工感染,则可使得鸭、鹅等其他家禽发病。ms感染会导致家禽发生上呼吸道炎症,滑膜炎,胴体质量下降,产蛋率下降,以及鸡的蛋壳顶端异常(eggshell apex abnormalities,eaa)。大多数情况下,滑液囊支原体的感染局限于气囊,而在混合感染或继发感染时,滑液囊支原体将在全身扩散,影响关节和肌腱的滑膜,进而导致急性或慢性感染性滑膜炎。患有感染性滑膜炎的鸡会出现跛足,生长迟缓,关节及腱鞘中通常含有粘稠的奶油状渗出物,以及肝脾肿大和斑驳肿胀的肾脏,同时其腱鞘滑膜中还存在广泛的炎性细胞浸润。
3.滑液囊支原体的诊断通常分为三种:支原体的分离鉴定、分子生物学诊断以及血清学诊断。支原体的分离鉴定一直都是滑液囊支原体诊断的金标准。滑液囊支原体的分离培养通常选用改良frey氏培养基,无菌采集患病家禽的咽拭子与关节渗出液进行培养接种培养,其中关节渗出液的分离概率最大。但是由于家禽处于非急性感染期时体内的滑液囊支原体含量较少难以分离,且滑液囊支原体培养要求较高,培养周期较长,通常需要5-7天才能达到对数生长期,因此滑液囊支原体的分离培养较为耗费时间与成本。分子生物学诊断方法主要为pcr与qpcr,这两种方法均可以快速准确的检测滑液囊支原体,但其需要专门的实验室设施与环境、熟练的操作人员,因此分子生物学诊断往往仅用于实验室诊断。而ms的血清学诊断方法主要有两种:血清平板凝集试验(spa)与酶联免疫吸附试验(elisa)。血清平板凝集试验具有操作简单,成本低,时间短等优点,但该方法特异性较低,易因血清冷冻或受到其他禽类支原体感染发生交叉反应而出现假阳性。而酶联免疫吸附试验因其可同时检测大量样品,特异性高、敏感性强,是目前滑液囊支原体血清学检测的首选方法,但目前商品化的elisa检测试剂盒价格昂贵,成本较高。
4.滑液囊支原体对各个年龄阶段的鸡均易感,雏鸡最易感染,但在养殖环境中,由于不能清除环境中ms的增长,导致随着鸡日龄的增加,滑液囊支原体的检出率业增加。且滑液囊支原体一年四季均可发病,而冬季多发。一般情况下滑液囊支原体常与其他病原体(如大肠杆菌、鸡毒支原体、传染性喉气管炎病毒、新城疫等)发生混合或继发感染。
5.目前根据国内学者对我国2019年至2021年的调查中显示:云南ms的阳性率为68.48%,且每一场户禽舍中均有检出ms;江苏盐城ms在调查的8个养殖场中就有7个检出ms血清阳性;在上海浦口的调查中,场户的阳性率亦达到85.45%;宁夏地区ms的血清阳性率达67.18%,其中种鸡的阳性率高达90.26%,最低的肉鸡血清阳性率亦是高达55.5%;北京地区场阳性率为88.4%,血清阳性率为77.1%。而据国外学者报道:在意大利,滑液囊支原
体的发病率为50.7%,血清阳性率为72.7%;在西班牙,滑液囊支原体的肉鸡血清阳性率为74%,蛋鸡为95%;在伊朗,滑液囊支原体的血清阳性率为72%;在法国,滑液囊支原体的场检出率为100%;在美国,滑液囊支原体的检出率达到73%。上述调查结果均表示滑液囊支原体在世界范围内内呈现流行趋势,对家禽养殖业造成巨大的损失。
6.dnak蛋白经证明其在滑液囊支原体中高度保守,且具有良好的免疫原性,大量分布于滑液囊支原体的膜表面。dnak蛋白又被称为热休克蛋白70(heat shock protein 70,hsp70),目前已有多篇报道证明病原体的dnak蛋白能够诱导机体产生免疫,改变宿主细胞周期,影响细胞凋亡,并能够作为亚单位疫苗的候选抗原。
7.随着滑液囊支原体在世界范围内的流行情况越发严重,对于滑液囊支原体诊断方法的研究也显得越发的重要。
技术实现要素:
8.为解决或部分解决相关技术中存在的问题,本发明申请提供一种用于检测滑液囊支原体的间接elisa试剂盒及其检测方法。
9.本发明申请第一方面提供了一种用于检测滑液囊支原体的间接elisa试剂盒,包括重组dnak蛋白,所述重组dnak蛋白的序列如seq id no:1所示。
10.进一步的,还包括酶标二抗、包被液、洗涤液、显色液、封闭液、稀释液、终止液中的一种或几种。
11.进一步的,所述包被液为索莱宝购置的elisa包被液,所述封闭液为含有5%bsa的pbst,所述洗涤液为pbst,所述显色液为tmb。
12.本发明申请第二方面提供了一种用于检测滑液囊支原体的间接elisa试剂盒的检测方法,包括以下步骤:
13.s1、将如seq id no:1所示的重组dnak蛋白包被20h后,使用pbst洗涤,再使用封闭液封闭2h后洗涤;
14.s2、将待检血清稀释至1:400后,于37℃孵育30min,将二抗稀释至1:250浓度在37℃温箱中进行孵育1.5h,孵育后洗涤3次,加入显色液于37℃反应0.5h后加入终止液,并通过酶标仪观察od450,判断阴阳性即可。
15.进一步的,所述检测方法具体为使用包被液将如seq id no:1所示的重组dnak蛋白以4ng/ml的浓度4℃包被20h,以pbst为洗涤液,洗涤3次后使用含有5%bsa的pbst作为封闭液,37℃封闭2h后,洗涤3次,将待检血清稀释至1:400后,于37℃孵育30min,洗涤3次后将二抗稀释至1:250浓度在37℃温箱中进行孵育1.5h,孵育后洗涤3次,加入tmb显色液于37℃反应0.5h后加入终止液,并通过酶标仪观察od450,若od450大于0.242188,则为阳性;反之则为阴性。
16.应当理解的是,以上的一般描述和后文的细节描述仅是示例性和解释性的,并不能限制本发明申请。
17.本发明的有益技术效果:
18.本发明通过原核表达滑液囊支原体的dnak蛋白主要抗原表位,并以纯化的dnak蛋白作为包被抗原建立检测滑液囊支原体抗体的ielisa方法,提供了一种简单方便,可准确、高灵敏度的elisa试剂盒。
附图说明
19.图1为本发明申请中dnak蛋白的基因分析;
20.图2为本发明申请中重组dnak蛋白的western bolt鉴定;
21.图3为本发明申请中重组dnak蛋白的肽段的二级质谱图;
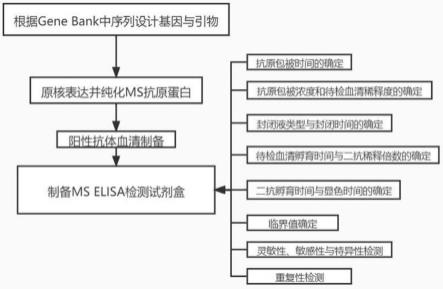
22.图4为本发明申请中一种实施方法的流程图;
具体实施方式
23.下面将参照附图更详细地描述本发明申请的可选实施方式。虽然附图中显示了本发明申请的可选实施方式,然而应该理解,可以以各种形式实现本发明申请而不应被这里阐述的实施方式所限制。相反,提供这些实施方式是为了使本发明申请更加透彻和完整,并且能够将本发明申请的范围完整地传达给本领域的技术人员。
24.在本发明申请使用的术语是仅仅出于描述特定实施例的目的,而非旨在限制本发明申请。在本发明申请和所附权利要求书中所使用的单数形式的“一种”、“所述”和“该”也旨在包括多数形式,除非上下文清楚地表示其他含义。还应当理解,本文中使用的术语“和/或”是指并包含一个或多个相关联的列出项目的任何或所有可能组合。
25.以下结合附图对本发明申请用于检测滑液囊支原体的间接elisa试剂盒及其检测方法,具体如下:
26.本发明申请提供了一种用于检测滑液囊支原体的间接elisa试剂盒,包括重组dnak蛋白,所述重组dnak蛋白的序列如seq id no:1所示。本发明的重组dnak蛋白根据ncbi网站所公布的ms wvu1853株dnak基因序列(genbank登录号:wp_020003200.1)通过抗原决定簇预测工具(http://www.detaibio.com/tools/epitope-prediction.html)与ncbi的blast系统进行分析,根据分析结果选定抗原决定簇密集且保守性较高的240aa-415aa区间使用大肠杆菌偏爱的密码子系统优化。
27.并根据上述密码子优化序列设计鉴定引物:上游鉴定引物rdnakf-tcggatccgctaaaatcgacctttcaaacca;下游鉴定引物rdnakr-acgcgtcgacttcaccttggataac。
28.在本发明申请的一种实施方式中,还包括酶标二抗、包被液、洗涤液、显色液、封闭液、稀释液、终止液中的一种或几种。
29.在本发明申请的一种实施方式中,所述包被液为索莱宝购置的elisa包被液,所述封闭液为含有5%bsa的pbst,所述洗涤液为pbst,所述显色液为tmb。
30.s1、将如seq id no:1所示的重组dnak蛋白包被20h后,使用pbst洗涤,再使用封闭液封闭2h后洗涤;
31.s2、将待检血清稀释至1:400后,于37℃孵育30min,将二抗稀释至1:250浓度在37℃温箱中进行孵育1.5h,孵育后洗涤3次,加入显色液于37℃反应0.5h后加入终止液,并通过酶标仪观察od450,判断阴阳性即可。
32.在本发明申请的一种实施方式中,所述检测方法具体为使用包被液将如seq id no:1所示的重组dnak蛋白以4ng/ml的浓度4℃包被20h,以pbst为洗涤液,洗涤3次后使用含有5%bsa的pbst作为封闭液,37℃封闭2h后,洗涤3次,将待检血清稀释至1:400后,于37℃孵育30min,洗涤3次后将二抗稀释至1:250浓度在37℃温箱中进行孵育1.5h,孵育后洗涤3次,加入tmb显色液于37℃反应0.5h后加入终止液,并通过酶标仪观察od450,若od450大于
0.242188,则为阳性;反之则为阴性。
33.为更清楚起见,下面通过以下试验例进行详细说明。
34.试验例1抗原最佳包被时间的确定
35.使用elisa包被液将纯化后的dnak蛋白稀释至8ng/ml,在酶标板上每孔加入100μl使用elisa包被液稀释后的rdnak蛋白,使用保鲜膜密封,4℃包被20h、16h、12h。包被时间结束后弃去包被液,并在每孔中加入200μl的pbst进行洗涤,洗涤4次后每孔加入200μl含有5%bsa的pbst后用保鲜膜密封,于37℃封闭2h。重复洗涤4次。将自制小鼠多抗血清作为阳性血清,小鼠抗pbs血清作为阴性血清,每份血清样品均重复4次,使用抗体稀释液将阴/阳性血清均稀释至1:200浓度后,在每孔中加入100μl稀释后的阴/阳性血清后使用保鲜膜进行密封,并置于37℃恒温培养箱中孵育1h。待孵育完成后,使用pbst对该elisa板进行洗涤,洗涤4次后于每孔中加入100μl hrp标记的山羊抗小鼠igg作为二抗进行孵育。待elisa板在37℃下孵育二抗1h后,使用pbst洗涤4次。洗涤后于elisa板的每孔中加入tmb显色液100μl,于37℃恒温培养箱中避光孵育10min,后加入50μl的elisa终止液。加入终止液后,使用酶标仪在450nm处测定elisa板的吸光度,根据p/n值(=阳性od450/阴性od450)确定抗原最佳包被时间。
36.表1elisa包被时间的确定
[0037][0038]
试验例2抗原最佳包被浓度和待检血清最佳抗体稀释度的确定使用elisa包被液将纯化后的rdnak蛋白稀释至8μg/ml、4μg/ml、2μg/ml、1μg/ml,每孔分别加入100ul稀释后不同浓度的抗原,根据3.4.1确定的最佳抗原包被时间,即每个孔包被的抗原总量依次为800ng、400ng、200ng、100ng,根据1.8.1筛选出的抗原包被时间在4℃进行包被,其余步骤按照3.4.1方法进行,通过方阵滴定法筛选出抗原最佳包被浓度和待检血清最佳抗体稀释度。
[0039]
表2elisa包被浓度及待检血清稀释度的确定
[0040][0041]
试验例3最佳封闭液类型与封闭时间的确定
[0042]
使用前面所筛选出的条件包被酶标板,后分别使用pbst/含有5%脱脂奶粉的pbst/含有5%bsa的pbst/含有10%胎牛血清的pbst进行封闭,每类封闭液的封闭时间均分别在37℃温箱中包被0.5h,1h,1.5h,2h。按照3.4.2筛选出的待检血清最佳抗体稀释度进行抗体血清稀释与孵育。其余步骤按照3.4.1方法进行,筛选出最佳封闭液类型与最佳封闭时间
[0043]
表3elisa封闭液类型及封闭时间的确定
[0044][0045]
试验例4最佳待检血清孵育时间与二抗稀释倍数的确定使用上述实验筛选出的条件进行抗原的包被、封闭与一抗血清的稀释,将一抗血清分别孵育0.5h,1h,1.5h,2h。将hrp标记的羊抗鼠igg作为二抗,使用抗体稀释液将其依次稀释为1:250,1:500,1:1000,1:2000浓度进行孵育,其余步骤均按照3.4.1方法进行,筛选出最佳待检血清孵育时间与二抗稀释倍数。
[0046]
表4elisa待检血清孵育时间及二抗稀释倍数的确定
[0047][0048]
试验例5最佳二抗孵育时间与显色时间的确定
[0049]
使用上述实验确认的条件进行elisa的包被、封闭、一抗血清的孵育与二抗血清的稀释。将二抗分别孵育0.5h,1h,1.5h,2h后,每孔均加入100μl的tmb显色液进行显色反应。显色反应的时间亦设置为3个时间点,分别是10min,20min,30min。在显色时间结束时加入终止液后,通过酶标仪进行数据分析,确认二抗最佳孵育时间与显色时间。
[0050]
表5elisa二抗孵育时间及显示时间的确定
[0051][0052]
试验例6临界值的确定
[0053]
取44份阴性血清,使用经上述试验优化后的elisa反应条件进行试验。计算出44份阴性血清的吸光度平均值与标准差(sd),根据公式判断阳性、阴性临界值
[0054]
表6elisa临界值的确定
[0055][0056]
试验例7灵敏性、特异性与敏感性检测
[0057]
使用抗体稀释液将阴性血清与阳性血清均进行1:100浓度稀释,后倍比稀释至1:204800,使用上述试验确定的elisa反应条件对每个浓度的血清均进行检测,以确定该elisa方法的灵敏性。同时随机选取36份阳性血清与阴性血清,使用上述方法进行检测,计算该elisa方法的敏感性与特异性。
[0058]
表7elisa灵敏性的检测
[0059][0060]
表8elisa敏感性与特异性
[0061][0062]
试验例8重复性检测
[0063]
将同一批次诱导表达并纯化的rdnak蛋白作为抗原进行包被,使用上述试验确定的elisa方法检测5份不同的血清,每份血清做3个重复,使用酶标仪测定od450,计算变异系数(cv),用此变异系数来确定批内试验的重复性。
[0064]
将不同批次纯化的3份rdnak蛋白作为抗原进行包被,使用上述试验确定的elisa方法检测5份不同的血清,每份血清做3个重复,按照上述方法计算变异系数,确定批间试验的重复性。
[0065]
表9elisa批内重复性的检测
[0066][0067]
表10elisa批间重复性的检测
[0068][0069]
以上已经描述了本发明申请的各实施例,上述说明是示例性的,并非穷尽性的,并且也不限于所披露的各实施例。在不偏离所说明的各实施例的范围和精神的情况下,对于本技术领域的普通技术人员来说许多修改和变更都是显而易见的。本文中所用术语的选择,旨在最好地解释各实施例的原理、实际应用或对市场中的技术的改进,或者使本技术领域的其它普通技术人员能理解本文披露的各实施例。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1