一种法莫替丁注射液中维生素C含量检测方法与流程
一种法莫替丁注射液中维生素c含量检测方法
技术领域
1.本发明涉及药品检测领域,具体涉及一种法莫替丁注射液中维生素c含量检测方法。
背景技术:
2.法莫替丁注射液属于抑制胃酸分泌药,有效成分法莫替丁是组胺h2受体阻滞药,对胃酸有明显的抑制作用,可以抑制胃蛋白酶分泌,对实验性胃溃疡有保护作用,因此,对于胃酸所致的胃炎以及相关的溃疡都有治疗作用。
3.法莫替丁注射液中的主药法莫替丁属氧敏感物质,易被氧化,通过加入另一种易感物质维生素c,可与法莫替丁竞争氧气,从而起到保护药物活性成分法莫替丁的作用。但由于维生素c在法莫替丁注射液中不稳定,也难被有效分离,故对加入维生素c的法莫替丁注射液的质量不易控制。
技术实现要素:
4.为解决上述问题,本发明提供了一种法莫替丁注射液中维生素c含量检测方法,它包括以下步骤:
5.a、对照品溶液的制备:取维生素c对照品,加溶剂溶解,即得;
6.b、供试品溶液的制备:取法莫替丁注射液,加溶剂稀释3~5倍,即得;
7.c、分别吸取对照品溶液和法莫替丁注射液注入液相色谱仪,色谱条件如下:
8.色谱柱:以十八烷基硅烷键合硅胶为填充剂;流动相:以磷酸二氢钾溶液为流动相a,以乙腈水溶液为流动相b;进样器温度:4℃;
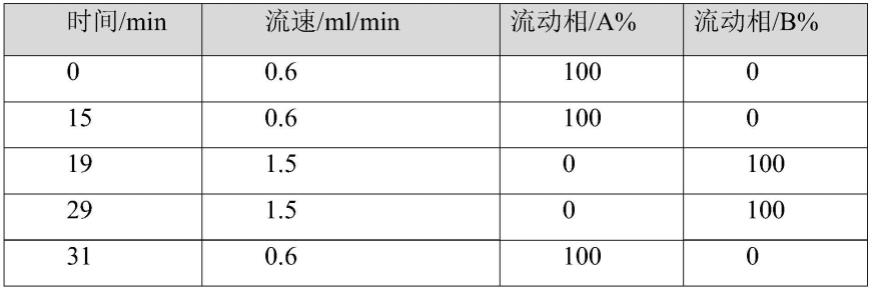
9.梯度洗脱程序为:
[0010][0011][0012]
d、按如下公式计算维生素c含量:
[0013][0014]
其中:a
供
:供试品溶液中主峰峰面积;v
供
:供试品溶液稀释倍数;标示装量:法莫替
丁注射液的体积;标示量:法莫替丁注射液中法莫替丁含量;多个对照品溶液的质量浓度与峰面积比值的平均值;
[0015]
所述溶剂为含乙二胺四乙酸二钠和磷酸二氢钾的水溶液;
[0016]
进一步地,步骤a所述维生素c对照品与溶剂的质量体积比为5mg:20ml。
[0017]
进一步地,步骤b所述法莫替丁注射液与溶剂的体积比为2.5ml:10ml。
[0018]
进一步地,步骤c所述色谱条件中色谱柱为gl inertsustain c18,250
×
4.6mm、5μm,波长200~250nm,柱温25~40℃,进样器温度4℃,进样量5~25μl。
[0019]
更进一步地,所述柱温30℃,波长210nm,进样量5μl。
[0020]
进一步地,所述溶剂为ph值2.0~4.0每1ml含0.3~0.67mg乙二胺四乙酸二钠和1.0~3.0mg磷酸二氢钾的水溶液。
[0021]
更进一步地,所述溶剂为ph值3.0每1ml含0.56mg乙二胺四乙酸二钠和2.0mg磷酸二氢钾的水溶液。
[0022]
进一步地,所述流动相a为1~5mg/ml磷酸二氢钾溶液;所述流动相b为70~80%,ml/ml乙腈水溶液。
[0023]
更进一步地,所述流动相a为2.04mg/ml磷酸二氢钾溶液;所述流动相b为73%,ml/ml乙腈水溶液。
[0024]
进一步地,步骤d所述为两个对照品溶液的质量浓度与峰面积比值的平均值,具体公式为:
[0025][0026][0027]
其中,a
对
:对照品溶液中主峰峰面积;m
对
:对照品重量,mg;v
对
:对照品溶液稀释倍数;p:对照品的含量。
[0028]
更进一步地,所述法莫替丁注射液的成分包括法莫替丁、烟酰胺、维生素c、d-甘露醇、乳酸、氢氧化钠和注射用水。
[0029]
经检测分析试验发现,组成成分中含维生素c的法莫替丁注射液,经高效液相色谱常温进样检测的准确性和精密度差,维生素c含量比实际添加量偏低2%~5%。本发明法莫替丁注射液中维生素c含量检测方法,通过特定的样品溶剂和色谱条件,可以检测法莫替丁注射液中维生素c,结果准确,快速、灵敏度高,为含维生素c的法莫替丁注射液的质量控制提供了新方法,也为法莫替丁注射液的质量控制标准的提高提供了方法依据,同时为扩大法莫替丁注射液的临床应用提供了参考依据,具有良好的应用前景。
[0030]
显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
[0031]
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
附图说明
[0032]
图1溶剂空白色谱图
[0033]
图2未降解空白辅料溶液色谱图
[0034]
图3未降解供试品溶液色谱图
[0035]
图4维生素对照品溶液色谱图
[0036]
图5强氧化降解空白辅料溶液色谱图
[0037]
图6强氧化降解供试品溶液色谱图
[0038]
图7强酸降解空白辅料溶液色谱图
[0039]
图8强酸降解供试品溶液色谱图
[0040]
图9强碱降解空白辅料溶液色谱图
[0041]
图10强碱降解供试品溶液色谱图
[0042]
图11高温降解空白辅料溶液色谱图
[0043]
图12高温降解供试品溶液色谱图
[0044]
图13强光降解空白辅料溶液色谱图
[0045]
图14强光降解供试品溶液色谱图
[0046]
图15维生素c线性图
具体实施方式
[0047]
实施例1法莫替丁注射液中维生素c含量测定
[0048]
a、对照品溶液的制备:取维生素c对照品5mg,精密称定,置20ml量瓶中,用ph值3.0每1ml含0.56mg乙二胺四乙酸二钠和2.0mg磷酸二氢钾的水溶液溶解并稀释至刻度,即得,平行配制2份对照品溶液。
[0049]
b、供试品溶液:精密量取法莫替丁注射液2.5ml,置10ml量瓶中,用ph值3.0每1ml含0.56mg乙二胺四乙酸二钠和2.0mg磷酸二氢钾的水溶液稀释至刻度,摇匀。
[0050]
c、分别吸取5μl对照品溶液和法莫替丁注射液注入液相色谱仪,记录色谱图,色谱条件如下:
[0051]
色谱柱:gl inertsustain c18,250
×
4.6mm、5μm;检测波长:210nm;柱温:30℃;流动相:以2.04mg/ml磷酸二氢钾溶液为流动相a,以73%乙腈水溶液为流动相b;进样器温度:4℃;梯度洗脱程序为:
[0052]
时间/min流速/ml/min流动相/a%流动相/b%00.61000150.61000191.50100291.50100310.61000380.61000
[0053]
d、按下式计算法莫替丁注射液的维生素c:
[0054][0055][0056][0057]
其中:a
对
:对照品溶液中主峰峰面积;m
对
:对照品重量,mg;
[0058]v对
:对照品溶液稀释倍数(20);p:对照品的含量;a
供
:供试品溶液中主峰峰面积;v
供
:供试品溶液稀释倍数(4);标示装量:法莫替丁注射液的体积;标示量:法莫替丁注射液中法莫替丁含量;
[0059]
以下通过试验例说明本发明的有益效果
[0060]
试验例1方法学研究
[0061]
1.用于验证的法莫替丁注射液
[0062]
法莫替丁注射液的处方(标示装量1ml)
[0063][0064]
法莫替丁注射液溶配工序:
[0065]
(1)主药及辅料溶解
[0066]
于500l浓配罐中加入注射用水,开启氮气,充氮至配液罐顶空残氧量<2.0%,控制注射用水温度40~50℃,备用。
[0067]
量取40~50℃充氮后注射用水置于稀配罐中,设置搅拌频率为30
±
2hz并开启搅拌,开启氮气,充氮至配液罐顶空残氧量<2.0%。依次加入乳酸、烟酰胺、维生素c、甘露醇和法莫替丁(避光操作),再次充氮至配液罐顶空残氧量<2.0%,搅拌30min至溶液澄清,开启小循环5min。
[0068]
(2)调节ph
[0069]
称取充氮后注射用水置于不锈钢桶中,加入氢氧化钠,搅拌至完全溶解,再次充氮
5min,即得0.2m氢氧化钠溶液。于配制罐加入氢氧化钠溶液约,调节溶液ph为5.8~6.2。
[0070]
(3)定容
[0071]
用35℃以下充氮后注射用水定容至,循环搅拌5min。过程中持续向罐内充氮,保证配液罐顶空残氧量<2.0%。
[0072]
2.验证内容
[0073]
维生素c分析方法的专属性、系统精密度、溶液稳定性、线性与范围、准确度、精密度(重复性与中间精密度)、耐用性。
[0074]
3.验证可接受标准
[0075]
表1.验证可接受标准
[0076][0077][0078]
4.验证的实施步骤
[0079]
4.1.仪器配置
[0080]
表2.仪器配置
[0081][0082]
4.2.验证所使用的试剂与对照品
[0083]
表3.试剂与对照品
[0084]
名称规格批号含量供应商磷酸二氢钾500g/瓶20180308——国药集团乙腈4l/瓶3jh0025——spzctaum磷酸500ml/瓶h2020219——阿拉丁乙二胺四乙酸二钠250g/瓶20200401——重庆川东化工维生素c对照品100mg/瓶100425-201504100%中检院法莫替丁注射液2ml;20mg210831——四川太极制药纯化水——————自制盐酸500ml/瓶20180401——重庆川东化工氢氧化钠500g/瓶20180207——沃凯30%双氧水500ml/瓶20190501——重庆川东化工
[0085]
4.3.待验证的分析方法
[0086]
4.3.1.实验条件
[0087]
检测波长:210nm;色谱柱:gl inertsustain c18,250
×
4.6mm、5μm;柱温:30℃;进样盘温度:4℃;进样量:5μl;流速:0.6~1.5ml/min;流动相a:磷酸二氢钾溶液(取磷酸二氢钾2.04g,加水1000ml使溶解,用磷酸调节ph值至3.0);流动性b:73%乙腈;洗针溶液:0.2%磷酸;梯度洗脱:
[0088][0089]
4.3.2.溶液配制
[0090]
溶剂:称取乙二胺四乙酸二钠0.56g与磷酸二氢钾2.0g,加入纯化水1000ml使溶解,用磷酸调节ph值至3.0。
[0091]
对照品溶液:取维生素c对照品约12.5mg,精密称定,置50ml量瓶中,用溶剂溶解并稀释至刻度。平行配制2份。
[0092]
供试品溶液:精密量取法莫替丁注射液2.5ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀。平行配制2份。
[0093]
4.3.3.系统适用性要求
[0094]
供试品溶液色谱图中,维生素c峰与相邻峰分离度应大于1.5,维生素c峰拖尾因子应不大于1.5,理论塔板数按维生素c峰计算不得低于5000。
[0095]
4.3.4.测定
[0096]
取空白(溶剂)、对照品溶液及供试品溶液各5μl,注入色谱仪,记录色谱图。
[0097]
表4.样品进样针数设置
[0098][0099][0100]
4.3.5.计算公式
[0101]
按下式计算供试品的维生素c:
[0102][0103]
[0104][0105]
其中:a
对
:对照品溶液中主峰峰面积;
[0106]m对
:对照品重量,mg;
[0107]v对
:对照品溶液稀释倍数;
[0108]
p:对照品的含量;
[0109]a供
:供试品溶液中主峰峰面积;
[0110]v供
:供试品溶液稀释倍数;
[0111]
4.3.6.标准规定
[0112]
含维生素c(c6h8o6)应为标示量的80.0%~110.0%,rsd应不大于2.0%。
[0113]
5.方法验证
[0114]
5.1.专属性试验
[0115]
5.1.1.干扰性试验
[0116]
①
溶液的配制:
[0117]
溶剂:称取乙二胺四乙酸二钠0.56g与磷酸二氢钾2.0g,加入纯化水1000ml使溶解,用磷酸调节ph值至3.0。
[0118]
空白溶剂:溶剂
[0119]
空白辅料溶液:精密量取空白辅料溶液(取烟酰胺约500mg、d-甘露醇约200mg、乳酸约35mg,用水10ml溶解)2.5ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀。
[0120]
维生素c定位溶液:取维生素c对照品约12.5mg,精密称定,置50ml量瓶中,用溶剂溶解并稀释至刻度,作为对照品溶液。
[0121]
供试品溶液:精密量取法莫替丁注射液2.5ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀。
[0122]
②
测定法:
[0123]
精密量取上述空白、空白辅料溶液、对照品溶液与供试品溶液各5μl,分别注入液相色谱仪,记录色谱图。
[0124]
③
测定结果:
[0125]
色谱图结果见图1~4,具体色谱图分析结果见表5。
[0126]
表5.干扰性试验测定结果
[0127][0128]
④
结论:
[0129]
空白溶剂、空白辅料不干扰维生素c测定;供试品溶液色谱图中,维生素c峰与相邻峰分离度为3.4大于1.5,拖尾因子为1.1小于1.5,理论塔板数按维生素c峰计算为15993大于5000。
[0130]
5.1.2.强制降解试验
[0131]
①
溶液的配制:
[0132]
空白:溶剂
[0133]
空白辅料溶液:精密量取空白辅料溶液(取烟酰胺约500mg、d-甘露醇约200mg、乳酸约35mg,用水10ml溶解)2.5ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀。
[0134]
(1)强氧化降解
[0135]
精密量取法莫替丁注射液2.5ml,置10ml量瓶中,加入0.03%双氧水0.5ml,混匀,放置10min,用溶剂稀释至刻度,摇匀,作为强氧化降解供试品溶液;精密量取空白辅料溶液2.5ml,置10ml量瓶中,同法操作,作为强氧化降解空白辅料溶液。
[0136]
(2)强碱降解
[0137]
精密量取法莫替丁注射液2.5ml,置10ml量瓶中,加入0.1mol/l氢氧化钠溶液0.3ml,40℃水浴加热10分钟后,再加入0.1mol/l的盐酸溶液0.3ml,用溶剂稀释至刻度,摇匀,作为强碱降解供试品溶液;精密量取空白辅料溶液2.5ml,置10ml量瓶中,同法操作,作为强碱降解空白辅料溶液。
[0138]
(3)高温降解
[0139]
取法莫替丁注射液适量,于60℃干燥箱中放置4小时,精密量取2.5ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀,作为高温降解供试品溶液;取空白辅料溶液,同法操作,作为高温降解空白辅料溶液。
[0140]
(4)强酸降解
[0141]
精密量取法莫替丁注射液2.5ml,置10ml量瓶中,加入1mol/l盐酸溶液0.5ml,40℃水浴加热10分钟后,再加入1mol/l氢氧化钠溶液0.5ml,用溶剂稀释至刻度,摇匀,作为强酸降解供试品溶液;精密量取空白辅料溶液2.5ml,置10ml量瓶中,同法操作,作为强酸降解空白辅料溶液。
[0142]
(5)强光照降解
[0143]
取法莫替丁注射液适量,同时置紫外光灯(能量不低于200w
·
hr/m2)和冷白荧光
灯(光照强度4500
±
500lux)下放置5天,精密量取2.5ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀,作为强光照降解供试品溶液;取空白辅料溶液,同法操作,作为强光照降解空白辅料溶液。
[0144]
(6)未降解试验
[0145]
精密量取法莫替丁注射液2.5ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀。
[0146]
②
测定法:
[0147]
精密量取上述溶液各5μl,分别注入液相色谱仪,记录色谱图。
[0148]
表6.样品进样针数设置
[0149][0150][0151]
③
测定结果:
[0152]
强降解色谱图结果见图5~14,具体色谱图分析结果见表7。
[0153]
表7.专属性测定结果
[0154][0155]
④
结论:
[0156]
各降解条件下供试品溶液的主峰纯度角度均小于纯度阈值,主峰与相邻杂质的分离度都大于1.5,符合方案要求。
[0157]
5.2.系统精密度试验
[0158]
①
溶液的配制:
[0159]
空白:溶剂
[0160]
对照品溶液:取维生素c对照品约12.5mg,精密称定,置50ml量瓶中,用溶剂溶解并稀释至刻度,作为对照品溶液。
[0161]
②
测定法:
[0162]
取空白与对照品溶液各5μl,注入色谱仪,记录色谱图。
[0163]
表8.样品进样针数设置
[0164][0165][0166]
③
测定结果:
[0167]
表9.系统精密度试验结果
[0168][0169]
④
结论:
[0170]
系统精密度实验中,连续6针维生素c保留时间rsd为0.23%,小于1.0%,峰面积rsd为0.61%,小于2.0%,仪器精密度符合要求。
[0171]
5.3.溶液稳定性
[0172]
①
溶液的配制:
[0173]
对照品溶液:取维生素c对照品约12.5mg,精密称定,置50ml量瓶中,用溶剂溶解并稀释至刻度,摇匀。
[0174]
供试品溶液:精密量取法莫替丁注射液2.5ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀。
[0175]
②
测定法:
[0176]
取对照品溶液5μl,于2℃~8℃条件下分别放置0h、2h、4h、8h、12h、24h注入液相色谱仪,记录色谱图;取供试品溶液5μl,于2℃~8℃条件下分别放置0h、2h、4h、8h注入液相色谱仪,记录色谱图;
[0177]
③
测定结果:
[0178]
表10.溶液稳定性测定结果
[0179][0180][0181]
④
结论:
[0182]
放置于2℃~8℃条件下,供试品溶液至少在8h内稳定,对照品溶液至少在24h内稳定。
[0183]
5.4.线性
[0184]
①
溶液的配制:
[0185]
对照品贮备溶液的配制:取维生素c对照品约50mg,精密称定,置20ml量瓶中,加溶剂稀释至刻度,摇匀,作为对照品贮备溶液。
[0186]
50%线性溶液:精密量取对照品贮备溶液0.5ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀。
[0187]
80%线性溶液:精密量取对照品贮备溶液0.8ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀。
[0188]
90%线性溶液:精密量取对照品贮备溶液0.9ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀。
[0189]
100%线性溶液:精密量取对照品贮备溶液1.0ml,置10ml量瓶中,用溶剂稀释至刻
度,摇匀。
[0190]
110%线性溶液:精密量取对照品贮备溶液1.1ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀。
[0191]
120%线性溶液:精密量取对照品贮备溶液1.2ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀。
[0192]
200%线性溶液:精密量取对照品贮备溶液2.0ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀。
[0193]
②
测定:
[0194]
取上述线性溶液各5μl,注入液相色谱仪,记录色谱图。
[0195]
表11.样品进样针数设置
[0196][0197][0198]
③
测定结果:
[0199]
以浓度为横坐标,峰面积为纵坐标,进行线性回归处理,计算回归方程、相关系数、截距与相当于供试品浓度100%所对应的峰面积比值。
[0200]
表12.维生素c测定线性测定结果
[0201][0202]
④
结论:
[0219]
式中:η:回收率,%;
[0220]m加
:加入量,mg;
[0221]m实测
:实际测得量,mg;
[0222]
f:校正因子;
[0223]
v:供试品溶液稀释体积,ml;
[0224]
a:供试品溶液主峰面积。
[0225]
表14.准确度测定结果
[0226][0227]
④
结论:
[0228]
本法测定50%限度水平、100%限度水平和120%限度水平的回收率均在98%~102%之间,平均回收率为100.67%,rsd为0.76%,小于2.0%,结果符合规定。
[0229]
5.6.精密度
[0230]
5.6.1.重复性
[0231]
①
溶液的配制:
[0232]
对照品溶液:取维生素c对照品约12.5mg,精密称定,置50ml量瓶中,用溶剂溶解并稀释至刻度,作为对照品溶液。
[0233]
供试品溶液:精密量取法莫替丁注射液2.5ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀,即得。平行配制6份。
[0234]
②
测定:
[0235]
精密量取供试品溶液与对照溶液各5μl,分别注入液相色谱仪,记录色谱图。按外标法计算维生素c含量。
[0236]
表15.样品进样针数设置
[0237]
序号样品名称进样针数1空白12对照品溶液-163对照品溶液-224重复性供试品溶液-1(规格2ml:20mg)25重复性供试品溶液-2(规格2ml:20mg)26重复性供试品溶液-3(规格2ml:20mg)27重复性供试品溶液-4(规格2ml:20mg)28重复性供试品溶液-5(规格2ml:20mg)29重复性供试品溶液-6(规格2ml:20mg)210对照品溶液-11
[0238]
③
测定结果:
[0239]
表16.重复性测定结果(规格2ml:20mg)
[0240][0241]
5.6.2.中间精密度
[0242]
由不同人员,不同时间,使用不同仪器,按“重复性”同法测定。
[0243]
①
溶液的配制:
[0244]
按“重复性”同法操作。
[0245]
②
测定:
[0246]
精密量取供试品溶液与对照溶液各5μl,分别注入液相色谱仪,记录色谱图。按外标法计算维生素c含量。
[0247]
表17.样品进样针数设置
[0248]
序号样品名称进样针数1空白12对照品溶液-163对照品溶液-224中间精密度供试品溶液-1(规格2ml:20mg)2
5中间精密度供试品溶液-2(规格2ml:20mg)26中间精密度供试品溶液-3(规格2ml:20mg)27中间精密度供试品溶液-4(规格2ml:20mg)28中间精密度供试品溶液-5(规格2ml:20mg)29中间精密度供试品溶液-6(规格2ml:20mg)210对照品溶液-11
[0249]
③
测定结果:
[0250]
表18.不同人员不同时间不同仪器维生素c含量测定结果(规格2ml:20mg)
[0251][0252]
表19.维生素c含量测定中间精密度试验结果(规格2ml:20mg)
[0253][0254]
④
结论:
[0255]
平行测定6份供试品溶液中维生素c平均含量为95.94%,rsd为0.83%,小于2.0%,重复性良好。12份供试品溶液中维生素c平均含量为94.81%,rsd为1.40%,小于2.0%,故中间精密度良好。
[0256]
5.7耐用性
[0257]
为了考察测试条件发生微小变动时,对测定结果的影响,考察了以下几个典型变动因素:流速、ph值、流动相比例、柱温、检测波长、色谱柱,考察情况如下:
[0258]
表20.耐用性试验考察指标
[0259][0260]
①
溶液的配制:
[0261]
对照品溶液:取维生素c对照品约12.5mg,精密称定,置50ml量瓶中,用溶剂溶解并稀释至刻度,作为对照品溶液。平行配制2份。
[0262]
供试品溶液:精密量取法莫替丁注射液2.5ml,置10ml量瓶中,用溶剂稀释至刻度,摇匀,即得。平行配制2份。
[0263]
②
测定:
[0264]
精密吸取对照品溶液与供试品溶液各5μl,注入液相色谱仪,记录色谱。
[0265]
表21.样品进样针数设置
[0266]
序号样品名称进样针数1空白12对照品溶液163对照品溶液224供试品溶液125供试品溶液226对照品溶液11
[0267]
③
测定结果:
[0268]
表22.耐用性测定结果
[0269][0270]
④
结论:
[0271]
当各色谱条件发生微小变动时,维生素c的含量均在80.0%-110.0%范围内,与正常条件的偏差小于2.0%,故本方法耐用性良好。
[0272]
综上,本发明通过特定的样品溶剂和色谱条件,可以检测法莫替丁注射液中维生素c,结果准确,快速、灵敏度高,为含维生素c的法莫替丁注射液的质量控制提供了新方法,也为法莫替丁注射液的质量控制标准的提高提供了方法依据,同时为扩大法莫替丁注射液的临床应用提供了参考依据,具有良好的应用前景。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1