PGⅠ蛋白检测的电化学免疫传感器及其制备方法与应用
pgⅰ蛋白检测的电化学免疫传感器及其制备方法与应用
技术领域
1.本发明涉及电化学免疫传感器技术领域,尤其涉及一种pgⅰ蛋白检测的电化学免疫传感器及其制备方法与应用。
背景技术:
2.胃癌是一种常见的消化道恶性肿瘤,胃镜检查和病理活检目前仍是确诊胃癌的唯一方法,但因其费用较高且为有创、侵入性操作,普通人群接受度低,难以应用于大规模普查。所以,先通过无创的检查手段将胃癌高风险人群筛查出来,然后进行胃镜下精查是较为理想的方法。
3.血清检测具有操作简单、人群接受度高及可重复等优点,比较适合应用于进行大规模人筛查。胃蛋白酶原(pg)作为胃蛋白酶的非活性前体因此成为胃癌血清学诊断的重要标志物。因为胃是pg的唯一来源,且它不受短期饮食或其他外部条件的影响,并通过胃粘膜进入血流。因此,每个独立个体血清中的pg水平相对稳定,能够准确反映胃粘膜的状态。
4.尽管有几种检测pg的方法可用,如放射免疫分析法(rias)、酶联免疫吸附分析法(elisa)、酶免疫分析法(eias)和时间分辨荧光免疫分析法(trfias)。然而,尽管这些方法能够检测pg,但需要采用大型仪器进行检测,使得检测成本较高。
技术实现要素:
5.本发明的目的在于提供一种pgⅰ蛋白检测的电化学免疫传感器及其制备方法与应用,旨在解决现有的检测pg的方法的检测成本较高的问题。
6.为实现上述目的,第一方面,本发明提供了一种pgⅰ蛋白检测的电化学免疫传感器制备方法,包括以下步骤:
7.在丝网印刷电极的工作电极表面电沉积苯胺,得到电沉积聚苯胺;
8.制备mos2和cu3pt;
9.将所述mos2与所述cu3pt依次进行振荡混合和离心洗涤再分散于3ml超纯水中,得到mos2@cu3ptnps混合溶液;
10.将所述mos2@cu3ptnps混合溶液滴加到经所述电沉积聚苯胺的修饰电极表面,在恒温孵育箱中恒温干燥;
11.使用超纯水对所述电极进行冲洗;
12.取pg i抗体滴加到冲洗后的所述电极上,直至所述pg i抗体完全固定;
13.将1%的牛血清白蛋白滴加到所述电极表面孵育30min,得到电化学免疫传感器。
14.其中,所述在丝网印刷电极的工作电极表面电沉积苯胺,得到电沉积聚苯胺包括:
15.取0.15m苯胺溶于超纯水中,随后加入0.5m h2so4混合均匀,得到苯胺溶液;
16.将50μl所述苯胺溶液滴加在丝网印刷电极的工作电极表面,以50mv/s的速率在-0.2v~1.1v范围通过循环伏安法对所述电极表面循环扫描15次,得到电沉积聚苯胺。
17.其中,所述制备mos2包括:
18.取1.24g七钼酸铵(nh4)6mo7o
24
·
4h2o溶于15ml超纯水中,随后加入1.67g苯胺,彻底溶解后,室温下磁性搅拌并逐滴加入1m hcl直至出现白色沉淀物,置于恒温孵育箱中50℃反应2h,得到溶液产物;
19.对所述溶液产物依次进行过滤、用乙醇洗涤和于50℃下干燥,得到moo3;
20.取0.1g moo3溶于20ml超纯水中并超声5min,直至所述moo3彻底溶解,得到第一溶解液;
21.在搅拌过程中向所述第一溶解液中加入0.28g l-半胱氨酸,得到第二溶解液;
22.将所得第二溶解液移入高压反应釜中,200℃下反应14h,随炉冷却至室温后取出依次离心洗涤、50℃干燥和研磨,得到mos2。
23.其中,所述制备cu3pt包括:
24.60℃,取160mg ctac加入到20ml油胺溶液中并搅拌,得到均相溶液;
25.依次在所述均相溶液中加入16mg pt(acac)2、7mg cucl2·
h2o和61mg tris溶液并搅拌,得到聚合溶液;
26.将所述聚合溶液超声30min后将转移入高压釜内,180℃加热10h,随炉冷却至室温后取出使用乙醇和环己烷进行离心洗涤,60℃烘干制得cu3ptnps。
27.其中,所述将所述mos2与所述cu3pt依次进行振荡混合和离心洗涤再分散于3ml超纯水中,得到mos2@cu3ptnps混合溶液包括:
28.将1ml所述mos2与2.5ml所述cu3pt混合,得到混合液;
29.将所述混合液避光低速振荡12h后离心洗涤分散于3ml超纯水中,得到mos2@cu3ptnps混合溶液。
30.第二方面,本发明提供了一种pgⅰ蛋白检测的电化学免疫传感器,包括丝网印刷电极、mos2、cu3pt、pg i抗体和牛血清白蛋白。
31.第三方面,本发明提供了一种pgⅰ蛋白检测的电化学免疫传感器的应用,应用于pgⅰ检测。
32.本发明的一种pgⅰ蛋白检测的电化学免疫传感器及其制备方法与应用,通过在丝网印刷电极的工作电极表面电沉积苯胺,得到电沉积聚苯胺;制备mos2和cu3pt;将所述mos2与所述cu3pt依次进行振荡混合和离心洗涤再分散于3ml超纯水中,得到mos2@cu3ptnps混合溶液;将所述mos2@cu3ptnps混合溶液滴加到经所述电沉积聚苯胺的修饰电极表面,在恒温孵育箱中恒温干燥;使用超纯水对所述电极进行冲洗;取pg i抗体滴加到冲洗后的所述电极上,直至所述pg i抗体完全固定;将1%的牛血清白蛋白滴加到所述电极表面孵育30min,得到电化学免疫传感器,本发明得到的电化学免疫传感器通过电化学方法检测血清中pg,成本更低,检测速度更快,且无需借助其他大型仪器,解决了现有的检测pg的方法的检测成本较高的问题。
附图说明
33.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
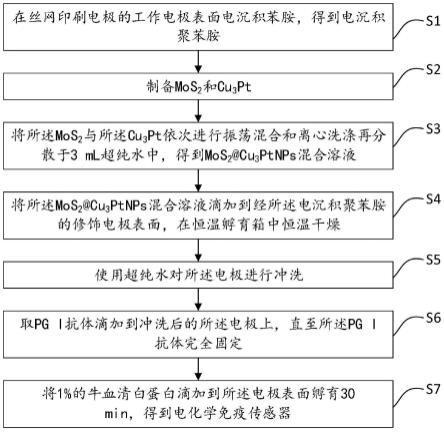
34.图1是本发明提供的一种pgⅰ蛋白检测的电化学免疫传感器制备方法的流程图。
35.图2是m[fe(cn)6]
3-/4-使用cv对传感器的分步制造过程进行表征的示意图。
[0036]
图3是m[fe(cn)6]
3-/4-使用eis对传感器进行表征的示意图。
[0037]
图4是mos2@cu3pt的结构通过能量色散x射线光谱仪进行表征的示意图。
[0038]
图5是当工作电极表面不存在修饰材料时的xps光谱的示意图。
[0039]
图6是在不同浓度的pgⅰ孵育后的免疫传感器的dpv响应的示意图。
[0040]
图7是pgⅰ的电流响应与浓度对数的线性关系的示意图。
具体实施方式
[0041]
下面详细描述本发明的实施例,所述实施例的示例在附图中示出,其中自始至终相同或类似的标号表示相同或类似的元件或具有相同或类似功能的元件。下面通过参考附图描述的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
[0042]
请参阅图1,第一方面,本发明提供一种pgⅰ蛋白检测的电化学免疫传感器制备方法,包括以下步骤:
[0043]
s1在丝网印刷电极的工作电极表面电沉积苯胺,得到电沉积聚苯胺;
[0044]
具体包括:
[0045]
s11取0.15m苯胺溶于超纯水中,随后加入0.5m h2so4混合均匀,得到苯胺溶液;
[0046]
s12将50μl所述苯胺溶液滴加在丝网印刷电极的工作电极表面,以50mv/s的速率在-0.2v~1.1v范围通过循环伏安法对所述电极表面循环扫描15次,得到电沉积聚苯胺。
[0047]
s2制备mos2和cu3pt;
[0048]
所述制备mos2包括:
[0049]
s201取1.24g七钼酸铵(nh4)6mo7o
24
·
4h2o溶于15ml超纯水中,随后加入1.67g苯胺,彻底溶解后,室温下磁性搅拌并逐滴加入1m hcl直至出现白色沉淀物,置于恒温孵育箱中50℃反应2h,得到溶液产物;
[0050]
s202对所述溶液产物依次进行过滤、用乙醇洗涤和于50℃下干燥,得到moo3;
[0051]
s203取0.1g moo3溶于20ml超纯水中并超声5min,直至所述moo3彻底溶解,得到第一溶解液;
[0052]
s204在搅拌过程中向所述第一溶解液中加入0.28g l-半胱氨酸,得到第二溶解液;
[0053]
s205将所得第二溶解液移入高压反应釜中,200℃下反应14h,随炉冷却至室温后取出依次离心洗涤、50℃干燥和研磨,得到mos2。
[0054]
所述制备cu3pt包括:
[0055]
s211在60℃下,取160mg ctac加入到20ml油胺溶液中并搅拌,得到均相溶液;
[0056]
s212依次在所述均相溶液中加入16mg pt(acac)2、7mg cucl2·
h2o和61mg tris溶液并搅拌,得到聚合溶液;
[0057]
具体的,依次在所述均相溶液中加入16mg pt(acac)2、7mg cucl2·
h2o和61mg tris溶液并搅拌,直至所述均相溶液颜色由黄色转变至蓝绿色,得到聚合溶液。
[0058]
s213将所述聚合溶液超声30min后将转移入高压釜内,180℃加热10h,随炉冷却至室温后取出使用乙醇和环己烷进行离心洗涤,60℃烘干制得cu3ptnps。
[0059]
s3将所述mos2与所述cu3pt混合后依次进行振荡混合和离心洗涤再分散于3ml超纯水中,得到mos2@cu3ptnps混合溶液;
[0060]
具体包括:
[0061]
s31将1ml所述mos2与2.5ml所述cu3pt混合,得到混合液;
[0062]
s32将所述混合液避光低速振荡12h后离心洗涤分散于3ml超纯水中,得到mos2@cu3ptnps混合溶液。
[0063]
s4将所述mos2@cu3ptnps混合溶液经所述苯胺电沉积滴加到所述电极表面,在恒温孵育箱中恒温干燥;
[0064]
s5使用超纯水对所述电极进行冲洗;
[0065]
具体的,用超纯水冲洗以去除未固定的复合材料并烘干以备下一步使用。
[0066]
s6取pg i抗体滴加到冲洗后的所述电极上,直至所述pg i抗体完全固定;
[0067]
具体的,取5.0μl的anti-pg i(200ng/ml)滴加到修饰电极上,在4℃冰箱里保存12h以使抗体完全固定。
[0068]
s7将1%的牛血清白蛋白滴加到所述电极表面孵育30min,得到电化学免疫传感器。
[0069]
具体的,将10μl 1%的牛血清白蛋白(bsa)滴加到修饰电极表面并孵育30min以避免可能的非特异性吸附。在每个步骤之后,用pbs(0.01m)彻底清洁所制备的传感器并烘干。
[0070]
有益效果:
[0071]
1.通过电化学方法检测血清中pg,相对于胃镜等侵入性检测方式,使得检查过程更加人性化;
[0072]
2.通过对血清的pg进行检测的方法有很多,所构造的无标记电化学传感器成本更低,检测速度更快,且无需借助其他大型仪器;
[0073]
3.所构建的电化学传感器,检测范围更广阔,能灵敏检测500pg ml-1
to 400ng ml-1
范围内的pg;
[0074]
4.所构建的电化学传感器储存方便,保存时间长(实验检测显示-4℃冰箱储存30天后,活性依旧保持在96%以上);
[0075]
5.所构建传感器特异性佳,与其他血清中经常出现的干扰物质进行混合检测时,未出现错检情况。
[0076]
第二方面,本发明提供了一种pgⅰ蛋白检测的电化学免疫传感器,包括丝网印刷电极、mos2、cu3pt、pg i抗体和牛血清白蛋白。
[0077]
具体的,本发明提供了一种pgⅰ蛋白检测的电化学免疫传感器。其中聚苯胺通过循环扫描的方式电沉积到丝网印刷电极表面,用以加速电极表面的电子转移速率,且因其表面具有一定粗糙度能够提高后续纳米材料附着的数量。cu3pt nps通过物理吸附的方式固定到mos2表面,通过cu-s和pt-s与pg i抗体(anti-pg i)结合,进一步提高免疫传感器的灵敏度和稳定性。
[0078]
请参阅图2至图7,第三方面,本发明提供了一种pgⅰ蛋白检测的电化学免疫传感器的应用,应用于pgⅰ检测。
[0079]
具体的,首先,通过循环伏安法将苯胺电沉积到丝网印刷电极(spe)的工作电极表面,形成灵敏pani层,用以加速电极表面的电子转移速率,又且因其表面具有一定粗糙度能
够提高后续纳米材料附着的数量。随后,将mos2@cu3ptnps滴加到修饰电极表面,为后续抗体的固定提供足够的活性位点,且由于其具有极佳的电化学性能,能够进一步加速电子转移。随后,anti-pg i通过cu-s和pt-s键固定到修饰电极表面,用以实现对不同浓度pg的实时检测。检测机制基于监测抗体和抗原之间的特异性识别进而结合产生的免疫蛋白阻碍了工作电极表面的电子转移速率,进而引起的峰值电流的变化。简而言之,在这种信号放大策略中,当抗原浓度增加时,电化学信号的值降低。因此,所提出的免疫传感器可以有效地检测目标分析物(pg i)。
[0080]
在5mm[fe(cn)6]
3-/4-溶液中,通过cv和eis对免疫传感器的逐步制造过程进行了表征。cv的结果如图2所示,裸spe的曲线(曲线a)在0.15v和0.29v下显示出两个特征氧化还原峰。这是因为在施加电压后,[fe(cn)6]
3-/4-溶液中电子对产生氧化还原反应。pani修饰电极后,峰值电流明显增加(曲线b)。当mos
2 nfs沉积在电极表面时,峰值电流继续增加(曲线c)。当滴加纳米复合材料mos2@cu3pt后,电化学响应显著增加(曲线d),这是因为cu3pt nps具有优异的电化学性能。然而,当修饰电极依次与anti-pg i(曲线e)、bsa(曲线f)和pg i(曲线e)进行孵育后,可以观察到峰值电流依次降低,因为特异性反应生成的免疫活性物质大大阻碍了电子转移效率。
[0081]
为了进一步验证逐步修饰过程,使用eis对免疫传感器进行了表征(图3)。裸spe的eis图像显示了一个半径相对较大的半圆(曲线a)。当聚苯胺修饰到电极上时,半圆直径显著减小(曲线b),这是因为它具有良好的电化学活性,能够提高电化学灵敏度。固定mos2 nfs后,半圆直径显著减小(曲线c)。当mos2@cu3pt纳米复合材料修饰了电极表面,阻抗值进一步降低(曲线b),表明纳米复合材料有利于电子的传输。然而,当anti-pg i固定在修饰电极表面时,半圆直径显著增大(曲线e)。当bsa封闭了电极表面的其他未结合的非特异性位点后,电阻进一步增大(曲线f)。当修饰电极与pg i孵育后,电阻进一步增加(曲线g)。所有上述现象都可以解释为特定抗原抗体反应产生的生物活性物质阻碍了电子转移的效率。此外,所获得的结果与cv结果相佐证,证明了免疫传感器的成功构建。
[0082]
mos2@cu3pt的结构通过能量色散x射线光谱仪(eds)进一步表征,如上图4所示,mo、s、cu和pt元素存在于eds光谱中,这意味着cu3pt nps成功固定到mos
2 nfs上。此外,采用x射线光电子能谱(xps)进行元素分析,进一步证实了mos2@cu3pt纳米复合材料合成成功。如上图5所示,当工作电极表面不存在修饰材料时,xps光谱中存在三个主要峰,分别为284.5ev(c 1s)、532.3ev(o 1s)和399.3ev(n 1s)(曲线a)。相比之下,在电沉积聚苯胺纳米复合物(曲线b)后,观察到一个新的峰值s 2p(226.7ev),表明聚苯胺已成功固定化。将mos2 nfs加载到修饰电极上后,检测到一个额外的峰值mo 3d(171.2ev)(曲线c)。曲线d显示了另外两个峰值,pt 4f(109.9ev)和cu 2p(904.3ev),支持cu3pt nps已成功修饰
[0083]
为了验证免疫传感器的分析检测性能,在最佳实验条件下,采用dpv对不同浓度的pgⅰ进行电化学检测。如上图6和图7所示,峰值响应随pgⅰ浓度的增加而降低,检测范围为0.5ng ml-1
至400ng ml-1
、pgⅰ浓度对数与电流响应的线性关系如上图7所示,回归方程为i(μa)=-7.81logc
pgⅰ(pg ml-1)+89.79,相关系数为0.983,检出限为166.67pg ml-1(s/n=3)。实验结果表明,由于所制备的三维纳米复合材料具有优异的电化学性能,检测范围较宽。
[0084]
图6中在不同浓度的pgⅰ孵育后的免疫传感器的dpv响应:0.5、0.75、1、2.5、5、10、
25、50、100、200、250、300和400ng ml-1
,检测溶液pbs(ph=7.4)。
[0085]
表1.使用构建的传感器和化学发光法对临床血清样本的检测结果对比
[0086][0087]
为了验证所构建的免疫传感器在临床实践中的可信性和准确性,对来自健康个体(样本3)和患者(样本1、2、4和5,表1)的人类血清样本中的pgⅰ浓度进行了测定。化学发光法在临床实践中常被用于检测pg i因此此处被视为标准值,构建传感器的检测结果与化学发光法的结果进行了比较。两种方法之间的相对误差范围为-15.07%-5.76%。这些数据表明,这两种分析方法之间具有良好的一致性,表明所设计的免疫传感器在pgⅰ检测的方面具有较大的潜在临床应用价值。
[0088]
以上所揭露的仅为本发明一种pgⅰ蛋白检测的电化学免疫传感器及其制备方法与应用较佳实施例而已,当然不能以此来限定本发明之权利范围,本领域普通技术人员可以理解实现上述实施例的全部或部分流程,并依本发明权利要求所作的等同变化,仍属于发明所涵盖的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1