一种食品中微塑料的快速检测方法
1.本发明涉及一种食品中微塑料的快速检测方法。
背景技术:
2.微塑料(microplastics,mps)是指直径小于5mm的塑料颗粒或碎片,因其分布的广泛性和对动植物体的毒害性,已经成为一种新型污染物,同时由于微塑料颗粒的粒径小、比表面积大、疏水性强等特点,成为环境中众多污染物的理想载体,对污染物的迁移转化过程有着显著的作用。
3.从现有的数据情况来看,食品中的微塑料分布较为广泛。微塑料的大小类似于某些浮游生物,可被许多海洋无脊椎动物摄取,也可以在沉积物中积累,因此底栖生物可能会摄入微塑料并在营养级之间转移,这就造成水产养殖食物中存在微塑料,并通过食物链传递给更高级别的生物体。全球累计发现120多种渔业物种中存在微塑料污染。另外农作物根部的裂缝可以吸收周围土壤与水中的微塑料,这些微塑料可以从作物根部上传到可食用部分,造成果蔬植物中存在微塑料颗粒。目前已有文献报道在苹果、梨、胡萝卜、生菜等果蔬食品中发现有微塑料。
4.但是食品中微塑料的研究相对薄弱,目前还没有建立起食品中微塑料采样和检测的标准方法。微塑料检测的方法大部分参考环境样品中的分析技术,包括样品分离、定性鉴别和定量分析。
5.其中,食品样品中微塑料颗粒的提取和样品基质干扰的去除是微塑料颗粒检测过程中的两个重点和难点。目前的样品基质干扰去除方法主要有通过化学或生物手段将样品消解,如碱消解、酸消解、氧化消解和酶消解等;还有采用仪器设备加速消解过程,如微波辅助萃取等。但是目前的这些方法会涉及一个问题,就是不同的消解方法在消解过程中有可能会造成微塑料的损失或者形态的破坏,最终对后续的定量造成影响。
6.其次是微塑料的提取方法,目前主要采用浮选法和筛分法,如采用不同浓度的盐溶液将微塑料粒子从消解液中浮选出来,然后利用目检法进行定性分析。另外也有采用滤网过滤消解液,得到微塑料粒子,然后利用显微镜、红外光谱仪、拉曼光谱仪、扫描电镜等方法对滤网上保留的微塑料进行定性定量分析。这几个方法操作较为复杂,同时在筛选过程中容易造成塑料粒子的损失,最终对结果造成影响。从定量方法上讲,主要通过颗粒计数方法进行定量,而非质量浓度定量,因此造成不同数据结果之间难以比较的问题。
7.目前还有采用有机溶剂萃取微塑料的方法,即样品消解后,将塑料颗粒用有机溶剂溶解,再采用其他仪器设备进行分析检测。该方法操作过程较为复杂,常温下,不同的微塑料颗粒在不同的有机溶剂中,有些溶解度较低,有些甚至根本不溶解;并非所有的微塑料颗粒都可溶于同一溶剂,因此需要采用不同的溶剂对微塑料进行提取,不是非常方便;某些微塑料的溶解需要用到大量有机溶剂,同时提取过程可能会有损失。
技术实现要素:
8.针对现有技术中,食品中微塑料采样和检测存在的问题,本发明提供一种食品中微塑料的快速检测方法,采用加速溶剂萃取的方式,将食品中的微塑料颗粒通过加热加压的方式溶解后直接用溶剂萃取,不需要对样品进行前处理消解后再通过不同的方式提取微塑料颗粒,因此从整体前处理周期上来讲,速度快,效率高,试剂使用量少。针对不同的微塑料颗粒,优化加速溶剂萃取的条件,防止塑料粒子在高温高压下降解。提取后的微塑料采用热裂解-气相色谱质谱联用仪进行后续检测分析,利用微塑料裂解碎片的特征峰的保留时间和质荷比进行定性鉴定,用特征定量离子进行定量计算,测定样品中特定微塑料的质量浓度。
9.本发明采用的技术方案是:
10.一种食品中微塑料的快速检测方法,所述方法包括以下步骤:
11.(1)样品采集:将待测食品样品,混匀制样,新鲜样品粉碎均匀后冻干,干燥样品粉碎后直接进行下一步骤;
12.一般来说,对食品样品选取可食部分进行制样,对于有特殊检测要求的样品,譬如需要选择非可食部分进行检测的,将非可食部分按照上述要求制样;
13.(2)加速溶剂提取:准确称取冻干或粉碎的样品,加入硅藻土混匀,用加速溶剂萃取仪进行提取;萃取溶剂为二氯甲烷、正己烷、丙酮中的一种或多种;
14.进一步,加速溶剂萃取条件为:萃取时间180-420s(优选300s),萃取压力8-12mpa(优选10mpa),萃取温度80-180℃(优选180℃),加热时间180-600s(优选540s),淋洗体积60-100%(优选80%),氮吹时间60-90s(优选75s),单次萃取的循环次数2-3次(优选3次),萃取次数1-2次(优选1次);
15.(3)样品检测:
16.将加速溶剂萃取仪提取出来的提取液蒸除溶剂,然后浓缩至近干,作为供试品溶液加入到样品杯中,在室温下或加热待溶剂挥发后,将样品杯放入进样口,用热裂解-气相色谱-质谱仪进行检测,根据不同塑料颗粒的特征峰进行塑料粒子类型的定性判定;制作塑料粒子的标准曲线,将供试品溶液的特征峰峰面积和标准曲线对比,进行微塑料粒子的定量检测。
17.进一步,在定性判定中,不同塑料颗粒的特征峰采用不同塑料的标准品用热裂解-气相色谱-质谱仪检测得到;
18.所述的特征峰为塑料标准品经过热裂解后,得到的特征小分子的色谱峰和相对应的质谱图,记录每种塑料标准品的特征峰,通过对样品的色谱峰和质谱峰的定性分析,来判定塑料粒子的成分;
19.在定量检测中,塑料粒子的标准曲线按以下方法制得:将不同质量的微塑料标准品按照步骤(2)的方法,加入硅藻土混匀,用加速溶剂萃取仪进行提取,浓缩后得到含有不同质量微塑料粒子的标准溶液系列,将该系列溶液用热裂解-气相色谱质谱仪在相同条件下检测,以微塑料粒子的特征小分子的定量离子峰面积作为纵坐标,微塑料粒子质量作为横坐标,绘制得到标准曲线;
20.热裂解-气相色谱-质谱仪的条件为:
21.裂解温度600℃,裂解时间1min,接口温度:300℃;
22.色谱条件:色谱柱:db-5ht柱;柱温:初温50℃,保持5min,以20℃/min的速率升温到270℃,保持14min;进样口温度:300℃,分流比20:1;溶剂延迟:0.10min;载气:高纯氦气,流量1.0ml/min;
23.质谱条件:接口温度:280℃;电离方式:ei;离子源温度:230℃;四极杆温度:150℃;采用全扫描模式(scan)进行定性,质谱扫描范围:29m/z-600m/z;选择离子监测模式(sim)定量;
24.优选色谱柱尺寸为30m
×
0.25mm
×
0.10μm。
25.所述步骤(2)中,萃取池的体积为33ml-100ml,通常为33ml、66ml或100ml,优选66ml,这是加速溶剂萃取仪配件的固有规格,根据购买的仪器具体型号而定。
26.所述步骤(2)中,优选萃取溶剂为二氯甲烷。
27.所述步骤(2)中,一般称取样品的质量以萃取池体积计为0.01~0.1g/ml。
28.所述硅藻土用来分散样品和填充萃取池,一般用量是将萃取池填充至满或填充到距萃取池口0.1-0.5cm。这是加速溶剂萃取仪的常规操作方法。
29.所述步骤(3)中,浓缩可以是加热浓缩或氮吹浓缩;
30.浓缩至近干一般是浓缩到体积小于1ml,更优选浓缩至10~200微升。
31.所述步骤(3)中,提取液蒸除溶剂一般需要将提取液从样品接收瓶转移到烧瓶中,一般需要用萃取溶剂洗涤样品接收瓶三次,将洗涤液全部转移到烧瓶中,减少目标物损失。一般提取液蒸除溶剂到体积1~2ml左右。
32.同样的,浓缩时一般将烧瓶中的溶液转移到进样瓶中再进行浓缩,也需要用萃取溶剂将烧瓶洗涤三次,将洗涤液转移到进样瓶中。
33.每次转移样品为了保证微塑料颗粒无损失,优选使用萃取溶剂洗涤转移前容器3次,然后将洗涤液转移到后接收容器中。
34.供试品溶液可以全部直接进样,对于微塑料含量较高的样品,也可以用1ml萃取溶剂定容后,再准确取部分(10~200微升)进样。这是本领域技术人员公知的方法。后续根据检测到的进样样品的微塑料质量和稀释比例来换算微塑料的含量。
35.本发明方法适用食品中特征峰较为明显的微塑料粒子的分析,如聚酰胺、聚苯乙烯、聚碳酸酯、聚丙烯、聚乙烯醇等。
36.为避免环境及实验器皿中可能带来的本底污染,本发明方法使用的器皿设备尽量不接触塑料,而采用玻璃器皿,玻璃器皿用超纯水超声清洗后烘干,称量好的样品用铝箔纸覆盖。使用的硅藻土进行空白实验,防止带有干扰物质。热裂解仪的样品杯使用前需要高温灼烧,同时进行空白实验,防止实验过程中带入污染。
37.本发明实施例中,提供了聚苯乙烯(ps)和聚碳酸酯这两种常见的微塑料粒子的定性和定量方法,前者常用于一次性塑料餐盒,后者常用于餐具和医疗器械中,与日常生活密切相关。对这两种微塑料粒子的加速溶剂萃取方法进行优化,比较了萃取温度和萃取时间,确定了最佳萃取溶剂。
38.本发明的有益效果在于:
39.本发明采用加速溶剂萃取的方法提取食品中的微塑料颗粒,一步式完成样品的消解和提取过程,将通常情况下的4-48小时的消解和提取过程缩短为1小时以内,大大加速了前处理效率。并且,高温高压下进行的萃取,使很多在常规条件下不能溶解的微塑料颗粒溶
解在萃取溶剂中,例如实施例中的ps和pc,常温条件下是不可能溶解在萃取溶剂二氯甲烷中的,但通过加速溶剂萃取法,实现了对难溶的微塑料颗粒的溶解和提取。
40.提取完毕后,采用热裂解-气相色谱质谱进行检测,食品样品中常见的脂肪等基质可能会在加速溶剂萃取中提取出来,但通过热裂解的方式,油脂基质被裂解,产生的特征小分子和微塑料的特征小分子不同,因此减少或排除了直接进样过程中油脂等基质干扰,从而可以舍弃净化步骤,直接将提取液进样,加速了检测周期。另外,加速溶剂萃取的萃取溶剂不可使用亲脂性过强的提取试剂,以尽量减少脂肪的溶出,降低基线噪音,提高检测灵敏度。
41.本发明方法对食品中的微塑料的提取较为全面,快速彻底,损失小,分析速度快,可同时实现定性和定量检测。
附图说明
42.图1聚苯乙烯和聚碳酸酯微塑料颗粒的总离子流图。
43.图2聚苯乙烯和聚碳酸酯微塑料颗粒的提取离子流图。
44.图3ps的特征小分子苯乙烯的质谱图。
45.图4pc的特征小分子双酚a的质谱图。
46.图5实施例2中的雪蟹腿中微塑料粒子的提取离子色谱图。
47.图6实施例3中的雪蟹加标样品的提取离子色谱图,图中1为苯乙烯,2为双酚a。
具体实施方式
48.下面通过具体实施例对本发明的技术方案进行详细说明,但本发明的保护范围不限于此。
49.实施例1标准曲线的制作
50.分别称取聚苯乙烯(ps)和双酚a聚碳酸酯(pc)粉末颗粒0mg、2mg、4mg、6mg、8mg和10mg,同质量的ps和pc混合后加入装有25克硅藻土的萃取池中,萃取池体积66ml。按照下述加速溶剂萃取条件进行萃取:萃取池体积66ml,萃取时间300s,萃取压力10.0mpa,萃取温度180℃,加热时间540s,淋洗体积80%,氮吹时间75s,循环次数3次,萃取次数1次,萃取溶剂二氯甲烷。萃取结束,将接收瓶中的溶剂完全转移到平底烧瓶中,旋蒸至剩余2毫升。将旋蒸后的溶液分次彻底转移到玻璃进样瓶中,在45℃下氮吹至干。每次转移为了保证微塑料颗粒无损失,需要用溶剂洗涤转移前容器3次,然后将洗脱液转移到接收容器中。最终用1ml二氯甲烷定容,得到聚苯乙烯和聚碳酸酯标准溶液系列。取10μl标准溶液注入热裂解-气相色谱质谱仪的样品杯中,45℃下挥发溶剂,用热裂解-气相色谱质谱进行检测,热裂解-气相色谱-质谱仪的条件为:
51.裂解温度600℃,裂解时间1min,接口温度:300℃;
52.色谱条件:色谱柱:db-5ht柱30m
×
0.25mm
×
0.10μm;柱温:初温50℃,保持5min,以20℃/min的速率升温到270℃,保持14min;进样口温度:300℃,分流比20:1;溶剂延迟:0.10min;载气:高纯氦气,流量1.0ml/min;
53.质谱条件:接口温度:280℃;电离方式:ei;离子源温度:230℃;四极杆温度:150℃;采用全扫描模式(scan)进行定性,质谱扫描范围:29m/z-600m/z;选择离子监测模式
(sim)定量;
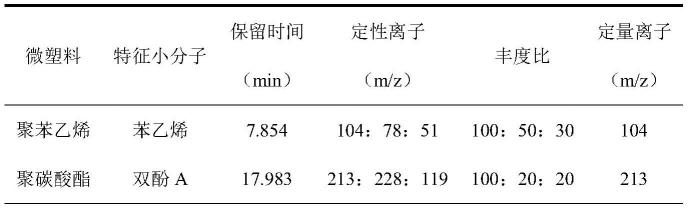
54.聚苯乙烯和聚碳酸酯的总离子流图,选择离子谱图分别如图1、2所示,特征小分子苯乙烯、双酚a的质谱图分别如图3、4所示。特征离子、保留时间如表1所示,利用特征定量离子峰面积作为纵坐标,微塑料颗粒质量作为横坐标,绘制得到标准曲线,如表2所示。可进行微塑料粒子的定量分析。
55.表1微塑料的特征小分子信息
[0056][0057]
表2方法学参数
[0058][0059]
实施例2雪蟹腿中微塑料粒子检测
[0060]
将市售冻煮雪蟹腿去壳取肉,粉碎均匀后放到冻干仪中冻干。称取冻干后的样品3g,与10g硅藻土混匀后,放入加速溶剂萃取池中,按照下述条件进行加速溶剂萃取:萃取池体积66ml,萃取时间300s,萃取压力10.0mpa,萃取温度180℃,加热时间540s,淋洗体积80%,氮吹时间75s,循环次数3次,萃取次数1次,萃取溶剂二氯甲烷。萃取结束,将接收瓶中的溶剂完全转移到平底烧瓶中,旋蒸至剩余2毫升。将旋蒸后的溶液分次彻底转移到玻璃进样瓶中,在45℃下氮吹至干。每次转移为了保证微塑料颗粒无损失,需要用溶剂洗涤转移前容器3次,然后将洗脱液转移到接收容器中。最终用1ml二氯甲烷定容。涡旋震荡混匀后根据样品中微塑料的含量,移取10μl进样瓶中的样品于热裂解-气相色谱质谱进样杯中,稍加热待溶剂挥发后,将样品杯放入进样口进行热裂解分析,条件同实施例1。根据表1中聚苯乙烯和聚碳酸酯的特征峰进行定性和定量检测,提取离子流图如图5所示,扣除空白后,样品中未检出这两种微塑料粒子。
[0061]
实施例3雪蟹腿中微塑料粒子加标回收测定
[0062]
将市售冻煮雪蟹腿去壳取肉,粉碎均匀后放到冻干仪中冻干。称取冻干后的样品3g,与10g硅藻土混匀放入加速溶剂萃取池中,再加入2mg聚苯乙烯和2mg聚碳酸酯微塑料颗粒进行加标实验。拧紧萃取池,按照下述条件进行加速溶剂萃取:萃取池体积66ml,萃取时间300s,萃取压力10.0mpa,萃取温度180℃,加热时间540s,淋洗体积80%,氮吹时间75s,循环次数3次,萃取次数1次,萃取溶剂二氯甲烷。萃取结束,将接收瓶中的溶剂完全转移到平底烧瓶中,旋蒸至剩余2毫升。将旋蒸后的溶液分次彻底转移到玻璃进样瓶中,在45℃下氮吹至干。每次转移为了保证微塑料颗粒无损失,需要用溶剂洗涤转移前容器3次,然后将洗
脱液转移到接收容器中。最终用1ml二氯甲烷定容。涡旋震荡混匀后根据样品中微塑料的含量,移取10μl进样瓶中的样品于热裂解-气相色谱质谱进样杯中,稍加热待溶剂挥发后,将样品杯放入进样口进行热裂解分析,条件同实施例1;根据表1中聚苯乙烯和聚碳酸酯的特征峰进行定性,根据表2的标准曲线进行定量检测,提取离子流图如图6所示,图6中1为苯乙烯,2为双酚a;测得聚苯乙烯和聚碳酸酯的回收率分别为94.5%和79.1%。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1