一种用于检测早期肝癌的试剂盒
1.本发明涉及生物医学技术领域,具体涉及一种用于检测早期肝癌的试剂盒。
背景技术:
2.肝癌是世界上六大常见癌症之一,也是极易引发肿瘤相关疾病的一种癌症。在临床由于肝癌的起病较为隐匿,早期肝癌诊断困难,预后不良。目前针对肝癌的诊断方法是基于成像,如超声、计算机断层扫描(ct)、磁共振成像(mri)等,再结合病患血浆中肿瘤标志物甲胎蛋白(afp)的检测结果来联合判断。然而,就现状而言,肝癌患者中有很大一部分的afp表达为阴性(afp<20ng/ml),尤其在小肝癌(<3cm)病患中,afp阴性的比率高达52%。所以在针对afp阴性肝癌(anhc)诊断中,只能仅仅依靠影像学。再者,影像学诊断往往结合多种方式,价格较为昂贵;对病患来说,影像学诊断也存在一定侵入性风险。而利用生物标志物在肝癌诊断中,较为安全、快捷、经济,且可以重复准确检测。因此,我们急需一种或者两种全新生物标志物来提高肝癌的早期诊断。
3.氨基酰化酶1(aminoacylase-1,acy1)是一种位于染色体3p21.1位置上的同源二聚体锌指结合酶,它主要分布在人源细胞的细胞核内。在非小细胞肺癌(sclc)细胞系以及肿瘤中,acy1的表达较少,这就说明该在非小细胞肺癌中,acy1很有可能是一个抑癌基因。高尔基蛋白73(gp73),也称高尔基膜蛋白1(golm1)或者高尔基磷酸化蛋白2(golph2),位于胆管上皮细胞,且在正常肝细胞是不表达的。只有当患者患有病毒性或者非病毒性肝病时,肝细胞的gp73才会大量表达。临床上常用elisa方法检测gp73。当血清gp73≥10u/ml(相对值)时,诊断肝细胞癌的敏感性为69%,特异性为75%。需要注意的是,gp73并不是一个肝细胞癌特异性标志物,它在肾细胞癌、前列腺癌中都有表达。同时,血清gp73升高不显著时,需与肝硬化相鉴别除此之外。目前也有很多研究表明,血浆中gp73浓度可以作为评估肝病,尤其是肝癌的指标之一。
4.因此,针对目前用于肝癌患者的肿瘤诊断方式单一、价格较为昂贵,且现有的生物分子标记物afp敏感度和特异性不足以辨别afp阴性肝癌或者小肝癌等现状,需要开发一类检测试剂盒,用来提示和诊断患者早期肝癌的进程,弥补afp阴性患者诊断手段缺失的状况,在一定程度上改善肝癌早期诊断困难,具有非常良好的临床应用价值。
技术实现要素:
5.针对现有肝癌的生物标志物afp灵敏度和特异性不足以完全筛选肝癌患者,肝癌早期的诊断方式较为匮乏。对此,本发明提供一种灵敏度和特异性更高的试剂盒,能够更为精准的发现潜在肝癌对象,为早期肝癌筛查提供一种方便、快捷、经济的方式。
6.本发明的技术方案如下:
7.本发明提供了生物分子标志物作为检测靶点在制备用于检测早期肝癌的试剂盒中的应用,所述生物分子标志物为acy1和gp73。
8.作为优选方案,检测的个体为生物标志物甲胎蛋白afp为阴性的个体。
9.作为优选方案,检测的个体为肝癌灶直径小于3cm的个体。
10.作为优选方案,生物标志物甲胎蛋白afp为阴性时,个体样本中生物标志物甲胎蛋白afp的浓度≤20ng/ml。
11.本发明还提供了一种用于检测早期肝癌的试剂盒,其通过检测个体样本中acy1和gp73的水平来确定个体是否为肝癌,所述试剂盒包括:
12.(1)能够结合acy1的抗体;
13.(2)当acy1结合于(1)中限定的抗体时,能够结合于(1)中限定的抗体或acy1的标记抗体;
14.(3)能够结合gp73的抗体;
15.(4)当gp73结合于(3)中限定的抗体时,能够结合于(3)中限定的抗体或gp73的标记抗体;
16.(5)由含有已知量acy1的溶液组成的标准样,以及由含有已知量gp73的溶液组成的标准样。
17.优选的,所述样本是血浆或者血清;(5)中作为标准样的acy1和gp73来源于基因工程细胞表达。
18.所述的试剂盒还包含引发剂溶液,如果将上述的(1)中限定的抗体称作acy1第一抗体,将上述的(2)中限定的标记抗体称作acy1第二抗体,将上述的(3)中限定的抗体称作gp73第一抗体,将上述的(4)中限定的标记抗体称作gp73第二抗体,所述引发剂溶液用于引发acy1第二抗体和gp73第二抗体上的标记物与分别作为标记物反应对象的化学发光化合物或显色底物或者荧光染料之间的化学反应;
19.其中,acy1第二抗体和gp73第二抗体上的标记物是过氧化物酶、磷酸酯酶或荧光素酶。
20.优选的,所述过氧化物酶为辣根过氧化物酶;acy1第一抗体和gp73第一抗体固定在不同的固相载体上,所述固相载体是选自下组的固体支持物:微孔板、试管、样品杯、塑料微球、纤维素、纸质或塑料试验条、胶乳粒子、二氧化硅粒子、磁性粒子。
21.作为优选方案,所述个体为生物标志物甲胎蛋白afp为阴性的个体。
22.作为优选方案,所述个体为肝癌灶直径小于3cm的个体。
23.本发明将acy1和gp73这两种生物标记物作为一个组合检测肝癌患者两种分子的抗体表达水平,利用两种分子的抗体表达水平筛查和诊断肝癌的进展程度,筛选低危风险对象,其检测灵敏度高达94.9%(即受试者为肝癌患者时,这两种分子表达水平联合预测确诊为肝癌的比率为94.9%),特异性达到了89.3%(即受试者为非肝癌患者时,这两种分子抗体表达水平联合预测为非肝癌患者的比率为89.3%),因此,本发明所述试剂盒具有较高的灵敏度和特异性,可用于早期肝癌的筛查和诊断,对早期病患进行及时的临床干预,一定程度上做到及早发现,提早对症治疗,降低不良预后比例,该试剂盒在临床上具有非常可观的指导意义。
24.与现有技术相比,本发明的有益效果:
25.(1)本发明将acy1和gp73这两种生物标记物作为一个组合检测肝癌患者两种分子的抗体表达水平,检测待确诊肝癌个体血浆中两种生物分子的表达水平,可以有效筛查肝癌早期患者,且该联合检测,对afp抗体表达阴性的个体也较为灵敏,其检测灵敏度为
94.9%,特异性达到89.3%。
26.(2)本发明制备的试剂盒可同时检测个体样品中两种与癌症发展相关的生物分子表达水平,与两种生物分子的单独检测相比,联合检测检出成功率高,结果重现性好,精准度高,成本低,方法便捷,在早期肝癌的筛查和诊断具有参考意义。
附图说明
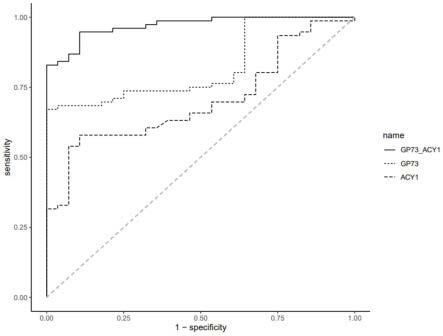
27.图1为试剂盒检测acy1和gp73表达水平,r语言计算后得出acy1,gp73或者两者联合的用于筛查和诊断肝癌患者的roc曲线。
28.图2为试剂盒检测acy1和gp73表达水平,r语言计算后得出acy1,gp73或者两者联合的用于筛查和诊断afp阴性肝癌患者的roc曲线。
29.图3为试剂盒检测acy1和gp73表达水平,r语言计算后得出acy1,gp73或者两者联合的用于筛查和诊断小肝癌的肝癌患者(<3cm)的roc曲线。
具体实施方式
30.下列实施例所述的实验方法,若无特殊说明,均为本技术领域常规技术,或按照生产厂商所建议条件;所用试剂、耗材和仪器未注明生产厂商者,均可通过购置获得。
31.本发明根据间接酶联免疫法制备了一种可用于筛查和诊断早期肝癌acy1和gp73联合检测的elisa试剂盒。间接酶联免疫法的原理是将相应抗体连接到固相载体上,样品中待测抗原与之结合成固相抗体-受检抗原复合物,再用酶标二抗与固相抗体-受检抗原复合物中结合,形成固相抗体-受检抗原-酶标二抗复合物,然后加底物,酶标检测底物反应后的显色程度,用来确定待测定样本中抗原的含量。
32.本发明研究得到浙江大学医学院附属第一医院科研伦理委员会同意,并遵循批准的指导方针和条例进行,批件号为(2018)科研快审第(768)号,实施例中所用血浆为浙江大学医学院附属第一医院提供。
33.实施例1:试剂盒的制备
34.1、实验材料及试剂
35.(1)两种与癌症发展相关抗体(anti-acy1和anti-gp73),购买于北京义翘神州科技股份有限公司;
36.(2)96孔酶标板:3590(costar,美国);
37.(3)包被液:pbs磷酸缓冲液(136.9mmol/l nacl,10.1mmol/l na2hpo4,2.7mmol/l kcl,1.8mmol/l kh2po4,ph 7.4,0.2μm过滤除菌);
38.(4)洗涤液:含0.05%(v/v)吐温20的pbs磷酸缓冲液;
39.(5)封闭液:含有2%(w/v)bsa的pbst磷酸缓冲液;
40.(6)样品稀释液:含有0.1%(w/v)bsa的pbst磷酸缓冲液;
41.(7)检测抗体稀释液:含有2%(w/v)bsa的pbst磷酸缓冲液;
42.(8)检测抗体:辣根过氧化物酶标记的reca蛋白(invitrogen);
43.(9)显色液a:0.02%(w/v)tmb,配制:取甲基联苯胺(tmb)0.005g,溶解于25ml去离子水;
44.(10)显色液b:0.006%(w/v)过氧化脲素,配制:取柠檬酸4.665g、na2hpo418.40g,
充分溶解于400ml去离子水中,加0.75%(w/v)过氧化脲素3.2ml,调整ph至5.0-5.5,加去离子水定容至500ml,混合均匀,于4℃保存;
45.(11)终止液:2mol/l硫酸;
46.(12)酶标仪:sid5(bd,美国)。
47.2、制备抗体包被的酶标板
48.(1)制备两种分子相关抗体溶液:将两种分子相关抗体以1:5000分别溶解于包被液种,充分混匀。
49.(2)包被酶标板:将制备好的两种分子抗体按照表1所示的布局分别加入到96孔酶标板的点样孔中,加样量为100μl/孔;空白对照孔加入包被液,4℃孵育过夜后去除孔板中液体,然后用洗涤液洗涤3次,每次洗涤3min。
50.表1
[0051] 123456789101112aacy1acy1acy1acy1acy1acy1acy1acy1acy1acy1acy1acy1bgp73gp73gp73gp73gp73gp73gp73gp73gp73gp73gp73gp73cacy1acy1acy1acy1acy1acy1acy1acy1acy1acy1acy1acy1dgp73gp73gp73gp73gp73gp73gp73gp73gp73gp73gp73gp73eacy1acylacy1acylacy1acy1acy1acy1acy1acy1acy1acy1fgp73gp73gp73gp73gp73gp73gp73gp73gp73gp73gp73gp73gacy1acy1acy1acy1acy1acy1acy1acy1acy1acy1acy1acy1hgp73gp73gp73gp73gp73gp73gp73gp73gp73gp73gp73gp73
[0052]
表1为本发明elisa试剂盒中96孔板酶标板的抗体包被布局表,其中,抗体名称代表该孔所包被抗体,用来检测待测血浆中相应抗原的表达水平。
[0053]
(3)封闭:向包被后的96孔酶标板的点样孔中加入封闭液(加样量为300μl/孔),室温孵育2h,然后去除封闭液,用洗涤液洗涤3次,每次洗涤3min。
[0054]
(4)干燥,包装:将封闭处理后的96孔酶标板放置干后,包装,得到抗体包被的96孔酶标板,4℃保存备用。
[0055]
3、本发明试剂盒的组成如下:
[0056]
(1)步骤2制备的抗体包被的96孔酶标板,4℃可保存一个月;
[0057]
(2)样品稀释液:含有0.1%bsa的pbst磷酸缓冲液,4℃保存;
[0058]
(3)检测抗体稀释液:含有2%bsa的pbst磷酸缓冲液,4℃保存;
[0059]
(4)检测抗体:辣根过氧化物酶标记的reca蛋白(invitrogen公司),4℃保存;
[0060]
(5)显色液:显色液有显示液a和显色液b组成,其中,显色液a为0.02%(w/v)tmb,显色液b为0.006%(w/v)过氧化脲素;使用时将显色液a和显色液b按照1∶1等体积混合均匀;
[0061]
(6)终止液:2mol/l的硫酸;
[0062]
(7)洗涤液:含0.05%吐温20的pbs磷酸缓冲液,4℃保存;
[0063]
(8)标准抗原蛋白:acy1为40ng,gp73为280ng,-80℃保存。
[0064]
试剂(2)-(8)分别包装后与抗体包被酶标板构成试剂盒。
[0065]
实施例2:试剂盒使用方法
[0066]
1、将所有待用试剂恢复至室温待用;
[0067]
2、acy1标准抗原蛋白标准曲线配备:
[0068]
(1)取样品稀释液1000μl加入acy1标准蛋白(北京义翘神州科技股份有限公司,货号:10549-h08b)中,轻柔的混合均匀,使其浓度为40ng/ml,记为s0;
[0069]
(2)取样品管6个,分别加入样品稀释液300μl,分别记为s1,s2,s3,s4,s5,s6;
[0070]
(3)从s0中取200μl至s1中,混合均匀后;再从s1中取200μl至s2,混合均匀;s3,s4,s5,s6依次稀释;再取一样品管加入500μl的样品稀释液,记为s7;
[0071]
则可以得到acy1标准蛋白的标准曲线,其具体浓度详见表2。
[0072]
表2
[0073]
样品名称s0s1s2s3s4s5s6s7浓度(ng/ml)40166.402.561.0240.4100.1640
[0074]
3、gp73标准抗原蛋白标准曲线配备:
[0075]
(1)取样品稀释液400μl加入gp73标准蛋白(北京义翘神州科技股份有限公司,货号:13066-h08h)中,轻柔的混合均匀,使其浓度为700ng/ml,记为s0;
[0076]
(2)取样品管6个,分别加入样品稀释液400μl,300μl,300μl,300μl,300μl,300μl分别记为s1,s2,s3,s4,s5,s6;
[0077]
(3)从s0中取100μl至s1中,混合均匀后;再从s1中取200μl至s2,混合均匀;再从s2中取200μl至s3,混合均匀;s4,s5,s6依次稀释;再取一样品管加入500μl的样品稀释液,记为s7;
[0078]
则可以得到gp73标准蛋白的标准曲线,其具体浓度详见表3。
[0079]
表3
[0080]
样品名称s0s1s2s3s4s5s6s7浓度(ng/ml)7001405622.48.963.5841.4340
[0081]
4、血浆样本准备
[0082]
将待检测血浆样本用样品稀释液稀释5倍,混合均匀;
[0083]
5、血浆样本和标准曲线孵育
[0084]
取稀释后的血浆样本和标准曲线样本分别置于包被抗体96孔酶标板的相应反应孔中,加样量为100μl/孔,置于室温孵育2.5h;弃去孔中液体,用洗涤液洗涤3次,每次300μl/孔,最后一次清洗,尽量将洗涤液去除干净;
[0085]
6、检测二抗孵育
[0086]
将辣根过氧化酶标记的reca蛋白用第二抗体稀释液按照1∶40000比例进行稀释,然后将稀释后的第二抗体加入相应96孔酶标板的反应孔中,加样量为100μl/孔,置于室温孵育1h;弃去孔中液体,用洗涤液洗涤3次,每次300μl/孔,最后一次清洗,尽量将洗涤液去除干净;
[0087]
7、显色及终止反应
[0088]
将显色液a和显色液b按照1∶1等体积混合均匀,然后将混合后的显色液迅速加入相应反应孔中,加样量为100μl/孔,置于室温孵育30min;孵育完成后,向反应孔中加入50μl终止液,轻轻摇匀,于20min内用酶标仪读取od450nm的光密度值。
[0089]
实施例3:运用试剂盒进行临床样本检测
[0090]
1、样本组成:76例肝癌患者血浆和28例健康人群血浆;
[0091]
2、实验方法:依照实施例2中试剂盒使用方法,对样本进行acy1和gp73含量进项检测;acy1和gp73以浓度平均值
±
标准差表示。roc曲线是用r(v.4.1.0)中proc绘制,用于评估不同生物标志物的诊断价值。
[0092]
3、结果分析
[0093]
(1)肝癌患者血浆中acy1的表达为7.48
±
2.91ng/ml,高于健康人群血浆中acy1表达5.48
±
1.61ng/ml,两组差异值p小于0.001;
[0094]
(2)肝癌患者血浆中gp73的表达为111.05
±
66.85ng/ml,高于健康人群血浆中acy1表达39.87
±
21.93ng/ml,两组差异值p小于0.001;
[0095]
(3)通过r语言分析,单独用acy1浓度作为诊断依据所得的roc曲线提示,曲线下面积(auc)为0.702,当acy1浓度截留至7.08ng/ml时,其用于诊断的敏感性和特异性性分别为57.9%和89.3%,见图1;
[0096]
(4)通过r语言分析,单独用gp73浓度作为诊断依据所得的roc曲线提示,曲线下面积(auc)为0.824,当acy1浓度截留至81.15ng/ml时,其用于诊断的敏感性和特异性性分别为67.1%和100%,见图1;
[0097]
(5)通过r语言分析,联合acy1和gp73浓度作为诊断依据所得的roc曲线提示,曲线下面积(auc)为0.970,其用于诊断的敏感性和特异性性分别为94.9%和89.3%,见图1。
[0098]
表4为运用r语言分析使用单独acy1、gp73以及联合使用acy1和gp73所得的诊断价值相关数值。
[0099]
表4
[0100][0101][0102]
实施例4:运用试剂盒进行临床样本检测
[0103]
1、样本组成:33例afp阴性(afp≤20ng/ml)肝癌患者血浆;
[0104]
2、实验方法:依照实施例2中试剂盒使用方法,对样本进行acy1和gp73含量进项检测;acy1和gp73以浓度平均值
±
标准差表示。roc曲线是用r(v.4.1.0)中proc绘制,用于评估不同生物标志物的诊断价值。
[0105]
3、结果分析:
[0106]
(1)afp阴性肝癌患者血浆中acy1的表达为6.88
±
2.73ng/ml;
[0107]
(2)afp阴性肝癌患者血浆中gp73的表达为82.60
±
70.04ng/ml;
[0108]
(3)通过r语言分析,单独用acy1浓度作为诊断依据所得的roc曲线提示,曲线下面
积(auc)为0.763,当acy1浓度截留至7.09ng/ml时,其用于诊断的敏感性和特异性性分别为67.7%和89.3%,见图2;
[0109]
(4)通过r语言分析,单独用gp73浓度作为诊断依据所得的roc曲线提示,曲线下面积(auc)为0.814,当acy1浓度截留至81.60ng/ml时,其用于诊断的敏感性和特异性性分别为66.7%和100%,见图2;
[0110]
(5)通过r语言分析,联合acy1和gp73浓度作为诊断依据所得的roc曲线提示,曲线下面积(auc)为0.974,其用于诊断的敏感性和特异性性分别为84.8%和100%,见图2。
[0111]
表5为运用r语言分析使用单独acy1、gp73以及联合使用acy1和gp73所得的诊断价值相关数值。
[0112]
表5
[0113]
生物分子敏感性特异性效能95%cip值acy10.6970.8930.8140.640-0.886<0.001gp7306671.0000.8140.705-0.923<0.001acy1_gp730.8481.0000.9740.943-1.000<0.001
[0114]
实施例5:运用试剂盒进行临床样本检测
[0115]
1、样本组成:33例小肝癌(<3cm)患者血浆;
[0116]
2、实验方法:依照实施例2中试剂盒使用方法,对样本进行acy1和gp73含量进项检测;acy1和gp73以浓度平均值
±
标准差表示。roc曲线是用r(v.4.1.0)中proc绘制,用于评估不同生物标志物的诊断价值。
[0117]
3、结果分析:
[0118]
(1)afp阴性肝癌患者血浆中acy1的表达为6.54
±
2.25ng/ml;
[0119]
(2)afp阴性肝癌患者血浆中gp73的表达为81.58
±
69.75ng/ml;
[0120]
(3)通过r语言分析,单独用acy1浓度作为诊断依据所得的roc曲线提示,曲线下面积(auc)为0.763,当acy1浓度截留至7.08ng/ml时,其用于诊断的敏感性和特异性性分别为61.8%和89.3%,见图3;
[0121]
(4)通过r语言分析,单独用gp73浓度作为诊断依据所得的roc曲线提示,曲线下面积(auc)为0.840,当acy1浓度截留至81.14ng/ml时,其用于诊断的敏感性和特异性性分别为70.6%和100%,见图3;
[0122]
(5)通过r语言分析,联合acy1和gp73浓度作为诊断依据所得的roc曲线提示,曲线下面积(auc)为0.954,其用于诊断的敏感性和特异性性分别为79.4%和100%,见图3。
[0123]
表6为运用r语言分析使用单独acy1、gp73以及联合使用acy1和gp73所得的诊断价值相关数值。
[0124]
表6
[0125]
生物分子敏感性特异性效能95%cip值acy10.6180.8930.7630.612-0.8610.001gp730.7061.0000.8400.738-0.943<0.001acy1_gp730.7941.0000.9540.907-1.000<0.001
[0126]
由图1-图3可知,acy1和gp73两种分子组合物联合筛查和诊断早期肝癌,在实施例3、实施例4和实施例5中,联合检测检出成功率高,精准度高,方便快捷,其诊断效能均优于
单个生物分子的诊断效能,在早期肝癌的筛查和诊断具有临床参考意义。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1