一种刺激响应型磁性SERS复合纳米探针及其制备方法和应用与流程
本发明属于医药,涉及一种刺激响应型磁性sers复合纳米探针及其制备方法和应用。
背景技术:
1、恶性肿瘤是严重危害全世界人类健康的重要疾病,循环肿瘤细胞(circulatingtumor cells,ctcs)是自发或者因诊疗操作由实体瘤亦或转移灶释放进入外周血循环系统中的肿瘤细胞,是引发肿瘤转移的必要条件,ctcs的监测对癌症的早期诊断、肿瘤的转移、预后及个体化治疗等方面有着重要意义。然而,ctcs在血液中数量极其稀少(1ml血液中仅有0-100个ctcs),如何从血液中分离并检测ctcs便是问题的关键。目前已有多种分离和检测方法,分离方法主要是基于ctcs的物理性质、免疫生物学方法和微流控技术,包括微孔滤膜、梯度密度离心、静电电场、免疫磁珠和侧向流体学分离等方法。而检测技术主要有流式细胞术、荧光光谱检测技术、pcr技术和电化学技术等。强生集团的系统是基于免疫磁珠的和流式细胞技术的分离检测系统,已经通过美国fda认证,但是该系统的灵敏度低、漏检率较高、造价昂贵、检测成本高,已于2015年年底停产。所以开发新的具有高检测灵敏度和低成本的新型检测技术十分必要。
2、表面增强拉曼散射(sers)技术因其具有超高的检测灵敏度而广受关注。sers是基于贵金属或金属化合物纳米结构的局域等离子共振,对拉曼信号显著增强的现象,可增强106-1010倍。sers光谱技术具有选择性好、灵敏度高、无光漂白、抗干扰、快速无损等优点,在环境分析和生物医学领域中有着广泛的应用。同样,分离富集技术在ctcs检测中至关重要,不仅因为可以提高检测的灵敏度,还可以利用富集的细胞进行溯源分析和药物筛选,有利于病发位置诊断和用药指导。在诸多分离方法中,免疫磁珠因其快速无损的分离而广被使用。例如,薛婷等人所开发的磁性sers纳米粒子,对ctcs进行快速分离和检测,其检测限可达到1cells/ml。所以将免疫磁性分离与sers技术相结合,可以实现ctcs的快速分离和高灵敏检测。但是,目前所报道的磁性sers纳米材料,多是利用晶体生长法或核壳结构将两种功能性纳米材料结合在一起,制备方法复杂繁琐、稳定性差、磁性或者sers信号大幅降低、检测模式单一等缺点。
技术实现思路
1、本发明针对现有技术中的不足,提供一种刺激响应型磁性sers复合纳米探针及其制备方法和应用。
2、本发明的一个目的在于提供一种刺激响应型磁性sers复合纳米探针,包括贵金属纳米粒子、磁性纳米粒子、拉曼信号分子、配体分子和有机构建单元。
3、作为优选,贵金属纳米粒子表面依次连接拉曼信号分子和配体分子,磁性纳米粒子表面连接配体分子,有机构建单元通过与配体分子结合,将贵金属纳米粒子和磁性纳米粒子自组装在一起形成自组装纳米结构。
4、作为优选,贵金属纳米粒子为金、银和铂族金属中的一种或多种。
5、作为优选,贵金属纳米粒子的粒径<1μm,进一步优选为1~500nm,可选地,贵金属纳米粒子的粒径为1、10、20、30、40、50、80、100、200、500nm中的任意一个值或任意两个值之间的范围值。
6、作为优选,贵金属纳米粒子的形貌包括但不限于球形、星形、片状、立方体、三角锥、棒形等形状中的一种或多种。
7、作为优选,所述磁性纳米粒子为磁性金属单质纳米粒子、磁性金属氧化物纳米粒子中的一种或多种;磁性金属单质包括但不限于fe、zn、co、ni、cr、mn中的一种或多种,磁性金属氧化物包括但不限于fe、co、ni、cr、mn中的一种或多种对应的氧化物中的一种或多种。
8、作为优选,磁性纳米粒子的粒径<1μm,进一步优选为1~500nm,可选地,磁性纳米粒子的粒径为1、10、20、30、40、50、80、100、200、500nm中的任意一个值或任意两个值之间的范围值。
9、作为优选,磁性纳米粒子的形貌包括但不限于球形、碟形、片状、立方体、三角型、棒形、花形等中的一种或多种。
10、作为优选,拉曼信号分子为在拉曼光谱中具有共轭振动的有机物,包括但不限于4-巯基苯甲酸、巯基吡啶、4-巯基苯胺、巯基萘、对氟硫酚、罗丹明、结晶紫、耐尔蓝等。
11、作为优选,有机构建单元为苯环羧酸类双巯基有机分子、蒽环羧酸类双巯基有机分子、萘环羧酸类双巯基有机分子中的一种或多种。可以举例为3,5-二巯基苯甲酸(如下b1所示)、2,5-二巯基对苯二甲酸(如下b2所示)、3,5-双(巯基甲基)苯甲酸(如下b3所示)、3,7-二巯基-2-萘甲酸(如下b4所示)、6,6'-双巯基-3,3'-甲叉基二苯甲酸(如下b5所示)等。
12、
13、作为优选,有机构建单元的分子量为60~10000da。
14、作为优选,配体分子为季铵盐类分子、吡啶盐类分子、氨基类分子中的一种或多种,配体分子连接在纳米粒子表面,使得表面带正电荷。
15、作为优选,季铵盐类分子为烷基季铵盐,吡啶盐类分子为烷基吡啶盐。
16、作为优选,烷基季铵盐具有如下式i或式ii所示的结构式:
17、
18、其中,x为卤族元素,n为1~30的整数。
19、作为优选,x为cl、br、i中的一种。
20、作为优选,烷基吡啶盐具有如下式iii或式iv所示的结构式:
21、
22、其中,x为卤族元素,n为1~30的整数。
23、作为优选,x为cl、br、i中的一种。
24、作为优选,所述磁性sers复合纳米探针还包括靶分子。
25、作为优选,靶分子连接在有机构建单元表面。
26、作为优选,靶分子为能与癌细胞表面抗原或受体发生特异性结合的抗体或配体,所述癌细胞可以为乳腺癌、肺癌、肝癌、食管癌等;作为优选,所述靶分子为多肽类物质或非多肽类物质,多肽类物质可列举为单克隆抗体(如epcam抗体、cd44抗体),非多肽类物质可列举为叶酸、半乳糖胺。
27、作为优选,所述磁性sers纳米探针粒径为5~10000nm。
28、作为优选,贵金属纳米粒子、磁性纳米粒子、拉曼信号分子、配体分子、有机构建单元和靶分子的质量比为1~1200:1~1200:1~2000:0.01~300:0.01~500:0.01~300。
29、本发明的另一个目的在于提供上述刺激响应型磁性sers复合纳米探针的制备方法,包括以下步骤:
30、(1)将拉曼信号分子溶液加入贵金属纳米粒子溶液中,搅拌反应,然后加入配体分子溶液继续搅拌反应;
31、(2)将配体分子溶液与磁性纳米粒子溶液搅拌反应;
32、(3)将包括步骤(1)的产物和步骤(2)的产物的混合物加入有机构建单元溶液中搅拌反应,获得自组装纳米结构;
33、(4)自组装纳米结构或靶分子溶液经催化剂活化后,将活化或未活化自组装纳米结构和活化或未活化靶分子溶液混合搅拌反应,得到刺激响应型磁性sers复合纳米探针。
34、步骤(1)中,拉曼信号分子溶液为拉曼信号分子溶于溶剂中形成,但凡能溶解拉曼信号分子的溶剂均可,如水、乙醇等,拉曼信号分子溶液浓度不作限制;贵金属纳米粒子溶液为贵金属纳米粒子分散于水中形成,贵金属纳米粒子溶液浓度不作限制;配体分子溶液为配体分子溶于溶剂中形成,但凡能溶解配体分子的溶剂均可,如水、乙醇等,配体分子溶液浓度不作限制。
35、作为优选,步骤(1)中,搅拌反应和继续搅拌反应的温度为5~40℃,优选为室温条件下进行,搅拌反应的反应时间为5~30min,继续搅拌反应的反应时间为1~20h,进一步优选为1~10h。
36、贵金属纳米粒子的制备方法可以列举如下这些:
37、a)金纳米球制备方法:1)柠檬酸三钠还原制备金纳米球,将氯金酸水溶液加热至沸,再加入柠檬酸三钠水溶液,反应一定时间后,制得金纳米球;或者将氯金酸和柠檬酸三钠的水溶液混合,加热至沸,反应一定时间后制得金纳米球。2)硼氢化钠还原制备金纳米球,将硼氢化钠的水溶液加至氯金酸的水溶液中,待反应一定时间后,制得金纳米球。3)柠檬酸还原制备金纳米球,将柠檬酸的水溶液加至氯金酸的水溶液中,待反应一定时间后,制得金纳米球。4)草酸钠还原制备金纳米球,将草酸钠的水溶液加至氯金酸的水溶液中,待反应一定时间后,制得金纳米球。5)没食子酸还原制备金纳米球,将没食子酸的水溶液加至氯金酸的水溶液中,待反应一定时间后,制得金纳米球。6)抗坏血酸还原制备金纳米球,将抗坏血酸的水溶液加至氯金酸的水溶液中,待反应一定时间后,制得金纳米球。7)水合肼还原制备金纳米球,将水合肼的水溶液加至氯金酸的水溶液中,待反应一定时间后,制得金纳米球。8)葡萄糖酸钠还原制备银纳米球,将葡萄糖酸钠的水溶液加至氯金酸的水溶液中,待反应一定时间后,制得金纳米球。9)葡聚糖还原制备银纳米球,将葡聚糖的水溶液加至氯金酸的水溶液中,待反应一定时间后,制得金纳米球。
38、b)金纳米棒的制备方法:利用金种生长法制备金纳米棒,1)金种制备:使用柠檬酸三钠或者硼氢化钠还原氯金酸制得金种;2)生长液准备,将十六烷基三甲基溴化铵(hexadecyl trimethyl ammonium bromide,ctab)与硝酸银混合,再加入氯金酸,混合均匀后加入抗坏血酸;3)把1)所述的金种加入到2)述生长液中,待反应一定时间后,制得金纳米棒。
39、c)金纳米星的制备方法:利用金种生长法制备金纳米星,1)金种制备:使用柠檬酸三钠或者硼氢化钠还原氯金酸制得金种;2)生长液准备,将十六烷基三甲基溴化铵与硝酸银混合,再加入氯金酸,混合均匀后加入抗坏血酸;3)把1)所述的金种加入到2)生长液中,待反应一定时间后,制得金纳米星。
40、d)银纳米球的制备方法:1)硼氢化钠还原制备银纳米球,将硼氢化钠的水溶液加至硝酸银的水溶液中,待反应一定时间后,制得银纳米球。2)柠檬酸还原制备银纳米球,将柠檬酸的水溶液加至硝酸银的水溶液中,待反应一定时间后,制得银纳米球。3)柠檬酸三钠还原制备银纳米球,将柠檬酸三钠的水溶液加至硝酸银的水溶液中,待反应一定时间后,制得银纳米球。4)抗坏血酸还原制备银纳米球,将抗坏血酸的水溶液加至硝酸银的水溶液中,待反应一定时间后,制得银纳米球。5)水合肼还原制备银纳米球,将水合肼的水溶液加至硝酸银的水溶液中,待反应一定时间后,制得银纳米球。
41、e)银纳米三角片的制备方法:将柠檬酸三钠水溶液、聚乙烯吡咯烷酮水溶液、硝酸银水溶液、过氧化氢混合均匀,再加入硼氢化钠水溶液,反应一定时间后避光,待避光一段时间后,制得银纳米三角片。
42、f)金@银纳米球的制备方法:利用金种生长法制备金@银纳米球,1)金种制备:使用柠檬酸三钠或者硼氢化钠还原氯金酸制得金种;2)生长液准备,将十六烷基三甲基溴化铵(ctab)与硝酸银混合均匀后加入抗坏血酸;3)把1)所述的金种加入到2)所述生长液中,待反应一定时间后,制得金@银纳米球。
43、g)银@金纳米球的制备方法:利用金种生长法制备银@金纳米球,1)金种制备:使用柠檬酸三钠或者硼氢化钠还原硝酸银制得银种;2)生长液准备,将十六烷基三甲基溴化铵(ctab)与硝酸银混合,再加入氯金酸水溶液,混合均匀后加入抗坏血酸;3)把1)所述的银种加入到2)所述生长液中,待反应一定时间后,制得银@金纳米球。
44、步骤(2)中,配体分子溶液同步骤(1)中,磁性纳米粒子溶液为磁性纳米粒子分散于水中形成,磁性纳米粒子溶液浓度不作限制。
45、作为优选,步骤(2)中,搅拌反应的温度为5~40℃,优选为室温条件下进行,反应时间为0.1~20h,进一步优选为1~10h。
46、磁性纳米粒子的制备方法可以列举如下这些:
47、a)非水相法:铁的有机金属化合物或配合物(五羰基铁、乙酰丙酮铁、油酸铁等)在高沸点溶剂和配体(如油酸和油胺)及还原剂的存在下,将反应混合物加热到250℃以上。最终的纳米粒子尺寸由温度和加热时间长短决定。使用这种方法可以密切控制纳米粒子的尺寸分布,同时也能获得较高结晶度的纳米粒子。这种方法已被证明是非常通用的,并扩展到不同性质的铁氧体纳米粒子(mfe2o4,m=mn、co、ni、zn)和其他磁性材料如fept的制备中。热分解法的主要缺点是,所获得的纳米粒子通常仅溶于非极性溶剂,因此必须在纳米粒子成核生长稳定之前通过中间配体引入功能化官能团。
48、b)水相法:1)微乳液法:在表面活性剂的作用下两种不相溶的溶剂形成均匀的微乳液,在获得纳米粒子的同时,纳米粒子的成核、生长避免了粒子之间的团聚。2)溶胶-凝胶法:溶胶-凝胶法是一种湿法制备金属氧化物的方法,溶胶-凝胶法一般是用氯化铁、硝酸铁为原料,一定温度下在水或醇中溶解,并加入定量碱(或氨水)和用于改性的表面活性剂,通过调节溶液的ph值使反应液成胶体,经过干燥、煅烧等步骤最后获得氧化铁纳米粒子。3)共沉淀法:共沉淀法是指在多组分的溶液中,将两种或更多的阳离子在沉淀剂的存在下同时沉淀出来的过程。用这种方法制备磁性纳米粒子是根据溶度积的原理,以沉淀反应为基础,在含有特定比例的阳离子溶液中,加入适当的沉淀剂后所形成的纳米粒子。其优点是反应原理简单,设备原料低廉,适合批量生产。但缺点是不易得到高质量的单分散胶体,而且通常饱和磁化强度较低。例如,使用共沉淀法制备铁氧化物(fe3o4或γ-fe2o3),在惰性气体保护氛围中,通过向一定比例的fe2+/fe3+盐溶液中加入沉淀剂,在室温或提供温度时即可获得纳米粒子。4)水热法和溶剂热法:水热反应是在高压釜中进行的。在高温高压下,反应物在水做溶剂的密闭的体系中反应,最终得到所需产物。5)化学还原法:采取金属还原法,原料可以是金属氯化物、硝酸盐、乙酰丙酮盐,还原剂选取超氢锂或硼氢化钠,此外还有一些有机还原剂如多醇、水合肼和双氢气体等。化学还原法可根据反应体系的不同分为水溶液法和有机溶液法。
49、步骤(3)中,有机构建单元溶液为有机构建单元溶于溶剂中形成,但凡能溶解有机构建单元的溶剂均可,如pbs缓冲液、水、乙醇等,有机构建单元溶液浓度不作限制。作为优选,有机构建单元溶液的ph为7.2~7.8。作为优选,有机构建单元溶液为有机构建单元溶于pbs缓冲液中形成,pbs缓冲液的ph为7.2~7.8。
50、作为优选,步骤(3)中,搅拌反应的温度为5~40℃,优选为室温条件下进行,反应时间为5~80h,进一步优选为10~70h。
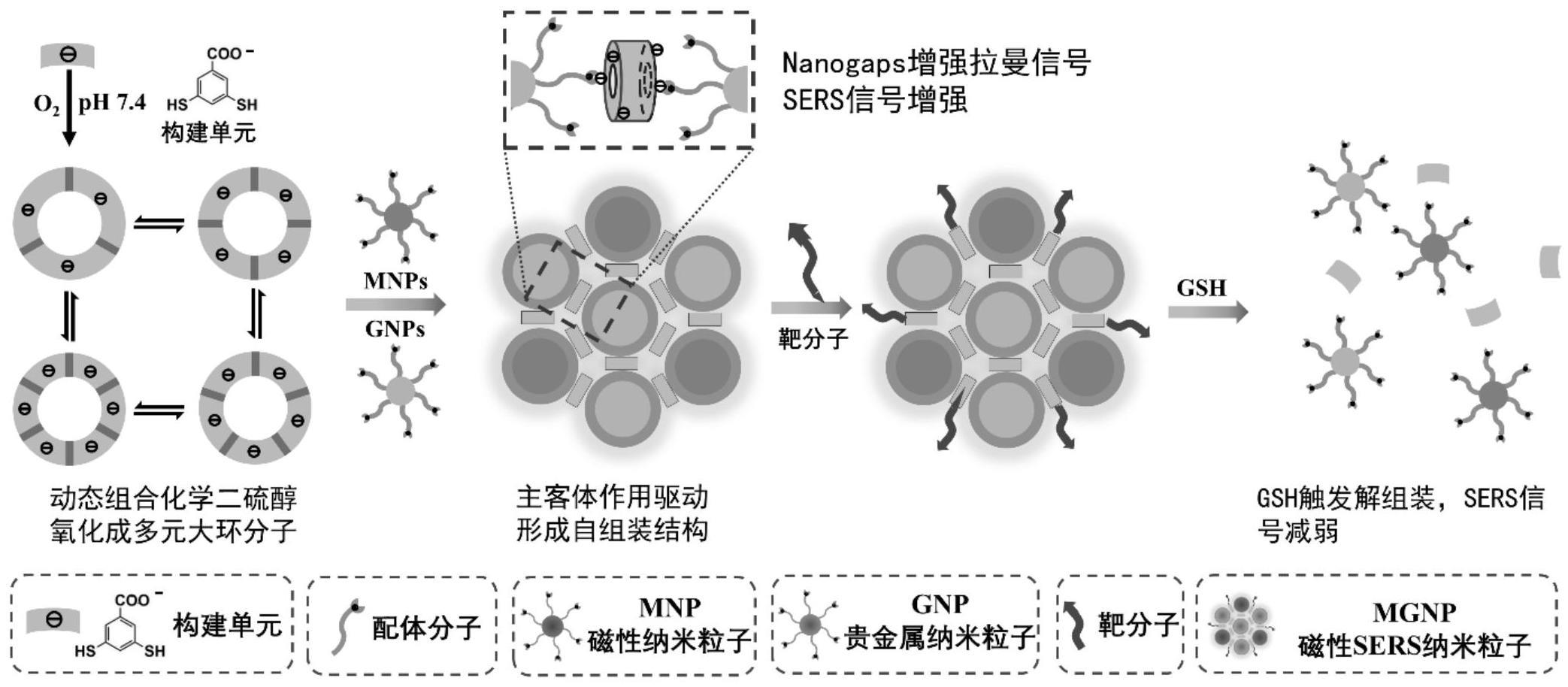
51、步骤(3)中,有机构建单元中的“-sh”通过空气和水中氧气的氧化作用形成“s-s”的动态共价键形成动态组合化学库,通过“s-s”的动态交换形成动态环状分子,配体分子与动态环状分子在非共价作用力(包括主客体相互作用、静电相互作用、氢键相互作用、π-π共轭相互作用、疏水相互作用、偶极相互作用力、范德华相互作用力等非共价相互作用)驱动下,将贵金属纳米粒子和磁性纳米粒子自组装在一起形成自组装纳米结构。因为该动态组合化学是热力学控制体系,也就是说某动态组合库达到热力学平衡时,这个体系中各组分处于热力学最低能量状态,也更加稳定。因此,该种基于动态组合化学的自组装方法的复合纳米材料更加稳定。在某一条件或者物质触发下,热力学平衡被打破,动态环状分子结构被破坏,进而使得自组装纳米结构解组装,实现刺激响应型解组装。
52、步骤(4)中,靶分子溶液为靶分子溶于溶剂中形成,但凡能溶解靶分子的溶剂均可,如水、乙醇等,靶分子溶液浓度不作限制。
53、步骤(4)中,催化剂活化自组装纳米结构或靶分子溶液,取决于:当自组装纳米结构材料含有羧基时,可以选择含有氨基的靶分子,然后用催化剂活化自组装纳米结构表面的羧基,再滴加含有氨基的靶分子溶液,使活化的羧基与靶分子的氨基共价反应形成稳定的酰胺键;当自组装纳米结构材料含有氨基时,可以选择含有羧基的靶分子,然后采取以上方法活化靶分子的羧基后使之嫁接于自组装纳米结构材料表面。
54、作为优选,步骤(4)中的催化剂为1-乙基-(3-二甲基氨基丙基)碳二亚胺(edc)、n-羟基琥珀酰亚胺(nhs)、含叠氮基团的化合物、多巴胺中的一种或多种。
55、作为优选,步骤(4)的活化在避光条件下进行,活化时间为1~20h。
56、作为优选,步骤(4)中,搅拌反应温度为5~40℃,优选为室温条件下进行,反应时间为5~40h,进一步优选为8~30h。
57、步骤(1)-(4)中的搅拌速度不作限定,可以列举为100~1000rpm。
58、本发明的另一个目的在于提供上述磁性sers复合纳米探针在体外检测中的应用。
59、作为优选,所述应用包括以下步骤:将上述磁性sers复合纳米探针加入到待测体系,上述磁性sers复合纳米探针与待测体系中的目标物结合,经过磁分离,再通过拉曼光谱检测,确定待测体系中目标物浓度。
60、在健康的人体血中的单核细胞表面不表达或很少量表达特异性抗原或受体,不能吸附或摄取上述磁性sers复合纳米探针,故不可在磁场中分离富集,也检测不到sers信号;而癌症患者血液内含有癌细胞,癌细胞高度表达特异性抗原或受体,故肿瘤细胞可吸附或摄取上述磁性sers复合纳米探针,可在磁场中分离富集并检测到sers信号,从而达到高灵敏检测癌细胞的目的。
61、另外,为避免癌症患者体内单核细胞(如白细胞等)的干扰,在不同时间点测试探针标记的癌细胞的sers信号,在癌细胞内gsh的触发下,磁性sers复合纳米探针解组装,sers信号明显降低,而白细胞内磁性sers复合纳米探针无法解组装,sres信号不变,因此通过不同时间点sers信号的比值,进一步提高ctcs检测灵敏度。
62、作为优选,待测体系包括但不限于血液、培养液、腹腔水、尿液等。
63、与现有技术相比,本发明具有以下有益效果:
64、1、本发明的刺激响应型磁性sers复合纳米探针包括贵金属纳米粒子、磁性纳米粒子、拉曼信号分子、配体分子和有机构建单元;磁性纳米粒子可在磁场中完成对肿瘤细胞的富集分离,贵金属纳米粒子对拉曼信号有显著的增强作用,通过拉曼光谱测试完成对肿瘤细胞的检测计数;贵金属纳米粒子表面依次连接拉曼信号分子和配体分子,磁性纳米粒子表面连接配体分子,有机构建单元通过与配体分子结合,将贵金属纳米粒子和磁性纳米粒子自组装在一起形成自组装纳米结构;
65、2、本发明的有机构建单元苯环羧酸类双巯基有机分子、蒽环羧酸类双巯基有机分子、萘环羧酸类双巯基有机分子中的一种或多种,有机构建单元中的“-sh”,可以通过空气和水中氧气的氧化作用形成“s-s”的动态共价键,通过“s-s”的动态交换形成动态环状分子,配体分子与动态环状分子在非共价作用力驱动下,将贵金属纳米粒子和磁性纳米粒子自组装在一起形成自组装纳米结构;
66、3、本发明的刺激响应型磁性sers复合纳米探针还包括偶联在自组装纳米结构表面的靶分子,提高自组装纳米结构对肿瘤细胞的靶向性能,提高纳米探针与肿瘤细胞的特异性结合;
67、4、本发明的刺激响应型磁性sers复合纳米探针在某一条件或者物质触发下,热力学平衡被打破,动态环状分子结构被破坏,进而使得自组装纳米结构解组装,sers信号明显降低,因此通过不同时间点sers信号的比值,进一步提高肿瘤细胞检测灵敏度;
68、5、本发明以贵金属纳米粒子和磁性纳米材料为基础,基于动态组合化学的自组装方法,发展合成简单、稳定性好、分离效果好、灵敏度高、特异性好的刺激响应型磁性sers复合纳米探针,为高性能肿瘤细胞检测方法与器件的研究提供理论与技术依据,并解决癌病诊断和预后等相关重要问题。
- 还没有人留言评论。精彩留言会获得点赞!