一种临床微生物单细胞耐药性检测仪器
1.本实用新型涉及微生物检测技术领域,尤其涉及一种临床微生物单细胞耐药性检测仪器。
背景技术:
2.临床上传统的致病菌耐药性的检测主要是通过培养法,该方法存在检测时间长、对实验操作人员专业要求高,而且容易出现假阳性等缺点。目前,遏制耐药性的蔓延不仅需要研发新型的抗生素,还需要研发耐药性快检检测仪器和方法,以提高现有抗生素使用的针对性和有效性,从而推迟与遏制耐药性的传播。目前,最有前景的方向之一是“单细胞”耐药检测技术,即跳过细胞培养增殖,直接针对样品中原有单细胞的“生长”或“代谢”表型、进行单细胞精度的表征,从原理上实现快速、基于表型、适用范围广的目标。
3.拉曼光谱是一种高效的信息识别技术,通过对特定入射光线对化合物的非弹性散射谱线分析,拉曼显微光谱可以直接检测化合物分子振动或转动能级。通过对拉曼特征谱线的分析,可以获得化合物分子构成和结构的信息。而现有使用拉曼光谱检测技术的仪器对临床微生物单细胞进行耐药性检测,仅能实现干片检测,无法检测液相中静止及流动状态下的微生物样品。
技术实现要素:
4.针对上述问题,本实用新型的目的是提供一种临床微生物单细胞耐药性检测仪器,对临床微生物单细胞进行耐药性检测,能够实现干片及液相中静止及流动状态下的微生物样品的耐药性检测。
5.为实现上述目的,本实用新型采取以下技术方案:
6.一种临床微生物单细胞耐药性检测仪器,包括电动位移平台、光镊模块、成像模块、激发光模块、显微聚焦模块、拉曼主光路及传输模块、同轴照明模块、自动采集控制模块;
7.所述电动位移平台,用于放置样品芯片;
8.所述光镊模块,用于捕获样品芯片中在液相状态下的待测细胞,并锁定所述待测细胞;
9.所述成像模块,用于拍摄样品芯片的全景信息,且配合所述电动位移平台快速定位所述样品芯片上的所述待测细胞,确定所述待测细胞的采集位置;
10.所述激发光模块,用于发射激光;
11.所述显微聚焦模块,用于将激光自动聚焦到采集位置处的所述待测细胞,使所述待测细胞产生拉曼信号;
12.所述拉曼主光路及传输模块,用于获取所述待测细胞的拉曼光谱;
13.所述同轴照明模块,用于为所述显微聚焦模块提供同轴照明光;
14.所述自动采集控制模块,与所述激发光模块、所述拉曼主光路及传输模块、所述显
微聚焦模块、所述同轴照明模块、所述成像模块、所述光镊模块和所述电动位移平台控制连接。
15.优选地,所述激发光模块包括第一激光器、第一电动快门、第一扩束镜、电动可调衰减器和第一反射镜;所述显微聚焦模块包括显微物镜;所述拉曼主光路及传输模块包括分光镜、第一二向色镜、第二透镜,针孔、光谱仪和探测器;
16.所述第一激光器发出的激光依次经过所述第一电动快门、第一扩束镜、电动可调衰减器和第一反射镜经分光镜和第一二向色镜经显微物镜聚焦待测细胞产生拉曼光谱,拉曼光谱经第一二向色镜、分光镜、第二透镜、针孔及光谱仪后发送到探测器,实现待测细胞拉曼信息的采集,上述光路为拉曼光路。
17.优选地,所述同轴照明模块包括led光源和半透半反镜;所述成像模块包括ccd 相机和第一透镜;
18.所述led光源发出的白光经半透半反镜反射进入所述显微聚焦模块照亮待测细胞,携带所述待测细胞图像信息的反射光进入所述成像模块,获取样品芯片图像信息,上述光路为成像光路。
19.优选地,所述光镊模块包括第二激光器,第二电动快门,第二衰减器,第二扩束镜、第二反射镜和第二二向色镜;
20.所述第二激光器发出的激光经过第二电动快门,第二衰减器,第二扩束镜、第二反射镜和第二二向色镜经过显微物镜后捕获住细胞,获取液相状态下细胞的图像信息,上述光路为光镊光路。
21.优选地,所述自动化微生物拉曼耐药性快速检测仪器包括四种光路组合:
22.成像光路,用于获取待测细胞的图像信息;
23.成像光路-拉曼光路,用于实现待测细胞拉曼信息的采集;
24.光镊光路-成像光路,用于获取液相状态下细胞的图像信息;
25.光镊光路-拉曼光路,用于实现液相状态下细胞拉曼信息的采集。
26.优选地,所述拉曼主光路及传输模块和所述成像模块交汇处设置有所述分光镜,所述光镊模块和所述拉曼主光路及传输模块交汇处设置有二向色镜,通过控制所述分光镜和/或所述二向色镜的移动切换成像光路、成像光路-拉曼光路、光镊光路-成像光路和光镊光路-拉曼光路。
27.优选地,该检测仪器还包括灭菌模块,用于消除环境中的微生物,防止交叉污染。
28.优选地,所述激发光模块、所述拉曼主光路及传输模块、所述同轴照明模块、所述成像模块和光镊模块固定在光学箱体内部,所述光学箱体为全封闭结构。
29.本实用新型由于采取以上技术方案,其具有以下优点:
30.1、本实用新型提供的临床微生物单细胞耐药性检测仪器,结合光镊模块实现了干片、液相中静止及流动状态下微生物样品的快速耐药性检测。
31.2、本实用新型提供的临床微生物单细胞耐药性检测仪器,具有多种工作模式,实现细胞成像、拉曼检测、细胞光镊捕获,满足不同需求的耐药性检测。
32.3、本实用新型提供的临床微生物单细胞耐药性检测仪器,光学箱体一体化铸造,全封闭设计,避光性好,防止细菌污染,能够大幅度提高仪器稳定性,保证单细胞检测结果的准确性。
附图说明
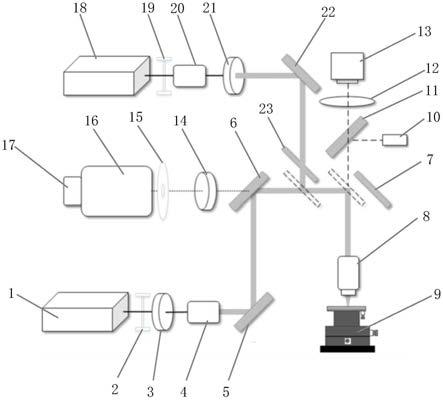
33.图1为本实用新型实施例1提供的检测仪器的光路示意图;
34.图2为本实用新型一实施例提供的检测仪器的光学箱体结构示意图;
35.图3为本实用新型一实施例提供的细胞定位示意图;
36.图4为本实用新型一实施例的不同浓度重水培养基中幽门螺旋杆菌单细胞拉曼图谱变化示意图。
具体实施方式
37.为使本实用新型的目的、技术方案和优点更加清楚,下面将结合附图对本实用新型的技术方案进行清楚、完整地描述。显然,所描述的实施例是本实用新型一部分实施例,而不是全部的实施例。基于本实用新型中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本实用新型保护的范围。
38.在本实用新型的描述中,需要说明的是,术语“上”、“下”、“前”、“后”等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本实用新型和简化描述,而不是指示或暗示所指的系统或组件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本实用新型的限制。
39.在本实用新型的描述中,需要说明的是,除非另有明确的规定和限定,术语“装配”、“设置”、“连接”应做广义理解,例如,可以是固定连接,也可以是可拆卸连接,或一体地连接;可以是机械连接,也可以是电连接;可以是直接相连,也可以通过中间媒介间接相连,可以是两个组件内部的连通。对于本领域的普通技术人员而言,可以具体情况理解上述术语在本实用新型中的具体含义。
40.本实用新型提供的临床微生物单细胞耐药性检测仪器,对临床微生物单细胞进行耐药性检测,通过激发光模块、显微聚焦模块、拉曼主光路及传输模块、同轴照明模块、成像模块、光镊模块、电动位移平台、自动采集控制模块的相互配合,实现干片及液相中静止及流动状态下自动化的微生物样品的快速耐药性检测。
41.下面,结合附图对本实用新型实施例提供的临床微生物单细胞耐药性检测仪器进行详细的说明。
42.实施例
43.如图1所示,本实施例提供的临床微生物单细胞耐药性检测仪器,包括电动位移平台、光镊模块、成像模块、激发光模块、显微聚焦模块、拉曼主光路及传输模块、同轴照明模块、自动采集控制模块;
44.电动位移平台,用于放置样品芯片;
45.光镊模块,用于捕获样品芯片中在液相状态下的待测细胞,并锁定待测细胞;
46.成像模块,用于拍摄样品芯片的全景信息,获得各细胞的位置信息,形成每个细胞与预设细胞对比所得的位置矫正信息,配合电动位移平台快速定位样品芯片上的待测细胞,确定待测细胞的采集位置;
47.激发光模块,用于发射激光;
48.显微聚焦模块,用于将激光自动聚焦到采集位置处的待测细胞,使待测细胞产生拉曼信号;
49.拉曼主光路及传输模块,用于获取待测细胞的拉曼光谱,并向自动采集控制模块传输细胞的拉曼光谱信息;
50.同轴照明模块,用于为显微聚焦模块提供同轴照明光;
51.自动采集控制模块,与激发光模块、拉曼主光路及传输模块、显微聚焦模块、同轴照明模块、成像模块、光镊模块和电动位移平台控制连接。
52.该实施例中,激发光模块包括第一激光器1、第一电动快门2、电动可调衰减器3、第一扩束镜4、和第一反射镜5;显微聚焦模块包括物镜转盘,显微物镜8;电动位移平台为三维电动位移平台9;拉曼主光路及传输模块包括分光镜7、第一二向色镜6、第二透镜14,针孔15、光谱仪16和探测器17;灭菌模块包括紫外灯。
53.第一激光器1发出的激光依次经过第一电动快门2、第一扩束镜4、电动可调衰减器3和第一反射镜5经分光镜7和第一二向色镜6经显微物镜8聚焦待测细胞产生拉曼光谱,拉曼光谱经第一二向色镜6、分光镜7、第二透镜14、针孔15及光谱仪16 后发送到探测器17,实现待测细胞拉曼信息的采集,上述光路为拉曼光路。
54.更具体地,第一激光器1可以为532nm或633nm或785nm或1064nm单纵模固体激光器,用于作为激发拉曼信号的激光源;电动快门2可电动控制开和关,用于控制第一激光器1在光路中的物理通断;第一扩束镜3的扩束比例为3:1或4:1或5:1;电动可调衰减器4具有不同衰减率,可通过自动采集控制模块调整衰减效果;衰减效果为10%、20%、30%、40%、50%、60%、70%、80%、90%,实现对第一激光器1发出的激光进行不同比例的衰减;第一反射镜5用于对第一激光器1发出的激光进行45 度转折。
55.更具体地,显微物镜8装于物镜转盘上,用于对激光进行聚焦、便于待测样品成像;物镜转盘为4孔或5孔或6孔电动或手动物镜转盘,物镜转盘用于切换不同倍率或不同na值的物镜;显微物镜8可以为4倍、10倍、50倍或100倍复/半复消色差物镜或水浸物镜;三维电动位移平台9用于放置待测样品芯片,可通过自动采集控制模块控制三轴移动;三维电动位移平台9上装有样品夹,待测样品放置于样品夹中,可通过自动采集控制模块控制三维移动,运动的最小步进值为0.1μm,运动过程中的重复定位精度为0.5μm,三维电动位移平台9和光学箱体30的左、右、后三组支撑架安装在同一块光学底板上。
56.更具体地,分光镜7为宽带反射镜,分光镜7安装在一维电动位移台上,用于将分光镜7移入或移出显微物镜8和半透半反镜11之间的光轴,分光镜7带宽范围覆盖第一激光器1的激发光和第二激光器18激发光,且反射率高于90%;分光镜7也可以为全反镜,全部反射拉曼信号。第一二向色镜6为高通低反镜,第一二向色镜6与光轴成45度夹角,其作用是使拉曼激发激光。例如,使532nm的激光反射并且使高于532nm的拉曼信号透射,反射率和透射率均高于90%。第二透镜14的作用是将透射回来的拉曼信号光聚焦于针孔15的小孔处;针孔15具有不同尺寸,可通过自动采集控制模块进行调节,防止显微镜焦平面以外不需要的信号抵达探测器,起到空间滤波的作用,提高仪器的空间分辨率,用于在共焦情况下阻挡杂散光的信号。光谱仪16 为光栅光谱仪,可配备不同刻线的光栅,从而对拉曼光进行不同程度的分光,分光后的拉曼信号成像由探测器17接收。探测器17为线阵或者面阵ccd或emccd,配合光谱仪16可获得不同分辨率的拉曼散射光的信号。
57.该实施例中,同轴照明模块包括led光源10和半透半反镜11,所述成像模块包括ccd相机和第一透镜;成像模块包括ccd相机13、第一透镜12。
58.更具体地,led光源10发出的白光经半透半反镜11反射进入所述显微聚焦模块照亮待测细胞,携带所述待测细胞图像信息的反射光进入所述成像模块,获取样品芯片图像信息,上述光路为成像光路。
59.更具体地,led光源10为显微照明光源,其出射的白光已经过准直;半透半反镜11为与光轴成45度放置,透反比为1:1,半透半反镜11可以将白光反射进入显微物镜8,细胞的白光成像可反射进入显微物镜8从而透过半透半反镜11。
60.更具体地,由显微物镜8收集反射回来的图像信号透过半透半反镜11进入第一透镜12进而聚焦到ccd相机13中。
61.该实施例中,光镊模块包括第二激光器18,第二电动快门19,第二衰减器20,第二扩束镜21、第二反射镜22、第二二向色镜23。
62.第二激光器18发出的激光经过第二电动快门19,第二衰减器20,第二扩束镜21、第二反射镜22和第二二向色镜23经过显微物镜8后捕获住细胞,获取液相状态下细胞的图像信息,上述光路为光镊光路。
63.更具体地,第二激光器18为1064nm固体激光器,最大功率为2w,用于产生光镊力的激光源;电动快门19可电动控制开和关,用于控制第二激光器18在光路中的物理通断;第二扩束镜21的扩束比例为3:1或4:1或5:1,对1064nm激光的透过率大于85%;第二衰减器20具有不同衰减率,可通过自动采集控制模块调整衰减效果;衰减效果为10%、20%、30%、40%、50%、60%、70%、80%、90%;第二反射镜22 放置于第二扩束镜21之后,与主光轴呈45度,用于对扩束后的激光进行45转折;第二二向色镜23安装在一维电动位移平台上,与光轴成45度夹角,第二二向色镜23 的截止波长大于第一激光器1激发激光的波长100nm以上,且1064nm的反射率高于 90%。第二二向色镜23与光轴成45度,可以把第二反射镜22转折过来的1064nm激光反射到分光镜7进入显微物镜8;可电动控制一维电动位移平台使二向色镜23离开主光路,从而获取最优的拉曼信号;分光镜7也可以被固定的一维电动位移平台移进移出主光路,从而切换各个工作模式;更进一步地,第二二向色镜23下的一维电动位移平台的移动方向与分光镜7下的一维电动位移平台的移动方向相互垂直,用于将第二二向色镜23移入或移出分光镜7、第一二向色镜6之间的光轴。
64.该实施例中,检测仪器还可以包括灭菌模块,灭菌模块包括紫外灯,紫外灯放置于显微物镜周围,用于进行杀菌操作防止细菌污染对耐药性检测结果的影响。
65.该实施例中,自动化微生物拉曼耐药性快速检测仪器包括四种光路组合,四种工作模式分别为成像光路、成像光路-拉曼光路、光镊光路-成像光路和光镊光路-拉曼光路,成像光路用于获取样品芯片的图像信息;成像光路-拉曼光路用于实现样品芯片待测细胞拉曼信息的采集;光镊光路-成像光路用于获取样品芯片中液相状态下细胞的图像信息;光镊光路-拉曼光路用于实现样品芯片中液相状态下细胞拉曼信息的采集。
66.四种光路组合分别对应四种工作模式,分别为成像模式、成像模式-拉曼测量模式、光镊模式-成像模式和光镊模式-拉曼模式。
67.更具体地,拉曼主光路及传输模块和成像模块交汇处设置有分光镜7,光镊模块和拉曼主光路及传输模块交汇处设置有第二二向色镜23,通过控制分光镜7和第二二向色镜7的移动切换成像光路、成像光路-拉曼光路、光镊光路-成像光路和光镊光路
‑ꢀ
拉曼光路,采用基于一维电动位移平台共光路切换的设计,使拉曼信号采集过程中移出非采集信号所需
光学元件,提高了光通量。
68.如图2所示,本实施例中激发光模块、拉曼主光路及传输模块、同轴照明模块、成像模块和光镊模块固定在同一光学箱体30内部,且所有模块平面化共光轴布置,即激发光模块、拉曼主光路及信号传输模块、同轴照明模块、相机观测模块、固定在光学箱体内呈平面化布局,所有光学元件光轴均在同一水平面内,使得各模块相对独立,即调试方便又降低模块间的相互干扰。各个模块的光学元件布局上均与光轴垂直或成 45
°
放置,便于各模块调试以及系统集成,同时也极大降低了系统后期维护成本。更具体的,光镊模块的光路与拉曼主光路及传输模块的主光路平行。
69.光学箱体30包括支撑架支撑31,支撑架可以包括左、右、后三组,使得光学箱体30具有预设高度。显微聚焦模块位于光学箱体30的下部;拉曼主光路及传输模块位于箱体内一侧,与显微聚焦模块处于同一基准面。光学箱体30为一体化铸造成型,全封闭设计,一方面实现完全避光,避免外接杂散光信号的干扰;另一方面整体刚性极好,既能够为各模块光学件提供可靠的物理支撑,又可以有效阻断外力的干扰,可满足整机挪动或长途运输后无需重新调试即可使用的需求,同时即使连续测量几十小时,也能一直稳定工作;最后箱体内大部分光学件支撑固定机构调试完成后均会锁死,装置整体的固化程度高,提升抗振动冲击能力,具有非常高的稳定性。
70.本实施例中临床微生物单细胞耐药性检测仪器的样品方法,包括成像检测、成像
‑ꢀ
拉曼检测、光镊-成像检测或光镊-拉曼检测:
71.成像检测,是将分光镜7和第二二向色镜23移出主光路,同轴照明模块开启led 光源10,led光源10发出的白光经半透半反镜11反射进入显微物镜8,由显微物镜8聚焦照亮待测样品,携带待测样品图像信息的反射光进入成像模块,由显微物镜 8收集准直返回透过半透半反镜11,经由第一透镜12聚焦于ccd相机13,调节三维电动位移平台9,使所观察的图像移动到视场中央,调节led光源10的亮度,ccd 参数至使整个观测图像清晰,成像模块获取样品芯片图像信息,对获取样品芯片图像信息处理后定位细胞的采集位置。
72.成像-拉曼检测,基于成像检测已经找寻到需要拉曼检测的样品,将同轴照明模块的led光源10关闭,将光镊模块的第二电动快门19关闭,通过分光镜7处的一维电动位移平台将分光镜7移入主光路,打开激发光模块的第一电动快门2,由第一激光器1发出的激光经过第一电动可调衰减器3衰减后进入第一扩束镜4,经由第一反射镜5反射到第一二向色镜6,45
°
反射到分光镜7后垂直进入显微物镜8,由显微物镜 8聚焦到待测样品上。三维电动位移平台9根据成像检测模式获取的细胞图像,判定细胞的位置信息,将细胞自动移动到显微物镜8的聚焦点从而产生拉曼信号,从而实现自动检测的目的;产生的拉曼信号和瑞利杂散光由显微物镜收集准直返回,经分光镜7反射透过第一二向色镜6,由第二透镜14聚焦于针孔15,经过针孔15空间滤波后进入光谱仪16进行分光,由探测器17获取拉曼图谱信息,实现样品芯片待测细胞拉曼信息的采集,最终由自动采集控制模块分析是否耐药,输出耐药检测结果。
73.光镊-成像检测,基于成像检测,将待测样品放置方式进行改变,具体地,是将清洗后的细胞样品菌液放入微流芯片,或者是采用水浸物镜进行观测;将第二二向色镜 23移入主光路,将激发光模块的第一电动快门2关闭,将分光镜7移入主光路,通过成像检测模式进一步获取待测样品图像信息,找到需要光镊捕获的细胞,打开第二电动开门19,第二激光器
18出射的1064nm激光捕获住细胞,获取样品芯片中液相状态下细胞的图像信息,然后三维电动位移平台9将细胞自动移动到指定位置。
74.光镊-拉曼检测,基于成像检测,将待测样品放置方式进行改变,具体地,是将细胞样品菌液放入微流芯片,或者是采用水浸物镜进行观测,将第二二向色镜23移入主光路,将激发光模块的第一电动快门2关闭,将分光镜7移入主光路,通过成像检测模式进一步获取待测样品图像信息,找到需要光镊捕获的细胞,打开第二电动快门19,第二激光器18出射的1064nm激光会捕获住细胞,关闭led光源10、将第一电动快门2打开,第一激光器1发出的激光经过分光镜7进入显微聚焦模块照亮待测样品,检测细胞拉曼信号,通过拉曼主光路及传输模块获取细胞的拉曼图谱信息,如图3所示,关闭电动快门2,获取样品芯片中液相状态下细胞的图像信息,经自动采集控制模块分析是否耐药,然后移动三维电动位移平台9将耐药细胞自动移动到指定位置。光镊-拉曼模式针对部分有鞭毛的细胞,或者布朗运动造成细胞位置偏移的细胞,采用光镊捕获后,再用拉曼激光激发拉曼信号采集拉曼光谱,保证了细胞信号采集的准确性。
75.本实施例中,自动采集控制模块包括数据分析处理设备,数据分析处理设备可以为计算机。
76.本实施例中,自动采集控制模块控制显微物镜8自动聚焦待测样品上,控制方法包括:
77.聚焦评价,对ccd相机13观测的图像引入评价函数对图像进行定量评价,通常使用清晰度比率、平缓区波动量的方法,基于具体数据计算评判聚焦函数的性能优劣。由于现有清晰度等方法在图片存在噪声时,容易产生“多峰”的现象,本技术对其进行了改进。首先进行待选区域选择,通常选择图片的中心位置,宽和长为原图的1/3;然后使用sobel对待选区域进行0
°
、45
°
、-45
°
、90
°
、135
°
、-135
°
、180
°
和 270
°
八个方向的边缘提取,并选择梯度最大的方向为最终方向;最后对边缘图像进行梯度计算,绘制清晰度评价函数。
78.聚焦位置搜索,依据清晰度评价函数,设置三维电动位移平台9聚焦搜索的初始大步长,每行进一步均通过ccd相机13采集数字图像并由聚焦评价函数计算出该位置点的清晰度评价值,根据图像清晰度评价结果对图像的离焦程度做出判断,最终完成系统正焦位置的最优搜索。
79.本实施例中,通过自动采集控制模块对细胞光谱自动定位采集,控制方法包括:
80.细胞分割,在空洞卷积网络fcn(fully convolutional networks)细胞分割方法基础上增加全卷积网络dcn(dilated convolution network)网络,dcn网络通过将普通卷积替换成空洞卷积,增大感受野大小,提高获得信息的丰富度,弥补传统fcn细胞分割方法信息丢失带来的误差。空洞卷积的空洞率为2,使感受野从普通卷积时的3
ꢀ×
3扩充到7
×
7。
81.细胞采集,分割后的细胞经过坐标转换,将每个细胞的二维位置进行记录,结合三维电动位移平台9来对每个细胞进行自动化光谱采集。
82.本实施例中,自动采集控制模块的数据分析处理设备对细胞进行耐药性分析,分析步骤包括:
83.光谱检测数量动态估算,以cdr(cd-rario)计算为例,单细胞拉曼光谱的测量,以1000次中30个测量光谱随机获得初始数据集xn,然后计算平均cdr和cdrn的差异。在1000次统计中,第n个cdr为cdrn,n为整数,取值范围为1到1000, cdrn与cdr群体的相对误差小于
5%的概率p;p为样本数为30时样本特征值趋于稳定的概率,一般认为p》95%是可靠的。当p小于95%时,继续对样本进行p重新计算,直到p大于95%;
84.单细胞耐药性检测,以cdr=(c-d/(c-d+c-h))作为主要参数来表示单个细胞的代谢活动,并用cdr的平均值衡量菌株的耐药性。针对不同类型的微生物,确定不同的cdr阈值,实现对单细胞耐药性的耐药性分析。
85.本实施例中c-d与c-h,是如图4所示拉曼光谱,采集到的拉曼光谱经去背景、基准线归一化和最大值标准化处理后,分析c-d峰面积(拉曼图谱中2050-2300cm-1
区域)和c-h面积(拉曼图谱中2800-3050cm-1
),计算不同药物浓度下的cdr。
86.最后应说明的是:以上实施例仅用以说明本实用新型的技术方案,而非对其限制;尽管参照前述实施例对本实用新型进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本实用新型各实施例技术方案的精神和范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1