抗MDA5抗体的检测试剂盒及其制备方法与流程
本发明涉及免疫学检测,具体涉及一种使用磁珠化学发光定量检测抗mda5抗体的试剂盒及其制备方法和检测方法。
背景技术:
1、特发性炎性肌病(idiopathic inflammatory myopathy,iim)是一种以侵害骨骼肌为主的全身性疾病,临床特点为骨骼肌无力、皮肤病变、系统性器官损害以及有特异性抗体的产生。多发性肌炎(polymyositis,pm)和皮肌炎(dermatomyositis,dm)是最常见的两种类型。皮肌炎是一组主要累积皮肤和肌肉的自身免疫性疾病,可能与自身免疫,遗传,感染等因素有关。黑色素瘤分化相关基因5(melanoma differentiation-associated gene5,mda5)已经被确认为与皮肌炎(dermatomyositis,dm)特定亚型高度相关的自身抗原。mda5+dm是一类好发于东亚地区的罕见自身免疫性疾病,是一组以间质性肺炎和皮肤皮疹为特点的多系统炎性病变,属于皮肌炎的一个特殊亚型。肺部影像学检查提示间质性肺炎,血清抗体检查可以发现抗mda5抗体阳性。
2、mda5由解旋酶c诱导干扰素结构域蛋白1基因(helicase cinduces interferondomain protein 1gene,ifih1)基因编码,生理状态下是识别病毒双链rna(double strandrna,dsrna)的关键蛋白。当个体暴露于某些环境因素,如甲型肝炎病毒、柯萨奇乙型病毒、肠道病毒和鼻病毒等,这些小核糖核酸病毒可激活mda5,产生ⅰ型ifn(ifnα和ifnβ)及其他参与抗病毒反应的炎性细胞因子。ⅰ型干扰素途径的过度激活可能导致自身炎症性疾病。
3、抗mda5抗体水平与疾病预后相关。sato等(sato et al.rna helicase encodedby melanoma differentiation-associated gene 5is a major autoantigen inpatients with clinically amyopathic dermatomyositis:association with rapidlyprogressive interstitial lung disease[j].arthritis rheum,2009,60(7):2193-2200.)的研究表明,治疗有效患者的抗mda5抗体水平明显低于治疗无效患者,治疗效果差者抗mda5抗体水平持续不下降。因此动态监测抗mda5抗体水平可帮助评估疾病预后。通过对血清抗mda5抗体滴度的检测不仅可以初步评估dm患者是否合并肺间质病变(interstiallung diseases,ild),还可以作为dm患者可能发展为急性进展性间质性肺炎(rpild)的血清学标记,且近几年的研究也提示,血清抗mda5抗体滴度与dm患者的疾病活动性紧密相关。由此可见,抗mda5抗体定量检测不仅有利于ild进展的早期判断,且对监测疾病活动及治疗效果评价也颇有意义。
4、目前针对抗mda5抗体的免疫学检测方法有定性的免疫印迹法、免疫膜条法和elisa法,但这些检测方法的检测结果一致性较差,检测灵敏度低、检测线性范围窄、重现性低、操作复杂(自动化程度低),检测通量较小,且无法定量检测患者血清中抗mda5抗体水平,仍然不能很好满足临床的应用。因此,如何快速准确诊断此类疾病并定量检测患者血清中抗mda5抗体水平,是目前亟需解决的重要问题。
5、另一方面,mda5抗原分子量大,表达困难。现有科研试剂均采用蛋白截短体进行研究应用,检出率较全长片段低。而且,全长蛋白价格昂贵,elisa方法灵敏度低,成本高。即使全长蛋白表达成功,但基于其特殊的序列结构信息原因,不能在常规的缓冲液中溶解,需引入尿素等试剂增加其溶解性,而这些试剂又严重影响磁珠-抗原的标记偶连效率,这也可能是此指标在此方法学上空白因素之一。
6、磁珠化学发光免疫分析法,较以前的膜条免疫法和酶联免疫吸附法,在检测灵敏度、检测范围、检测时间及自动化操作上有了大大提高,且没有污染,临床应用广。目前,使用磁珠化学发光分析法在抗mda5抗体igg免疫分析产品的应用仍未见。
技术实现思路
1、本发明人经过大量的实验研究,出人意料地发现:在抗mda5抗体定量检测过程中,通过使用特定的试剂组合物,能够在待测样品降低磁珠对样本中的生物类物质的非特异性吸附,使其偶连效率、稳定性和灵敏度得到大幅提升。基于这一发现,本发明人开发了一种抗mda5抗体的化学发光免疫定量检测试剂盒。
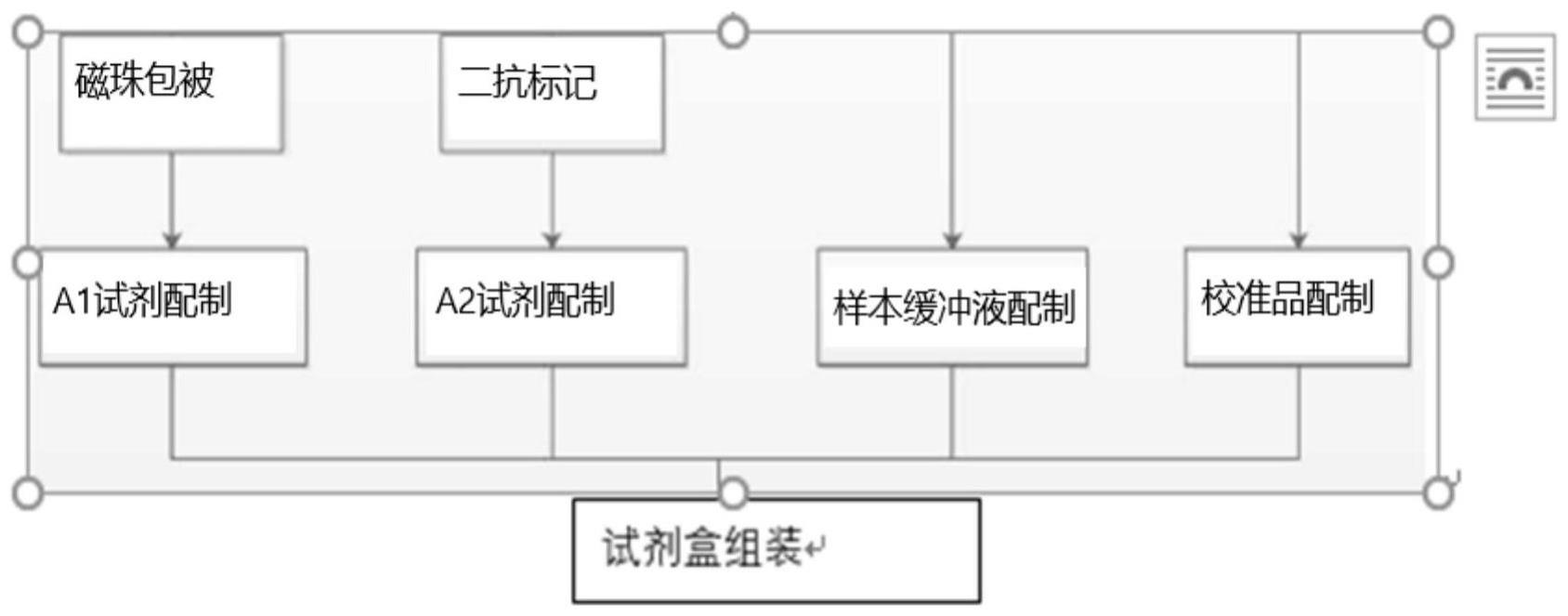
2、在一个方面,本发明提供了一种抗mda5抗体的化学发光免疫定量检测试剂盒,其包括a1试剂、a2试剂和a3试剂;所述a1试剂包括包被有mda5的磁珠;所述a2试剂包括标记的抗人igg偶联物;所述a3试剂包括校准品。
3、在一些实施方案中,所述a1试剂由磁珠,mda5抗原,标记缓冲液,封闭缓冲液,清洗液和磁珠稀释液制备。
4、在一些实施方案中,所述a2试剂由化学发光标记物,抗人igg,标记缓冲液制备。
5、在一些实施方案中,所述磁珠颗粒的粒径为1-3μm。
6、在一些优选的实施方案中,所述磁珠颗粒的粒径为1μm。
7、在一些实施方案中,所述标记缓冲液包括0.015mol/l的吗啉乙磺酸(mes),ph为6.0~7.0。
8、在一些实施方案中,所述封闭缓冲液选自第一封闭缓冲液和第二封闭缓冲液中的任意一种,其中第一封闭缓冲液包括0.05mol/l tris和0.5%明胶;第二封闭缓冲液包括5%bsa和mpc聚合物。
9、在一些优选的实施方案中,所述mpc聚合物biolipidure206。
10、在一些实施方案中,所述清洗液包括精氨酸和brij35。
11、在一些实施方案中,所述磁珠稀释液包括0.05mol/l tris、0.5%casein、0.2%proclin 300和多糖。
12、在一些优选的实施方案中,所述多糖为普兰多糖和硫酸葡聚糖。
13、在一些实施方案中,所述a1试剂中mda5抗原的用量为10-30μg抗原/mg磁珠。
14、在一些优选的实施方案中,所述a1试剂中mda5抗原的用量为20μg抗原/mg磁珠。
15、在一些实施方案中,所述a2试剂中标记的抗人igg偶联物的浓度为0.05-0.2ng/ml。
16、在一些优选的实施方案中,所述所述a2试剂中标记的抗人igg偶联物的浓度为0.1ng/ml。
17、在一些实施方案中,所述a3试剂中校准品为camd患者免疫印迹法检测抗mda5抗体阳性血清稀释。
18、在一些实施方案中,所述a3试剂中校准品的浓度为5-400ru/ml。
19、在一些优选的实施方案中,所述a3试剂中校准品的浓度为15-200ru/ml
20、在一些实施方案中,所述化学发光标记物为鲁米诺、异鲁米诺、三联吡啶钌或吖啶酯。
21、在一些实施方案中,所述试剂盒还包括样本缓冲液,所述样本缓冲液包括0.05mtris、1%明胶和0.2%吐温20。
22、在一些实施方案中,所述a1试剂的使用方法包括以下步骤:
23、1)磁珠原液放入离心管中,去上清液;加入标记缓冲液,去上清液,重悬;加入edc,室温滚动混匀30min;加入标记缓冲液,去上清液;加入标记缓冲液,加入mda5抗原,室温滚动混匀2h;
24、2)弃步骤1)中的上清液,加入封闭缓冲液,去上清液;加入封闭缓冲液混匀,37度1500rpm封闭5-18h;
25、3)弃步骤2)中的上清液,加入清洗液,去上清液;加入清洗液混匀,室温1500rpm清洗过夜;
26、4)加入磁珠稀释液,去上清液;加入磁珠稀释液,得到终浓度为0.1-0.2mg/ml的a1试剂。
27、在一些实施方案中,所述a1试剂的使用方法包括以下步骤:
28、1)取磁珠原液放入离心管中,去上清液;加入标记缓冲液,充分混匀,吸附,去上清液,重复3次;加入标记缓冲液,重悬;加入edc,室温滚动混匀30min;加入标记缓冲液混匀,吸附,去上清液,重复1次;加入标记缓冲液,加入mda5抗原,室温滚动混匀2h;
29、2)弃步骤1)中的上清液,加入封闭缓冲液混匀,吸附,去上清液,重复1次,共计2次;弃上清液,加入封闭缓冲液混匀,37度1500rpm封闭5-6h;
30、3)弃步骤2)中的上清液,加入清洗液混匀,吸附,去上清液,重复1次,共计2次;弃上清液,加入清洗液混匀,室温1500rpm清洗过夜;
31、4)加入磁珠稀释液,混匀,吸附,去上清液,重复1次,共计2次;加入磁珠稀释液,得到终浓度为0.1-0.2mg/ml的a1试剂。
32、在一些实施方案中,所述a2试剂的使用方法包括以下步骤:
33、1)取抗人igg到ep管中,加入标记缓冲液,加入化学发光标记物,将离心管外包裹一层铝箔纸避光,放置于旋转混匀仪上,室温,混匀反应一段时间;
34、2)加入1%lys,避光状态放置于旋转混匀仪上,室温混匀反应30min;
35、3)将化学发光标记物-抗体偶连物进行纯化,加入甘油,保存于-20度备用;
36、4)取化学发光标记物-抗体偶连物,加入a2试剂稀释液,充分混匀后,得到终浓度为0.05ng/ml-0.2ng/ml的a2试剂。
37、在一些实施方案中,所述a2试剂的使用方法包括以下步骤:
38、1)取抗人igg到ep管中,加入标记缓冲液至0.3ml,取吖啶酯工作液,加入到上述蛋白溶液中,立即混匀,将离心管外包裹一层铝箔纸避光,放置于旋转混匀仪上,室温,混匀反应一段时间;
39、2)取1%lys,加入到上述离心管中,保存避光状态,放置于旋转混匀仪上,室温混匀反应30min;
40、3)将吖啶酯-抗体偶连物进行纯化,加入甘油,保存于-20度备用;
41、4)取化学发光标记物-抗体偶连物,加入a2试剂稀释液,充分混匀后,得到终浓度为0.05ng/ml-0.2ng/ml的a2试剂。
42、在一些实施方案中,所述a3试剂的使用方法包括以下步骤:
43、取校准品母液,加入校准品稀释液,得到终浓度分别为15ru/ml和200ru/ml的a3试剂,所述校准品稀释液选自第一校准品稀释液和第二校准品稀释液中的任意一种,其中第一校准品稀释液包括1%casein和0.1%吐温20;第二校准品稀释液包括5%bsa。
44、在第二个方面,本发明提供了一种上述试剂盒的使用方法,其包括使用a1试剂、a2试剂、a3试剂测定待测样本中的抗mda5-igg抗体浓度。
45、本发明所述试剂盒的优异技术效果主要在于以下几个方面:
46、1、在经过了大量的原料筛选,调试,配对等一系列条件组合后,本发明的试剂盒选用了小粒径磁珠,较高的标记ph和活化比,并且在封闭液中添加biolipidure206或者明胶和biolipidure206可以降低磁珠对样本中的生物类物质的非特异性吸附。
47、2、在磁珠标记完成后用精氨酸和brij35的组合对磁珠进行清洗,以增加磁珠的稳定性。
48、3、在磁珠稀释液中添加了多糖,使其偶连效率、稳定性和灵敏度都得到了很大提高。
49、4、常规检测系统p/n差,通过在反应体系中引入多糖、casein等试剂,以及外加二抗的配对组合,能够明显提高p/n。
- 还没有人留言评论。精彩留言会获得点赞!