一种凝血酶抗凝血酶复合物检测试剂盒的制作方法
本发明涉及生物,具体涉及一种凝血酶抗凝血酶复合物检测试剂盒。
背景技术:
1、血栓是一种严重的疾病,其发生发展过程极其复杂,内皮细胞、凝血系统、抗凝系统和纤溶系统都参与了这一过程。早期针对血栓的诊断主要以一些常见的凝血指标为主,然而,这些参数主要涉及血栓形成后的后期筛查,指标出现异常时,疾病已进入中后期,失去了最佳治疗时机。而现有研究已经证实机体处于血栓前状态时,血管内皮系统、凝血系统和纤溶系统已经发生改变,凝血酶抗凝血酶复合物(thrombin-antithrombin,tat)、纤溶酶-a2纤溶酶抑制剂复合物(plasmin-a2-plasmininhibitor,pic)、血栓调节蛋白((thrombomodulin,tm)和组织纤溶酶原激活物-纤溶酶原激活物抑制剂1复合物(tissueplasminogen activator inhibitor1 complex,tpaic)是反应机体血管内皮、凝血和纤溶系统早期改变的有效生物标志物,适用于各临床学科血栓高危人群的早期诊断、风险评估和治疗疗效评价及健康人群血栓风险筛查,对不同基础疾病的血栓患者具有良好的诊断和预后价值。
2、tat是凝血酶和抗凝血酶ⅲ(at ⅲ)形成的复合物,凝血酶的生成是静脉血栓形成的关键环节,它主要作用于纤维蛋白原使之形成纤维蛋白,进而导致血栓的生成。体内生成极少量凝血酶(thrombint)很快会被抗凝血酶-iii(antithrombin-iii,at-iii)以1:1的比例结合生成tat复合物而灭活,以维持内环境的稳定,单纯的检测凝血酶很难检测,因其半衰期较短,由此认为血浆tat水平可以间接反映凝血酶的生成量,来衡量体内的高凝状态。而tat的血液半衰期为3~15分钟而能够测定,正常参考区间为0-4ng/ml。
3、性能优良的单克隆抗体对于tat的检测至关重要,但目前国内缺乏tat单克隆抗体的研究,而且tat在正常人群中含量在0-4ng/ml,凝血酶与凝血酶原在一段氨基酸序列中一致,且凝血酶原与at-iii在血液当中含量是tat复合物的上千倍,因此极易对tat检测产生干扰。
技术实现思路
1、本发明的目的在于提供一种凝血酶抗凝血酶复合物检测试剂盒,能够实现凝血酶抗凝血酶复合物的特异准确的检测,且不会产生交叉反应。
2、本发明通过研究发现要完成tat的准确检测,需要制备出两种单克隆抗体。
3、一种单克隆抗体不与凝血酶原、凝血酶反应,但与tat、at-iii反应;
4、一种单克隆抗体不与at-iii,但与凝血酶原、凝血酶、tat反应;
5、这两种抗体测定tat时添加凝血酶原不影响两个抗体对tat的检测。
6、因此,本发明的目的在于提供能够特异性识别tat并且与tat显示出高亲和力的单克隆抗体,并且进一步提供使用这些单克隆抗体测量tat的方法。
7、本发明具体实现如下:一种凝血酶抗凝血酶复合物检测试剂盒,包括用于检测凝血酶抗凝血酶复合物的第一抗体和第二抗体,
8、其中所述第一抗体结合所述凝血酶抗凝血酶复合物的抗凝血酶ⅲ部分,所述第二抗体结合所述凝血酶抗凝血酶复合物的抗凝血酶部分。
9、更进一步地,所述第一抗体结合所述凝血酶抗凝血酶复合物的抗凝血酶ⅲ中17-30和/或340-350之间的片段,所述第二抗体结合所述凝血酶抗凝血酶复合物的抗凝血酶中的240-260和/或12-30之间的片段。
10、进一步地,所述第一抗体具有如下互补决定区:
11、cdr-vh1:d-y-x1-m-x2,其中x1是a或n,x2是n或y;
12、cdr-vh2:y-i-e-x1-y-d-g-x2-t-s-y-n-q-k-x3-k-g,其中x1是i或p,x2是g或s,x3是f或l;
13、cdr-vh3:d-x1-d-r-d-r-v-x2-y,其中x1是y、k或a,x2是d;
14、cdr-vl1:s-a-s-x1-n-v-x2-y-m-h,其中x1是q或s,x2是r、s或n;
15、cdr-vl2:x1-t-s-n-l-x2-s,其中x1为t或y,x2是h或a;
16、cdr-vl3:q-q-x1-s-s-y-p-x2-t,其中x1是y或r,x2是p或l。
17、或
18、所述第二抗体具有如下互补决定区:
19、cdr-vh1:x1-d-y-a-x2-n,其中x1是s或t,x2是m或w;
20、cdr-vh2:x1-i-s-y-s-x2-s-t-s-y-n-x3-s-l-k-s,其中x1是f或y,x2是g或d,x3是q或p;
21、cdr-vh3:a-k-x1-a-x2-a-y,其中x1是r或d,x2是v或m;
22、cdr-vl1:s-a-s-q-x1-i-s-n-y-l-x2,其中x1是a,x2是n或h;
23、cdr-vl2:y-x1-s-x2-l-h-s,其中x1是t或y,x2是n或s;
24、cdr-vl3:q-q-y-s-x1-x2-p-l-t,其中x1是s或k,x2是l或y。
25、进一步地,所述第一抗体的cdr-vh1中x2是y,cdr-vh2种x1是p,cdr-vh3种x2是d,cdr-vl1种x1是s,cdr-vl2中x2是a,cdr-vl3中x1是r;
26、或所述第二抗体的cdr-vh1中x2是w,cdr-vh2种x1是y,cdr-vh3种x2是m,cdr-vl1种x1是a,cdr-vl2中x2是s,cdr-vl3中x1是k。
27、本发明所述cdr标识采用kabat编号方案。
28、本发明的发明人发现,在各互补决定区中的上述突变位点为上述氨基酸残基时,该抗体对游离的生物素表现出更好的亲和力。
29、在可选的实施方式中,所述第一抗体的cdr-vh1中x1是a。
30、在可选的实施方式中,所述第一抗体的cdr-vh1中x1是n。
31、在可选的实施方式中,所述第一抗体的cdr-vh1中x2是n。
32、在可选的实施方式中,所述第一抗体的cdr-vh1中x2是y。
33、在可选的实施方式中,所述第一抗体的cdr-vh2中x1是i。
34、在可选的实施方式中,所述第一抗体的cdr-vh2中x1是p。
35、在可选的实施方式中,所述第一抗体的cdr-vh2中x2是g。
36、在可选的实施方式中,所述第一抗体的cdr-vh2中x2是s。
37、在可选的实施方式中,所述第一抗体的cdr-vh2中x3是f。
38、在可选的实施方式中,所述第一抗体的cdr-vh2中x3是l。
39、在可选的实施方式中,所述第一抗体的cdr-vh3中x1是y。
40、在可选的实施方式中,所述第一抗体的cdr-vh3中x1是k。
41、在可选的实施方式中,所述第一抗体的cdr-vh3中x1是a。
42、在可选的实施方式中,所述第一抗体的cdr-vl1中x1是q。
43、在可选的实施方式中,所述第一抗体的cdr-vl1中x1是s。
44、在可选的实施方式中,所述第一抗体的cdr-vl1中x2是r。
45、在可选的实施方式中,所述第一抗体的cdr-vl1中x2是s。
46、在可选的实施方式中,所述第一抗体的cdr-vl1中x2是n。
47、在可选的实施方式中,所述第一抗体的cdr-vl2中x1是t。
48、在可选的实施方式中,所述第一抗体的cdr-vl2中x1是y。在可选的实施方式中,所述第一抗体的cdr-vl2中x2是h。在可选的实施方式中,所述第一抗体的cdr-vl2中x2是a。在可选的实施方式中,所述第一抗体的cdr-vl3中x1是y。在可选的实施方式中,所述第一抗体的cdr-vl3中x1是r。在可选的实施方式中,所述第一抗体的cdr-vl3中x2是p。
49、在可选的实施方式中,所述第一抗体的cdr-vl3中x2是l。
50、在可选的实施方式中,所述第二抗体的cdr-vh1中x1是s。
51、在可选的实施方式中,所述第二抗体的cdr-vh1中x1是t。
52、在可选的实施方式中,所述第二抗体的cdr-vh1中x2是m。
53、在可选的实施方式中,所述第二抗体的cdr-vh1中x2是w。
54、在可选的实施方式中,所述第二抗体的cdr-vh2中x1是f。
55、在可选的实施方式中,所述第二抗体的cdr-vh2中x1是y。
56、在可选的实施方式中,所述第二抗体的cdr-vh2中x2是g。
57、在可选的实施方式中,所述第二抗体的cdr-vh2中x2是d。
58、在可选的实施方式中,所述第二抗体的cdr-vh2中x3是q。
59、在可选的实施方式中,所述第二抗体的cdr-vh2中x3是p。
60、在可选的实施方式中,所述第二抗体的cdr-vh3中x1是r。
61、在可选的实施方式中,所述第二抗体的cdr-vh3中x1是d。
62、在可选的实施方式中,所述第二抗体的cdr-vh3中x2是v。
63、在可选的实施方式中,所述第二抗体的cdr-vh3中x2是m。
64、在可选的实施方式中,所述第二抗体的cdr-vl1中x1是a。
65、在可选的实施方式中,所述第二抗体的cdr-vl1中x2是n。
66、在可选的实施方式中,所述第二抗体的cdr-vl1中x2是h。
67、在可选的实施方式中,所述第二抗体的cdr-vl2中x1是t。
68、在可选的实施方式中,所述第二抗体的cdr-vl2中x1是y。
69、在可选的实施方式中,所述第二抗体的cdr-vl2中x2是n。
70、在可选的实施方式中,所述第二抗体的cdr-vl2中x2是s。
71、在可选的实施方式中,所述第二抗体的cdr-vl3中x1是s。
72、在可选的实施方式中,所述第二抗体的cdr-vl3中x1是k。
73、在可选的实施方式中,所述第二抗体的cdr-vl2中x2是l。
74、在可选的实施方式中,所述第二抗体的cdr-vl2中x2是y。
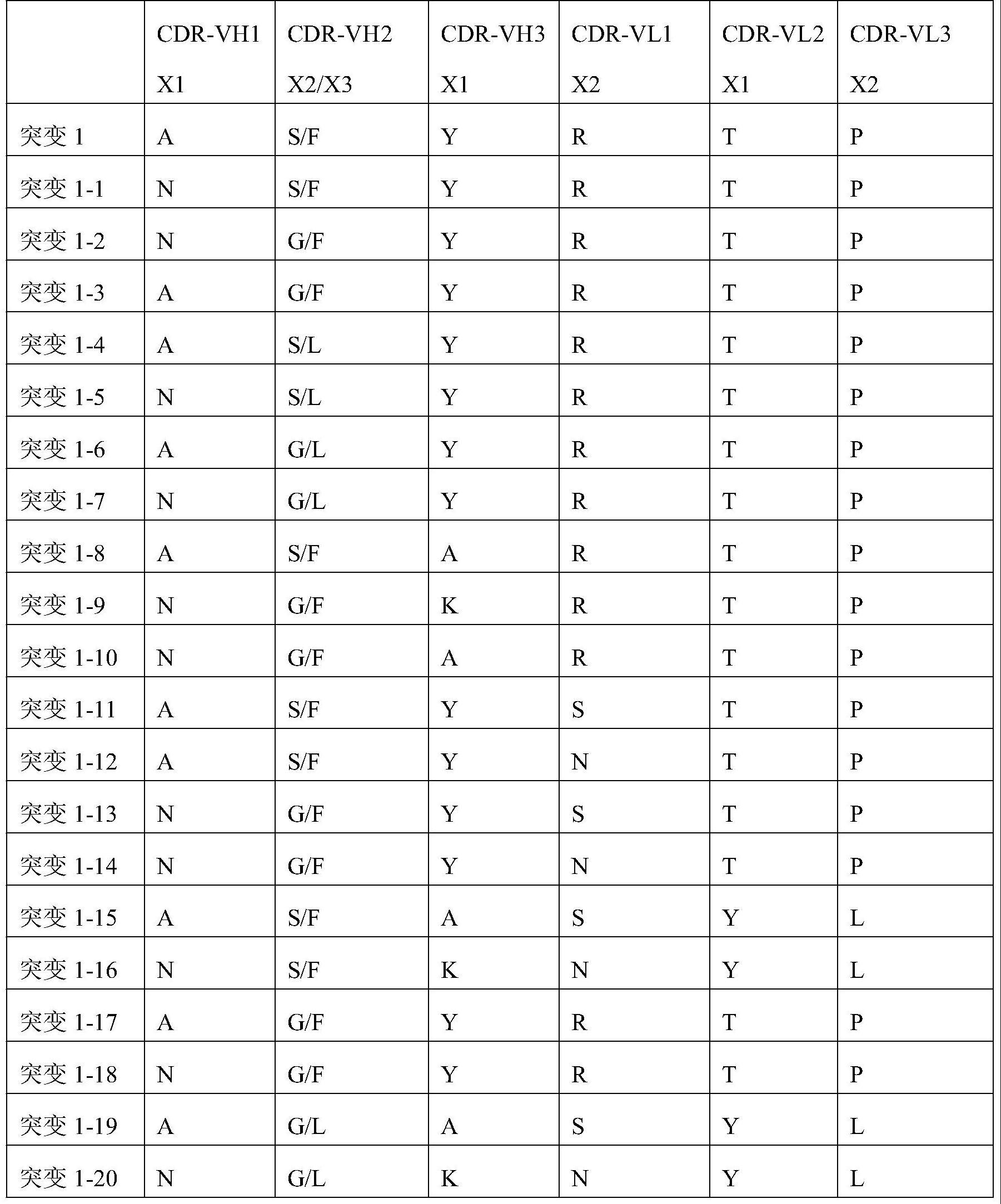
75、优选的,所述第一抗体的各互补决定区选自如下突变组合中任意一种:
76、
77、
78、和/或所述第二抗体的各互补决定区选自如下突变组合中任意一种:
79、
80、进一步地,所述第一抗体和第二抗体包括轻链骨架区fr1-l、fr2-l、fr3-l及fr4-l和重链骨架区fr1-h、fr2-h、fr3-h及fr4-h;所述轻链骨架区fr1-l、fr2-l、fr3-l及fr4-l依次选自seq id no:1-4或seq id no:5-8;所述重链骨架区fr1-h、fr2-h、fr3-h及fr4-h依次选自seq id no:9-12或seq id no:13-16。
81、进一步地,所述第一抗体和第二抗体还包含恒定区。
82、优选的,所述恒定区选自igg1、igg2、igg3、igg4、iga、igm、ige和igd中的任意一者的恒定区,优选的,所述恒定区的种属来源为牛、马、乳牛、猪、绵羊、山羊、大鼠、小鼠、狗、猫、兔、骆驼、驴、鹿、貂、鸡、鸭、鹅、火鸡、斗鸡或人。
83、优选的,所述功能性片段选自所述抗体的vhh、f(ab’)2、fab’、fab、fv和scfv中的任意一种。
84、进一步地,所述试剂盒检测的样本选自全血、血清、血浆、尿液或唾液的体液。
85、进一步地,所述第一抗体和第二抗体均为标记抗体。
86、本发明所述“标记抗体”为标记有可被检测的标记物。
87、术语“抗体”包括各种形式的抗体结构,包括但不限于完整抗体和抗体片段。根据本发明的抗体优选是山羊、绵羊、小鼠、兔或大鼠抗体,嵌合抗体或进一步的基因工程抗体,只要保留根据本发明的特征性质。“抗体片段”包含全长抗体的一部分,优选其可变结构域,或至少其抗原结合部位。抗体片段的实例包括双抗体、单链抗体分子和由抗体片段形成的多特异性抗体。抗体片段的实例包括fab、fab'、f(ab')2和fv片段;单链抗体分子;scfv、sc(fv)2;双抗体;和由抗体片段形成的多特异性抗体。
88、优选的,所述可被检测的标记物包括但不限于生物素、荧光染料、催化底物显色的酶、放射性同位素、化学发光试剂和纳米颗粒类标记物;
89、优选的,所述荧光染料包括但不限于荧光素类染料及其衍生物、罗丹明类染料及其衍生物、cy系列染料及其衍生物、alexa系列染料及其衍生物和蛋白类染料及其衍生物;
90、所述酶为催化底物显色的酶所述催化底物显色的酶包括但不限于辣根过氧化物酶、碱性磷酸酶、β-半乳糖苷酶、葡萄糖氧化酶、碳酸酐酶、乙酰胆碱酯酶以及6-磷酸葡萄糖脱氧酶。优选的,所述催化底物显色的酶包括但不限于辣根过氧化物酶、碱性磷酸酶、β-半乳糖苷酶、葡萄糖氧化酶、碳酸酐酶、乙酰胆碱酯酶以及6-磷酸葡萄糖脱氧酶;
91、优选的,所述放射性同位素包括但不限于212bi、131i、111in、90y、186re、211at、125i、188re、153sm、213bi、32p、94mtc、99mtc、203pb、67ga、68ga、43sc、47sc、110min、97ru、62cu、64cu、67cu、68cu、86y、88y、121sn、161tb、166ho、105rh、177lu、172lu和18f;
92、优选的,所述化学发光试剂包括但不限于鲁米诺及其衍生物、光泽精、甲壳动物荧光素及其衍生物、联吡啶钌及其衍生物、吖啶酯及其衍生物、二氧环乙烷及其衍生物、洛粉碱及其衍生物和过氧草酸盐及其衍生物;
93、优选的,所述纳米颗粒类标记物包括但不限于纳米颗粒、胶体、有机纳米颗粒、磁性纳米颗粒、量子点纳米颗粒和稀土络合物纳米颗粒;
94、优选的,所述胶体包括但不限于胶体金属、分散型染料、染料标记的微球和乳胶;
95、优选的,所述胶体金属包括但不限于胶体金、胶体银和胶体硒。
96、进一步地,所述第一抗体标记生物素形成生物素-第一抗体偶联物,所述第二抗体标记酶,形成酶-第二抗体偶联物。
97、优选的,所述试剂盒为化学发光检测试剂盒。
98、有益效果:
99、本发明公开的两种单克隆抗体,一种单克隆抗体不与凝血酶原、凝血酶反应,但与tat、at-iii反应;一种单克隆抗体不与at-iii,但与凝血酶原、凝血酶、tat反应;这两种抗体测定tat时添加凝血酶原不影响两个抗体对tat的检测,不会对凝血酶原产生交叉反应,且能够应用到不同的试剂盒中实现高灵敏度和高精度的检测。
- 还没有人留言评论。精彩留言会获得点赞!