并用抗癌剂的感受性判定标记的制作方法
本发明涉及用于判定作为对象的患者的癌症对于所使用的抗癌剂是否具有治疗反应性的抗癌剂感受性判定标记和其利用。
背景技术:
1、抗癌剂有烷基化剂、铂制剂、代谢拮抗剂,抗癌性抗生素,抗癌性植物生物碱等的种类。并且,这些抗癌剂存在因癌症的种类不同而显示疗效和不显示疗效的情况。然而,已知即使是对于被认为有效的种类的癌症,也存在因患者个体不同而显示疗效和不显示疗效的情况。抗癌剂对于这样的各个患者的癌症是否显示疗效被称为抗癌剂感受性。
2、奥沙利铂(sp-4-2)-[(1r,2r)-cyclohexane-1,2-diamine-κn,κn’][ethanedioato(2-)-κo1,κo2]platinum(iupac)是第三代铂配位化合物系抗恶性肿瘤药。其作用机理被认为与以往药剂的顺铂(cddp)、卡铂(cbdca)同样,通过与dna碱基形成交联来抑制dna合成、抑制蛋白合成,奥沙利铂(l-ohp)对于cddp、cbdca无法产生疗效的大肠癌也显示抗肿瘤效果,显示出了与现有的铂配位化合物系抗恶性肿瘤药不同的抗肿瘤谱。在美国于2004年1月,奥沙利铂与氟尿嘧啶(5-fu)/左亚叶酸(lv)的联合使用(并用)被许可用于治疗转移性结肠-直肠癌的一线治疗,在日本也于2005年4月,对于“无法靠切除治愈的晚期、复发的结肠-直肠癌”,以奥沙利铂与其他抗恶性肿瘤剂的联合使用(本剂在与左亚叶酸和氟尿嘧啶的静脉内持续给药法等联合使用的情况下被确认有用)的方式被药价收录。对于晚期复发大肠癌的治疗,利用20世纪90年代前半叶之前所进行的5-fu/lv疗法时的生存率为10~12个月,与此相对,加入了奥沙利铂的folfox疗法的生存期为19.5个月,几乎达到2倍。而且在2009年8月,作为效能、效果追加了同样利用奥沙利铂与左亚叶酸和氟尿嘧啶的静脉内持续给药法的联合使用的“结肠癌中的术后辅助化疗”,奥沙利铂是能够期待对大肠癌患者的扩大使用和有益性的药剂。在大肠癌以外,在2009年8月,对于不能通过切除治愈的胰腺癌,在2015年3月对于胃癌,都以与其他化疗剂的联合使用的方式追加了效能、效果。
3、然而,即便如此,对于晚期复发大肠癌的folfox疗法的反应率为50%左右,换言之就是接受治疗的患者的一半没有获得疗效。另外,还因为使用奥沙利铂除了会导致中性粒细胞减少症,还会导致多发性末梢神经障碍,这虽然不是致死性的副作用,但也成为导致难以继续治疗的因素。因此,利用能够在治疗开始前预测能够期待疗效的患者(反应者)和不能够期待疗效的患者(非反应者)而能够早期诊断治疗反应性的生物标记,能够实现有效性和安全性高的化学疗法。
4、而且,一般来说,癌症化学疗法的治疗疗程较长,因此在持续治疗中经时性地监测对于抗癌剂的感受性,能够实现能否持续治疗的判定,不仅能够减少患者负担和副作用,而且从医疗经济学的观点出发也被认为是有用的。为了实现预测各个患者的治疗反应性、以及进行早期诊断和选择适当的药剂和治疗方案的“个性化治疗”,确立能够进行对于奥沙利铂等抗癌剂的效果预测或治疗应答性的早期诊断的生物标记是当务之急。
5、从该观点出发,本发明人通过使药剂感受性不同的多个人癌细胞系或者移植有该细胞系的荷瘤小鼠暴露于药剂,对于药剂暴露后的细胞内代谢变动使用毛细管电泳-飞行时间型质谱仪(ce-tof ms)进行全面分析,比较分析药剂感受性,搜索抗癌剂感受性判定标记,由此报告了几种标记(专利文献1~4)。然而,这些标记还未达到实用化。另外,近年来,在folfox疗法中加入了贝伐单抗、西妥昔单抗、帕尼单抗等抗体药的联合疗法也被确立,因此能够进行folfox疗法的效果预测或者早期诊断治疗应答性的生物标记的重要性日益增加。
6、现有技术文献
7、专利文献
8、专利文献1:国际专利公开第2009/096189号
9、专利文献2:国际专利公开第2011/052750号
10、专利文献3:国际专利公开第2012/127984号
11、专利文献4:国际专利公开第2013/125675号
技术实现思路
1、发明所要解决的问题
2、本发明的课题在于,提供一种能够判别各个患者的治疗反应性的抗癌剂感受性判定标记和使用了它的新的癌症治疗手段。
3、用于解决问题的方案
4、在此,本发明人以结肠-直肠癌症患者的血液样本作为对象,对于贝伐单抗联用mfolfox6疗法开始前的血中代谢物利用ce-q-tof ms和ce-tof ms进行全面分析,结果发现,对于贝伐单抗联用mfolfox6疗法的治疗反应性高的反应者组的患者中,2-脱氧葡萄糖6-磷酸酯(2dg6p)、2-甲基丝氨酸(2mse)、半胱氨酸-谷胱甘肽二硫化物(cssg)、多巴胺(dopm)、氧化型谷胱甘肽(gssg)、咪唑-4-乙酸酯(i4a)和吡啶-2-羧酸丁酯(p2cb)的浓度与治疗反应性低的非反应者组的患者相比更高。另外,在反应者组的患者中、1-甲基-2-吡咯烷酮、天冬氨酸(asp)、苯甲酰胺、葡萄糖二酸、6-磷酸葡萄糖(gl6p)、双甘氨肽(gly-gly)、亚牛磺酸(hypt)和次黄嘌呤(hypx)的浓度与非反应者组的患者相比更低。
5、基于该发现,经过进一步的探讨,结果发现,测定来自癌症患者的生物体试样中的选自2dg6p、2mse、cssg、dopm、gssg、i4a、p2cb、1-甲基-2-吡咯烷酮、asp、苯甲酰胺、葡萄糖二酸、gl6p、gly-gly、hypt和hypx中的1种以上的分子的浓度,就能够判定该癌症患者的癌症对于抗癌剂是否具有感受性。另外发现,测定来自癌症患者的生物体试样中的(1)2dg6p、cssg、hypt、i4a和p2cb的浓度、(2)2dg6p、2mse、asp、cssg、dopm、gl6p和hypt的浓度、或(3)cssg、dopm和hypt的浓度,通过将该浓度是否在反应者的截止值以上(或者,以下)进行数值化后代入特定的计算式,就能够判定该癌症患者的癌症对于抗癌剂是否具有感受性,具体来说,能够判定该癌症患者是否为反应者。另外发现,测定来自癌症患者的生物体试样中的选自asp和cssg中的1种以上的分子的浓度,则能够预测治疗开始前的肿瘤的大小。另外发现,测定来自癌症患者的生物体试样中的选自2-氨基丁酸、cssg、γ-谷氨酰半胱氨酸(γ-glu-cys)、甘油-3-磷酸酯、奎尼酸、asp、甘氨胆酸、hypx和乳酸中的1种以上的分子的浓度,能够预测抗癌剂治疗时的预后预测。
6、而且发现,将来自癌症患者的生物体试样中的选自2dg6p、2mse、cssg、dopm、gssg、i4a、p2cb、1-甲基-2-吡咯烷酮、asp、苯甲酰胺、葡萄糖二酸、gl6p、gly-gly、hypt、hypx、2-氨基丁酸、γ-glu-cys、甘油-3-磷酸酯、奎尼酸、甘氨胆酸和乳酸中的1种以上的分子的表达变动作为指标,能够筛选抗癌剂感受性增强剂,而且发现,将该抗癌剂感受性增强剂与成为感受性增强的对象的抗癌剂联合使用,能够飞跃性地提高该抗癌剂的治疗效果,从而完成了本发明。
7、即,本发明提供下面的〔1〕~〔22〕的发明。
8、〔1〕一种抗癌剂感受性判定标记,其中,上述抗癌剂包含奥沙利铂或它的盐、氟尿嘧啶或它的盐和左亚叶酸或它的盐,
9、上述抗癌剂感受性判定标记包含选自2dg6p、2mse、cssg、dopm、gssg、i4a、p2cb、1-甲基-2-吡咯烷酮、asp、苯甲酰胺、葡萄糖二酸、gl6p、gly-gly、hypt和hypx中的1种以上的分子。
10、〔2〕如〔1〕所述的抗癌剂感受性判定标记,其中,抗癌剂还包含贝伐单抗。
11、〔3〕一种抗癌剂感受性判定方法,其中,上述抗癌剂包含奥沙利铂或它的盐、氟尿嘧啶或它的盐和左亚叶酸或它的盐,
12、上述抗癌剂感受性判定方法包括测定来自癌症患者的生物体试样中的选自2dg6p、2mse、cssg、dopm、gssg、i4a、p2cb、1-甲基-2-吡咯烷酮、asp、苯甲酰胺、葡萄糖二酸、gl6p、gly-gly、hypt和hypx中的1种以上的分子的量的工序。
13、〔4〕如〔3〕所述的判定方法,其还包括:通过将上述测定的结果与对照水平进行比较,来判定该癌症患者对于抗癌剂的感受性的工序。
14、〔5〕如〔4〕所述的判定方法,其中,上述对照水平为反应者的截止值,该截止值在2dg6p时为5.304×10-4≤,在2mse时为1.404×10-3≤,在cssg时为2.223×10-2≤,在dopm时为1.153×10-3≤,在gssg时为1.061×10-3≤,在i4a时为3.316×10-3≤,在p2cb时为5.952×10-4≤,在1-甲基-2-吡咯烷酮时为≤8.422×10-2,在asp时为≤3.401×10-2,在苯甲酰胺时为≤9.859×10-2,在葡萄糖二酸时为≤1.058×10-3,在gl6p时为≤8.167×10-4,在gly-gly时为≤5.349×10-3,在hypt时为≤1.837×10-2,在hypx时为≤1.050×10-1。
15、〔6〕如〔3〕所述的判定方法,其还包括通过下式(1)算出反应者的概率(p),判定该癌症患者是否为反应者的工序,
16、
17、(式中,2dg6p、cssg、i4a和p2cb在各分子的测定结果为各分子的截止值以上时表示1,低于截止值时表示0,hypt在测定结果为截止值以下时表示1,超过截止值时表示0,
18、该截止值在2dg6p时为5.304×10-4,在cssg时为2.223×10-2,在i4a时为3.316×10-3,在p2cb时为5.952×10-4,在hypt时为1.837×10-2。)
19、〔7〕如〔3〕所述的判定方法,其还包括通过下式(2)算出反应者的概率(p),判定该癌症患者是否为反应者的工序,
20、
21、(式中,2dg6p的测定结果为截止值以上时,2dg6p表示10.2190,低于截止值时,2dg6p表示-10.2190,2mse的测定结果为截止值以上时,2mse表示1.4778,低于截止值时,2mse表示-1.4778,asp的测定结果为截止值以上时,asp表示-1.4976,低于截止值时,asp表示1.4976,cssg的测定结果为截止值以上时,cssg表示2.0937,低于截止值时,cssg表示-2.0937,dopm的测定结果为截止值以上时,dopm表示2.2258,低于截止值时,dopm表示-2.2258,gl6p的测定结果为截止值以上时,gl6p表示-1.6623,低于截止值时,gl6p表示1.6623,hypt的测定结果为截止值以上时,hypt表示-2.3200,低于截止值时,hypt表示2.3200,
22、该截止值在2dg6p时为5.304×10-4,在2mse时为1.404×10-3,在asp时为3.401×10-2,在cssg时为2.223×10-2,在dopm时为1.153×10-3,在gl6p时为8.167×10-4,在hypt时为1.837×10-2。)
23、〔8〕如〔3〕所述的判定方法,其还包括通过下式(3)算出反应者的概率(p),判定该癌症患者是否为反应者的工序;
24、
25、(式中,cssg的测定结果为截止值以上时,cssg表示1.8701,低于截止值时,cssg表示-1.8701,dopm的测定结果为截止值以上时,dopm表示1.4081,低于截止值时,dopm表示-1.4081,hypt的测定结果为截止值以上时,hypt表示-1.0869,低于截止值时,hypt表示1.0869,
26、该截止值在cssg时为2.223×10-2,在dopm时为1.153×10-3,在hypt时为1.837×10-2。)
27、〔9〕如〔3〕~〔8〕中任一项所述的判定方法,其中,生物体试样为来自投予了抗癌剂的癌症患者的生物体试样。
28、〔10〕如〔3〕~〔9〕中任一项所述的判定方法,其中,抗癌剂还包含贝伐单抗。
29、〔11〕一种癌症患者的肿瘤直径之和的判定方法,其包括测定来自该癌症患者的生物体试样中的选自asp和cssg中的1种以上的分子的量的工序。
30、〔12〕一种抗癌剂治疗时的预后预测标记,其中,上述抗癌剂包含奥沙利铂或它的盐、氟尿嘧啶或它的盐和左亚叶酸或它的盐,
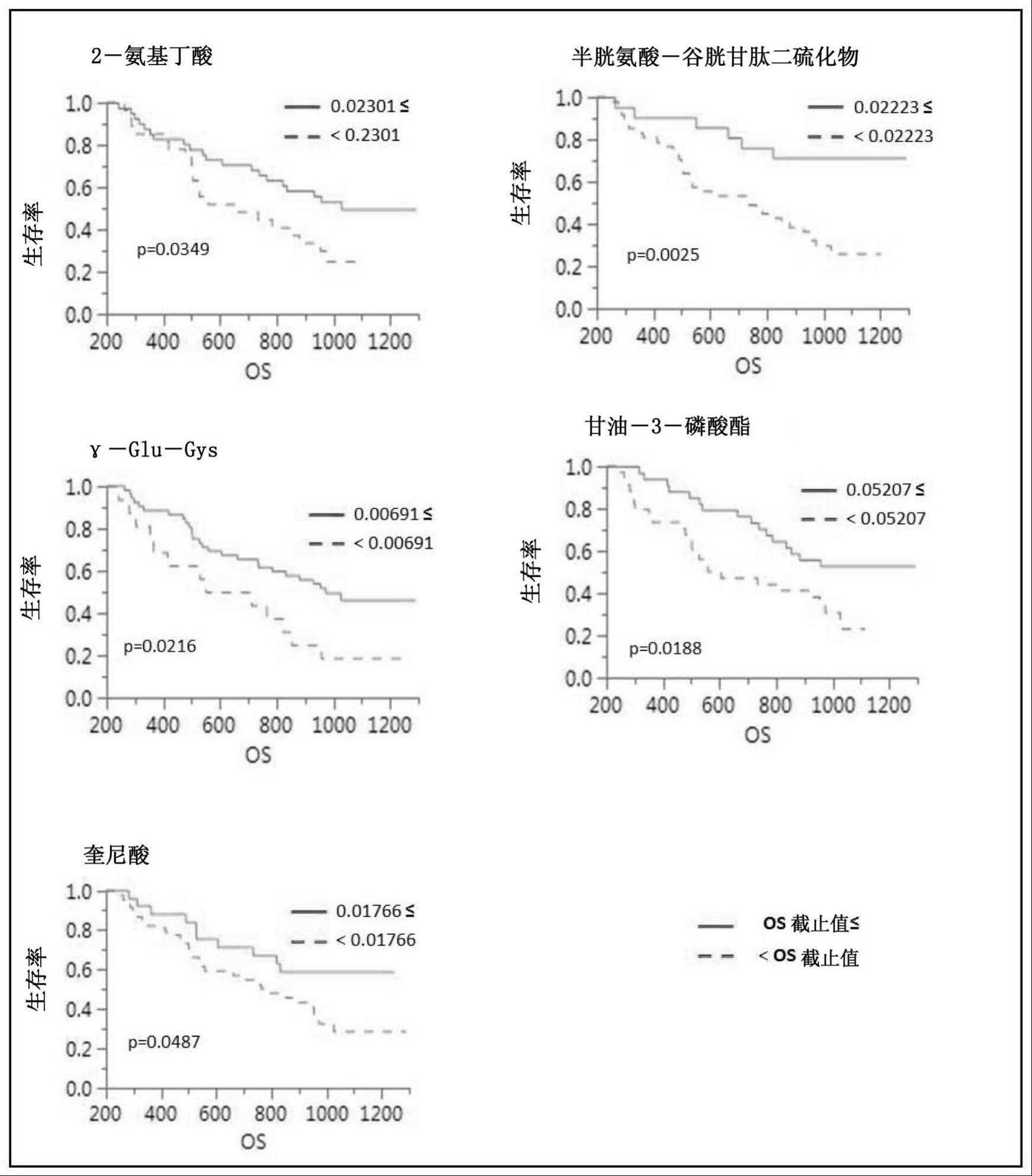
31、上述预后预测标记包含选自2-氨基丁酸、cssg、γ-glu-cys、甘油-3-磷酸酯、奎尼酸、asp、甘氨胆酸、hypx和乳酸中的1种以上的分子。
32、〔13〕如〔12〕所述的预后预测标记,其中,抗癌剂还包含贝伐单抗。
33、〔14〕一种治疗时的预后预测方法,其中,上述抗癌剂包含奥沙利铂或它的盐、氟尿嘧啶或它的盐和左亚叶酸或它的盐,
34、上述预后预测方法包括测定来自癌症患者的生物体试样中的选自2-氨基丁酸、cssg、γ-glu-cys、甘油-3-磷酸酯、奎尼酸、asp、甘氨胆酸、hypx和乳酸中的1种以上的分子的量的工序。
35、〔15〕如〔14〕所述的预后预测方法,其中,抗癌剂还包含贝伐单抗。
36、〔16〕一种试剂盒,其用于实施〔3〕~〔11〕中任一项所述的判定方法,该试剂盒的特征在于:
37、包含用于测定来自癌症患者的生物体试样中的选自2dg6p、2mse、cssg、dopm、gssg、i4a、p2cb、1-甲基-2-吡咯烷酮、asp、苯甲酰胺、葡萄糖二酸、gl6p、gly-gly、hypt和hypx中的1种以上的分子的量的方案。
38、〔17〕一种试剂盒,其用于实施〔14〕或〔15〕所述的判定方法,该试剂盒的特征在于:
39、包含用于测定来自癌症患者的生物体试样中的选自2-氨基丁酸、cssg、γ-glu-cys、甘油-3-磷酸酯、奎尼酸、asp、甘氨胆酸、hypx和乳酸中的1种以上的分子的量的方案。
40、〔18〕一种抗癌剂感受性增强剂的筛选方法,其中,在包含奥沙利铂或它的盐、氟尿嘧啶或它的盐和左亚叶酸或它的盐的抗癌剂的存在下,将癌细胞系或来自荷瘤动物的生物体试样中的选自2dg6p、2mse、cssg、dopm、gssg、i4a、p2cb、1-甲基-2-吡咯烷酮、asp、苯甲酰胺、葡萄糖二酸、gl6p、gly-gly、hypt、hypx、2-氨基丁酸、γ-glu-cys、甘油-3-磷酸酯、奎尼酸、甘氨胆酸和乳酸中的1种以上的分子的表达变动作为指标。
41、〔19〕如〔18〕所述的筛选方法,其中,抗癌剂还包含贝伐单抗。
42、〔20〕一种感受性增强剂,其为通过〔18〕或〔19〕所述的方法得到的对于抗癌剂的感受性增强剂,
43、上述抗癌剂包含奥沙利铂或它的盐、氟尿嘧啶或它的盐和左亚叶酸或它的盐。
44、〔21〕一种癌症治疗用组合物,其为通过组合〔20〕所述的感受性增强剂和抗癌剂而成的癌症治疗用组合物,
45、上述抗癌剂包含奥沙利铂或它的盐、氟尿嘧啶或它的盐和左亚叶酸或它的盐。
46、〔22〕如〔21〕所述的癌症治疗用组合物,其中,抗癌剂还包含贝伐单抗。
47、发明效果
48、使用本发明的抗癌剂感受性判定标记,就能对各个患者的抗癌剂感受性、预后或肿瘤的抗癌剂耐性在治疗开始前或治疗开始后早期准确地进行判定,结果能够选择治疗效果高的抗癌剂。而且能够避免使用得不到效果的抗癌剂,因此能够避免不必要的副作用。另外,由于使用抗癌剂的疗程期间较长,所以在继续治疗中也可以在每个治疗周期判定抗癌剂感受性,由此,能够进行对于该癌症的抗癌剂感受性的经时性评价,能够判定是否应该继续治疗。作为其结果,能够防止伴随继续投予得不到治疗效果的抗癌剂的癌症的进展,防止副作用的增大,还能够减轻患者的负担,削减医疗费。
49、而且,另外,如果使用该标记,能够筛选使抗癌剂感受性增强的药剂,通过并用成为其对象的抗癌剂和抗癌剂感受性增强剂,能够飞跃性地提高癌症治疗效果。本发明的抗癌剂感受性判定标记的测定试剂作为抗癌剂感受性判定试剂是有用的。
- 还没有人留言评论。精彩留言会获得点赞!