一种快速鉴别检测SADS-CoV与TGEV的乳胶双联免疫层析试纸条及其制备方法
本发明属于生物,具体涉及一种快速鉴别检测猪急性腹泻综合征冠状病毒(sads-cov)与猪传染性胃肠炎冠状病毒(tgev)的乳胶双联免疫层析试纸条及其制备方法。
背景技术:
1、由于近年来我国猪群饲养方式的改变以及从国外引进种猪的频率不断增加,在一定程度导致引起猪腹泻的病因变得复杂。其中最为复杂的则是病毒性腹泻,对仔猪的危害极大。临床上腹泻病毒经常以两种或更多种病毒混合感染的方式存在,无疑增加了防控的难度,同时对国家养殖业造成了巨大的经济损失。在当前尚无有效疫苗的条件下,建立能够快速且便捷的对多种病毒同时鉴别检测的诊断方法就显得尤为重要。
2、猪急性腹泻综合征冠状病毒(swine acute diarrhea syndrome virus,sads-cov)与猪传染性胃肠炎冠状病毒(porcine transmissible gastroenteritis virus,tgev)是猪的两种肠道冠状病毒,其临床症状均表现为急性腹泻、呕吐、新生仔猪由于严重脱水、体重下降而死亡。两种病原常用的病原学检测方法均包括病毒分离鉴定、免疫组化、酶联免疫吸附试验(elisa)或聚合酶链式反应(pcr)和实时定量pcr等方法。然而,这些方法检测时间长、操作复杂,需特定的或昂贵的大型仪器以及专业的技术人员,很难满足基层养殖场快速、廉价、高效监测的要求。相较于上述方法,免疫层析检测技术能够在保证高灵敏度和强特异性的条件下将整体反应时间严格控制在10~15min内,极大的缩短了操作时间,提高了检测效率,非常适用于基层或现场的快速筛查。
3、免疫层析检测技术常用的标记物包括胶体金、乳胶、量子点以及时间分辨荧光微球等。其中胶体金最为常用,但其在反应过程中容易受ph和盐离子等的影响,因此稳定性欠佳。基于乳胶微球表面链接有羧基基团,其在水溶性二亚胺(edc)的作用下发生活化,能够与蛋白或抗体的氨基基团发生共价结合,形成稳定且牢固的化学键,在反应过程中不易受到ph和高浓度盐离子的影响,因此,乳胶微球的稳定性强于胶体金。相较于胶体金,乳胶微球内部填充了油溶性彩色染料,对比度高、颜色深、可视化程度,在显色效果上同样优于胶体金。
4、冠状病毒核衣壳蛋白(n)保守性好,且在病毒感染的整个过程中均能大量表达,能够刺激机体产生特异性抗体。n蛋白在免疫学诊断和新型疫苗研发方面均具有重要的应用价值。
技术实现思路
1、本发明基于冠状病毒核衣壳蛋白(n蛋白)的特性,同时结合乳胶微球的优势,提供一种可以快速鉴别检测sads-cov与tgev的乳胶双联免疫层析试纸条,该试纸条耗时短、操作简便、可不借助任何仪器直接用肉眼观察、且显色明显,灵敏度强,可用于临床上tgev与sads-cov混合感染样本的检测,为tgev与sads-cov的防控提供新的技术支撑,同时这也是当前第一个能够同时检测tgev与sads-cov的双联乳胶试纸条。
2、本发明具体包括以下内容:
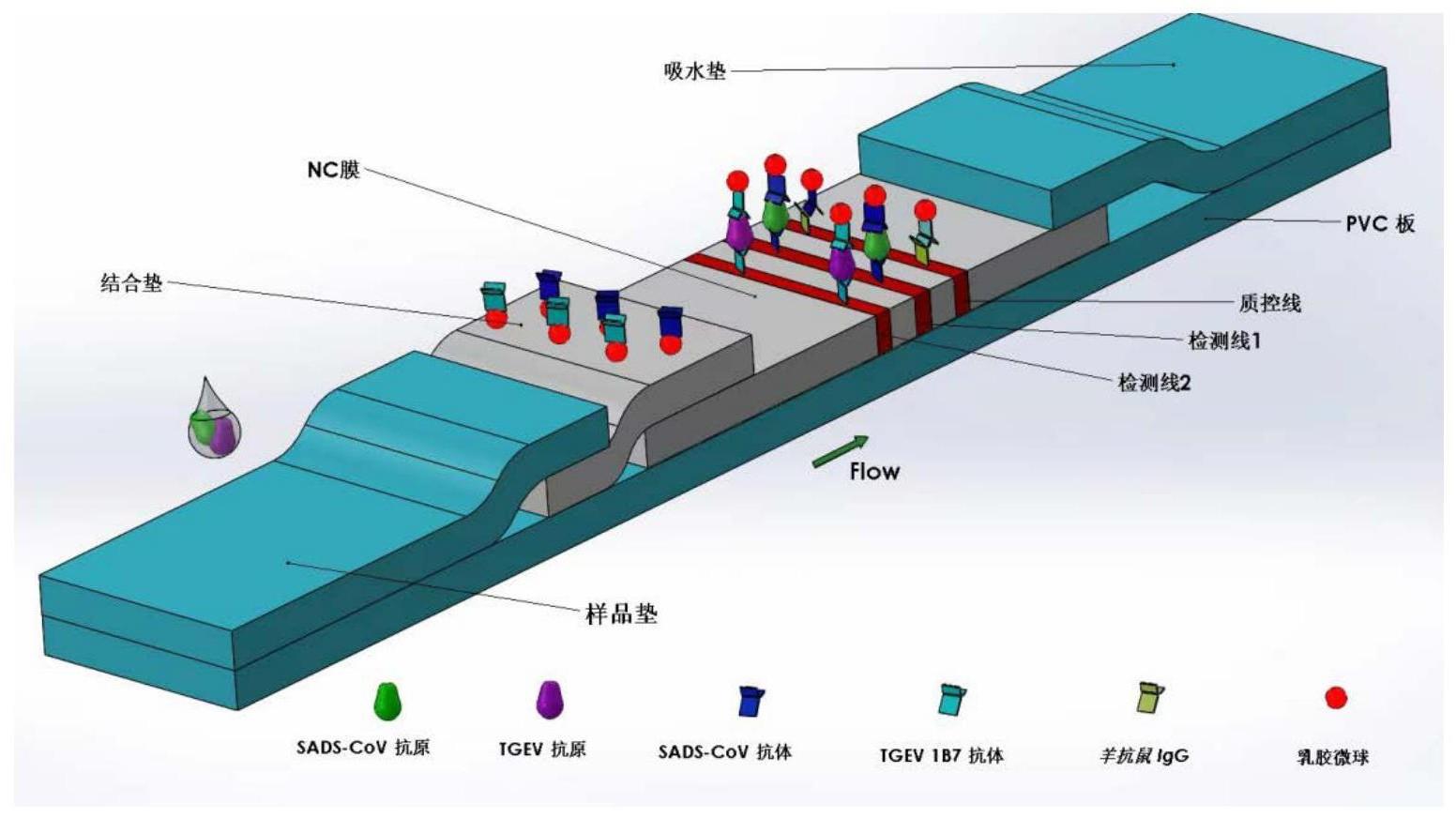
3、第一方面,本发明提供了一种用于快速检测猪传染性胃肠炎与猪急性腹泻综合征乳胶双联免疫层析试纸条。该试纸条包括pvc底板、样品垫、结合垫、硝酸纤维素膜和吸水垫;所述结合垫上喷涂乳胶微球标记的抗tgev n蛋白的单克隆抗体1b7和抗sads-cov n蛋白的单克隆抗体6e8。硝酸纤维素膜上设有质控线c和检测线t1和检测线t2,检测线t1线处包被抗sads-cov n蛋白的单克隆抗体6e8,检测线t2线处包被抗tgev n蛋白的单克隆抗体2a9,质控线c线处包被羊抗鼠igg。
4、其中,本发明的抗tgev n蛋白的单克隆抗体1b7的重链可变区包括氨基酸序列为gfnikdty的cdr1、氨基酸序列为idpadgyt的cdr2、氨基酸序列为arpgtldy的cdr3,本发明的抗tgev n蛋白的单克隆抗体2a9的重链可变区包括氨基酸序列为gytftdfn的cdr1、氨基酸序列为inpnngrs的cdr2、氨基酸序列为arrhwdwyfdv的cdr3。
5、本发明的抗tgev n蛋白的单克隆抗体1b7的轻链可变区包括氨基酸序列为ksvstsgysy的cdr1、氨基酸序列为lvs的cdr2、氨基酸序列为qhireltr的cdr3,本发明的抗tgev n蛋白的单克隆抗体2a9的轻链可变区包括氨基酸序列为ksllhsn的cdr1、氨基酸序列为qms的cdr2、氨基酸序列为aqnlefpwt的cdr3。
6、本发明的抗tgev n蛋白的单克隆抗体1b7的重链可变区的氨基酸序列如seq idno:1所示、轻链可变区的氨基酸序列如seq id no:2所示;本发明的抗tgev n蛋白的单克隆抗体2a9的重链可变区的氨基酸序列如seq id no:3所示、轻链可变区的氨基酸序列如seqid no:4所示。
7、本发明的抗tgev n蛋白的单克隆抗体1b7的重链可变区的dna序列如seq id no:5所示、轻链可变区的dna序列如seq id no:6所示;本发明的抗tgev n蛋白的单克隆抗体2a9的重链可变区的dna序列如seq id no:7所示、轻链可变区的dna序列如seq id no:8所示。
8、本发明的抗tgev n蛋白单克隆抗体重链恒定区为igg1或igg2b型。本发明的抗tgev n蛋白单克隆抗体轻链恒定区为kappa型。
9、另外,本发明的抗sads-cov n蛋白的单克隆抗体6e8采用公开号为cn113956353a的发明的专利方法制备得到,单克隆抗体6e8的重链可变区包括氨基酸序列为gytftdya的cdr1、氨基酸序列为fstyygna的cdr2和氨基酸序列为arggdyygssnvdyamdy的cdr3,单克隆抗体6e8的轻链可变区包括氨基酸序列为ksvstsgysy的cdr1、氨基酸序列为lvs的cdr2和氨基酸序列为qhireltrcdr3。
10、进一步的,抗sads-cov n蛋白的单克隆抗体6e8的重链可变区的氨基酸序列如seqid no:9所示、轻链可变区的氨基酸序列如seq id no:10所示。
11、优选地,所述样品垫采用样品垫封闭液浸泡处理;所述样品垫封闭液为含有2%bsa、0.5%s17、2%peg20000及0.5%酪蛋白酸钠的tris-hcl溶液。其中s17为表面活性剂。
12、优选地,所述结合垫的制备方法为:
13、将结合垫采用结合垫封闭液封闭处理;
14、将乳胶微球用n-乙基-n′-(3-二甲基氨丙基)碳二亚胺(edc)和n-羟基琥珀酰亚胺(nhs)活化后,离心,用mes缓冲液重悬,超声使乳胶微球充分分散,随后加入抗tgev n蛋白的单克隆抗体1b7和抗sads-cov n蛋白的单克隆抗体6e8,室温孵育,再加入封闭液进行封闭,室温孵育,离心;用乳胶微球标记物保护剂将沉淀重悬,即得抗tgev n蛋白的单克隆抗体1b7和抗sads-cov n蛋白的单克隆抗体6e8的乳胶微球标记混合溶液;
15、将上述制备的抗tgev n蛋白的单克隆抗体1b7和抗sads-cov n蛋白的单克隆抗体6e8的乳胶微球标记混合溶液均匀喷涂在已封闭好的结合垫上。
16、所述结合垫封闭液为含有5%m/v蔗糖、1.5%m/v bsa、2%m/v tween-20和1.5%m/v pvp-40的超纯水溶液。
17、所述乳胶微球标记物封闭液为含有10%m/v bsa的超纯水溶液。
18、所述乳胶微球标记物保护剂为含有3%m/v蔗糖、1%m/v pvp-40、1%v/v tween-20的tris-hcl溶液。
19、所述抗tgev n蛋白的单克隆抗体1b7和sads-cov n蛋白的单克隆抗体6e8的乳胶微球标记混合溶液组成为:每1ml乳胶微球溶液含80μg tgev n蛋白单克隆抗体1b7和80μgsads-cov n蛋白的单克隆抗体6e8。
20、优选地,所述检测线t1包被有1mg/ml sads-cov n蛋白单克隆抗体6e8。
21、优选地,所述检测线t2包被有1mg/ml的tgev n蛋白单克隆抗体2a9。
22、优选地,所述质控线c包被有1mg/ml的羊抗鼠igg。
23、第二方面,本发明提供了一种上述快速检测tgev与sads-cov乳胶双联免疫层析试纸条的制备方法。所述方法包括以下步骤:
24、(1)制备样品垫和包被有抗tgev n蛋白的单克隆抗体1b7和抗sads-cov n蛋白的单克隆抗体6e8的乳胶微球标记的结合垫;
25、(2)将抗sads-cov n蛋白的单克隆抗体6e8(1mg/ml)和羊抗鼠igg抗体(1mg/ml)间隔3mm喷在硝酸纤维膜上,分别作为检测线t1和质控线c;将抗tgev蛋白单克隆抗体2a9(1mg/ml)喷在离抗sads-cov n蛋白的单克隆抗体6e8(1mg/ml)5mm处,作为检测线t2。
26、(3)将样品垫、结合垫、硝酸纤维素膜和吸水垫依次搭接在pvc底板上,得到鉴别检测tgev与sads-cov乳胶双联免疫层析试纸条。
27、第三方面,本发明试纸条的检测方法,其步骤如下:
28、(1)准备待检样品。
29、(2)检测:取出试纸条平衡至室温,在加样区加入待检样品,室温静置不超过15min。
30、(3)结果判定:反应结束后,通过肉眼对阴阳性进行定性判断。
31、本发明的有益效果是:
32、本发明提供的鉴别检测tgev与sads-cov乳胶双联免疫层析试纸条,单独检测tgev或sads-cov时没有非特异性反应,且与临床症状相似的其他猪源肠道冠状病毒pedv和pdcov不发生交叉反应。同时试纸条能够检出tgev和sads-cov阳性对照中病毒的最低限位分别为104.69tcid50/0.1ml和103.39tcid50/0.1ml,所制备的试纸条具有较好的特异性、灵敏性、操作简单、时间短等优点,为两种腹泻病毒的现场或者实验室的快速鉴别检测提供了一种快速检测方法。
- 还没有人留言评论。精彩留言会获得点赞!