一种红细胞膜中38种脂肪酸的检测方法
本发明涉及分析检测,尤其涉及一种红细胞膜中38种脂肪酸的检测方法。
背景技术:
1、由于不同地区的膳食结构存在较明显的区域差异,同时城乡居民之间的营养与健康状况仍有明显的差异。因此,对人体不同种类的脂肪酸水平进行较为准确的定性和定量检测有助于预防和控制脂类物质相关的代谢性疾病的发生和发展。
2、红细胞膜脂肪酸是衡量人体脂质水平的一个较为客观且稳定的标志,与血清或血浆中的游离脂肪酸相比,红细胞膜脂肪酸更能反映人体内中长期脂肪酸的代谢状态。膳食脂肪酸摄入和内源性脂质代谢共同决定了人血红细胞膜脂肪酸组成,红细胞膜脂肪酸主要包括饱和脂肪酸系列(saturated fatty acids,sfas)、单不饱和脂肪酸系列(monounsaturated fatty acids,mufas)和多不饱和脂肪酸系列(polyunsaturated fattyacids,pufas),其中多不饱和脂肪酸系列还包括ω-3脂肪酸和ω-6脂肪酸。
3、国内外现已有部分研究报道了红细胞膜脂肪酸,陈俊铭(陈俊铭,基于gc-ms技术分析强直性脊柱炎患者红细胞膜脂肪酸的组成及其临床意义[d],南方医科大学,2022年)介绍了采用盐酸甲醇为衍生化试剂,以二十三碳酸为内标,并使用气质联用仪为检测仪器检测红细胞膜中脂肪酸,但是其仅检测了31种脂肪酸,并且其论文中并没有完整的描述提取红细胞膜的过程,也没有对该检测方法进行质量控制实验,以验证其检测方法的准确性。2023年,n.n.eroshchenko等(n.n.eroshchenkoa,*,v.v.veselova,a.v.pirogovb,e.y.danilovab,a.n.kirushina,a.l.paravyana,g.cravottoc,development andvalidation of a hplc-ms/ms method for the analysis of fatty acids-in the formof fame ammonium adducts-in human whole blood and erythrocytes to determineomega-3 index,journal of chromatography b,1227(2023)123799)报道了以十七碳酸为内标,采用液质联用仪正离子模式检测红细胞膜中脂肪酸,但是其仅检测了24种脂肪酸,论文中也没有公布其检测方法的质量控制实验。2023年,erin d.clarke等(erin d.clarke1,2,*,jordan stanford 1,2,jessica j.a.ferguson1,2,lisa g.wood3,4and claree.collins1,2,red blood cell membrane fatty acid composition,dietary fatty acidintake and diet quality as predictors of inflammation in a group ofaustralian adults.nutrients.2023,15(10):2405)报道了以十三碳酸和十九碳酸为内标,气相色谱仪检测红细胞膜中脂肪酸,但其仅检测了18种脂肪酸,论文中同样没有公布其检测方法的质量控制实验。
技术实现思路
1、有鉴于此,本发明的目的在于提供一种红细胞膜中38种脂肪酸的检测方法。本发明提供的检测方法实现了红细胞膜中38种脂肪酸的定性和定量分析。
2、为了实现上述发明目的,本发明提供以下技术方案:
3、本发明提供了一种红细胞膜中38种脂肪酸的检测方法,包括以下步骤:
4、将待测红细胞膜进行脂质提取,得到红细胞膜脂质;
5、将所述红细胞膜脂质进行甲酯化,得到脂肪酸甲酯;
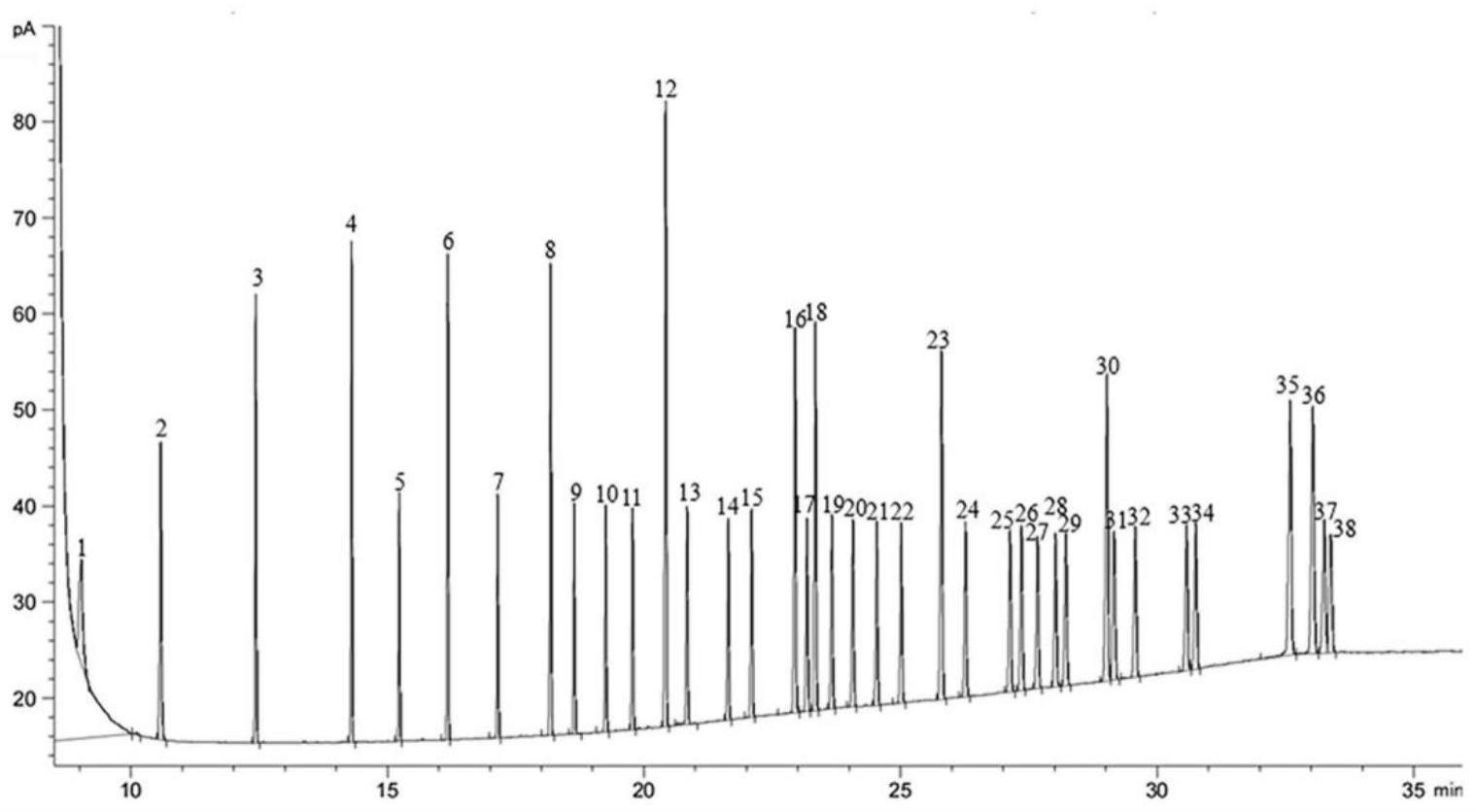
6、将所述脂肪酸甲酯进行气相色谱检测,得到脂肪酸甲酯的色谱信息;
7、基于38种脂肪酸甲酯预制的标准曲线、脂肪酸甲酯的色谱信息和校正因子,实现待测红细胞膜中脂肪酸的检测;
8、所述气相色谱检测的参数包括:
9、色谱柱为(50%-氰丙基)-甲基聚硅氧烷色谱柱;
10、载气为氮气;
11、进样分流比为10:1;
12、进样温度为250℃;
13、检测温度为280℃;
14、色谱柱升温程序为:起始温度为50℃,保持1min,以25℃/min的速率从50℃升温至175℃,然后以4℃/min的速度升温至230℃,保持5min。
15、优选地,所述待测红细胞膜以待测红细胞膜悬浮液的形式使用;所述待测红细胞膜悬浮液的制备方法包括以下步骤:
16、将全血样品进行第一离心,得到血红细胞;
17、将所述血红细胞和预冷的缓冲液混合,进行溶血,得到溶血溶液;
18、将所述溶血溶液进行离心-吹打,得到红细胞膜样品;
19、将所述红细胞膜样品经第二吹打悬浮于等渗pbs缓冲液中,得到所述待测红细胞膜悬浮液;
20、所述第一离心的转速为3800~4000r/min,时间为5~10min;
21、所述预冷的缓冲液的温度为4℃;
22、所述缓冲液为10mml/l、ph值为7.4的tris-hcl缓冲液;
23、所述溶血的温度为4℃,时间为1~2h;
24、所述离心-吹打包括依次进行第二离心和吹打;
25、所述第二离心的转速为12000r/min,时间为30min,温度为4℃;
26、所述离心-吹打的次数为3次;
27、所述待测红细胞膜悬浮液的质量浓度为2.0%~2.5%。
28、优选地,所述脂质提取的试剂包括氯仿和甲醇;所述氯仿和甲醇的体积比为2:1;
29、所述脂质提取的试剂和待测红细胞膜悬浮液的体积比为2:1。
30、优选地,所述脂质提取的方式为涡旋震荡,所述涡旋震荡的时间为10~15min。
31、优选地,所述脂质提取后,还包括离心,将离心所得氯仿层进行氮气吹干;所述离心的转速为3000~3500r/min,时间为3~5min。
32、优选地,所述甲酯化的试剂为三氟化硼甲醇溶液;所述三氟化硼甲醇溶液中三氟化硼的质量浓度为14%。
33、优选地,所述甲酯化的温度为55℃~60℃,时间为10~12h。
34、优选地,所述校正因子的获取方法包括以下步骤:
35、将待测红细胞膜和内标物混合,进行脂质提取,得到含内标物的红细胞膜脂质;
36、将所述含内标物的红细胞膜脂质进行甲酯化,得到含内标物酯化物的脂肪酸甲酯;
37、将所述含内标物酯化物的脂肪酸甲酯进行气相色谱检测,得到内标物酯化物的色谱信息;
38、基于内标物酯化物预制的标准曲线和内标物酯化物的色谱信息,得到内标物酯化物的测定浓度;
39、基于内标物的实际添加浓度和所述内标物酯化物的测定浓度,得到所述校正因子;
40、所述内标物为十一烷酸甘油三脂,所述内标物酯化物为十一烷酸甲酯。
41、优选地,所述待测红细胞膜和内标物混合所得体系中,内标物的浓度为20.00μg/ml~20.82μg/ml。
42、优选地,所述38种脂肪酸包括:丁酸、己酸、辛酸、癸酸、十一烷酸、月桂酸、十三烷酸、肉豆蔻酸、肉豆蔻脑酸、十五烷酸、顺-10-十五碳烯酸、棕榈酸、棕榈酸油、十七烷酸、顺-10-十七碳烯酸、硬脂酸、反油酸、油酸、反亚油酸、亚油酸、γ-亚麻酸、α-亚麻酸、花生酸、顺-11-二十碳烯酸、顺-11,14-二十碳二烯酸、二十一烷酸、顺-8,11,14-二十碳三烯酸、花生四烯酸、顺-11,14,17-二十碳三烯酸、二十二烷酸、顺-5,8,11,14,17-二十碳五烯酸、芥酸、顺-13,16-二十二碳二烯酸、二十三烷酸、木蜡酸、顺-7,10,13,16,19-二十二碳五烯酸、神经酸和顺-4,7,10,13,16,19-二十二碳六烯酸。
43、本发明提供了一种红细胞膜中38种脂肪酸的检测方法,包括以下步骤:将待测红细胞膜进行脂质提取,得到红细胞膜脂质;将所述红细胞膜脂质进行甲酯化,得到脂肪酸甲酯;将所述脂肪酸甲酯进行气相色谱检测,得到脂肪酸甲酯的色谱信息;基于38种脂肪酸甲酯预制的标准曲线、脂肪酸甲酯的色谱信息和校正因子,实现待测红细胞膜中脂肪酸的检测;所述气相色谱检测的参数包括:色谱柱为(50%-氰丙基)-甲基聚硅氧烷色谱柱;载气为氮气;进样分流比为10:1;进样温度为250℃;检测温度为280℃;色谱柱升温程序为:起始温度为50℃,保持1min,以25℃/min的速率从50℃升温至175℃,然后以4℃/min的速度升温至230℃,保持5min。本发明提供的检测方法能够使得38种脂肪酸甲酯很好地分离,进而实现红细胞膜中38种脂肪酸的定性和定量检测。同时,本发明的检测方法依托预制的标准曲线和校正因子,补偿了红细胞膜脂肪酸在样品前处理时的损失,克服了单一采用外标法或内标法带来的检测不便,以实现红细胞膜中38种脂肪酸的准确定性和定量。另外,本发明的检测方法具有优异的重现性和精密度。
- 还没有人留言评论。精彩留言会获得点赞!