外泌体上表面活性物质在制备辅助诊断间质性肺疾病产品中的应用的制作方法
本发明涉及标志物检测,尤其涉及一种肺疾病相关蛋白检测。
背景技术:
1、间质性肺疾病(interstitial lung disease,ild)主要是由于肺实质发生炎症或纤维化,并引起肺泡-毛细血管功能单位丧失的一类肺部异质性疾病,以炎症浸润、纤维化、细胞增殖等病理变化累及肺间质为共同特征。ild包括了200余种疾病亚型,其诊断依赖于病史、体格检查、肺功能测试、高分辨率计算机断层扫描(hrct)以及必要时的支气管肺泡灌洗和肺活检结果,但该类疾病起病隐匿,缺乏早期诊断、疾病监测以及预后评估的敏感指标。相较于传统的hrct、肺功能等检查,血清学检测更加简单易普及,目前通过血清标志物对ild疾病进行早筛已经成为研究热点。
2、表面活性物质(sp)是一种分布于肺泡液体分子层表层的复杂脂蛋白复合物,主要由肺泡ii型上皮细胞(aecii)产生和分泌。表面活性物质包括肺泡表面活性蛋白a(sp-a)、肺泡表面活性蛋白b(sp-b)、肺泡表面活性蛋白c(sp-c)及肺泡表面活性蛋白d(sp-d)。sp-a和sp-d是亲水性表面活性蛋白,与肺的先天宿主防御直接相关。sp-b和sp-c是疏水性表面活性蛋白,在呼吸循环期间可保持脂质膜的稳定性。
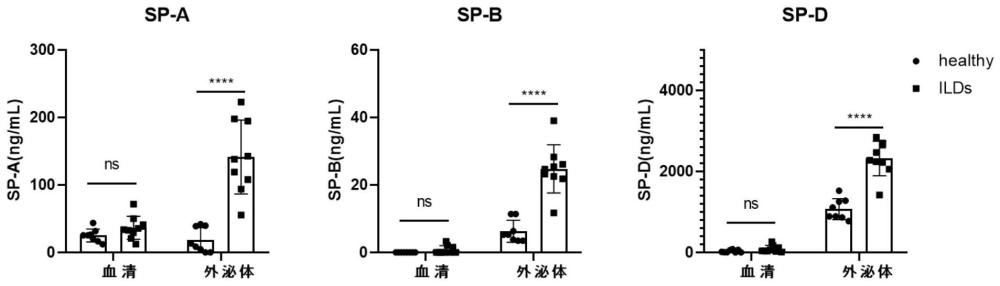
3、sp-a和sp-d的水平与间质性肺疾病的严重程度有关,并且已被广泛研究。但由于sp-a和sp-d的血清检测灵敏度和特异性不够,因此目前在临床中应用受到限制。sp-b和sp-c在脂质在气-液界面的吸附过程中起到了促进作用,有助于肺表面活性物质脂类对气–液界面的吸附。但是,由于sp-b和sp-c为疏水性蛋白,在血清中被检测的困难度较高。因此,为了更好地评估肺疾病的严重程度,需要对sp的检测方法进行进一步的优化和改进。
4、外泌体是一种细胞外的小囊泡,直径在40nm-160nm之间,负责在细胞内和细胞间传递信息。不同种类的细胞在正常和病变状态下都能够分泌外泌体,用于细胞间通讯和信号传递。在外泌体形成的过程中,表面活性蛋白可以被保留在其表面,并随着外泌体的分泌进入到血流中。外泌体表面活性蛋白在血清学诊断方面具有很大的潜在临床价值。然而,目前尚未见报道使用外泌体表面活性物质用于间质性肺部疾病诊断的研究。因此,利用外泌体表面活性蛋白进行间质性肺部疾病的临床诊断具有很大的发展潜力,但需要进一步的研究和探索,建立一种通过准确检测外泌体上间质性肺疾病相关蛋白质的方法,用于诊断间质性肺疾病以及预测其疾病进展具有重要的临床价值和研究价值。
技术实现思路
1、本发明的目的在于提供外泌体上表面活性物质在制备辅助诊断间质性肺疾病产品中的应用,以解决现有技术中缺少将外泌体表面活性物质应用在诊断间质性肺部疾病的相关技术等问题。
2、肺表面活性蛋白如sp-a、sp-b、sp-d蛋白都表达于ⅱ型肺泡上皮细胞表面,在肺损伤、炎症和肺泡毛细血管通透性屏障改变的情况下,肺表面活性物质会泄漏到血液中。因此,血液中肺表面活性蛋白可以作为肺损伤和呼吸病理的早期标志物辅助诊断间质性肺疾病。其在血液中以游离蛋白和细胞外囊泡(主要为外泌体)膜载蛋白两种形式存在。
3、为解决上述问题,本发明提供技术方案如下:
4、外泌体上表面活性物质在制备辅助诊断间质性肺疾病产品中的应用,外泌体上表面活性物质选自sp-a、sp-b。
5、所述辅助诊断间质性肺疾病产品包括辅助诊断间质性肺疾病检测试剂或试剂盒。
6、进一步地,所述产品包括磁珠包被物、发光物标记的检测抗体、外泌体样本处理液、预激发液、激发液、标准品。
7、进一步地,所述产品包括磁珠包被物工作液、发光物标记的检测抗体工作液、外泌体样本处理液、预激发液、激发液、标准品。
8、进一步地,磁珠包被物工作液制备过程包括:edc和nhs活化磁珠,活化后的磁珠与捕获抗体偶联得到磁珠-抗体偶联物,磁珠-抗体偶联物与封闭剂孵育,得到磁珠包被物,使用磁珠包被物稀释液稀释磁珠包被物,得到磁珠包被物工作液。
9、进一步地,所述磁珠包被物工作液详细制备过程包括:
10、往1ml磁珠缓冲液中加入5-20mg磁珠,加入25μl浓度为20mg/ml的edc溶液和25μl浓度为40mg/ml的nhs溶液,室温反应15-120min,使磁珠活化,分离去上清;
11、1ml磁珠缓冲液重悬活化后的磁珠,加入100-300μg待包被的捕获抗体,室温孵育1-2h,得到含有磁珠-抗体偶联物的溶液;
12、向含有磁珠-抗体偶联物的溶液中加入100μl封闭剂,含有磁珠-抗体偶联物的溶液与封闭剂的体积比为1:0.1,室温孵育1-2h,磁分离去除上清后,加入1ml磁珠稀释液,得到磁珠包被物重悬液,使用磁珠包被物稀释液稀释磁珠包被物重悬液,得到浓度为0.1-1.5mg/ml的磁珠包被物工作液。优选浓度为0.3-0.8mg/ml的磁珠包被物工作液。
13、进一步地,所述磁珠缓冲液为含质量分数1%mes的水溶液;
14、所述捕获抗体选自sp-a捕获抗体、sp-b捕获抗体;
15、所述封闭剂为含质量分数1%牛血清白蛋白的水溶液;
16、所述磁珠稀释液为含质量分数1%bsa、质量分数0.1%proclin 300的pbs缓冲液;
17、所述磁珠包被物稀释液为按质量分数计,含0.05-0.1%tris、0.9-3.0%nacl、1-3%bsa、0.1-0.5%tween-20,0.1%叠氮钠,其余为水,ph7.5。
18、进一步地,所述发光物标记的检测抗体工作液的制备过程包括:检测抗体和发光物反应,淬灭反应,纯化,使用发光标记物稀释液稀释,得到发光物标记的检测抗体工作液。
19、进一步地,所述发光物标记的检测抗体工作液的制备过程是:1.25mmol/l发光物工作液5μl、1μg/μl检测抗体溶液400μl避光室温标记反应0.5-2h,加入100μl标记终止缓冲液,室温混匀30-120min,纯化,得到发光物标记的检测抗体,将发光物标记的检测抗体使用标记物稀释液稀释,得到浓度为0.05-1.00μg/ml的发光物标记的检测抗体工作液。特别优选浓度为0.1-0.6μg/ml的发光物标记的检测抗体工作液。
20、进一步地,所述发光物工作液是使用无水dmf稀释发光物配制而成;
21、所述发光物选自吖啶酯、碱性磷酸酶、辣根过氧化物酶;
22、所述检测抗体溶液是使用ph=9.0的0.2m nahco3溶液稀释检测抗体配制而成,所述检测抗体选自sp-a检测抗体、sp-b检测抗体;
23、所述标记终止缓冲液是含质量分数10%赖氨酸的0.2m nahco3溶液,ph9.0;
24、发光标记物稀释液是按质量分数计,含mes 0.1%、nacl 2%、bsa 3%、tween-200.1%、叠氮钠0.1%,其余为水,ph6.5。
25、进一步地,所述外泌体样本处理液是按质量分数计,含有0.1%proclin300、1%bsa、0.1%tween-20、0.05%edta-2na,1%蔗糖的pbs缓冲液,ph=7.4;
26、在本说明书公开的前提下,本领域技术人员能够准确理解所述预激发液、激发液是视发光物具体种类而进行具体选择,比如,发光物为吖啶酯时,预激发液、激发液可以选择为:ae预激发液、激发液;
27、所述标准品选自sp-a标准品、sp-b标准品。
28、进一步地,所述辅助诊断肺部疾病产品包括辅助诊断间质性肺疾病检测试剂盒。
29、上述试剂盒用于检测外泌体上蛋白含量的方法,步骤如下:
30、先对待测外泌体样本进行预处理,将待测外泌体样本与样本处理液混合,得到预处理后的待测外泌体样本;
31、待测外泌体样本中含有sp-a蛋白和/或sp-b蛋白的外泌体通过与磁珠包被物工作液和发光物标记的抗体工作液反应,形成免疫复合物,利用化学发光法检测发光强度并根据标准曲线计算浓度值。
32、在一个具体的可实施方案中,试剂盒用于外泌体上sp-a和/或sp-b蛋白含量的检测方法,具体步骤如下:
33、(1)对待测外泌体样本进行预处理:待测外泌体样本与样本处理液混合反应;
34、(2)将步骤(1)得到的预处理后的待测外泌体样本与磁珠包被物工作液混合反应,得到磁珠-抗原复合物;
35、(3)将步骤(2)得到的磁珠-抗原复合物与发光物标记抗体工作液的检测抗体混合反应,得到磁珠-抗原-检测抗体复合物;
36、(4)将步骤(3)得到的磁珠-抗原-检测抗体复合物与发光底物(预激发液、激发液)混合反应,检测发光强度。
37、(5)使用标准曲线法,根据步骤(4)检测得到的发光强度计算得到待测外泌体样本中蛋白的含量。
38、待测外泌体样本可以为全血、血清、血浆、支气管肺泡灌注液或尿液中的任意一种待测样本制备得到。
39、待测外泌体样本的制备方法为全自动外泌体提取仪器或试剂盒法,优选地,使用全自动外泌体提取仪器。
40、本发明与现有技术相比具有以下优点:
41、1、本发明对外泌体上的sp-a、sp-b、sp-d蛋白检测减少了血清中游离的sp-a、sp-b、sp-d蛋白以及其他血清内源性干扰物的影响,具有更高的灵敏度。而进一步研究发现,血液中外泌体上sp-a和/或sp-b蛋白检测比外泌体上sp-d具有更高的临床符合率。外泌体上sp-a蛋白和/或sp-b蛋白检测结果可以用于间质性肺部疾病辅助诊断;
42、2、外泌体上sp-a和/或sp-b蛋白检测结果具有高临床符合率,可以有效辅助诊断出间质性肺疾病的患者,有助于更早给予有效治疗,避免耽误病情;
43、3、本发明针对外泌体sp-a和/或sp-b蛋白检测的特异性和敏感度均优于血清sp-a和/或sp-b蛋白检测、外泌体sp-d蛋白检测,外泌体上的sp-a和/或sp-b可能可以超越血清sp-a和/或sp-d在临床中的诊断价值;
44、4、本发明实现了外泌体上蛋白的稳定检测,对于外泌体蛋白质的研究具有重要价值。
- 还没有人留言评论。精彩留言会获得点赞!