人绒毛膜促性腺激素β亚单位含量检测方法及试剂盒与流程
本发明涉及生物检测领域,尤其涉及人绒毛膜促性腺激素β亚单位含量检测方法及试剂盒。
背景技术:
1、人绒毛膜促性腺激素亚单位(human chorionic gonadotropin,hcg)是由胎盘合体滋养细胞分泌的一种糖蛋白激素,其反映的滋养层细胞绒毛的功能状态。hcg结构中包括α和β两种亚基,α链与β链由11或12个二硫键相连结,α链与黄体生成素(lh)、卵泡刺激素(fsh)和促甲状腺激素(tsh)相类似。β-hcg是hcg中的一个分子β亚基,由145个氨基酸组成,其相对分子质量为23kd,在血液中即可检测到。在正常怀孕周期,妊娠早期浓度偏低,从妊娠第5周其浓度迅速上升,至妊娠8~10周血清浓度达高峰近200000iu/l,11~16周有所下降,此后基本稳定至分娩,产后1周左右血中hcg基本消失,因此,根据怀孕周期不同,其血清浓度值跨度极大。
2、现有的检测方法如:免疫层析法和化学发光法,其中,免疫层析法技术一般是将其中抗体或抗原固定于载体(如硝酸纤维素膜)上,同时将另一个抗体标记上示踪剂或者荧光物质(如胶体金颗粒、镧系元素及螯合剂标记微球、彩色微球等)或抗原固定于玻璃纤维上,当样本中含有待检测物质时,标记的抗原或抗体与硝酸纤维素膜上的抗体反应,而载体硝酸纤维素膜留有金颗粒、荧光物质或者彩色微球,而其t条带上(t线)荧光或者显色物质的强弱与待测物质的浓度呈线性关系。产品检测通量较低,一般都需要手工加样操作,并且其容易受其他因素影响,如检测环境中的温度、适度,膜条平整度,脏污程度,样本一致性、粘度等。
3、化学发光法,原理是采用辣根过氧化物酶(hrp)标记抗体(或抗原),在与反应体系中的待测标本和固相载体发生免疫反应后,形成固相包被抗体-待测抗原-酶(hrp)标记抗体复合物,这时加入鲁米诺发光剂、h2o2和化学发光增强剂使产生化学发光,通过hrp催化反应,在增强剂的存在下生成平面共轭结构,使得其发光强度增强很多倍。由于鲁米诺类的各衍生物引入的功能集团不同,在发光幅度的增强上也会有不同。另外,hrp催化反应受限于hrp酶活,长时间液体环境中,酶会逐渐失活,导致检测发光值下降,因而在稳定性上略差。
4、现有技术中,针对人绒毛膜促性腺激素β亚单位的免疫学检测有免疫层析法、化学发光法等常见检测方法,受检测方法和固相载体形式的影响,检测盒的检测上限大多不超过10000iu/l,若样本浓度超出该试剂盒的检测上限值则需稀释样本后再测,如申请公布号为cn114002444a,名称为《β-人绒毛膜促性腺激素检测试剂盒》的发明专利,公开了一种β-人绒毛膜促性腺激素检测试剂盒,包括有试剂r1、试剂r3和试剂r4;其中,所述试剂r1具有链霉亲和素包被的磁性微粒和三羟甲基氨基甲烷tris缓冲液,所述试剂r3具有吖啶酯标记的鼠抗人hcg抗体和磷酸盐缓冲液,所述试剂r4具有生物素标记的鼠抗人hcg抗体和吗啉乙磺酸mes,该试剂盒的检测上限为8000miu/ml,需先判断样本中hcg+β的浓度是否超过8000miu/ml,当样本中hcg+β的浓度超过8000miu/ml时,需用样本稀释液对样本进行稀释(推荐稀释倍数为100倍)后再进行检测。
5、在稀释样本再测试前,需先判断样本浓度是否超过试剂盒的检测上限,因此,授权公告号为cn108152505b,名称为《免疫测定方法、用于鉴定免疫测定的系统和试剂盒》,提供一种免疫测定方法,用于判断样本是否需稀释再测定;采用化学发光免疫法读取两次读数,并记录两次读数所得信号值的增幅制作标准曲线,在后续的检测中,若待测目标抗原或抗体的待测样本的两次读数的增幅大于所述标准曲线的最大值,则需要对样品进行稀释后再进行测定,在该发明中,其检测上限为10000miu/ml。
6、因此,现有技术中,必须先待测样本浓度是否超出该试剂盒的检测上限值,若样本浓度超出该试剂盒的检测上限值则需稀释样本后再测,当样本浓度过高时,需重复测试多次后将每次所测得的信号值叠加才能获得最终结果,而多次判断样本是否超出浓度上限、读取样本信号值以及计算样本最终信号值,不仅过程复杂、检测、计算量较大,而且其中任一一次检测或者计算出现错误,都会影响样本的最终检测结果,同时,在多次稀释和检测过程中,hrp酶会逐渐失活,导致检测发光值下降,影响测试的稳定性。
技术实现思路
1、因此,为解决上述问题,实现人绒毛膜促性腺激素β亚单位含量检测的简便性、检测结果的稳定性和准确性,本发明提供了人绒毛膜促性腺激素β亚单位含量检测方法及试剂盒。
2、本发明是通过以下技术方案实现的:
3、人绒毛膜促性腺激素β亚单位含量检测方法,包括以下步骤:
4、s1:配备人绒毛膜促性腺激素β亚单位含量检测试剂盒;
5、所述试剂盒包括石英针生物传感器、用于容纳样本的试剂孔1、容纳有标记生物素的抗人绒毛膜促性腺激素β亚单位抗体的试剂孔2、容纳有多聚糖标记的链霉亲和素荧光物质的试剂孔3以及容纳有清洗液的清洗孔1、清洗孔2、清洗孔3、清洗孔4、清洗孔5、清洗孔6、清洗孔7、清洗孔8和清洗孔9,所述清洗孔9为读数孔;
6、s2:将校准品放入试剂盒的试剂孔1中,用石英针生物传感器依次放入试剂孔1、试剂孔2和试剂孔3中,完成第一次反应后读数,读取第一次读取信号;
7、s3:将石英针放入试剂盒中清洗后,继续将石英针生物传感器依次放入试剂孔2和试剂孔3中,完成第二次反应后读数,读取第二次读取信号;
8、s4:对不同浓度的校准品重复进行步骤s2和s3,并依次记录每个浓度的校准品的第一次读取信号和第二次读取信号;
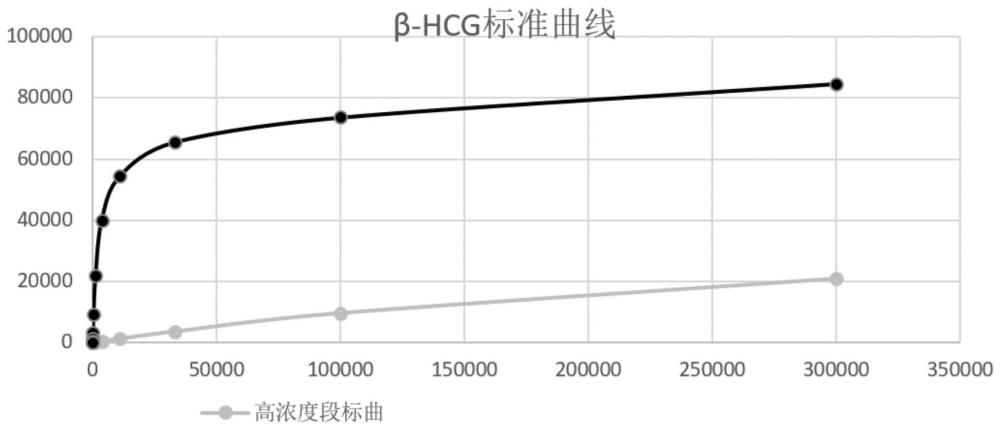
9、s5:根据步骤s4中获得的第一次读取信号和第二次读取信号依次获得高浓度段信号标准曲线和低浓度段信号标准曲线;
10、s6:检测待测样本的信号值,并利用高浓度段信号标准曲线和/或低浓度段信号标准曲线对待测样本进行回算得到其浓度;
11、上述步骤s2和步骤s3中,每次反应时,在石英针生物传感器放入下一个试剂孔前,均需放入清洗孔中清洗。
12、优选的,所述石英针为氨丙基修饰后的石英针,所述石英针生物传感器的底部表面在包被捕获抗体后烘干。
13、优选的,所述第一次反应的反应时间小于所述第二次反应的反应时间。
14、优选的,第一次反应时石英针生物传感器的转速低于第二次反应时石英针生物传感器的转速。
15、优选的,步骤s4中,“对不同浓度的校准品重复进行步骤s2和s3”是指,对浓度范围在试剂盒的检测上限之内的多个已知的不同浓度的人绒毛膜促性腺激素β亚单位抗原校准品分别进行步骤s2和s3。
16、优选的,所述步骤s5还包括:根据步骤s4记录的每个浓度的校准品的第一次读取信号和第二次读取信号,并将多个第一次读取信号制作成高浓度段信号标准曲线,将多个第二次读取信号制作成低浓度段信号标准曲线,并设定高浓度段信号标准曲线和低浓度段信号标准曲线的决断点。
17、优选的,所述步骤s2包括:
18、s2.1:将石英针生物传感器置入试剂孔1内的样本中反应10s-20s,转速1000rpm-1200rpm;
19、s2.2:将反应过的生物传感器到清洗孔7,清洗孔8中清洗5s-10s,转速1000rpm-1200rpm;
20、s2.3:将清洗后的生物传感器置入试剂孔2中反应10s-20s,转速1000rpm-1200rpm;
21、s2.4:将反应过的生物传感器到清洗孔5,清洗孔6中清洗5s-10s,转速1000rpm-1200rpm;
22、s2.5:将清洗后的生物传感器置入试剂孔3中反应10s-20s,转速1000rpm-1200rpm;
23、s2.6:将循环反应好的生物传感器置入清洗孔9中读数,读取第一次读取信号。
24、优选的,所述步骤s3包括:
25、s3.1:将反应好的生物传感器置入清洗孔3,清洗孔4中清洗5s-10s,转速1000rpm-1200rpm;
26、s3.2:再将清洗后的生物传感器置入试剂孔2中反应40s-80s,转速1200rpm-1500rpm;
27、s3.3:将反应过的生物传感器到清洗孔5,清洗孔6中清洗5s-10s,转速1000rpm-1200rpm;
28、s3.4:再将清洗好的生物传感器置入试剂孔3中反应10s-20s,转速1000rpm-1200rpm;
29、s3.5:将反应好的生物传感器到清洗孔1,清洗孔2中清洗5s-10s,转速1000rpm-1200rpm;
30、s3.6:将循环反应好的生物传感器置入清洗孔9中读数,读取第二次读取信号。
31、优选的,所述步骤s6包括:
32、s6.1:将待测样本放入试剂盒的试剂孔1中,用石英针生物传感器依次放入试剂孔1、试剂孔2和试剂孔3中,完成第一次反应后读数,读取第一次读取信号;
33、s6.2:将石英针放入试剂盒中清洗后,继续将石英针生物传感器依次放入试剂孔2和试剂孔3中,完成第二次反应后读数,读取第二次读取信号;
34、s6.3:若样本低于决断点的浓度值,则仅能读取到第二次读取信号,并将样本放入低浓度段信号标准曲线上回算,比对后获得样本浓度值;
35、若样本高于决断点的浓度值,则仅能读取到第一次读取信号,并将样本放入高浓度段信号标准曲线上回算,比对后获得样本浓度值;
36、若样本位于决断点附近,则可同时读取到第一次读取信号和第二次读取信号,此时分别将样本放入低浓度段信号标准曲线和高浓度段信号标准曲线上回算,比对获得两个样本浓度值,并计算两个样本浓度值的平均值作为样本浓度值。
37、人绒毛膜促性腺激素β亚单位含量检测试剂盒,包括石英针生物传感器、用于容纳样本的试剂孔1、容纳有标记生物素的抗人绒毛膜促性腺激素β亚单位抗体的试剂孔2、容纳有多聚糖标记的链霉亲和素荧光物质的试剂孔3以及容纳有清洗液的清洗孔1、清洗孔2、清洗孔3、清洗孔4、清洗孔5、清洗孔6、清洗孔7、清洗孔8和清洗孔9,所述清洗孔9为读数孔;
38、所述石英针生物传感器的底部表面在包被捕获抗体后烘干,所述捕获抗体包括抗fitc抗体和荧光素标记的人绒毛膜促性腺激素β亚单位抗体,其中,抗fitc抗体和荧光素标记的人绒毛膜促性腺激素β亚单位抗体的浓度比为2:3;
39、所述试剂孔2中的标记生物素的抗人绒毛膜促性腺激素β亚单位抗体中,生物素与抗人绒毛膜促性腺激素β亚单位抗体的比例为(5-10):1,且所述标记生物素的抗人绒毛膜促性腺激素β亚单位抗体用保存液室温下稀释到1ug/ml;
40、所述试剂孔3中的多聚糖标记的链霉亲和素荧光物质用保存液室温下稀释到5ug/ml。
41、本发明技术方案的有益效果主要体现在:
42、1、本方案采用的试剂盒中,利用氨丙基修饰后的石英针放入试剂盒内各试剂孔中进行反应,便于控制探针在各试剂内的反应时间和转速,在高浓度段时其反应时间短,转速低,而低浓度段时其反应时间长,转速更高,结合更饱和,充分区分高浓度和低浓度样品,提升低端检测灵敏度和检验范围,通过调整两次反应的反应时间和转速,从而可在同一试剂盒内的同次检测中获得不同浓度段的信号值,相对于现有技术,其检测上限提高30倍,可涵括β-hcg的浓度上限,无需通过多次稀释和检测获得信号值,可以避免同一个样本的多次检测,节约了检测时间和成本。
43、2、预先通过重复检测位于检测上限值内的多个不同浓度的样本,分别获得高浓度段和低浓度段对应浓度与信号值的标准曲线,在测试待测样本时,先通过试剂盒反应,并读取两次信号后,对比标准曲线即可获得待测样本的浓度,简化了检测过程,极大地提高了检测的便利性,同时无需多次稀释、读取以及计算,避免hrp酶在长时间的液体环境中逐渐失活,提高了检测结果的准确性和稳定性。
44、3、试剂盒内的石英针生物传感器表面预先通过aps修饰,aps作为疏水性介质,既保证抗体结合时的有效性,也能去除其他杂蛋白或者杂质对石英针的吸附,因而抗体在石英探针表面的致密度高,检测准确性效果好,通过aps修饰后的石英针包被捕获抗体,捕获抗体包括抗fitc抗体(荧光素抗体)和荧光素标记的人绒毛膜促性腺激素β亚单位抗体,荧光素标记的人绒毛膜促性腺激素β亚单位抗体可以通过荧光素测定标记抗体的浓度,抗fitc抗体可以和荧光素标记的人绒毛膜促性腺激素β亚单位抗体的荧光素特异性的共价结合反应,使捕获抗体通过疏水性结合牢固、均一地固定于石英针生物传感器表面。
45、4、试剂盒中标记生物素的人绒毛膜促性腺激素β亚单位检测抗体与多糖骨架偶联生物素-sa标记结合,经过生物素亲和素放大,其检测背景保持不变,通过循环增强,检测信号增大了数十上百倍,大大提升了检测信号水平,因而可以检测到更低浓度人绒毛膜促性腺激素β亚单位,提高了检测灵敏度。
- 还没有人留言评论。精彩留言会获得点赞!