微尺度细胞检测传感器、测量方法、求解方法、成像方法
本发明涉及传感器电子元器件这一,特别的,涉及一种微尺度细胞检测传感器、测量方法、求解方法、成像方法。
背景技术:
1、细胞和组织的传统检测方法是光学影像方法、体外毒理学方法。然而,人们对高通量筛选的可靠技术的需求日益增加,电学检测这种低成本、更通用普适的方法引起了广泛关注。
2、电阻抗断层成像技术(electrical impedance tomography,eit)作为一种新的检测技术,可进行功能性成像,有无辐射、非侵入性、实时监测的优点,十分适用于医学成像和生物研究,如下述文献:
3、文献1:徐德洪,邓琪,姚佳烽.基于电阻抗成像技术的细胞检测传感器开发[j].传感器与微系统.2023,42(11)。
4、文献2:张益嘉.用于细胞检测的电阻抗成像系统开发[d].南京航空航天大学,2021。
5、对于电阻抗成像而言,其在微尺度细胞成像上具有挑战性,这主要是因为检测信号受到微尺度下双电层等因素致使的噪声影响,其空间分辨率有限,难以准确区分和捕捉到微小的细胞,测量计算出的电阻率差异不够显著,导致电导率图像重建后成像质量较差,伪影较多。
6、有机电化学晶体管(organic electrochemical transistors,oect)是一种将被检测物的生物信号转换为清晰可读的电信号的生物电子器件,凭借其高灵敏度和低检测限等优点在生物传感领域得到了广泛的应用。
7、因此,如何将oect与eit传感器融合在一起,以提升eit在细胞尺寸下的检测精度,就成为一个研究热点。
技术实现思路
1、本发明的目的在于提供一种微尺度细胞检测传感器,以解决现有技术的不足。
2、本发明的另一目的在于提供一种测量方法。
3、本发明的又一目的在于提供一种求解方法。
4、本发明的再一目的在于提供一种成像方法。
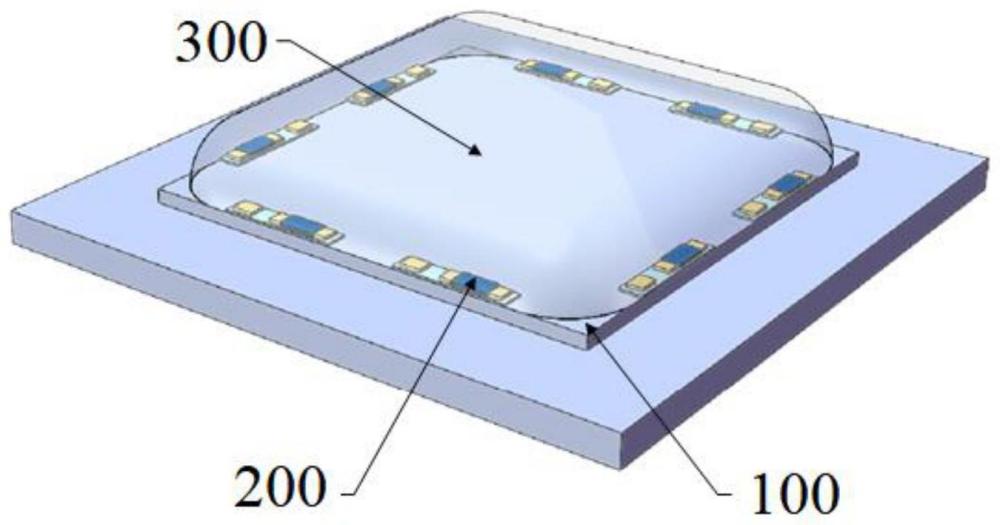
5、一种微尺度细胞检测传感器,其包括:基底(100)、oect阵列电极组件(200)、电解液(300);
6、其中,基底使用不导电材料制成,其形状为长方形;
7、其中,oect阵列电极组件(200)包括八个oect,在基底的每边上设置2个oec;每个所述oect均包括:源极、栅极、漏极以及沟道;所述沟道用于连接源极和漏极的通道,使用有机材料pedot:pss制备而成;
8、其中,在基底的上方还设置有电解液。
9、进一步,所述的电解液为1mol/l的nacl溶液。
10、一种测量方法,八个oect阵列顺序编号为:第1~8号oect;依次对第1~8号oect的栅极进行激励,在激励时同时测量第1~8号oect的源漏输出电流、8个栅极的输入电流。
11、进一步,对任意第i号oect的栅极激励,对1~8号oect的源漏输出电流以及第i号栅极的输入电流的方法测量的方法如下:
12、激励条件:使用给定的频率f和栅极激励电压vgi的交流信号对第i号oect的栅极进行激励,第1~8号oect的漏极均接固定电压vd,第1~8号oect的源极均接地;
13、测量条件:依次测量第1~8号oect的源漏输出电流idi1~idi8;同时,测量第i号oect的栅极的输入电流igi(igi表示第i号oect的栅极受激励时,经第i号oect的栅极输入传感器的栅极电流)。
14、一种求解方法,用于求解栅极分流电流矩阵,其包括如下步骤:
15、步骤一,输入:测量数据和结构参数;
16、所述测量数据包括:栅极激励电压向量vg、源漏测量电流向量id、栅极测量电流向量ig、漏极激励电压vd、截止电压vt、激励频率f;
17、vg=(vg1,vg2,……,vg8),其为8个数据;
18、id=(id11,id12,……idij……id88),其为64个数据;
19、ig=(ig1,ig2,……igi……ig8),其为8个数据;
20、其中,vgi表示第i号oect的栅极激励电压,i为1至8的自然数;
21、其中,idij表示第i号oect的栅极受激励时,第j号oect源漏输出电流,i、j均为1至8的自然数;
22、其中,igi表示第i号oect的栅极受激励时,经第i号oect的栅极输入传感器的栅极电流,i为1至8的自然数;
23、所述结构参数包括:w、d、l;w和d是沟道宽和深,l是沟道长度;
24、步骤二,计算比例等效电容μ×c*11~μ×c*88:
25、
26、其中,μ×c*ij表示第i号oect的栅极受激励时,第j号oect的沟道与电解液之间的比例等效电容,i、j均为1至8的自然数;
27、步骤三,计算比例等效阻抗
28、
29、其中,表示第i号oect的栅极受激励时,第j号oect的沟道与电解液之间的比例等效阻抗,i、j均为1至8的自然数;
30、步骤四,计算栅极分流电流矩阵:
31、
32、其中,任意元素igij采用下式计算:
33、
34、igij表示第i号oect的栅极受激励时,第i号oect的栅极到第j号oect的沟道之间的电流,i、j均为1至8的自然数。
35、一种成像方法,其特征在于,其包括如下步骤:
36、第一,利用有限元仿真方法计算场域在激励频率在f下的灵敏度矩阵s;
37、第二,计算空的敏感场栅极分流电流矩阵i'g-空;i'g-空的获取方法是:首先,在微尺度细胞检测传感器未添加细胞时采用前述的测量方法获取基础数据;然后,采用前述的栅极分流电流矩阵的求解方法求解空的敏感场时的栅极分流电流矩阵;
38、第三,计算待测细胞或组织放置在电解液时的栅极分流电流矩阵i′g-细胞;i′g-细胞的获取方法是:首先,添加待测细胞或组织放置在电解液,采用前述的测量方法获取基础数据;然后,采用前述的栅极分流电流矩阵的求解方法求解待测细胞或组织放置在电解液时的敏感场时的栅极分流电流矩阵;
39、第四,计算栅极分流电流差矩阵δi'g:δi'g=i'g-细胞-i'g-空;
40、第五,根据δi'g,绘制图像。
41、本技术的有益效果在于:
42、第一,本技术提出的传感器,其在传统的eit传感器中,加入了oect阵列,oect栅极电压直接调控离子注入,对于外界信号引起栅极电压微小的变化,沟道电流会产生较大量级变化,可以弥补传统eit方法电极测量在微尺度的不足。另外,考虑对细胞或组织进行监测,若细胞与组织在监测过程中其生理结构、形态功能等发生了巨大的变化,或者与外界产生离子、有机物交换,oect由于其良好的生物相容性可以捕捉到这一变化,然后通过成像技术对这种变化进行可视化分析。
43、第二,本技术提出了一种针对oect阵列的成像方法,其包括如下步骤:
44、2.1,计算空的敏感场栅极分流电流矩阵i'g-空;i'g-空的获取方法是:首先,在微尺度细胞检测传感器未添加细胞时采用权利要求3的激励-测量方法获取基础数据;然后,采用权利要求5的栅极分流电流矩阵的求解方法求解空的敏感场时的栅极分流电流矩阵;
45、2.2,计算待测细胞或组织放置在电解液时的栅极分流电流矩阵i'g-细胞;i'g-细胞的获取方法是:首先,添加待测细胞或组织放置在电解液,采用权利要求3的激励-测量方法获取基础数据;然后,采用权利要求5的栅极分流电流矩阵的求解方法求解待测细胞或组织放置在电解液时的敏感场时的栅极分流电流矩阵;
46、2.4,计算栅极分流电流差矩阵δi'g:δi'g=i'g-细胞-i'g-空;
47、2.4,根据δi'g,绘制图像。
- 还没有人留言评论。精彩留言会获得点赞!