一种对蜂产品中八种抗病毒药物残留量测定的方法与流程
本发明涉及药物残留量测定,尤其是涉及一种对蜂产品中八种抗病毒药物残留量测定的方法。
背景技术:
1、蜂群中存在疾病和感染的情况时,养蜂人员常使用抗病毒类药物进行治疗,例如金刚烷胺、金刚乙胺、美金刚、利巴韦林、吗啉胍、阿昔洛韦、奥司他韦及更昔洛韦。这些药物被添加到蜂饲料或饮用水中,以帮助蜜蜂抵抗病毒感染或治疗已经感染的蜜蜂,同时为了防止疾病在蜂群中传播,养蜂人员可能会在蜂巢和蜜蜂周围使用抗病毒类药物。但这些药物可能会在蜂产品中残留。
2、液相色谱-串联质谱(lc-ms/ms)测定方法在蜂产品中抗病毒药物残留量的检测方面具有重要意义。这些抗病毒类药物在蜂产品中的残留量检测是为了确保食品安全和监测药物残留对蜂产品质量的影响。但是,目前还没有合适的液相色谱-串联质谱测定方法能够同时而稳定地检测出金刚烷胺、金刚乙胺、美金刚、利巴韦林、吗啉胍、阿昔洛韦、奥司他韦及更昔洛韦这八种蜂产品中残留的抗病毒类药物。首先,蜂产品样品复杂,含有丰富的蛋白质和脂质成分,这给药物残留的提取和净化带来了一定的困难。其次,需要建立高灵敏度和高选择性的测定方法,以确保即使在低水平下也能准确测定这些抗病毒类药物的残留量。此外,不同药物的化学性质各异,需要针对性地选择适当的色谱柱和质谱条件,以实现对多种药物的同时检测和定量。
3、基于此,亟需开发一种高灵敏度和高选择性的测定方法以同时测定峰产品中八种抗病毒药物残留量。
技术实现思路
1、本发明所要解决的技术问题是:
2、提供一种蜂产品中药物残留量测定的方法。
3、为了解决所述技术问题,本发明采用的技术方案为:
4、一种蜂产品中药物残留量测定的方法,包括以下步骤:
5、s1采用酸性乙腈混合提取液提取蜂产品中的金刚烷胺、金刚乙胺、美金刚、利巴韦林、吗啉胍、阿昔洛韦、奥司他韦和更昔洛韦,得到提取液;
6、s2采用querchers、prime hlb和emr增强去脂型分散spe中的至少一种方法以净化所述提取液,得到净化后提取液;
7、s3以sb-aq c18作为色谱柱,采用高效液相色谱串联质谱法检测步骤s2中净化后提取液,其中,流动相包括甲酸、甲醇和乙酸铵中的至少一种。
8、根据本发明的实施方式,所述技术方案中的一个技术方案至少具有如下优点或有益效果之一:
9、采用本发明的方法,能同时在蜂产品中定性、定量测定包括金刚烷胺、金刚乙胺、美金刚、利巴韦林、吗啉胍、阿昔洛韦、奥司他韦和更昔洛韦在内的八种抗病毒药物残留,对上述8种药物都具有极低的检测限,极佳的准确度和精密度。
10、其中,由于8种药物性质差异较大,利巴韦林和吗啉胍属于强极性物质,易溶于水,微溶于甲醇;而其他几种物质属于中低极性化合物,微溶于水,易溶于甲醇;并且利巴韦林与糖结构相似。本发明采用酸性乙腈混合提取液,能确保八种抗病毒类药物的提取,并且酸性乙腈混合提取液能很好的去除蜂蜜中的糖分,得到较为满意的色谱图;
11、其中,由于8种化合物含有胺基、呈碱性,且利巴韦林和吗啉胍极性较强,较难被洗脱或回收率较低,为避免采用分步洗脱或将利巴韦林和吗啉胍单独洗脱导致程序繁琐,本发明选用querchers、prime hlb和emr增强去脂型分散spe中的至少一种方法以净化所述提取液,保证同时净化8种抗病毒类药物,并得到较好的回收率;
12、由于利巴韦林和吗啉胍极性较强,在色谱分离中需要高比例水相,其他6种属于中等或弱极性药物,在色谱分离中需要高比例有机相,且金刚乙胺和美金刚属于同分异构体,其在相对分子质量和化学性质上的相似性,因此选用合适的色谱柱对8种物质的分离至关重要,常规的色谱柱如hilic色谱柱难以分离金刚乙胺和美金刚、石墨化碳色谱柱对于基质复杂的样品分析,具有不稳定性,本发明采用的sb-aq c18色谱柱是一种c18表面改性的反相柱,能够耐受100%水相,既能实现利巴韦林和吗啉胍的保留又能实现金刚乙胺和美金刚的分离。
13、其中,常用的流动相通常含有乙腈,但乙腈洗脱能力较强,会导致金刚乙胺和美金刚分离效果并不完美,因此本发明流动相包括甲酸、甲醇和乙酸铵中的至少一种。
14、根据本发明的一种实施方式,所述酸性乙腈混合提取液包括甲酸乙腈混合提取液,且甲酸在所述酸性乙腈混合提取液中的质量百分数为1-1.5%。
15、根据本发明的一种实施方式,在蜂产品中加入1-1.5%甲酸乙腈后会出现分层现象,上层清液为乙腈体系,下层为糖。
16、根据本发明的一种实施方式,当蜂产品提取后出现分层现象时,若将上层有机层用氮气吹干,再用下层水相层复溶上层有机层后,会发现蜂产品中含有的大量内源性物质,如尿苷等,结构与利巴韦林相似,无法分离,造成峰型杂乱无法分析。
17、根据本发明的一种实施方式,所述酸性乙腈混合提取液中还含有甲醇和/或水,所述酸性乙腈混合提取液包括质量比7-7.5:3-2.5的乙腈:甲醇。将蜂产品中8种物质提取后,下层水相经过滤后分析发现,水相层中检测到较高含量的利巴韦林、吗啉胍,以及少量更昔洛韦。说明酸性乙腈混合提取液虽然能够很好的去除蜂产品中的糖分,得到较为满意的色谱图,但对于利巴韦林、吗啉胍、更昔洛韦等更易溶于水的物质,提取效率不高,因此本发明在酸性乙腈混合提取液的基础上,再加入不同比例的水、甲醇等溶剂以提高提取效率。研究发现,在酸性乙腈混合提取液中加入低比例的甲醇后,8种抗病毒类药物的提取效率显著提高。
18、根据本发明的一种实施方式,所述酸性乙腈混合提取液包括质量比为7-7.5:2-2.5:1的乙腈:甲醇:水。
19、根据本发明的一种实施方式,当本发明流动相中不包含乙酸铵时,当标准品浓度过高时,吗啉胍峰型出现会出现分叉。
20、根据本发明的一种实施方式,采用querchers或prime hlb,两方法均能同时净化蜂产品中的8种抗病毒类药物,并得到较好的回收率。并且上述两方法对于蜂蜜样品的净化效果是相当的。
21、根据本发明的一种实施方式,步骤s2中,采用emr增强去脂型分散spe方法净化蜂产品中的蜂王浆;采用querchers方法净化蜂产品中的蜂蜜。因为蜂王浆中蛋白质和脂质含量高,提取液通过prime hlb流出时阻力较大,造成小柱堵塞。因此蜂王浆选用了emr增强去脂型分散spe,在去除脂质的同时还能保证满意的回收率,而蜂蜜样品选用同种类型的querchers小柱。
22、根据本发明的一种实施方式,所述sb-aq c18色谱柱的粒径为2.7-3μm,内径为2.1-2.5mm,柱长为100-120mm。选用其他的色谱柱会导致无法同时分离上述8种物质,比如hilic色谱柱难以分离金刚乙胺和美金刚;比如石墨化碳色谱柱分析蜂蜜和蜂王浆样品具有不稳定性;只有sb-aq c18色谱柱既能实现利巴韦林和吗啉胍的保留又能实现金刚乙胺和美金刚的分离,从而保证8种物质的分离效果优良。
23、根据本发明的一种实施方式,步骤s3中流动相包括乙酸铵,且乙酸铵的浓度为5-10mmol/l。合适浓度的乙酸铵能够进一步提高电离效率,保证吗啉胍保留的稳定性得以增强,保证更昔洛韦响应值提高。
24、根据本发明的一种实施方式,所述检测过程中采用梯度洗脱程序,并设置如下:
25、洗脱时间,甲酸、乙酸铵混合溶液与甲醇的体积比;
26、0-1.5min,100:0;
27、1.5-4.5min,70-100:0-30;
28、4.5-7.5min,10-70:30-90;
29、7.5-8.0min,10:90:
30、8.0-8.1min,10-100:0-90;
31、8.1-10min,100:0。
32、根据本发明的一种实施方式,所述检测过程中液相色谱条件包括:
33、柱温:30-35℃;
34、流速:0.3-0.6ml/min;
35、进样量:10-15μl。
36、根据本发明的一种实施方式,步骤s3中,采用高效液相色谱串联质谱法检测的过程中,以正离子扫描模式进行质谱分析。8种抗病毒药物都含有胺基基团,在离子化过程中,易于h质子结合,带正电荷,因此选用正离子扫描模式进行质谱分析。
37、根据本发明的一种实施方式,步骤s3中,采用高效液相色谱串联质谱法检测的过程中,质谱条件包括:
38、离子源:电喷雾离子源(esi);
39、毛细管电压(capillary voltage):3500-3600v;
40、雾化温度(gas temp):300-350℃;
41、雾化器流速(gas flow):7-10l/min;
42、雾化器压力(nebulizer):40-50psi;
43、鞘气温度(shealth gas temp):350-450℃;
44、鞘气流速(shealth gas flow):12-20l/min。
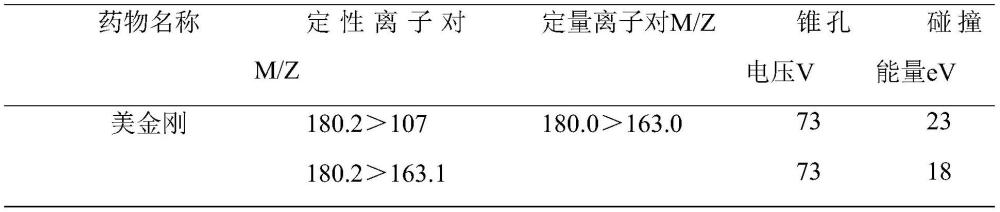
45、根据本发明的一种实施方式,步骤s3中,采用高效液相色谱串联质谱法检测的过程中,各种药物的mrm参数见表1。
46、表1选择离子设定参数
47、
48、
49、根据本发明的一种实施方式,所述采用内标法对目标物进行定量。本发明考察了基质效应,结果表明吗啉胍、利巴韦林、更昔洛韦、阿昔洛韦、金刚烷胺、金刚乙胺、美金刚、奥司他韦的基质效应分别为16.1%、13.4%、41.4%、37.4%、61.8%、85.3%、69.7%、92.2%。通常认为当基质效应<80%时,需要用基质标准品或者内标定量的办法抵消基质效应。从实验结果可以看出,部分待测物基质效应严重,因此本发明采用内标法定量,可大大抵消基质效应。
50、根据本发明的一种实施方式,蜂产品中药物残留量测定的方法中,还包括蜂蜜样品前处理的步骤:
51、称取蜂蜜,置于离心管内,加入内标标准工作液,加入1-1.5%甲酸乙腈甲醇溶液,于涡旋混合器上涡旋混匀,振动器匀速震荡。于4-6℃下离心,取上层清液至分散固相萃取柱中,涡旋震荡。于4-6℃下离心,取上清液至离心管中,于40-50℃下氮吹至近干,取1-2ml复溶液复溶,经0.22-0.3μm pes滤膜过滤待测。
52、根据本发明的一种实施方式,蜂产品中药物残留量测定的方法中,还包括蜂王浆样品前处理的步骤:
53、称取蜂王浆,置于离心管内,加入内标标准工作液,加入1-1.5%甲酸乙腈甲醇溶液,于涡旋混合器上涡旋混匀,振动器匀速震荡。于4-6℃下离心,取上层清液至预先加入2-4ml水活化的emr净化包中,涡旋震荡。于4-6℃下离心,取上清液至离心管中,于40-50℃下氮吹至近干,取1-2ml复溶液复溶。复溶后如有浑浊,可于4-6℃下离心后经0.22-0.3μm pes滤膜过滤待测。
54、根据本发明的一种实施方式,蜂产品中药物残留量测定的方法中,定性测定方法包括以下步骤:
55、每种被测组分选择1个母离子,2个子离子,在相同试验条件下,样品中待测物质的保留时间与标准溶液中对应的保留时间偏差在±2.5%之内;且样品谱图中各组分的两个子离子的相对丰度与浓度接近的标准溶液的相对丰度一致,偏差不超过以下规定的范围,则可判定为样品中存在对应的待测物。在定性确证时相对离子丰度的最大允许偏差为:当相对离子丰度(%)分别为>50、>20~50、>10~20和≤10,允许的相对偏差(%)依次为±20、±25、±30和±50。
56、根据本发明的一种实施方式,蜂产品中药物残留量测定的方法中,定量测定方法包括以下步骤:
57、分别取适量试样溶液和相应浓度的标准工作液,作单点校准或多点校准,内标法定量。标准工作液及试样液中药物的响应值均应在仪器检测的线性范围内,试样液进样过程中应参插标准工作液,以便准确定量。
58、本发明的其它特征和优点将在随后的说明书中阐述,并且,部分地从说明书中变得显而易见,或者通过实施本发明而了解。
- 还没有人留言评论。精彩留言会获得点赞!