一种免疫层析试纸条、制备方法及使用方法
本技术涉及医学检测,特别涉及一种免疫层析试纸条、制备方法及使用方法。
背景技术:
1、目前主要采用s蛋白、n蛋白、特异性抗体(igm、igg和中和抗体n ab)、rna基因作为检测sars-cov-2感染的指标。基于核酸扩增的检测,如实时逆转录聚合酶链式反应(rt-pcr),是目前诊断sars-cov-2感染最准确的方法然而,取样困难、繁琐的程序、测试时间冗长以及缺乏合格的人员和实验室限制了rt-pcr检测的应用。由于纳米技术和生物传感器的进步,基于纸层析的横向流动免疫测定(lfia)平台已越来越多地用于covid-19诊断。选择合适的生物标志物对于准确诊断covid-19至关重要。目前,s蛋白、n蛋白、特异性抗体(igm、igg和中和抗体n ab)和rna基因大多被用作检测sars-cov-2感染的指标。理论上,整个sars-cov-2病毒及其结构蛋白都可以作为靶抗原,sars-cov-2s蛋白可与宿主细胞上的受体相互作用,介导病毒-细胞膜融合。sars-cov-2n蛋白参与多种细胞过程,如病毒生长、rna复制和mrna转录。s和n蛋白都具有免疫原性,在病毒组装过程中大量表达。然而,目前大多数抗原测试都是基于n抗原进行的,由于n抗原的检测比s抗原产生更好的检测灵敏度。因此,检测这些蛋白可以有效筛查早期患者。使用lfia进行抗原检测的特点是高效、低成本,因为抗原检测可以直接使用各种生物样本(例如从前鼻腔和喉咙中提取的组织样本以及唾液)进行检测,而无需复杂的实验室程序。抗原检测诊断sars-cov-2已广泛应用于临床。
2、为了提高抗原检测的灵敏度,目前主要采用的方法有:1.探针比色度的优化:经100份临床样品检测,aunp-lfia试纸的视觉检出限为1ng/ml,灵敏度为94.3%。shen等人使用乳胶微球标记抗原,以进一步降低成本并提高检测的性能该方法的检出限为25ng/ml,灵敏度为98.22%。进一步提高比色测定灵敏度的一般思路包括放大aunps的血浆活性。等离子体扩增最常用的策略是将许多aunp聚集在较大尺寸的载体粒子上。oh等人开发了等离子体aunp簇,aunp簇之间的间隙大于15nm,以避免平衡激子耦合,从而在保持等离子体颜色的同时增加了整体光吸收。panferov等采用了三种原位改性方法(银增强、电助金沉积和金强化)来降低lfia对sars-cov-2rbd的检出限。2.荧光探针的优化:许多研究将免疫测定的特异性与荧光物质的高光强相结合,应用新型荧光标记材料和信号增强策略来提高定量检测性能。zhang等建立了基于聚集诱导发射(aie)试剂的检测sars-cov-2rbd和n抗原的lfia平台,该试剂具有高亮度和耐光漂等优异的荧光特性。xu等人开发了一种基于时间分辨荧光铕颗粒的lfia平台,可直接检测鼻咽拭子样本中的rbd蛋白铕荧光材料的长寿命和大stocks位移导致检测限为2ng/ml,灵敏度高于80%。
3、lfia检测的低灵敏度问题仍然需要解决。目前为了提高lfia检测sars-cov-2灵敏度的方法主要基于aunp的比色法lfia在sars-cov-2抗原和抗体识别分析中占多数,但使用原始材料和优化不同的信号标记(比色、荧光、磁、拉曼、光热等)是提高检测灵敏度的最常用方法。开发更先进的具有强信号响应能力的纳米材料和更高分辨率的信号读取仪器,需要复杂的实验操作过程及昂贵的科研仪器。
技术实现思路
1、鉴于此,有必要针对现有技术存在的操作复杂成本高昂的技术缺陷提供一种操作简便,成本低,检测限低,非特异性吸附小的免疫层析试纸条、制备方法及使用方法。
2、为解决上述问题,本技术采用下述技术方案:
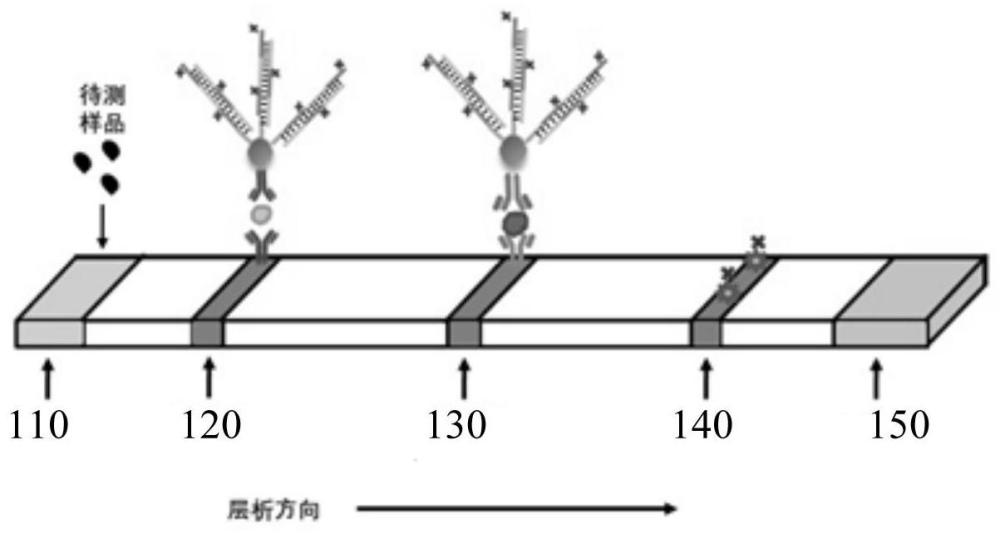
3、本技术目的之一,提供了一种免疫层析试纸条,包括:沿层析方向依次间隔设置样品垫、第一检测线、第二检测线、质控区以及吸水垫;所述第一检测线为rbd蛋白检测区,所述第二检测线为n蛋白检测区,所述rbd蛋白检测区包括rbd捕获抗体,所述n蛋白检测区包括n蛋白捕获抗体,所述质控区包括bsa-biotin。
4、本技术目的之二,提供了一种所述的免疫层析试纸条的制备方法,包括下述步骤:
5、将所述样品垫使用预处理液进行预处理;
6、将所述rbd捕获抗体和所述n蛋白捕获抗体分别设置在nc膜的所述第一检测线及所述第二检测线上;
7、将所述bsa-biotin设置在所述nc膜的所述质控线上;
8、将划好线的所述nc膜固定于底板上;
9、将所述吸水垫固定于所述底板上并与所述nc膜部分重叠;
10、将所述样品垫固定于所述底板上并与所述nc膜部分重叠。
11、在其中一些实施例中,在将所述样品垫使用预处理液进行预处理的步骤中,具体包括下述步骤:
12、将所述样品垫使用预处理液预处理2-16℃过夜再氮气吹干,所述预处理液为0.001-1g蔗糖、0.001-0.01g聚乙二醇、1-5μl吐温-20 00磷酸盐缓冲溶液。
13、在其中一些实施例中,在将所述新型冠状病毒刺突蛋白捕获抗体和所述新型冠状病毒核衣壳蛋白捕获抗体分别设置在nc膜的所述第一检测线及所述第二检测线上的步骤中,所述nc膜为硝酸纤维膜。
14、在其中一些实施例中,在将所述rbd捕获抗体和所述n蛋白捕获抗体分别设置在nc膜的所述第一检测线及所述第二检测线上的步骤中,具体包括下述步骤:
15、使用划膜液分别对所述rbd捕获抗体和所述n蛋白捕获抗体进行稀释使抗体终浓度为4-6μm,所述划膜液为0.01 -0.1g蔗糖、100-200μl 3%甲醇磷酸盐缓冲溶液;
16、采用喷膜机将稀释后的所述rbd捕获抗体和所述n蛋白捕获抗体印在nc膜的检测线上,所述喷膜机设置的划线量如下:所述第一检测线、所述第二检测线及所述质控线均为0.2-0.8μl/cm。
17、在其中一些实施例中,所述样品垫为磷酸盐缓冲液浸泡过的玻璃纤维膜,所述吸水垫为玻璃纤维膜,所述底板为白色塑料底板。
18、本技术目的之三,提供了一种所述的免疫层析试纸条的使用方法,包括下述步骤:
19、在所述nc膜上分别喷涂牛血清白蛋白生物素偶联物、新型冠状病毒核衣壳蛋白捕获抗体、新型冠状病毒刺突蛋白捕获抗体,分别作为所述质控线、所述第一检测线及所述第二检测线;
20、将带有生物素标签的杂交链式反应产物、新型冠状病毒核衣壳蛋白检测抗体、新型冠状病毒刺突蛋白检测抗体共修饰的纳米金探针和待检样品共孵育后滴加到所述样品垫,随后在所述样品垫上滴加链霉亲和素修饰的纳米金探针;
21、根据所述第一检测线及所述第二检测线的颜色强度定量分析待测样品中新冠病毒rbd蛋白和n蛋白的浓度,由此判断体内病毒含量。
22、在其中一些实施例中,所述杂交链式反应产物通过下述步骤获取:
23、双功能化纳米金探针包括金纳米颗粒表面的触发链引发杂交链式反应并结合rbd蛋白检测抗体或n蛋白检测抗体,所述触发链标记量为aunps:ps1:n/r antibody=1:(0-25):(0-50)=1:20:5。
24、在其中一些实施例中,所述触发链的序列为5
25、‘-aaaaaaaaaatttttcgtttaggatttgtg-3’。
26、在其中一些实施例中,所述触发链的标记量为每983μl纳米金原液加入10μm的17μl的触发链。
27、在其中一些实施例中,所述触发链标记量为纳米金粒子:触发链1:新型冠状病毒核衣壳蛋白/刺突蛋白检测抗体=1:20:5。
28、在其中一些实施例中,所述杂交链式反应的原料为核酸链发夹1/发夹2,用量为每50μl双功能化纳米金探针加入20μl发夹1/发夹2,所述杂交链式反应条件为室温静置0.2-3小时。
29、在其中一些实施例中,在根据所述第一检测线及所述第二检测线的颜色强度定量分析待测样品中新冠病毒rbd蛋白和n蛋白的浓度,由此判断体内病毒含量的步骤中,具体包括下述步骤:
30、若所述质控线、所述第一检测线和所述第二检测线均显颜色,则表明感染新冠病毒,并且根据所述第一检测线和所述第二检测线的颜色强度判断新冠病毒rbd蛋白和n蛋白的浓度;若仅所述质控线显颜色,表明未感染新冠病毒。
31、本技术采用上述技术方案,其有益效果如下:
32、本技术提供的免疫层析试纸条、制备方法及使用方法,通过非酶杂交链式反应进行核酸扩增,将扩增后修饰了生物素的核酸链通过巯基连接在金纳米粒子的表面,提供了许多生物素位点,可供链霉亲和素修饰的胶体金粒子结合,进而达到信号放大的效果;此外,本技术可实现病毒多靶标同时检测,病毒mrna转录的s和n蛋白都具有免疫原性,在病毒组装过程中大量表达,此方法针对新型冠状病毒的n蛋白和s蛋白的受体结合域(rbd)进行同时检测,有望提高检测的准确性。并且可经过信号放大,将检测限明显降低至0.05ng/ml。与未经信号放大相比,将检测限降低10倍。
- 还没有人留言评论。精彩留言会获得点赞!